Mechanische Kreislaufunterstützung im Infarkt-bedingten kardiogenen Schock
Autor: Priv.-Doz. Dr. Christoph Brenner
Univ.-Klinik für Innere Medizin III
Medizinische Universität Innsbruck
E-Mail: christoph.brenner@i-med.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der Infarkt-bedingte kardiogene Schock (AMI-CS) ist trotz der enormen Fortschritte in der interventionellen Versorgung des akuten Myokardinfarktes in den vergangenen Jahrzehnten weiterhin mit einer hohen Mortalität von bis zu 50% assoziiert. Mechanische Herz-Kreislauf-Unterstützungssysteme (MCS) bieten das Potenzial, die Schockspirale frühzeitig zu durchbrechen und zu einer relevanten Verbesserung des Outcomes beizutragen. Die aktuelle Datenlage zu VA-ECMO und Impella präzisiert nun das Patientenkollektiv, das vom Einsatz dieser invasiven Maßnahmen profitieren könnte.
Keypoints
-
Mit der VA-ECMO steht heute ein maximalinvasives Verfahren zur Verfügung, das Herz- und Lungenfunktion im Bedarfsfall komplett ersetzen kann. Nachteile sind die myokardiale und pulmonale Belastung durch die Nachlasterhöhung, die großlumigen Gefäßzugänge und die großen Fremdoberflächen im Schlauchsystem.
-
Die mikroaxiale Impella-Flusspumpe kann zur Unterstützung der LV-Funktion minimal-invasiv implantiert werden. Eine Blutoxygenierung findet bei diesem System jedoch nicht statt. Spezifisch limitierende Faktoren sind außerdem die Hämolyse und Durchblutungsstörungen im Zugangsgefäß.
-
Bei ausgewählten Patienten (mit neurologisch guter Prognose) kann der Einsatz von mechanischen Unterstützungssystemen im Infarkt-bedingten kardiogenen Schock eine deutliche Prognoseverbesserung bewirken.
Patienten im Infarkt-bedingten kardiogenen Schock
Etwa 10% aller Patienten mit akutem Herzinfarkt entwickeln im Rahmen des Akutgeschehens einen kardiogenen Schock,1 der glücklicherweise in mehr als der Hälfte aller Fälle durch eine rasche koronare Revaskularisation, gegebenenfalls einer Gabe von Vasopressoren und ohne Einsatz einer mechanischen Herz-Kreislauf-Unterstützung erfolgreich behandelt werden kann.
Die zweitgrößte Gruppe der Schockpatienten wird jedoch bereits von den Patienten gebildet, deren Ausgang aufgrund einer intraktablen Komorbidität (hypoxischer Hirnschaden oder Multiorganversagen) letal verläuft. Durchschnittlich sterben etwa 24% aller AMI-CS-Patienten an einer neurologischen Ursache. Im extrahospital reanimierten Kollektiv (OHCA) steigt die Quote der Patienten, deren Prognose aufgrund einer schweren zerebralen Hypoxie durch den Einsatz einer mechanischen Kreislaufunterstützung nicht verbessert werden kann, auf bis zu 57%.2 Zudem muss beim MCS-Einsatz berücksichtigt werden, dass die heute zur Verfügung stehenden Verfahren invasiv und komplikationsbehaftet sind. Für einen undifferenzierten Einsatz der venoarteriellen extrakorporalen Membranoxygenierung (ECMO) hat sich deshalb z.B. bei AMI-CS-Patienten auch kein Vorteil nachweisen lassen.3 Durch eine optimale Patientenselektion kann der positive Effekt einer mechanischen Kreislaufunterstützung vermutlich jedoch deutlich verbessert werden.4
Systeme zur mechanischen Kreislaufunterstützung
Aktuell sind in Österreich mit der ECMO und der mikroaxialen Flusspumpe Impella® zwei mechanische Kreislaufunterstützungssysteme in Verwendung, die sich in ihrer Funktionsweise, der Leistungsfähigkeit und ihren Nebenwirkungen grundsätzlich unterscheiden.
ECMO
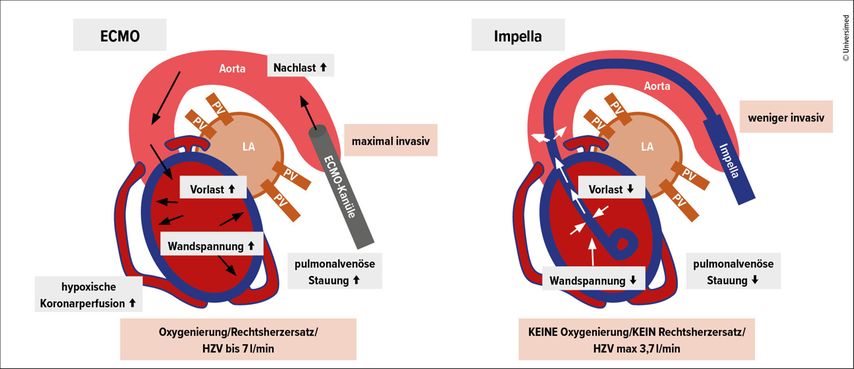
Die ECMO ist mit einem Blutfluss von bis zu 7l/min nicht nur in der Lage, sowohl Links- als auch Rechtsherzfunktion, sondern auch den Gasaustausch der Lunge komplett zu ersetzen (Abb. 2). Nachteile dieses maximalinvasiven Verfahrens liegen dabei nicht nur in den zwei großlumigen Gefäßzugängen (sowie den damit assoziierten Blutungskomplikationen) und den extensiven Fremdoberflächen des Schlauchsystems und des Oxygenators (mit dem Risiko für Inflammation, Gerinnselbildung und Notwendigkeit der Antikoagulation). Bauartbedingt entsteht zudem durch die arterielle Nachlasterhöhung eine relevante Belastung des bereits erkrankten linken Ventrikels, die der myokardialen Erholung des infarzierten Herzens entgegenwirkt und im schwersten Fall durch den maschinell induzierten Gegendruck die Öffnung der Aortenklappe verhindern kann (mit Gefahr der Thrombosierung des linken Ventrikels). Die durch die Nachlasterhöhung zudem nicht selten entstehende pulmonale Stauung kann zudem zu einer ausgeprägten Hypoxämie im pulmonalvenösen Blut und mit dem sogenannten Harlekin-Phänomen zu einer hypoxischen Perfusion der rechten Gehirnhälfte sowie der Koronararterien führen.5
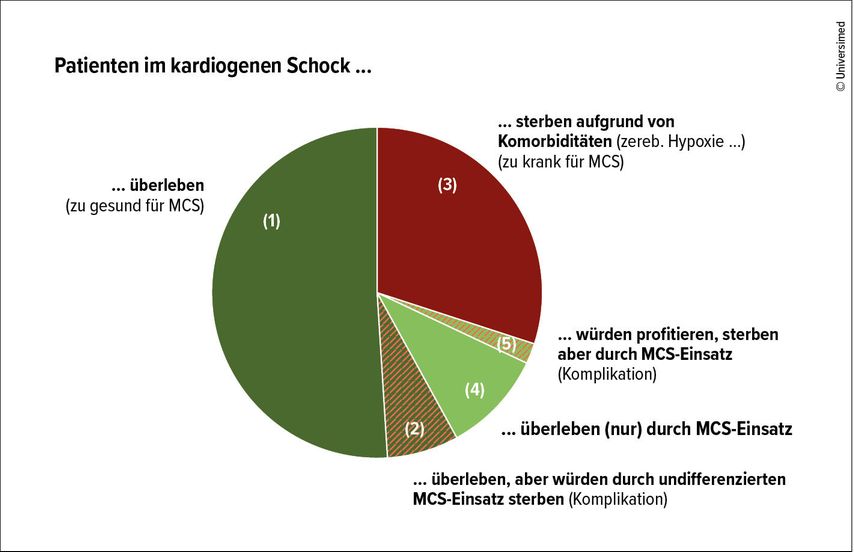
Abb. 1: Patienten im kardiogenen Schock überleben in der Mehrheit der Fälle ohne Einsatz einer mechanischen Kreislaufunterstützung (1). Der undifferenzierte Einsatz von MCS-Systemen in dieser Patientengruppe würde komplikationsbedingt eine Prognoseverschlechterung bewirken (2). Patienten, die an einer zerebralen Hypoxie versterben, können von einem MCS-Einsatz nicht profitieren (3). Der Anteil der Patienten im AMI-CS, der von der Verwendung einer mechanischen Kreislaufunterstützung langfristig profitiert (4) und keine MCS-assoziierte Komplikation (5) erleidet, ist damit begrenzt
Impella-Pumpe
Die Impella-Pumpe dagegen reduziert durch ihre Blutaspiration im linken Ventrikel die Vorlast und damit die pulmonalvenöse Stauung (Abb. 2). Sie ist zudem mit nur einem notwendigen arteriellen Gefäßzugang sowie der fehlenden extrakorporalen Blutzirkulation deutlich weniger invasiv als die ECMO. Allerdings ist ihre Wirkung auf das kardiopulmonale System dadurch limitiert, dass die mittlere Flussrate maximal 3,7l/min erreichen kann und keine maschinelle Oxygenierung des transportierten Blutes erfolgt. Das Impella-System ist damit nur in der Lage, eine kardiale Unterstützung zu bieten, kann jedoch nicht wie die ECMO das kardiopulmonale System ersetzen. Nebenwirkung des mit bis zu 46000 Umdrehungen pro Minute rotierenden Impellers ist dabei unter anderem eine mitunter deutliche Hämolyse mit der Gefahr eines daraus resultierenden Nierenversagens.
Abb. 2: Einsatz von Herz-Kreislauf-Unterstützungssystemen (MCS) bei Infarkt-bedingtem kardiogenem Schock (AMI-CS): Patienten- und Behandlungsauswahl
Kombination ECMELLA
Die gleichzeitige Kombination beider Systeme in einem Patienten („ECMELLA“) ist zwar kostenintensiv, jedoch potenziell in der Lage, die wechselseitigen Limitationen beider Systeme auszugleichen. Limitierend für eine regelhafte Kombinationstherapie ist neben den wirtschaftlichen Faktoren die relevant erhöhte Komplikationsrate.6
Aktuelle Datenlage
Im ECLS-SHOCK-Trial konnte bei routinemäßiger Anwendung der VA-ECMO im Infarkt-bedingten kardiogenen Schock bei (weitgehend unselektierten) Patienten kein signifikanter Vorteil hinsichtlich der 30-Tage-Mortalität nachgewiesen werden. Der Einsatz der ECMO war jedoch mit einem deutlich erhöhten Risiko für Blutungs- und Gefäßkomplikationen assoziiert.3,7 Im Gegensatz dazu konnte in der DanGer-Shock-Studie gezeigt werden, dass der Einsatz der Impella® CP bei Patienten im AMI-CS bei einer „number needed to treat“ von 8 mit einer signifikanten Reduktion der 180-Tage-Mortalität um 26% verbunden war.8 In einer umfassenden Metaanalyse aus neun randomisierten klinischen Studien zur mechanischen Kreislaufunterstützung im kardiogenen Schock von Thiele et al. konnte zudem nachgewiesen werden, dass die Gesamtmortalität insbesondere bei Patienten ohne erhöhtes Risiko für einen hypoxischen Hirnschaden durch den Einsatz von MCS-Systemen signifikant reduziert werden kann.4
Welche Patienten profitieren?
Insgesamt wird damit aus der heute verfügbaren Datenlage deutlich, welche Patienten vom Einsatz der mechanischen Kreislaufunterstützung profitieren können.
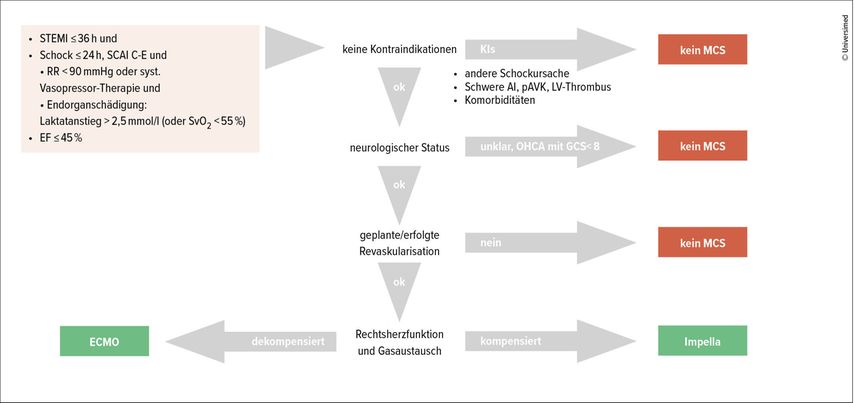
Voraussetzungen für den Einsatz der komplikationsträchtigen Devices in einem günstigen Nutzen-Risiko-Verhältnis sind das Vorliegen eines Infarkt-bedingten kardiogenen Schocks mindestens im SCAI-Stadium C und, das Fehlen von Kontraindikationen wie z.B. einer schweren pAVK oder anderen Komorbiditäten, die eine Device-Implantation nicht komplikationsarm ermöglichen (Abb. 3).
Die mechanische Kreislaufunterstützung ist in der Lage, ein kollabierendes Kreislaufsystem temporär zu stabilisieren – ein MCS-vermittelter kurativer Effekt ist nicht zu erwarten. Vielmehr führt der MCS-Einsatz zu einer weiteren Belastung des Gesamtorganismus und ist deshalb nur sinnvoll, wenn eine gute neurologische Prognose (z.B. GCS ≥8 zum Implantationszeitpunkt) und eine gute kardiale Erholung (durch Revaskularisation oder in Grenzfällen durch LVAD/HTx) zu erwarten sind.
Bei kompensierter Rechtsherzfunktion und intaktem pulmonalem Gasaustausch sollte aufgrund der geringeren Invasivität der Impella®-Flusspumpe der Vorzug gegeben werden. In Fällen mit begleitendem Rechtsherzversagen oder ARDS steht die VA-ECMO als temporärer Ersatz für das kardiopulmonale System zur Verfügung.
Literatur:
1 Lusebrink E et al.: Cardiogenic shock. Lancet 2024; 404(10466): 2006-20 2 Davodian LW et al.: Timing and causes of death in acute myocardial infarction complicated by cardiogenic shock (from the RETROSHOCK cohort). Am J Cardiol 2022; 171: 15-22 3 Thiele H et al.: Extracorporeal life support in infarct-related cardiogenic shock. N Engl J Med 2023; 389(14): 1286-97 4 Thiele H et al.: Temporary mechanical circulatory support in infarct-related cardiogenic shock: an individual patient data meta-analysis of randomised trials with 6-month follow-up. Lancet 2024; 404(10457): 1019-28 5 Rupprecht L et al.: Pitfalls in percutaneous ECMO cannulation. Heart Lung Vessel 2015; 7(4): 320-6 6 Schrage B et al.: Left ventricular unloading is associated with lower mortality in patients with cardiogenic shock treated with venoarterial extracorporeal membrane oxygenation: results from an international, multicenter cohort study. Circulation 2020; 142(22): 2095-106 7 Zeymer U et al.: Venoarterial extracorporeal membrane oxygenation in patients with infarct-related cardiogenic shock: an individual patient data meta-analysis of randomised trials. Lancet 2023; 402(10410): 1338-46 8 Moller JE et al.: Microaxial flow pump or standard care in infarct-related cardiogenic shock. N Engl J Med 2024; 390(15): 1382-93
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Load Monitoring in der modernen Sportmedizin: Zytokine vs. cfDNA vs. miRNA
Load Monitoring wird als ein auf individuelle Anforderungen zugeschnittener Prozess verstanden, dem durch molekulare Biomarker zukünftig neue Möglichkeiten im Leistungssport und in der ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...