La stéatose hépatique non alcoolique: sous-diagnostiquée et sous-estimée
Auteurs:
Dre méd. Sena Blümel
PD Dr méd. Christoph Jüngst
Klinik für Gastroenterologie und Hepatologie
Universitätsspital Zürich
E-mail: sena.bluemel@usz.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La stéatose hépatique non alcoolique (NAFLD) est étroitement associée au syndrome métabolique et constitue aujourd’hui l’hépatopathie la plus fréquente dans le monde. À mesure que la maladie évolue, la NAFLD peut entraîner le développement d’une fibrose, voire d’une cirrhose du foie. Il est important d’identifier les patients présentant un risque plus élevé d’évolution progressive ou de fibrose hépatique déjà avancée pour les soumettre à un diagnostic et une surveillance plus approfondis.
Keypoints
-
Les patients souffrant d’obésité et de syndrome métabolique présentent un risque élevé de développer une NAFLD.
-
Le dépistage de ces populations à risque par les médecins traitants de premier recours en vue de détecter la présence d’une NAFLD et l’évaluation du stade de la maladie est essentiel pour détecter précocement et pouvoir contrecarrer une hépatopathie avancée.
-
Le score de fibrose de la NAFLD et le FIB-4 sont de bonnes méthodes de dépistage pour évaluer la fibrose et peuvent être réalisés sans avoir besoin d’instruments.
-
Le nom de la maladie, NAFLD, fait actuellement l’objet d’une discussion, étant donné que d’autres causes d’hépatopathie peuvent être concomitantes. Pour mettre l’accent sur l’étiologie, on tend à renommer la maladie stéatose hépatique associée au métabolisme (MAFLD).
La NAFLD est l’hépatopathie la plus fréquente dans le monde occidental. Dans les pays où la proportion de personnes en surpoids et atteintes d’obésité est élevée, environ un quart à un tiers des adultes sont atteints de NAFLD. La prévalence croissante de l’obésité et des affections associées telles que le diabète de type 2, la dyslipidémie, l’hypertension et l’apnée obstructive du sommeil a augmenté rapidement, tout comme la prévalence de la NAFLD. Par exemple, alors que la NAFLD touchait 6% des adultes aux États-Unis en 2003, ce chiffre est passé à 18% en 2011 et est actuellement proche de 25%.1 Dans les populations à risque, c’est-à-dire les patients souffrant d’obésité et de diabète de type 2, la prévalence de la NAFLD dépasse même 50%.2 Outre les principaux facteurs de risque mentionnés ci-dessus, une perte de poids rapide, une nutrition parentérale totale, une infection par le génotype 3 de l’hépatite C, la maladie de Wilson et certains médicaments (p.ex. le méthotrexate) peuvent également entraîner le développement d’une stéatose hépatique. En outre, il existe des gènes de risque tels que PNPLA3 («patatin-like phospholipase domain containing 3»), TM6SF2 («transmembrane 6 superfamily member 2»), HSD17B13 («17-beta hydroxysteroid dehydrogenase 13») ou MBOAT7 («membrane-bound O-acyltransferase domain-containing 7») qui influent sur le développement de la stéatose hépatique et de la fibrose chez certains patients présentant une NAFLD. La majorité des patients atteints de NAFLD présentent une stéatose hépatique pure et chez environ 15 à 30% de ces patients, elle peut évoluer vers une stéatohépatite non alcoolique (NASH). Une partie de ces patients développent une fibrose hépatique importante et jusqu’à 12% des patients atteints de NASH développent par la suite une cirrhose du foie.2 Ils sont donc exposés à un risque de décompensation hépatique et de développement d’un carcinome hépatocellulaire (CHC), ce qui augmente considérablement la morbidité et la mortalité de la maladie. Il est donc important d’identifier les patients à risque d’évolution progressive ou ceux qui présentent déjà une fibrose avancée en vue d’un traitement précoce et d’un dépistage du CHC. Cependant, la mortalité des patients atteints de NAFLD est principalement déterminée par les maladies cardiovasculaires, de sorte que le risque cardiovasculaire de ces patients devrait être vérifié chaque année (p.ex.) en utilisant le calculateur de risque de la Société suisse d’athérosclérose AGLA).
Dépistage et diagnostic
Le diagnostic présomptif de NAFLD est posé après exclusion d’autres causes d’hépatopathie (notamment les hépatites virales chroniques, les hépatopathies alcooliques ou auto-immunes) et en présence d’un profil de risque métabolique avec signes concomitants d’une stéatose à l’échographie. Les lignes directrices actuelles prévoient une biopsie du foie pour la détection de la stéatose, bien qu’en raison de son caractère invasif et du nombre élevé de patients dans la pratique clinique, la procédure ci-dessus se soit désormais imposée.3
L’étape suivante du diagnostic est importante et consiste à évaluer s’il y a déjà fibrose hépatique, laquelle détermine le pronostic du patient. Indépendamment de la présence d’une activité inflammatoire (NASH), les patients présentant une fibrose hépatique existante ont une mortalité à long terme globale et due à des causes hépatiques significativement plus élevée que les patients sans fibrose.4
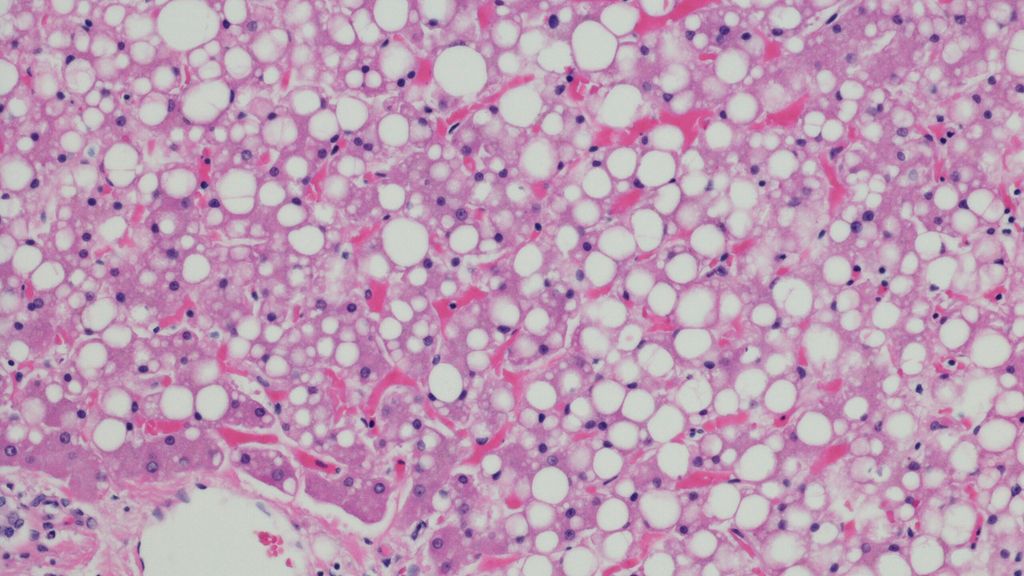
La biopsie du foie est la référence pour le diagnostic de la fibrose. D’un point de vue histologique, on distingue 5 stades de fibrose: de F0=pas de fibrose à F4=cirrhose. En outre, l’histologie est le seul moyen de différencier la présence d’une NAFLD et d’une NASH. Dans la NAFLD, plus de 5% des hépatocytes sont affectés par une stéatose.3 Dans la NASH, on trouve également des hépatocytes ballonnés et des infiltrats avec des cellules inflammatoires.5 Ces changements favorisent la formation d’une fibrose jusqu’à la cirrhose. Lorsque le problème est spécifique, la biopsie du foie est généralement effectuée par un spécialiste en gastroentérologie et en hépatologie. Elle peut être réalisée en cas de suspicion de fibrose de haut grade dans le cadre d’un diagnostic non invasif de la fibrose (voir ci-dessous) ou pour un diagnostic différentiel en cas d’une autre cause concomitante possible d’hépatopathie (voir ci-dessus), étant donné que ceci est pertinent pour le traitement et le suivi du patient.
En outre, il existe des moyens non invasifs d’évaluer la présence et l’étendue d’une fibrose hépatique. De quoi permettre aux confrères tels que les médecins de premier recours, les diabétologues et les cardiologues qui traitent fréquemment des patients dans les populations à risque pour une NAFLD d’effectuer un dépistage simple. En général, il est recommandé de débuter le dépistage de la NAFLD par une échographie chez tous les patients qui appartiennent à l’une des populations à risque (Fig. 1). Si une stéatose hépatique est suspectée, les transaminases et d’autres paramètres cliniques, tels que l’indice de masse corporelle, l’âge et la formule sanguine, doivent être déterminés afin d’évaluer le risque d’une maladie hépatique existante de grade supérieur. Il existe de nombreux scores basés sur les signes cliniques ou les taux sériques qui peuvent être utilisés principalement pour écarter une hépatopathie avancée. Parmi ceux-ci, le NAFLD-Fibrosis Score (NAFLD-FS) et le Fibrosis-4 Score (FIB-4) sont suffisamment validés pour être recommandés ici (Tab. 1).
Fig. 1: Algorithme de dépistage et de clarification d’une éventuelle NAFLD en fonction des résultats initiaux de l’échographie réalisée au cabinet du médecin de premier recours et basé sur le score de fibrose NAFLD (NAFLD-FS) et le score de fibrose 4 (FIB-4) (adapté d’après Angulo et al. et Sterling et al.)11, 12
Des valeurs de NAFLD-FS et FIB-4 aux stades de fibrose F0 à F2 excluent pratiquement toute hépatopathie sévère. Si ces scores permettent de suspecter une fibrose hépatique de plus haut grade (scores dans la zone grise ou aux stades de fibrose F3/F4), il convient de diriger le patient vers un gastroentérologue pour un diagnostic approfondi au moyen d’une élastographie transitoire (FibroScan®) ou d’une élastographie par ondes de cisaillement et, le cas échéant, d’une biopsie du foie (Fig. 1). En utilisant la vitesse de propagation d’une impulsion ultrasonore dans le foie, l’élastographie transitoire ou par ondes de cisaillement peut être utilisée pour estimer le grade de fibrose hépatique de manière non invasive et également pour diagnostiquer sa progression au cours du traitement. Les patients présentant une surcharge pondérale, un diabète de type 2 ou un prédiabète ainsi que des transaminases élevées doivent généralement être orientés vers un spécialiste en gastroentérologie et en hépatologie pour une échographie abdominale avec élastographie en raison de la prévalence élevée de la NAFLD dans cette population.3,6
Possibilités de traitement
Le traitement de la NAFLD ou de la NASH vise spécifiquement à empêcher une progression de la maladie et à réduire le risque cardiovasculaire des patients. De nombreux essais de traitement médicamenteux, y compris des essais de phase III, ont été et sont menés, mais aucune thérapie spécifique n’a encore été autorisée. Les substances à l’étude comprennent des approches thérapeutiques métaboliques, anti-inflammatoires et antifibrotiques. Les essais en cours portent également sur l’association de différentes préparations. Une prévention de la progression de la maladie semble plus facile à réaliser qu’une régression de la fibrose hépatique. Un traitement médicamenteux pourrait être particulièrement utile pour les patients à un stade avancé de la maladie, mais à ce jour, une guérison pharmacologique n’est pas encore possible.3
Le traitement de la NAFLD est donc axé sur une perte de poids accompagnée de la modification du mode de vie. Des études ont montré des effets significatifs sur le grade de stéatose hépatique et d’inflammation, et dans certains cas une régression de la fibrose. Cette approche thérapeutique a également un effet positif sur les comorbidités pertinentes, comme par exemple un diabète, un syndrome d’apnée du sommeil ou un risque cardiovasculaire accru. La Société allemande des maladies digestives et métaboliques et la Société européenne des maladies du foie recommandent une réduction du poids de 7–10%, qui doit être obtenue par des modifications du régime alimentaire et une augmentation de l’activité physique.3, 7 À cet égard, la chirurgie bariatrique est également citée comme traitement possible s’il existe une indication de chirurgie en raison de la présence d’une obésité.
Les comorbidités éventuelles doivent être traitées conformément aux recommandations actuelles des sociétés professionnelles respectives. Il n’existe actuellement aucune recommandation concernant l’utilisation d’agents hypolipidémiants, de statines, de biguanides, d’inhibiteurs du SGLT2 ou d’agonistes du GLP-1 chez les patients atteints de NAFLD sans comorbidités, mais des données démontrent un bénéfice en termes de régression de la stéatose et de l’inflammation chez les patients atteints de NAFLD.8, 9
Les patients atteints de stéatose hépatique et de syndrome métabolique présentent souvent des taux élevés de ferritine sérique en présence d’une saturation normale de la transferrine ou en l’absence d’une mutation génétique compatible avec l’hémochromatose. Cette hyperferritinémie est généralement le reflet d’une inflammation du foie. Chez ces patients, le bénéfice de la phlébotomie pour épuiser les réserves de fer est controversé et ne peut être recommandé en raison des données limitées.3
MAFLD – de quoi s’agit-il?
La distinction entre stéatose hépatique alcoolique et non alcoolique est souvent difficile. Par définition, la consommation d’alcool dans la NAFLD doit se situer dans des limites généralement sans danger, c’est-à-dire <20g/j chez les femmes et <30g/j chez les hommes.3 Comme indiqué plus haut, la NAFLD est donc un diagnostic d’exclusion.
Cependant, il est souvent impossible de délimiter le rôle de la consommation d’alcool ou d’une autre hépatopathie coexistante par rapport à une NAFLD, par exemple chez un patient souffrant d’obésité, de diabète et d’hépatite B chronique. C’est pourquoi on s’efforce d’introduire une nouvelle terminologie mettant l’accent sur l’étiologie avec le terme de stéatose hépatique associée au métabolisme (MAFLD). Cette définition prend en compte les maladies métaboliques concomitantes et la présence d’autres maladies du foie n’est pas une contre-indication au diagnostic.10 La MAFLD peut être diagnostiquée en présence d’une stéatose hépatique (imagerie ou biopsie) avec en plus une obésité (IMC ≥25kg/m2) ou un diabète de type 2. Chez les personnes de poids normal, deux facteurs du syndrome métabolique doivent en outre être présents. Cette définition est partiellement appliquée dans les centres mais n’a pas encore été établie dans les lignes directrices existantes des sociétés professionnelles et dans la pratique clinique.
Littérature:
1 Arshad T et al.: Epidemiology of non-alcoholic fatty liver disease in North America. Curr Pharm Des 2020; 26: 993-70 2 Vieira Barbosa J, Lai M: Nonalcoholic fatty liver disease screening in type 2 diabetes mellitus patients in the primary care setting. Hepatol Commun 2021; 5: 158-67 3 European Association for the Study of the Liver, European Association for the Study of Diabetes, and European Association for the Study of Obesity: EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J Hepatol 2016; 64: 1388-402 4 Angulo P et al.: Liver fibrosis, but no other histologic features, is associated with long-term outcomes of patients with nonalcoholic fatty liver disease. Gastroenterology 2015; 149: 389-97.e10 5 Kleiner DE et al.: Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005; 41: 1313-21 6 American Diabetes Association: 4. Comprehensive Medical evaluation and assessment of comorbidities: standards of medical care in diabetes - 2021. Diabetes Care 2021; 44: S40-52 7 Roeb E et al.: [S2k Guideline non-alcoholic fatty liver disease]. Z Gastroenterol 2015; 53: 668-723 8 Lai LL et al.: Empagliflozin for the treatment of nonalcoholic steatohepatitis in patients with type 2 diabetes mellitus. Dig Dis Sci 2020; 65: 623-31 9 Newsome PN et al.: A placebo-controlled trial of subcutaneous semaglutide in nonalcoholic steatohepatitis. N Engl J Med 2021; 384: 1113-24 10 Eslam M et al.: A consensus-driven proposed nomenclature for metabolic associated fatty liver disease. Gastroenterology 2020; 158: 1999-2014.e1 11 Angulo P et al.: The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007; 45: 846-54 12 Sterling RK et al.: Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection. Hepatology 2006; 43: 1317-25
Das könnte Sie auch interessieren:
Tachycardie supraventriculaire
Les tachycardies paroxystiques supraventriculaires régulières apparaissent généralement chez des patients sans cardiopathie structurelle. Dans cet article, nous discutons de l’importance ...
Risques du tabagisme pour la santé – sevrage tabagique
«Un fumeur avide qui lit et relit l’importance des risques du tabagisme pour sa santé cesse dans la plupart des cas ... de lire», avait déclaré Winston Churchill. «Le tabac est le seul ...
L’élastographie hépatique
En hépatologie, l’élastographie hépatique est l’instrument central de la prise en charge des patient·es atteint·es d’une maladie hépatique chronique. Les nouvelles conclusions permettent ...