Isthmozele und Fertilität
Autorinnen:
Dr.med. Angela Vidal
Dr.med. Marietta Gulz
Universitätsklinik für Frauenheilkunde
Inselspital Bern
E-Mail: angela.vidal@insel.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine Isthmozele, auch als «Nischenbildung» bekannt, ist ein Defekt in der Gebärmutterwand, der nach einem Kaiserschnitt entstehen kann. Die Bildung einer Isthomzele kann die Fertilität einer Frau auf verschiedene Weise beeinflussen, indem sie die Funktion der Gebärmutter und die Prozesse, die für eine erfolgreiche Schwangerschaft notwendig sind, stört. Die richtige Diagnose und Therapie sind daher entscheidend.
Keypoints
-
Die Isthmozele ist eine häufige Folge nach einem Kaiserschnitt.
-
Isthmozelen führen häufig zur Infertilität und haben einen negativen Einfluss auf die Ergebnisse im Rahmen von ART.
-
Verschiedene Mechanismen sind an der Isthmozelen-assoziierten Infertilität beteiligt: Endometriose, Flüssigkeitskollektion in der Isthmozele und chronische Endometritis sind zu berücksichtigen.
-
Die Therapie der Isthmozelen-assoziierten Infertilität stellt aufgrund der mangelnden Evidenz eine grosse Herausforderung dar und muss auf jede Patientin individuell abgestimmt werden. Zukünftige qualitativ hochwertige Studien sind notwendig.
Die Kaiserschnittrate hat in den letzten Jahrzehnten kontinuierlich zugenommen. Während die Weltgesundheitsorganisation (WHO) die optimale Kaiserschnittrate auf 15% schätzt,1 liegt derzeit der Anteil der Kaiserschnittgeburten in der Schweiz bei 33,0%.2 Aufgrund der steigenden Zahlen besteht ein zunehmendes Interesse an der potenziellen Langzeitmorbidität von Kaiserschnittnarben.3,4
Die Isthmozele ist ein komplexes gynäkologisches Krankheitsbild. Die Ursache dieser anatomischen Anomalie kann eine unzureichende oder unvollständige Heilung der Gebärmutterwand nach einem Kaiserschnitt sein. Eine Isthmozele kann auch nach anderen chirurgischen Eingriffen an der Gebärmutter auftreten, z.B. nach einer Myomektomie.5
Führt jeder Kaiserschnitt zu einer Beeinträchtigung der Fertilität?
Mehrere Studien weisen darauf hin, dass sich Kaiserschnitte negativ auf die Fruchtbarkeit und die nachfolgende Lebendgeburtrate (9–15%) auswirken.6–8 Dabei spielt das Vorliegen einer Isthmozele eine grosse Rolle.
Die Wahrscheinlichkeit des Auftretens einer Isthmozele nach einem Kaiserschnitt liegt bei 40% der Patientinnen mit anfänglicher Zervixdilatation und bei 20% der Patientinnen, die sich einem Kaiserschnitt bei fortgeschrittener Dilatation unterziehen.9,10
Liegt eine Isthmozele vor, so hat diese folgende Konsequenzen für eine IVF-Therapie: Im Jahr 2023 untersuchten Yao W. et al. in einer retrospektiven Kohortenstudie die Beziehung zwischen Kaiserschnittnarbendefekt und den Ergebnissen nach assistierten reproduktiven Technologien (ART). Die Studie umfasste 2231 Frauen, die sich insgesamt 2515 IVF-Zyklen unterzogen.
Frauen mit einer Isthmozele wiesen im Vergleich zu Frauen ohne Isthmozele eine reduzierte Rate an
-
Lebendgeburten (18,99% vs. 31,51%, aOR: 0,51, 95% CI: 0,34–0,77),
-
positiven Schwangerschaftstests (34,08% vs. 46,40%, aOR: 0,61, 95% CI: 0,43–0,87),
-
klinischen Schwangerschaften (29,05% vs. 42,25%, aOR: 0,57, 95% CI: 0,39–0,82) und
-
Implantationen (25,87% vs. 36,95%, aOR: 0,53, 95% CI: 0,38–0,76) auf.
Zudem war in der Gruppe mit Isthmozele die Fehlgeburtenrate mit 7,28% bis 18,22% höher, jedoch statistisch nicht signifikant.
Dieses Jahr führten Vitagliano et al. eine systematische Übersicht und Metaanalyse über die Auswirkungen einer Isthmozele bei ART durch.11 Der primäre Endpunkt war die Lebendgeburtenrate. Insgesamt wurden 10873 Zyklen des Embryotransfers berücksichtigt. Die Studie führte zu folgenden Ergebnissen:
-
Frauen mit einer Isthmozele hatten eine niedrigere Lebendgeburtenrate als Frauen nach Sectio ohne Isthmozele (aOR: 0,62, 95% CI: 0,53–0,72) oder Frauen nach einer vaginalen Geburt (aOR: 0,55, 95% CI: 0,42–0,71).
-
Die Lebendgeburtenrate war nach vorausgegangenem Kaiserschnitt ohne Isthmozele und nach vaginaler Entbindung ähnlich (aOR: 0,74, 95% CI: 0,47–1,15).
-
Beim Vorliegen einer Isthmozele und intrakavitärer Flüssigkeit (ICF) lag eine geringere Lebendgeburtenrate vor (uOR: 0,36, 95% CI: 0,18–0,75) als bei Isthmozele ohne ICF.
Zusammenfassend lässt sich sagen, dass weniger der Kaiserschnitt, sondern eher das Vorliegen einer Isthmozele als Folge des Kaiserschnitts zu einer Beeinträchtigung der Fertilität führt.
Welche Mechanismen stecken hinter der Isthmozelen-assoziierten Infertilität?
In der Literatur wird das Risiko für das Auftreten von Infertilität bei Frauen mit einer Isthmozele mit 4 bis 19% angegeben.9,12,13
Der genaue dazu führende Mechanismusist jedoch noch nicht ganz geklärt. Vermutet werden entzündliche Prozesse, die unter anderem durch eine Flüssigkeitskollektion (Blut, Mukus) in der Isthmozele verursacht werden und mit einer gestörten Kontraktilität des Uterus einhergehen können.
Die 3 wichtigsten Mechanismen
1. Flüssigkeitskollektion in der Isthmozele
Florio et al. postulieren, dass fibrotisches Gewebe im verbliebenen Myometrium die Kontraktilität der Uterusmuskulatur beeinträchtigt, was zur Blut- oder Mukusansammlung und zu Symptomen wie postmenstruellem Spotting führt.14 Bestärkt wird diese Theorie durch eine Studie von Donnez et al., in der die Isthmozele eine geringere Muskeldichte aufwies als das gesunde Myometrium.15 Morris et al. vermuten, dass auch eine mögliche Adenomyose/Endometriose in der Isthmozele zu einer lokalen Produktion von Blut und folglich zur Flüssigkeitskollektion führen könnte.16 Persistierendes Menstrualblut in der Isthmozele beeinträchtigt die Qualität des Zervixschleims und der Spermien. Einerseits kann der Spermientransport gestört, andererseits die Embryoimplantation aufgrund eines chronisch-entzündlichen Milieus und aufgrund von Eiseneinlagerungen erschwert werden.
2. Chronische Endometritis
Chronische Endometritis (CE) tritt bei Frauen mit Isthmozele und Unfruchtbarkeit häufiger auf.
Nobuta et al. stellten fest, dass CE, die oft symptomlos verläuft, bis zu 40% der unfruchtbaren Patientinnen betrifft und zu wiederholtem Implantationsversagen und wiederkehrenden Fehlgeburten führt. Eine bestehende CE macht eine erfolgreiche Konzeption auch beim Transfer hochwertiger Embryonen im Rahmen von ART unwahrscheinlich.17
Die Inzidenz von CE bei Patientinnen mit Isthmozelen-assoziierter Infertilität ist signifikant höher im Vergleich zu infertilen Frauen ohne Isthmozele (66% vs. 46%; p=0,03).17
Zudem zeigen Frauen mit Isthmozelen-assoziierter Infertilität höhere Konzentrationen an entzündlichen Zytokinen wie TNF-alpha und IL-1beta sowohl in der Gebärmutterhöhle als auch in der Beckenflüssigkeit im Vergleich zu unfruchtbaren Frauen ohne Isthmozele. Bi et al. führten eine Studie mit 60 unfruchtbaren Patientinnen durch und stellten fest, dass eine Isthmozele mit teilweise blockierten Eileitern, intraabdominalen Verwachsungen und nachfolgender Unfruchtbarkeit verbunden war.18
3. Koexistenz von Endometriose
Endometriose tritt häufig zusammen mit einer Isthmozele auf. Endometriose kann ebenfalls zu Infertilität führen, bedingt durch chronische Entzündung und anatomische Veränderungen durch Verwachsungen. In einer retrospektiven Studie von Gulz et al. wiesen 27% der Patientinnen mit Isthmozele, die sich einer laparoskopischen Resektion unterzogen, eine Endometriose auf.19 Nobuta et al. fanden eine höhere Inzidenz von Endometriose bei Patientinnen mit Isthmozelen-assoziierter Infertilität (70%), wobei die meisten Fälle leichtgradig waren.17
Endometriose in der Isthmozele, gekennzeichnet durch das Vorhandensein von Endometriumdrüsen oder Stromagewebe innerhalb der Narbe, wurden in zwei anderen Studien bei 21 bis 27% der Fälle festgestellt.15,19,20
Welche Behandlungsmöglichkeiten gibt es für die Isthmozelen-assoziierte Infertilität?
Die Behandlung der Isthmozele bei Frauen mit unerfülltem Kinderwunsch ist vielfältig und muss individuell an jede Patientin angepasst werden. Derzeit gibt es keine allgemeinen Guidelines zur Behandlung der Isthmozele bei Infertilität. Denn nur wenige Studien haben sich mit diesem Thema befasst und die Evidenz ist von geringer Qualität.21 Im folgenden Abschnitt werden die verschiedenen Behandlungsmöglichkeiten kurz angeschnitten.
Vor der Wahl eines Therapieverfahrens sollten die sonografisch gemessene Restdicke des Myometriums (RMT; Abb. 1a)), das Vorliegen anderer Pathologien (Endometriose, Adhäsionen, verschlossene Eileiter, pathologisches Spermiogramm des Partners etc.) und die finanziellen Möglichkeiten der Patientin berücksichtigt werden
Bei einer RMT ≥3mm kann ART in Erwägung gezogen werden. Jedoch sollten die Frauen darüber informiert werden, dass die Ergebnisse nach dieser deutlich schlechter ausfallen und Isthmozelen mit Schwangerschaftskomplikationen wie Sectionarbenschwangerschaft, Plazentationsstörungen, Placenta praevia und Uterusruptur assoziiert sind.
Wenn eine chirurgische Therapie indiziert wird, sollte die Entscheidung zwischen einer hysteroskopischen Resektion und einer laparoskopischen oder vaginalen Reparatur von Faktoren wie der RMT und den chirurgischen Fertigkeiten abhängen.22
Als am wenigsten invasive Operationstechnik eignet sich die hysteroskopische Resektion, sofern die RMT ≥3mm ist. Hierbei werden die obere und untere Kante der Isthmozele reseziert, sodass eine möglichst ebene Fläche entsteht. Gleichzeitig werden atypische Gefässe in der Isthmozele koaguliert.23
Bei einer RMT <3mm sollte die laparoskopische oder vaginale Repairtechnik durchgeführt werden. Hierbei wird der Defekt komplett exzidiert und das Myometrium durch Nähte neu adaptiert.
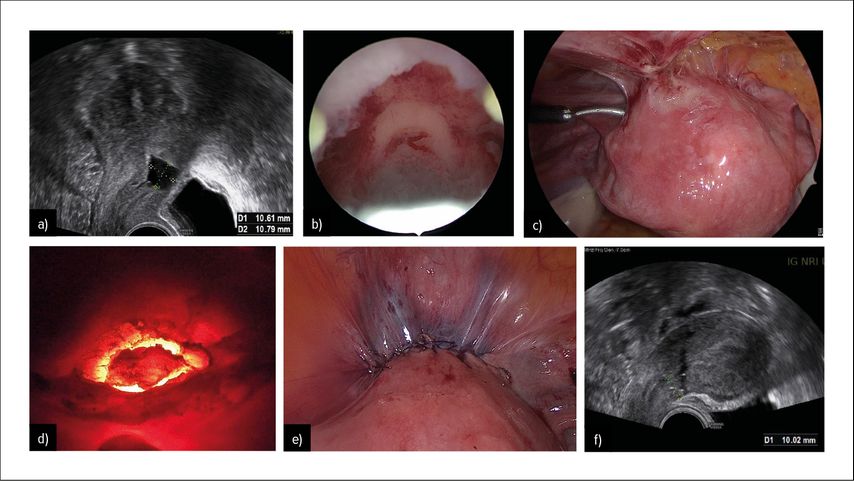
Beide Methoden haben gleichwertig gute Ergebnisse in Bezug auf die postoperativ gemessene RMT gezeigt. Die Laparoskopie bietet den zusätzlichen Vorteil, dass gleichzeitig andere mögliche Ursachen für Infertilität diagnostiziert und behandelt werden können.24 Da häufig eine koexistente Endometriose vorliegt, kann diese im selben Eingriff reseziert werden.19 In einigen Fällen wird die Laparoskopie mit einer Hysteroskopie zur besseren Visualisierung der Isthmozele kombiniert. Diese Technik wurde erstmals durch Mueller et al. beschrieben und Isthmozelenkorrektur in «Rendez-vous-Technik» genannt.25 Ein Beispiel zu dieser Technik wird in Abbildung 1 dargestellt.
Abb. 1: Prä-, intra- und postoperative Bilder einer 36-jährigen Patientin mit sekundärer Sterilität zwei Jahre nach sekundärer Sectio caesarea. Die Patientin unterzog sich im Verlauf einer Isthmozelenkorrektur in Rendez-vous-Technik: a) Präoperativer transvaginaler Ultraschall: grosse Isthmozele ohne messbares Restmyometrium. b) Hysteroskopie mit Darstellen der Isthmozele. c) Laparoskopisch zeigt sich die Uterusvorderwand zur Abdominalwand adhärent. d) Laparoskopische Sicht auf das untere Uterinsegment. Nach Visualisierung der Isthmozele durch simultane Hysteroskopie (sog. «Halloween sign») Exzision der Isthmozele mit der monopolaren Nadel. e) Verschluss der Uterotomie mit PDS 2-0 Einzelknopfnähten extrakorporal geknüpft, dann Verschluss des Peritoneums fortlaufend mit V-Loc 3-0. f) Transvaginaler Ultraschall 3 Monate postoperativ: keine Isthmozele mehr sichtbar, die Restmoymetriumdicke beträgt 10mm
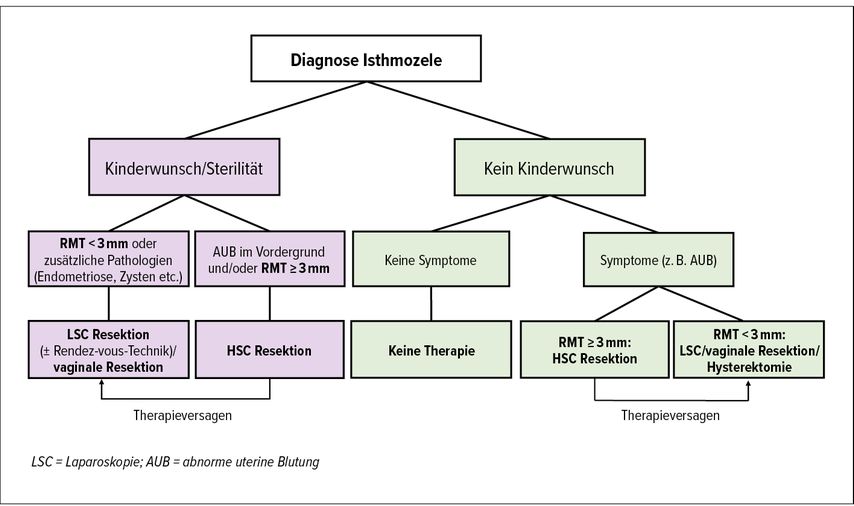
Ein allgemeiner möglicher Algorithmus zur Behandlung der Isthmozele ist in Abbildung 2 abgebildet.
Abb. 2: Vorschlag eines Algorithmus zur Behandlung der Isthmozele (modifiziert nach Vitale SG et al. 2020 und Harjee R et al. 2021)21, 26
Zum postoperativen Management gibt es auch keine allgemeinen Richtlinien. Postoperativ macht es Sinn, bei Methoden der Isthmozelenexzision wie bei der Myomektomie mindestens sechs Monate bis zum erneuten Konzeptionsversuch zuzuwarten, gute Wundheilung vorausgesetzt. Bezüglich Schwangerschaftsüberwachung und Geburtsmodus gibt es derzeit noch keine offiziellen Leitlinien. In den vergangenen Studien haben die Frauen nach erfolgter Isthmozelenexzision mehrheitlich per Sectio entbunden. Der Geburtsmodus muss jedoch mit jeder Patientin individuell besprochen werden und unter anderem die RMT berücksichtigt werden.
Literatur:
1 World Health Organization Human Reproduction Programme: WHO statement on caesarean section rates. Reprod Health Matters 2015; 23(45): 149-50 2 Bundesamt für Statistik und Sektionen Gesundheitsversorgung (BFS) Reproduktive Gesundheit. BFS-Nummer 238-2201. Verfügbar unter: https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/reproduktive.html ; zuletzt aufgerufen am 21.8.2024 3 Clark EAS, Silver RM: Long-term maternal morbidity associated with repeat cesarean delivery. Am J Obstet Gynecol 2011; 205(6 Suppl): S2-10 4 Diaz SD et al.: Uterine rupture and dehiscence: ten-year review and case-control study. South Med J 2002; 95(4): 431-5 5 Baldini GM et al.: Isthmocele and infertility. J Clin Med 2024; 13(8): 2192 6 Ohashi M et al.: Influence of cesarean section on postpartum fertility and dysmenorrhea: a retrospective cohort study in Japan. Womens Health Rep (New Rochelle) 2024; 5(1): 22-9 7 Vissers J et al.: Reduced pregnancy and live birth rates after in vitro fertilization in women with previous caesarean section: a retrospective cohort study. Hum Reprod 2020; 35(3): 595-604 8 Gurol-Urganci I et al.: A population-based cohort study of the effect of caesarean section on subsequent fertility. Hum Reprod 2014; 29(6): 1320-6 9 Kamel R et al.: Position and integrity of uterine scar are determined by degree of cervical dilatation at time of cesarean section. Ultrasound Obstet Gynecol 2021; 57(3): 466-70 10 Bij de Vaate AJM et al.: Prevalence, potential risk factors for development and symptoms related to the presence of uterine niches following cesarean section: systematic review. Ultrasound Obstet Gynecol 2014; 43(4): 372-82 11 Vitagliano A et al.: Isthmocele, not cesarean section per se, reduces in vitro fertilization success: a systematic review and meta-analysis of over 10,000 embryo transfer cycles. Fertil Steril 2024; 121(2): 299-313 12 Morris JM et al.: Mind the gap—isthmoceles and infertility. Fertil Steril 2023; 119(2): 326-7 13 CORONIS Collaborative Group et al.: Caesarean section surgical techniques: 3 year follow-up of the CORONIS fractional, factorial, unmasked, randomised controlled trial. Lancet 2016; 388(10039): 62-72 14 Florio P et al.: Hysteroscopic treatment of the cesarean-induced isthmocele in restoring infertility. Curr Opin Obstet Gynecol 2012; 24(3): 180-6 15 Donnez O et al.: Gynecological and obstetrical outcomes after laparoscopic repair of a cesarean scar defect in a series of 38 women. Fertil Steril 2017; 107(1): 289-296.e2 16 Morris H: Surgical pathology of the lower uterine segment caesarean section scar: is the scar a source of clinical symptoms? Int J Gynecol Pathol 1995; 14(1): 16-20 17 Nobuta Y et al.: Decreased fertility in women with cesarean scar syndrome is associated with chronic inflammation in the uterine cavity. Tohoku J Exp Med 2022; 258(3): 237-42 18 Bi B et al.: Analysis on clinical association of uterine scar diverticulum with subsequent infertility in patients underwent cesarean section. Medicine 2021; 100(41): e27531 19 Gulz M et al.: Endometriosis and isthmocele: common or rare? J Clin Med 2022; 11(5): 1158 20 Tanimura S et al.: New diagnostic criteria and operative strategy for cesarean scar syndrome: endoscopic repair for secondary infertility caused by cesarean scar defect. J Obstet Gynaecol Res 2015; 41(9): 1363-9 21 Vitale SG et al.: From hysteroscopy to laparoendoscopic surgery: what is the best surgical approach for symptomatic isthmocele? A systematic review and meta-analysis. Arch Gynecol Obstet 2020; 301(1): 33-52 22 Chang Y et al.: Resectoscopic treatment combined with sonohysterographic evaluation of women with postmenstrual bleeding as a result of previous cesarean delivery scar defects. Am J Obstet Gynecol 2009; 200(4): 370.e1-4 23 Raimondo G et al.: Hysteroscopic treatment of symptomatic cesarean-induced isthmocele: a prospective study. J Minim Invasive Gynecol 2015; 22(2): 297-301 24 Donnez O: Cesarean scar defects: management of an iatrogenic pathology whose prevalence has dramatically increased. Fertil Steril 2020; 113(4): 704-16 25 Nirgianakis K et al.: The rendez-vous technique for treatment of caesarean scar defects: a novel combined endoscopic approach. Surg Endosc 2016; 30(2): 770-1 26 Harjee R et al.: Reproductive outcomes following surgical management for isthmoceles: a systematic review. J Minim Invasive Gynecol 2021; 28(7): 1291-1302.e2
Das könnte Sie auch interessieren:
HPV-Selbsttestung in Westafrika
In Ländern mit niedrigem und mittlerem Einkommen (LMIC) stellt das Zervixkarzinom eine der häufigsten krebsbedingten Todesursachen bei Frauen dar, weshalb die WHO drei konkrete Cut-offs ...
Sport und Krebserkrankungen
In den letzten Jahzehnten hat sich insgesamt ein Paradigmenwechsel in der Medizin vollzogen – von der körperlichen Schonung hin zur Aktivität und frühen Mobilisierung im Rahmen von ...
Hormonelle Gesundheit nach der Menopause
Frauen verbringen heute rund ein Drittel ihres Lebens in der Postmenopause. Diese Lebensphase ist mit einer hohen Symptomlast und langfristigen gesundheitlichen Risiken verbunden, was ...