Akute Herzinsuffizienz: Appell des Herzens für bewährte Therapien der chronischen Herzinsuffizienz
Autorinnen:
Priv.-Doz. Dipl.-Ing. Dr. Noemi Pavo, PhD
Dr. Suriya Prausmüller
Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
E-Mail: noemi.pavo@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das Krankheitsbild der akuten Herzinsuffizienz (HI) ist vielfältig. Eine einheitliche Definition gibt es nicht, daher gestaltet sich das Design von Studien schwierig. Nach rascher klinischer Beurteilung der Vitalparameter und auslösender Faktoren wird der Patient stabilisiert, mit dem Hauptziel einer Euvolämie. Die Therapie der chronischen HI sollte in dieser vulnerablen Patientengruppe nicht nur weitergeführt, sondern noch im Spital mit den neuen Substanzklassen optimiert werden.
Keypoints
-
Die akute Herzinsuffizienz (HI)geht mit einer inakzeptabel hohen Mortalitäts- und Rehospitalisierungsrate einher.
-
Bei der größten Gruppe der Patienten mit akuter HI stellt die Hospitalisation eine Verschlechterung der vorbekannten Erkrankung dar.
-
In dieser vulnerablen Patientengruppe kann man mit einer raschen Intervention im Sinne der Therapieoptimierung mit bekannten wirksamen Therapien der chronischen HI große Effekte erzielen.
-
Neue Studien weisen auf die Sicherheit von ARNI, SGLT2-I und i.v. Eisen in dieser Patientengruppe hin, sodass eine Therapie nach Stabilisierung bereits im Spital begonnen werden sollte.
Akute HI: ein ungelöstes Problem
Derzeit gibt es keine allgemeingültige Definition der akuten HI. Selbst die kürzlich veröffentlichte universelle Definition der HI verzichtet auf eine genaue Begriffsbestimmung.1 Die akute HI ist durch eine schnell einsetzende HI (<48 Stunden) oder sich verschlechternde Zeichen und Symptome einer HI mit der Notwendigkeit einer raschen Behandlung gekennzeichnet. In Österreich gibt es laut Statistik Austria jährlich rund 24000 Hospitalisierungen aufgrund von HI, wobei vermutlich ein deutliches Underreporting vorliegt. Die HI (ICD-10: I50) ist in Österreich die häufigste Hauptdiagnose bei Krankenhauseinweisungen bei über 65-Jährigen und hat aufgrund der demografischen Entwicklung eine steigende Tendenz: In den vergangenen drei Dekaden hat sich die Entlassungsdiagnose „Herzinsuffizienz“ verdreifacht.
Die akute HI kann als De-novo-Erkrankung auftreten, häufiger tritt sie jedoch als akute Dekompensation einer bekannten chronischen HI auf. Verantwortlich für eine akute HI/kardiale Dekompensation können direkt kardiale Ursachen wie Herzrhythmusstörungen oder eine verminderte Durchblutung des Herzmuskels, aber auch extrakardiale Ursachen wie Infektionen, Aggravierung von Komorbiditäten wie der chronischen Niereninsuffizienz oder eine hypertensive Entgleisung, aber auch mangelnde Therapieadhärenz sein. Die Analyse des großen europäischen Langzeitregisters für HI, ESC-HF-LT, zeigt, dass die meisten Patienten eine vorbekannte HI (60%) haben, während ca. 14% aufgrund einer kardialen Verschlechterung im Rahmen eines akuten Koronarsyndroms, also Herzinfarktes, behandelt werden müssen (Abb. 1).2 Andere klinische Phänotypen wie kardiogener Schock oder Rechtsherzinsuffizienz stellen besonders schwere Krankheitsbilder dar, bewegen sich aber jeweils nur im Bereich von 2–3% aller Aufnahmen. Dass die größte Gruppe die dekompensierte chronische HI darstellt, ist nicht verwunderlich, da HI eine häufige Erkrankung mit steigender Prävalenz im Alter ist, wobei über 10% der über 65-Jährigen betroffen sind und man in Österreich von rund 300000 Fällen ausgeht.
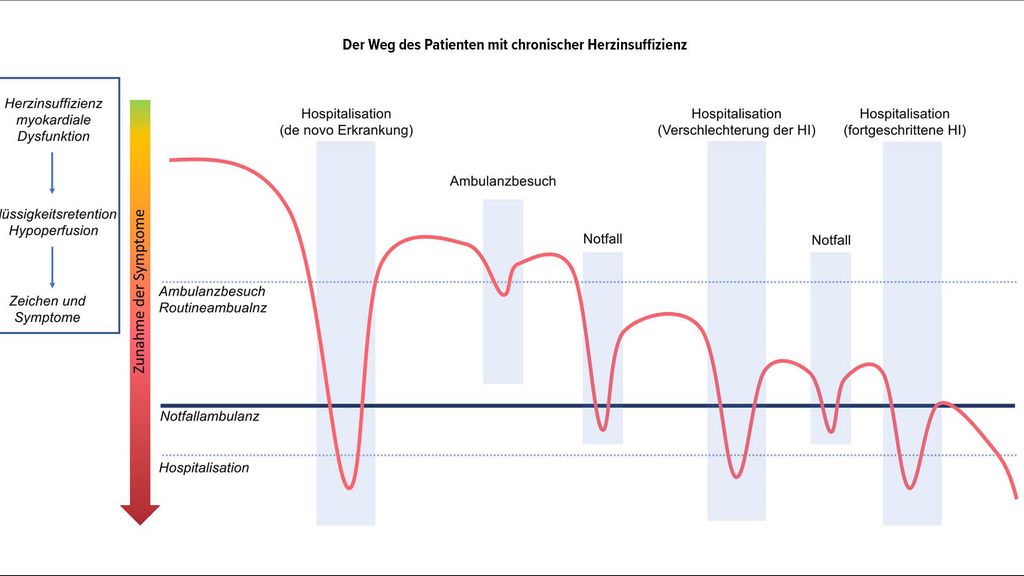
Der Krankheitsverlauf ist trotz optimaler Therapie durch eine kontinuierliche Abnahme der kardialen Funktion mit Phasen akuter Verschlechterung gekennzeichnet (Abb. 2). Die Prognose der Betroffenen ist schlecht. Eine Hospitalisierung aufgrund einer sich verschlechternden HI bedeutet für den Patienten eine Änderung seines Erkrankungswegs in die Richtung eines deutlich höheren Risikos für eine schlechtere Lebensqualität und vermehrte Hospitalisierungen und eines erhöhten Mortalitätsrisikos. Innerhalb des ersten Jahres muss fast jeder zweite Patient mit einer Rehospitalisierung rechnen und jeder vierte Patient verstirbt in dieser Zeit. Der Trend der letzten 20 Jahre für Europa ist ernüchternd, denn diese Zahlen sind seit 2004 unverändert und damit inakzeptabel hoch geblieben.3
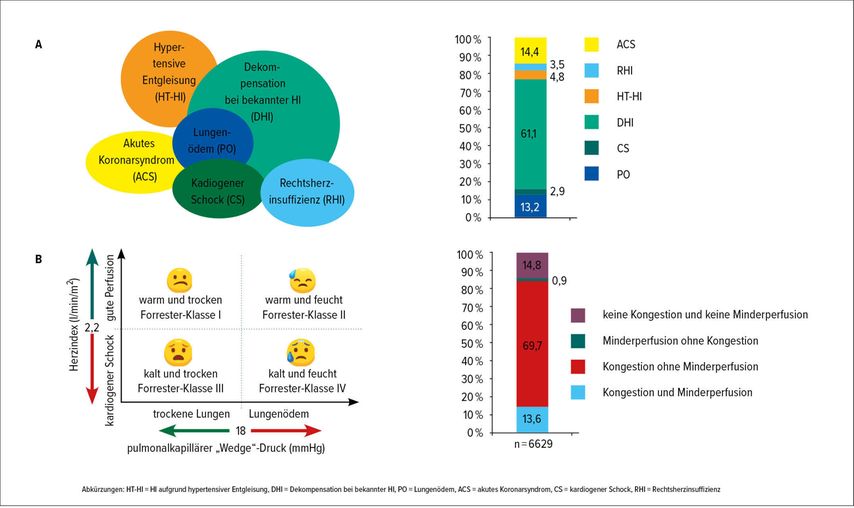
Abb. 2: Nach „onset“ der Erkrankung kommt es zu einem kontinuierlichen myokardialen Funktionsverlust, der durch eine Dysbalance zu einer Flüssigkeitsretention oder Hypoperfusion mit entsprechenden Zeichen und Symptomen führt. Je nach Schweregrad dieser Events muss die versorgende Ambulanz oder die Notfallambulanz besucht werden bzw. wird eine Hospitalisation notwendig. Wird eine Notfallbehandlung oder eine Spitalsaufnahme in Anspruch genommen, ist das mit einer deutlich schlechteren Prognose assoziiert. Spätestens dann muss die Herzinsuffizienz-spezifische Medikation optimiert werden
Stabilisierung der akuten HI
Die Behandlung der akuten HI gilt als weit weniger evidenzbasiert als die der chronischen HI, nicht zuletzt deshalb, weil sich das Durchführen von Studien in diesem Notfallsetting schwieriger gestaltet. So hat sich der Behandlungsalgorithmus der akuten HI in den letzten 40–50 Jahren kaum geändert. Der zum Teil negative Ausgang groß angelegter Studien in der Vergangenheit liegt möglicherweise an der extremen Heterogenität der untersuchten Studienkollektive.
Die Therapie unterscheidet sich nach klinischer Präsentation der Erkrankung, wobei einerseits die Perfusion (Herzminutenvolumen/periphere Widerstände), andererseits das Vorhandensein einer Flüssigkeitshomöostase (Kongestion/Exsikkose) beurteilt wird (kalt/warm und trocken/feucht). Diese Klassifikation nach Forrester ist stark mit der Prognose assoziiert und wird von den gültigen internationalen Leitlinien empfohlen, da sie zur Steuerung der Therapie in der Initialphase hilfreich sein kann.4 Wesentlich sind zudem die Identifikation und die spezifische Behandlung auslösender oder perpetuierender Faktoren, ohne die der Patient nicht aus der kritischen Situation herauskommt. Die häufigsten Probleme sind Hypoxie, Hypotonie, Tachy-/Bradyarrhythmie, akutes Koronarsyndrom, akute mechanische Ursachen oder schwere Klappenerkrankungen.
Bei hämodynamischer Instabilität mit unzureichender Organperfusion („low output“, „kalter Typ“) steht die Stabilisierung des Patienten im Vordergrund. Zu den am häufigsten eingesetzten Therapien der akuten HI gehören die Gabe von Sauerstoff, Diuretika, Analgetika, Vasodilatatoren, Inotropika und Vasopressoren. Sauerstoff sollte bei Patienten mit einer O2-Sättigung unter 90% verabreicht werden (Empfehlungsgrad I, Evidenz C), da dieser Zustand mit einer erhöhten Mortalität assoziiert ist. Die Gabe von Opiaten kann bei Patienten mit schwerer Dyspnoe zur Linderung von Atemnot und Angstzuständen erfolgen (Empfehlungsgrad IIa, Evidenz C). Der Einsatz von vasodilatierenden Substanzen sollte bei Patienten mit systolischen Blutdruckwerten >90mmHg (ohne symptomatische Hypotonie) zur symptomatischen Therapie erwogen werden (Empfehlungsgrad IIa, Evidenz B). Letztendlich stellt der kardiogene Schock das schwerwiegendste klinische Zustandsbild der akuten HI dar. Inotropika und Vasopressoren (Dobutamin, Dopamin, Levosimendan, Phosphodiesterase-III-Hemmer, Noradrenalin) sind ein wichtiger Bestandteil der Therapie, um den Kreislauf zu stabilisieren und Endorganschäden zu vermeiden (Empfehlungsgrad IIa, Evidenz C). Diese Therapien zeigen im klinischen Setting eine deutlich wahrnehmbare Wirkung, die Anwendung vasoaktiver Medikamente kann jedoch mit beträchtlichen Nebenwirkungen, insbesondere Hypertonie, Herzrhythmusstörungen und möglicherweise einer erhöhten Langzeitsterblichkeit, einhergehen.5 Diese Therapien sollten (mangels Alternativen) frühzeitig bei Zeichen von Minderperfusion sowie symptomatischer Hypotonie angewandt werden (Empfehlungsgrad III, Evidenz A), deren Notwendigkeit ist jedoch engmaschig zu reevaluieren und auf das Minimum zu limitieren.
Der Großteil der Patienten mit akuter HI präsentiert sich mit erhaltener Perfusion, ausreichendem Blutdruck, Stauungszeichen sowie Gewichtszunahme („warm-feuchter Typ“) und profitiert sehr gut von einer diuretischen Therapie. Diuretika sind in der Behandlung der akuten HI weit verbreitet und nehmen vor allem in der symptomatischen Therapie einen wichtigen Stellenwert ein (Empfehlungsgrad I, Evidenz C). Insgesamt gilt als Hauptziel der Therapie das Erreichen der Euvolämie. Patienten, die mit residualen Stauungszeichen entlassen werden, haben ein höheres Risiko für eine erneute Rehospitalisierung und Tod.6 Schleifendiuretika wie Furosemid sind Mittel der ersten Wahl und können bei einer unzureichenden diuretischen Antwort mit Thiaziden oder Mineralokortikoidrezeptorantagonisten (MRA) kombiniert werden. In ausgewählten Fällen kann die Ultrafiltration zum Einsatz kommen.7 Wichtig hierbei ist, dass es während der Rekompensation zu einer Verschlechterung der Nierenfunktion kommen kann, die jedoch immer zusammen mit dem Erfolg der Rekompensation beurteilt werden muss und in Kauf genommen werden kann („pseudo worsening of renal function).8
Besonders im Fall einer Dekompensation bei bekannter HI gelten weiterhin sämtliche Behandlungsrichtlinien der chronischen HI. Für die HFrEF gilt, dass die bereits etablierten medikamentösen Therapien nach Möglichkeit weitergeführt werden sollten. Sofern keine symptomatische Hypotonie oder ausgeprägte Hyperkaliämie besteht, sollte auch hierbei eine Verschlechterung der Nierenfunktion bis zu einem Kreatinin-Anstieg von 30% nicht automatisch zu einer Unterbrechung oder Reduktion der Therapie führen. Erst ab >30% und >50% sollte eine transiente Therapiereduktion erwogen bzw. eine kurzfristige Unterbrechung durchgeführt werden.9 Für die HFpEF gelten diese Empfehlungen aufgrund mangelnder Evidenz für den Benefit der RAAS-Blocker nicht.

Abb. 1: Klinische Phänotypen der akuten Herzinsuffizienz: Verteilung der klinischen Phänotypen der akuten Herzinsuffizienz basierend auf den Daten von 6629 Fällen aus dem ESC-HF-LT-Register nach (A) Ätiologie und (B) Hämodynamik. Der weitaus größte Teil der Patienten hat eine vorbekannte chronische Herzinsuffizienz und zeigt Zeichen der Flüssigkeitsretention bei normaler Perfusion (adaptiert nach Chioncel O et al.)2
Therapie der akuten HI nach Stabilisierung/Rekompensation
Die Zeit der Hospitalisierung sollte sinnvoll genutzt werden, um auslösende Faktoren, die zur kardialen Verschlechterung geführt haben, zu identifizieren und ihnen vorzubeugen, Komorbiditäten festzustellen und zu behandeln sowie effektive HI-spezifische Langzeittherapien zu implementieren und zu optimieren. Medikamentöse Therapien, für die bei HFrEF eine Mortalitätsreduktion als erwiesen gilt, sind ACE-Hemmer, Betablocker, MRA und Angiotensinrezeptor/Neprilysin-Inhibitoren (ARNI). Rezente Studien zeigen, dass SGLT2-Hemmer (SGLT2-I) unabhängig vom Vorliegen eines Diabetes den kombinierten Endpunkt Tod und Hospitalisierung bei HFrEF effektiv senken können. Intravenöses Eisen verbessert bei chronisch symptomatischer HI und Eisenmangel die Leistungsfähigkeit und könnte sich positiv auf die Hospitalisierung auswirken. Inzwischen liegen für all diese Therapieformen Daten aus teils kleineren und teils größeren Studien vor, die zeigen, dass die Implementierung der Therapien nach einer akuten Dekompensation und Stabilisierung noch während des Spitalsaufenthaltes sicher ist und ähnliche Effekte hat wie in den entsprechenden Studien der chronischen stabilen HI. Die Studien TRANSITION und PIONEER-HF zeigten die Sicherheit von ARNI im akuten Setting und dass Patienten mit einem ARNI deutlich niedrigere NT-proBNP-Spiegel aufwiesen, was möglicherweise auch mit einer Abnahme der Hospitalisierung und Mortalität einhergeht.10,11 Mit SOLOIST-WHF liegen uns Daten vor, die die Sicherheit des Therapiebeginns mit dem SGLT2-I Sotagliflozin aufzeigen und demonstrieren, dass diese Patienten durch eine Reduktion der ambulanten und stationären Besuche aufgrund akuter HI und der Mortalität profitieren.12 Schließlich zeigte AFFIRM-AHF die Sicherheit der i.v. Eisentherapie für diese Population, wobei die Therapie mit einer Reduktion der Rehospitalisierungsrate verbunden war.13
Obwohl in diesen Studien keine neuen Substanzklassen für die Behandlung der HI angewendet werden, sind die Daten besonders relevant, stellen sie doch die ersten Studien dar, die positive Ergebnisse für die Behandlung einer akuten HI, zumindest nach erfolgreicher Stabilisierung, aufweisen. Sie unterstreichen den Stellenwert einer optimierten HI-Therapie, die allerspätestens nach einer Aufnahme wegen Verschlechterung implementiert werden sollte. In dieser vulnerablen Patientengruppe mit hohen Eventraten kann man mit einer raschen Intervention große Effekte erzielen. Im Sinne des Patientenwohls sollte deswegen eine Therapieoptimierung unbedingt bereits während des Spitalsaufenthalts eingeleitet und weiter geplant werden.
Als Unterstützung kann hierbei auch die Entlassungsmanagement-Checkliste der Arbeitsgruppe Herzinsuffizienz der ÖKG dienen. Die Checkliste hilft bei der strukturierten Aufarbeitung des Falles, beinhaltet die Dokumentation aller für eine optimale Betreuung der Patienten wichtigen Informationen und bietet somit eine Grundlage für das weitere ambulante Management und die Optimierung der Therapie. Die Checkliste für das Entlassungsmanagement ist unter folgendem Link verfügbar:
https://www.fachkreise.novartis.at/sites/fachkreise.novartis.at/files/nov_pos_entresto-im-notfallsetting_tip-on_105x210_020920.pdf
In Hinblick auf die nächsten ESC-Guidelines für HI wird es sicherlich Änderungen im Therapiealgorithmus geben. Unter anderem ist zu erwarten, dass die strikt hierarchische Struktur bei der Einführung der evidenzbasierten Therapien zumindest abgeschwächt wird und es somit eine Empfehlung geben wird, die Therapie mit mehreren Substanzklassen gleichzeitig zu beginnen und zu optimieren. Dies führt hoffentlich dazu, dass der Anteil an optimal oder zumindest gut behandelten Patienten signifikant ansteigt, wenn man bedenkt, dass so eine Optimierung mit weniger Arzt-Patienten-Kontakten durchführbar ist.
Literatur:
1 Bozkurt B et al.: Universal Definition and Classification of Heart Failure: A Report of the Heart Failure Society of America, Heart Failure Association of the European Society of Cardiology, Japanese Heart Failure Society and Writing Committee of the Universal Definition of Heart Failure. J Card Fail 2021: S1071-9164(21)00050-6
2 Chioncel O et al.: Clinical phenotypes and outcome of patients hospitalized for acute heart failure: the ESC Heart Failure Long-Term Registry. Eur J Heart Fail 2017; 19(10): 1242-54
3 Chioncel O et al.: Improving postdischarge outcomes in acute heart failure. Am J Ther 2018; 25(4): e475-e86
4 Ponikowski P et al.: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J 2016; 37(27): 2129-200
5 Mebazaa A et al.: Long-term safety of intravenous cardiovascular agents in acute heart failure: results from the European Society of Cardiology Heart Failure Long-Term Registry. Eur J Heart Fail 2018; 20(2): 332-41
6 Rubio-Gracia J et al.: Prevalence, predictors and clinical outcome of residual congestion in acute decompensated heart failure. Int J Cardiol 2018; 258: 185-91
7Verbrugge FH et al.: Management of the cardiorenal syndrome in decompensated heart failure. Cardiorenal Med 2014; 4(3-4): 176-88
8 Metra M et al.: Is worsening renal function an ominous prognostic sign in patients with acute heart failure? The role of congestion and its interaction with renal function. Circ Heart Fail 2012; 5(1): 54-62
9Clark AL et al.: Change in renal function associated with drug treatment in heart failure: national guidance. Heart 2019; 105(12): 904-10
10 Wachter R et al.: Initiation of sacubitril/valsartan in haemodynamically stabilised heart failure patients in hospital or early after discharge: primary results of the randomised TRANSITION study. Eur J Heart Fail 2019; 21(8): 998-1007
11 Velazquez EJ et al.: Angiotensin-neprilysin inhibition in acute decompensated heart failure. N Engl J Med 2019; 380(6): 539-48
12 Bhatt DL et al.: Sotagliflozin in patients with diabetes and recent worsening heart failure. N Engl J Med 2021; 384(2): 117-28
13 Ponikowski P et al.: Ferric carboxymaltose for iron deficiency at discharge after acute heart failure: a multicentre, double-blind, randomised, controlled trial. Lancet 2020; 396(10266): 1895-904
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Immunsuppression und Infektion: Durchimpfen so gut wie möglich
Autoimmunerkrankungen sind mit erhöhtem Infektionsrisiko verbunden, das durch immunsupprimierende Therapien weiter verstärkt wird. Impfungen sind also in der betroffenen Patient: ...