Kardiale Magnetresonanztomografie: ihre Stärken und Schwächen
Univ.-Prof. Dr. Julia Mascherbauer Universitätsklinik für Innere Medizin II Klinische Abteilung für Kardiologie Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die kardiale Magnetresonanztomografie (MRT) stellt eine strahlenfreie und sichere Ergänzung zu Echokardiografie und Computertomografie (CT) bei der Abklärung kardialer Erkrankungen dar. Neue Methoden erlauben tiefere Einblicke in strukturelle und funktionelle Veränderungen des Herzens. In diesem Artikel werden Stärken und Schwächen der kardialen MRT zusammengefasst, um Patienten zielgerecht der richtigen kardialen Bildgebung zuzuführen.
Keypoints
-
Die kardiale MRT erlaubt
eine präzisere Bestimmung von Größe, Funktion und
Myokardmasse beider Ventrikel als die Echokardiografie, was vor allem bei suboptimalen Schallbedingungen in der Echokardiografie von Bedeutung ist. -
Mittels MRT ist eine nicht invasive Charakterisierung des Myokards möglich, die bei der Abklärung wichtiger Differenzialdiagnosen hilfreich ist.
Wichtige Begriffe und Techniken der kardialen MRT
Die durchgeführten Sequenzen und die benötigte Dauer einer kardialen MRT richten sich nach den klinischen Fragestellungen. Die Zuweisung sollte daher detailliert darüber informieren, wonach im MRT gesucht wird, und eine kurze klinische Anamnese sowie wichtige Vorbefunde (vor allem Echokardiografie, CT, Herzkatheter) beinhalten. Wenn nach der Untersuchung eine andere Fragestellung beantwortet werden soll, ist oft eine neuerliche MRT mit ergänzenden Sequenzen erforderlich. Wie schon Mark Twain sagte: „Wer nicht weiß, wohin er will, der darf sich nicht wundern, wenn er ganz woanders ankommt.“ Typischerweise dauert eine kardiale Standard-MRT-Untersuchung, bei der auch Kontrastmittel verabreicht wird, ungefähr 45 Minuten.
Häufig verwendete Sequenzen
Im Folgenden ein Überblick über die am häufigsten verwendeten Sequenzen der kardialen MRT (Abb. 1):
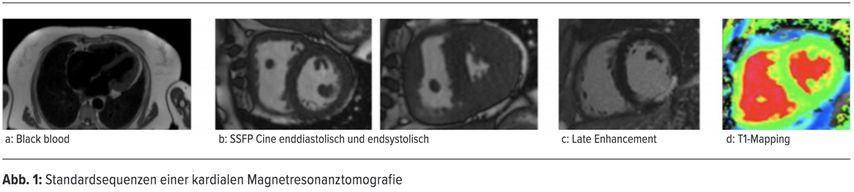
T1-gewichtete axiale „Black blood“- Sequenzen (Abb. 1a; vom Aortenbogen bis Diaphragma) dienen der Orientierung zu Beginn der Untersuchung und erlauben die Vermessung der herznahen Gefäße. Darüber hinaus können Pleura- und Perikardergüsse sowie nichtkardiale Strukturen beurteilt werden.
Die Bestimmung der links- und rechtsventrikulären Größe und Funktion ist ein zentrales Element jeder kardialen MRT. Typischerweise werden Cine-SSFP-Sequenzen („steady-state free precession“) im Kurzachsenstapel von der Mitralklappenebene bis zur Herzspitze über den gesamten Herzzyklus akquiriert (Abb. 1b). Dies erlaubt die Quantifizierung der enddiastolischen und endsystolischen Volumina und somit der Ejektionsfraktion sowie die Beurteilung von Wandbewegungsstörungen. Standardmäßig werden darüber hinaus Cine-SSFP-Sequenzen im 2-, 3- und 4-Kammer-Blick durchgeführt. Diese Methode stellt den Goldstandard in der Beurteilung der Rechts- und Linksventrikelfunktion dar. Bei stark arrhythmischer Herzaktion kann sich jedoch eine exakte Quantifizierung als schwierig erweisen.
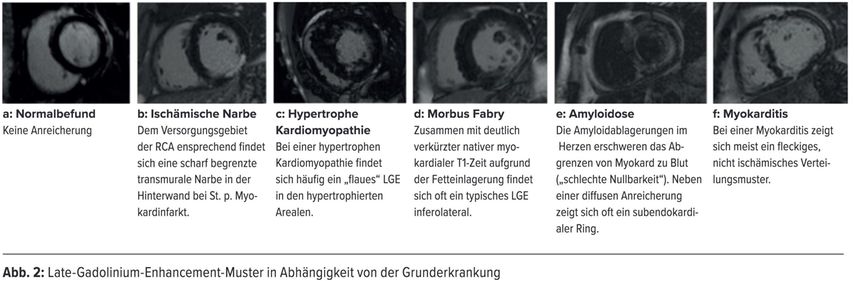
Late Gadolinium Enhancement (LGE, oft auch nur „Late Enhancement“ genannt, Abb. 1c): Gadolinium-haltiges Kontrastmittel kann aus dem Gefäßsystem in den Extrazellulärraum eindringen, jedoch nicht in Zellmembranen von Myozyten. Da Gadolinium die T1-Zeiten verändert, kommt es bei regionalen Verteilungsunterschieden von extrazellulärer Matrix, etwa bei einer Narbe nach einem Myokardinfarkt, zu typischen Signalmustern. Es werden ischämische und nichtischämische Verteilungsmuster unterschieden, die in Abbildung 2 kurz zusammengefasst sind. Eine homogene Veränderung über das gesamte Myokard kann jedoch mit dieser Methode nicht suffizient dargestellt werden, da nur regionale Unterschiede zu „gesundem Myokard“ visualisiert werden können.
Parametrische Mapping-Sequenzen: Fortschritte bei den Untersuchungssequenzen erlauben mittlerweile das Messen von T1- und T2-Zeiten im Myokard. Da die Zusammensetzung des myokardialen Gewebes die gemessenen Werte bestimmt, kann auf pathologische Veränderungen rückgeschlossen werden. Diffuse Fibrose, Eisenüberladung, Fettanreicherung und Ödeme führen zu charakteristischen Veränderungen, die sich im T1- und T2-Mapping ohne Kontrastmittel untersuchen lassen. Nach Gabe von Kontrastmittel kann zusätzlich das Extrazellulärvolumen (ECV, „extracellular volume“, Abb. 1d) berechnet werden, das gut mit histologischen Untersuchungen korreliert.
Eine Vielzahl anderer Untersuchungstechniken kommt zur Anwendung bei spezifischen Fragestellungen wie Charakterisierung von Tumoren, Darstellungen von Fettgewebe, Thromben oder myokardialem Ödem, Perfusionsmessungen u.v.m. Diese werden exemplarisch bei den unten folgenden Krankheitsbildern besprochen.
Übersetzung der europäischen Empfehlungen
Die Deutsche Gesellschaft für Kardiologie bietet eine übersichtliche Übersetzung der europäischen Empfehlungen als Pocket Guide mit praktischen Tipps und Tricks kostenlos unter folgendem Link an:
https://leitlinien.dgk.org/files/PL_DGK_kardiale_MR_innen_2_Auflage_korr.pdf
Verdachtsdiagnosen, bei denen eine kardiale MRT sinnvoll ist
Die kardiale MRT ist für viele kardiale Verdachtsdiagnosen eine sinnvolle bildgebende Untersuchung. Aus Effizienz- und Kostengründen ist – den Leitlinien entsprechend – die Echokardiografie immer die primäre kardiale Bildgebung. Im Folgenden werden Anwendungsgebiete dargestellt, bei denen die kardiale MRT die Abklärung wichtiger Differenzialdiagnosen erlaubt. Schlussendlich werden auch Fragestellungen besprochen, die mit dem kardialen MRT nicht ideal beantwortet werden können.
Linksventrikuläre Hypertrophie
Eine der Kernkompetenzen der kardialen MRT ist die weiterführende Abklärung einer linksventrikulären Hypertrophie, deren Ursache echokardiografisch häufig nicht festgestellt werden kann.
Hypertrophe Kardiomyopathie
Der Phänotyp der hypertrophen Kardiomyopathie kann sehr stark variieren (Abb. 2c). Vor allem Wandabschnitte, die in der Echokardiografie oft nur insuffizient darstellbar sind, wie etwa bei der apikalen hypertrophen Kardiomyopathie, lassen sich im MRT sehr gut darstellen.1
Kardiale Amyloidose
Die kardiale Amyloidose wurde lange Zeit in ihrer Häufigkeit unterschätzt. Nicht zuletzt dem Vormarsch der kardialen MRT ist es zu verdanken, dass diese Erkrankung wesentlich häufiger diagnostiziert wird. Die zwei häufigsten Subformen, die AL- und die TTR-Amyloidose, zeigen im Spätstadium ein typisches Vollbild in den Late-Enhancement-Aufnahmen (Abb. 2e) sowie deutlich verlängerte T1-Zeiten und ein hohes ECV. Es gibt jedoch auch immer wieder bioptisch verifizierte Fälle, bei denen sich ein relativ unauffälliger MRT-Befund findet, sodass ein definitiver Ausschluss im MRT nicht möglich ist.2,3
Morbus Fabry
Die Fetteinlagerungen (Glycosphingolipide) beim Morbus Fabry führen zu pathognomonischer Verkürzung der T1-Zeiten, welche bei anderen Pathologien wie Fibrose und Ödem verlängert sind. Gemeinsam mit einer ausgeprägten Linksventrikelhypertrophie und oft typischem Late-Enhancement-Muster (Abb. 2d) kann eine kardiale Beteiligung im MRT diagnostiziert werden.4
Eisenüberladung
Kardiale Eisenüberladung im Rahmen der Transfusionstherapie der Thalassaemia major kann mit der speziellen T2*-Messung(sprich „T2 star“ oder „T2 Stern“) quantifiziert werden. Die Einführung dieser Methode und die daran angepasste Chelattherapie gingen nachweislich mit einem verbesserten Überleben von Thalassaemia-major-Patienten einher.5
Herzinsuffizienz
Generell stellt die kardiale MRT den Goldstandard zur Quantifizierung der Links- und Rechtsventrikelfunktion dar. Es gilt jedoch zu beachten, dass Grenzwerte von Ventrikelvolumina und Auswurffraktionen, die in den aktuellen Guidelines für Therapieentscheidungen angeführt sind, ausschließlich aus echokardigrafischen Studien stammen.
Dilatative Kardiomyopathie
Häufig findet sich bei der nichtischämischen Kardiomyopathie (CMP) ein midmyokardiales Late Enhancement. Dieses wurde unabhängig von der linksventrikulären Auswurffraktion mit einer erhöhten Mortalität und plötzlichem Herztod in Zusammenhang gebracht.6 Analog dazu konnte für das T1-Mapping ein unabhängiger prognostischer Wert gezeigt werden.7
Das Ausmaß des Late Enhancements wird immer wieder als Indikation für einen implantierbaren Defibrillator (ICD) diskutiert.8 In den aktuellen amerikanischen Leitlinien für das Management ventrikulärer Arrhythmien und Prävention des plötzlichen Herztodes wird zwar erwähnt, dass das Late Enhancement hilfreich bei der Risikostratifizierung sein kann,9 jedoch findet sich dieser Faktor weder in den europäischen noch in den amerikanischen Empfehlungen zur Indikationsstellung für einen ICD.9–11
Ischämische CMP
Die große Stärke der kardialen MRT bei der ischämischen CMP zeigt sich in der Quantifizierung des postischämischen Narbengewebes. Typischerweise zeigt sich ein subendokardiales Late Enhancement dem versorgenden Koronargefäß entsprechend bis hin zu einer transmuralen Narbe (Abb. 2b). Das Ausmaß der Narbe kann hilfreich sein, wenn die Sinnhaftigkeit einer Intervention in dem betroffenen Versorgungsareal evaluiert wird (Fragestellung: Vitalität).
Herzinsuffizienz mit erhaltener Linksventrikelfunktion
Die HFpEF („heart failure with preserved ejection fraction“) zeichnet sich durch klinische Zeichen und Symptome der Herzinsuffizienz, erhöhte natriuretische Peptidwerte, eine diastolische Dysfunktion bei linksventrikulärer Auswurffraktion ≥50% aus. Die Rechtsventrikelfunktion in der kardialen MRT konnte als unabhängiger Prädiktor bei diesen Patienten identifiziert werden, ebenso das Ausmaß der diffusen Fibrose im T1-Mapping.12,13
Myokarditis
In der Abklärung bei Verdacht auf eine akute Myokarditis kommt der kardialen MRT eine zentrale Rolle zu. T2-gewichtete Ödemsequenzen (STIR, „shorttauinversionrecovery“) sowie T2-Mapping zielen darauf ab, interstitielle Wasseransammlungen zu messen. Zusätzlich findet sich häufig ein typisch fleckiges Verteilungsmuster im Late Enhancement, das einerseits im akuten Geschehen im Rahmen des Ödems, anderseits als Spätfolge im Sinne von Narbengewebe dargestellt werden kann (Abb. 2f). Bei Patienten mit Troponin-Auslenkung trotz blander Herzkranzgefäße kann die kardiale MRT hilfreich sein, um Differenzialdiagnosen wie die Myokarditis oder andere Erkrankungen nachzuweisen.
Kardiale Tumoren
Die kardiale MRT stellt ein zentrales Element bei der Abklärung kardialer Raumforderungen dar. Es sei hier auf exzellente Review-Artikel verwiesen, in denen typische Befundkonstellationen übersichtlich zusammengefasst sind.14, 15
Ischämiediagnostik mittels Stress-MRT
Zur Ischämiediagnostik stehen mehrere Möglichkeiten in der kardialen MRT zur Verfügung. Mittels Vasodilatation durch Adenosinrezeptor-Agonisten (z.B. Adenosin oder Regadenosin) können induzierbare Perfusionsdefekte nachgewiesen werden. Analog zur Stress-Echokardiografie können mittels Belastung durch Dobutamin Wandbewegungsstörungen im Rahmen einer induzierbaren Ischämie demaskiert werden. Indikationen und Kontraindikationen unterscheiden sich nicht von anderen kardialen Stress-Untersuchungen.
Strukturelle Ursachen für Rhythmusstörungen
Für eine Vielzahl von Rhythmusstörungen kann die kardiale MRT ein morphologisches Substrat darstellen, wodurch invasive elektrophysiologische Untersuchungen besser geplant werden können.
Wann ist eine kardiale MRT nicht sinnvoll?
Trotz beeindruckender technischer Fortschritte der letzten Jahre ist die kardiale MRT mit einigen Limitationen behaftet und bei gewissen Fragestellungen der Echokardiografie unterlegen. In den meisten Zentren dauert eine kardiale MRT-Untersuchung zwischen 30 und 60 Minuten, wodurch sich – von den Kosten abgesehen – ein großes Ressourcenproblem ergibt. Dies wird dadurch verstärkt, dass generell MRT-Untersuchungen in beinahe allen Fachdisziplinen einen immer größeren Stellenwert bekommen, wodurch die derzeit verfügbaren Kapazitäten an ein Limit gebracht werden.
Platzangst stellt ein scheinbar banales, jedoch häufiges Problem dar und sollte schon vor der Zuweisung ausführlich mit dem Patienten besprochen werden. Patienten, die bereits einmal klaustrophobe Zustände in der wesentlich kürzer andauernden Computertomografie-Untersuchung hatten, sollten einer alternativen Bildgebung zugeführt werden. Obwohl so gut wie alle Herzschrittmacher und implantierbaren Defibrillatoren (ICD) bei entsprechender Programmierung im Herz-MRT sicher untersucht werden können, erschweren die daraus resultierenden Artefakte häufig die Beurteilung. Herzkranzgefäße lassen sich in einer computertomografischen Angiografie (CTA) wesentlich besser darstellen und die MRT ist hier nur bei sehr seltenen Fragestellungen sinnvoll.
Die kardiale MRT erlaubt als komplementäre Methode das Abklären wichtiger Differenzialdiagnosen und sollte bei unklaren Fällen früh zum Einsatz kommen, wobei die Echokardiografie das primäre kardiale Bildgebungstool bleibt. Je exakter die Information auf der Zuweisung an das MRT-Zentrum ist, desto wahrscheinlicher können spezifische Ursachen gefunden oder ausgeschlossen werden. Die Zuweisungsdiagnose „kardiale Abklärung“ gilt es zu vermeiden.
Literatur:
1 Rowin EJ et al.: The hypertrophic cardiomyopathy phenotype viewed through the prism of multimodality imaging: clinical and etiologic implications. JACC Cardiovasc Imaging 2019; S1936-878X(19)30947-7 2 Martinez-Naharro A et al.: Magnetic resonance in transthyretin cardiac amyloidosis. J Am Coll Cardiol 2017; 70: 466-477 3 Nitsche C et al.: Light-chain and transthyretin cardiac amyloidosis in severe aortic stenosis: prevalence, screening possibilities, and outcome. EurJHeart Fail 2020; doi: 10.1002/ejhf.1756 4 Perry R et al.: The role of cardiac imaging in the diagnosis and management of Anderson-Fabry disease. JACC Cardiovasc Imaging 2019; 12: 1230-1242 5 Modell B et al.: Improved survival of thalassaemia major in the UK and relation to T2* cardiovascular magnetic resonance. J Cardiovasc Magn Reson 2008; 10: 42 6 Gulati A et al.: Association of fibrosis with mortality and sudden cardiac death in patients with nonischemic dilated cardiomyopathy. JAMA 2013; 309: 896-908 7 Puntmann VO et al.: T1-mapping and outcome in nonischemic cardiomyopathy: all-cause mortality and heart failure. JACC Cardiovasc Imaging 2016; 9: 40-50 8 Neilan TG et al.: CMR quantification of myocardial scar provides additive prognostic information in nonischemic cardiomyopathy. JACC Cardiovasc Imaging 2013; 6: 944-54 9 Al-Khatib SM et al.: 2017 AHA/ACC/HRS Guideline for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: areport of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol 2018; 72(14): 1677-74910 Ponikowski P et al.: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J 2016; 37: 2129-2200 11 Yancy CW et al.: 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2013; 62: e147-239 12Duca F et al.: Interstitial fibrosis, functional status, and outcomes in heart failure with preserved ejection fraction: insights from a prospective cardiac magnetic resonance imaging study. Circulation Cardiovasc Imaging 2016; 9(12): e005277 13 Aschauer S et al.: The right heart in heart failure with preserved ejection fraction: insights from cardiac magnetic resonance imaging and invasive haemodynamics. Eur J Heart Fail 2016; 18: 71-80 14 Fieno DS et al.: Cardiovascular magnetic resonance of primary tumors of the heart: A review. J Cardiovasc Magn Reson 2006; 8: 839-53 15 Pazos-Lopez P et al. Value of CMR for the differential diagnosis of cardiac masses. JACC Cardiovasc Imaging 2014; 7: 896-905 16 Kammerlander AA et al.: Diagnostic and prognostic utility of cardiac magnetic resonance imaging in aortic regurgitation. JACC Cardiovasc Imaging 2019; 12: 1474-83
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Immunsuppression und Infektion: Durchimpfen so gut wie möglich
Autoimmunerkrankungen sind mit erhöhtem Infektionsrisiko verbunden, das durch immunsupprimierende Therapien weiter verstärkt wird. Impfungen sind also in der betroffenen Patient: ...