Optimale Therapie bei reduzierter LVEF sowie bei Auftreten von Nebenwirkungen
Autor:innen:
Dr. Noel Gilian Panagiotides
Priv.-Doz. Dipl.-Ing. Dr. Noemi Pavo, PhD
Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die medikamentöse Behandlung der Herzinsuffizienz (HF) hat in den letzten Jahrzehnten bedeutende Fortschritte gemacht, sodass mittlerweile eine Vielzahl hochwirksamer Therapien zur Verfügung steht. Die aktuellen Leitlinien der European Society of Cardiology (ESC) empfehlen bei Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) vier Substanzklassen, um die Überlebensrate zu verbessern und die Hospitalisierung aufgrund einer Herzinsuffizienz (HHF) zu reduzieren.1
Keypoints
-
HF-Medikamente reduzieren das Risiko für eine HF-Hospitalisation und Tod.
-
Alle Patient:innen mit HFrEF sollten die 4-Säulen-Therapie mit BB, RASi, MRA und SGLT2i erhalten und die Aufdosierung auf Zieldosierungen für die volle Risikoreduktion.
-
Die GDMT kann sowohl ambulant als auch stationär sicher und zügig aufdosiert werden.
-
Medikamenteninduzierte Nebenwirkungen bei Aufdosierung der GDMT sind selten und in vielen Fällen einfach zu handhaben.
-
Bei komplexen Fällen ist eine Überweisung zum Facharzt oder ins Zentrum empfehlenswert.
Aktuell wird seitens der ESC der Einsatz von Betablockern (BB), Renin-Angiotensin-System-Inhibitoren (RASi; einschließlich ACE-Hemmern [ACEi], Angiotensin-Rezeptorblockern [ARB] und Angiotensin-Rezeptorblockern und Neprilysin-Inhibitoren [ARNI]), Mineralokortikoid-Rezeptor-Antagonisten (MRA) sowie SGLT2-Inhibitoren (SGLT2i) in der Therapie der HFrEF empfohlen.1 Damit diese Medikamente ihr volles Potenzial entfalten können, ist neben der Verschreibung aller vier Substanzklassen eine Aufdosierung auf die in klinischen Studien erprobten Zieldosierungen entscheidend.1 Doch in der Praxis stellt die korrekte Anwendung und Auftitration dieser lebensrettenden Therapien eine große Herausforderung dar. Registerdaten aus den USA und Europa zeigen, dass die leitliniengerechte Therapie (GDMT) oft unzureichend verschrieben und unzureichend dosiert wird. Fachgesellschaften und Experten auf nationaler und internationaler Ebene suchen intensiv nach Wegen, die Implementierung der HF-Therapie zu optimieren. Eine konsequentere Anwendung würde das Überleben verbessern und die Zahl der Krankenhausaufenthalte deutlich reduzieren.
Wie stark ist die Herzinsuffizienztherapie etabliert? – Zahlen aus Registerstudien
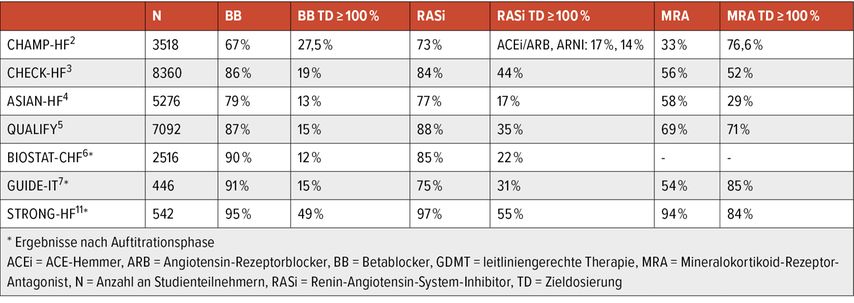
Zahlreiche internationale Register weisen auf den suboptimalen Einsatz der GDMT bei Patient:innen mit HFrEF hin (Tab. 1).2 Im amerikanischen CHAMP-HF-Register hatten nur 28%, 17%, 14% und 77%der Patient:innen die Zieldosis für BB, ACEi/ARB, ARNI und MRA erhalten. Besonders alarmierend ist, dass lediglich 1% der Patient:innen die empfohlene Dreifachtherapie in der Zieldosis erhielt.2
Das niederländische CHECK-HF-Register zeigte ähnlich niedrige Raten: Nur 19%, 44% und 52% der Patient:innen bekamen die Zieldosis für BB, RASi und MRA.3 Auch das ASIAN-HF-Register zeigte vergleichbar erschreckende Zahlen mit 13%, 17% und 29% für BB, ACEi/ARB und MRA in der Zieldosis.4 Im internationalen QUALIFY-Register erhielten immerhin 15%, 35% und 71% die Zieldosis für BB, ACEi/ARB und für MRA.5
Prospektive Studien wie GUIDE-IT und BIOSTAT-CHF, die eine Hochdosierung der GDMT im Protokoll vorsahen, berichteten selbst nach der Auftitrierungsphase und einer Nachbeobachtungszeit von 12 bzw. 21 Monaten weiterhin suboptimale Ergebnisse.6,7 In GUIDE-IT erreichten nur 15% und 31% der Patient:innen die Zieldosis für BB und ACEi/ARB, während es in der BIOSTAT-CHF-Studie nur 12% und 22% für BB und RASi waren.6,7 Diese Daten zeigen deutlich die unzureichende Behandlung von HF-Patient:innen weltweit.
Gründe für das Nichterreichen der Zieldosierung: Angst vor Nebenwirkungen
Verschiedene Faktoren tragen dazu bei, dass die Zieldosierungen der HF-Medikamente oft nicht erreicht werden. Bestimme Patient:innenmerkmale, strukturelle Faktoren, aber auch ärztliche Faktoren wie Motivation, klinische Trägheit und Ausbildung scheinen einen wesentlichen Beitrag zu leisten.8 Die unzureichende Aufdosierung von Medikamenten durch Ärzte kann wahrscheinlich zum Großteil auf die Angst vor Nebenwirkungen wie Hypotonie, Bradykardie, Nierenfunktionsstörungen und Hyperkaliämie zurückgeführt werden. Eine Umfrage der HFA zeigt, dass befragte Ärzte diese Risiken zusammen mit mangelnder Therapieadhärenz als die größten Hürden für die vollständige Umsetzung der GDMT betrachten.9
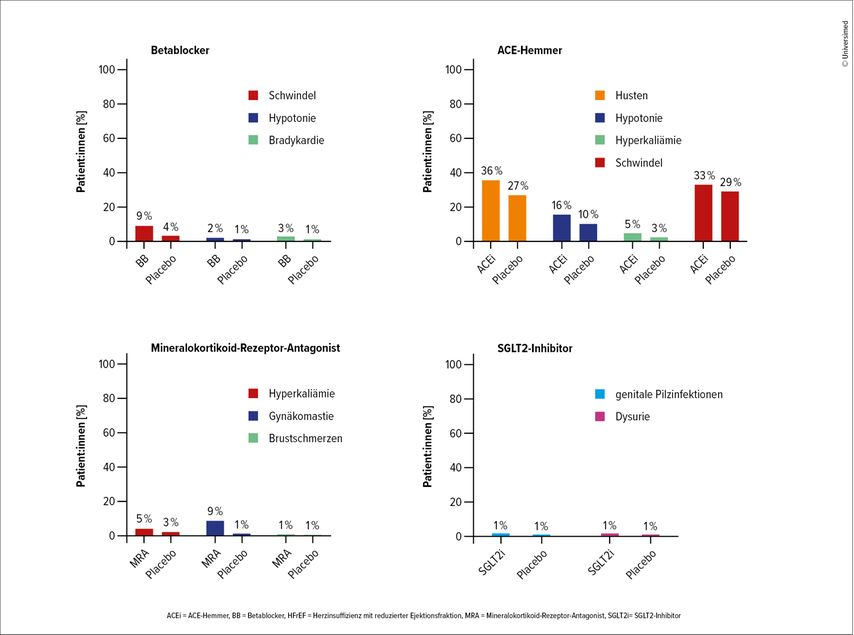
Dabei zeigte eine aktuelle Metaanalyse der 17 großen, randomisierten Studien zu den HF-Medikamenten, dass die Befürchtungen vor medikamenteninduzierten Nebenwirkungen meist unbegründet sind.10 Fast alle klinisch relevanten unerwünschten Ereignisse (UE) unter Behandlung mit BB, RASi, MRA und SGLT2i im Vergleich zu Placebo traten insgesamt selten auf und in Behandlungs- und Kontrollgruppen zumeist ähnlich häufig (Abb. 1).10 Das legt nahe, dass diese nicht primär auf die spezifischen Therapien zurückzuführen sind, sondern vielmehr Ereignisse wie insbesondere Blutdruckabfall, Verschlechterung der Nierenfunktion oder Hyperkaliämie die allgemeine Risikobelastung bei Herzinsuffizienz widerspiegeln. Möglicherweise sind sie als ein Voranschreiten der Erkrankung selbst zu werten. Einige spezifische Ereignisse sind auch medikamentenbedingt eingestuft.10 Insgesamt traten unter BB 5,5% vermehrt Schwindel, unter ACEi 8,9% vermehrt Husten sowie 5,6% vermehrt Hypotonie und unter MRA 5,7% vermehrt Gynäkomastie als in den Kontrollgruppen auf. Besonders interessant sind die UE unter SGLT2i. Obwohl Harnwegsinfekte und Ketoazidose häufig als Limitierung der Therapie genannt werden, traten sie in den Behandlungs- und Placebogruppen mit gleicher Häufigkeit auf. Genitale Pilzinfektionen und Dysurie waren unter SGLT2i um 1% und 1,3% häufiger.
Abb. 1: Vergleich von unerwünschten Ereignissen bei Herzinsuffizienztherapien: HF-Medikamente vs. Placebo (nach Harrington J et al. 2023)10
Real-World-Daten: Evidenz zu unerwünschter Wirkung während HFrEF-Therapieoptimierung
UE, die während der medikamentösen Therapie und Auftitrierung bei Herzinsuffizienzpatient:innen auftreten, können auch als Ausdruck eines fortgeschrittenen Stadiums der HF gewertet werden. Insbesondere ist der Zusammenhang zwischen der Hochdosierung von HF-Medikamenten und dem Auftreten von Nebenwirkungen bei fortgeschrittener HF bislang noch nicht genau untersucht worden. Dies ist aktuell Gegenstand einer Studie der Herzinsuffizienzforschungsgruppe der Medizinischen Universität Wien.
Vorläufige Ergebnisse zeigten, dass nach 6 Monaten Betreuung in der HFrEF-Ambulanz der Medizinischen Universität Wien 69%, 61% und 69% der Patient:innen die Zieldosis für BB, RASi und MRA erhielten. Eine vollständige Dreifachtherapie in Zieldosis erhielten 38% der Patient:innen, unabhängig vom HF-Schweregrad. Neue Nebenwirkungen traten nur selten auf. Hyperkaliämie und eine Verschlechterung der Nierenfunktion waren die häufigsten und betrafen vor allem Hochrisikopatient:innen mit erhöhtem NT-proBNP (präsentiert am ESC 2024). Die Ergebnisse der Daten nach 12 Monaten sind noch nicht publiziert. Insgesamt bestätigen diese vorläufigen Ergebnisse, dass eine optimale medikamentöse Therapie auch bei fortgeschrittener HF bei den meisten Patient:innen innerhalb kurzer Zeit erreichbar ist. Nebenwirkungen bleiben, wie auch in der Metaanalyse genannt, selten.
Wege zur optimalen Therapie: ambulante und stationäre Hochdosierung
Bei der Behandlung von HFrEF-Patient:innen ist zu beachten, dass diese ein sehr hohes Risiko und eine hohe Sterblichkeit aufweisen, während HF-Therapien nachweislich die Überlebensrate verbessern.1 Viele UE sind nicht medikamenteninduziert, sondern könnten auf eine Krankheitsprogression hindeuten. Das Reduzieren oder Absetzen der Therapie kann die Herzinsuffizienz verschlimmern und das Risiko für HF-bedingte Hospitalisierungen und Mortalität erhöhen. Dabei lassen sich viele UE ganz einfach handhaben: Gynäkomastie kann durch Wechsel zu Eplerenon vermieden werden, Hyperkaliämie mithilfe von Kaliumbindern behandelt und Husten durch den Wechsel von ACEi zu ARB oder ARNI verhindert werden. Bei einer Medikamentenreduktion ist eine kurzfristige Reevaluation entscheidend. Persistieren UE, könnte dies darauf hindeuten, dass die Symptome nicht durch das Medikament bedingt sind, was eine erneute Gabe, eventuell mit kleinteiligeren Schritten, sinnvoll machen könnte. Allenfalls sollten die Patient:innen über die Wirksamkeit der Therapie aufgeklärt sein. Die rasche Auftitrierung der GDMT auf die empfohlenen Zieldosierungen lässt sich sowohl ambulant als auch stationär effektiv und sicher umsetzen. Dabei sind insbesondere in der Anfangsphase engmaschige Kontrollen notwendig. Hochrisikopatient:innen und komplexe Fälle profitieren idealerweise von der Betreuung durch spezialisierte Ambulanzen oder Fachärzte. Dass eine Auftitration selbst bei Hochrisikopatient:innen nach einer akuten Hospitalisierung aufgrund der HF machbar und sinnvoll ist, zeigt die STRONG-HF-Studie.11 Der Therapieplan für die intensiv behandelte Gruppe sah vor, alle HF-Medikamente kurz vor Entlassung auf 50% der Zieldosis zu steigern und diese zwei Wochen später auf 100% zu bringen. Ambulante Nachsorgetermine waren 1, 2, 3 und 6 Wochen nach Entlassung angesetzt. Nach 3 Monaten erreichten 49%, 55% und 84% der Patient:innen die Zieldosis für BB, RASi und MRA, wobei 43% eine Dreifachtherapie mit über 90% der Zieldosierung erhielten.11,12 Die intensive Behandlung führte zu höheren Zieldosen, verbesserten Symptomen und Lebensqualität sowie einem geringeren Eintreten des Endpunkts „180-Tage-Sterblichkeit oder HF-Rehospitalisierung“ im Vergleich zur Standardbehandlung.11
Fazit
In der Praxis wird die Verschreibung und Aufdosierung der HF-Medikamente oft durch die Angst vor UE oder deren voreilige Zuschreibung zu GDMT verzögert, obwohl diese nachgewiesenermaßen selten aufgrund der Therapie selbst auftreten. Kliniker:innen sollten diese Befürchtungen gegen die bewiesenen Vorteile der GDMT, wie geringere Sterblichkeit und weniger Krankenhausaufenthalte, sorgfältig abwägen.13 Die GDMT kann sowohl ambulant als auch stationär sicher und zügig aufdosiert werden. Ambulant lassen sich Titrationsschritte festlegen und engmaschige klinische sowie labormedizinische Kontrollen durchführen. Während eines Spitalsaufenthalts steht die Optimierung der Therapie im Vordergrund, die durch rasche Nachsorgetermine nach Entlassung weitergeführt wird. Die aktualisierten ESC-Leitlinien betonen, dass die Therapie bereits im Krankenhaus eingeleitet und aufdosiert werden sollte, gefolgt von zeitnahen Nachsorgeuntersuchungen zur weiteren Anpassung.14
Literatur:
1 McDonagh TA et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021; 42(36): 3599-726 2 Greene SJ et al.: Medical therapy for heart failure with reduced ejection fraction: the CHAMP-HF registry. J Am Coll Cardiol 2018; 72(4): 351-66 3 Brunner-La Rocca HP et al.: Contemporary drug treatment of chronic heart failure with reduced ejection fraction: the CHECK-HF registry. JACC Heart Fail 2019; 7(1): 13-21 4 Teng THK et al.: Prescribing patterns of evidence-based heart failure pharmacotherapy and outcomes in the ASIAN-HF registry: a cohort study. Lancet Glob Heal 2018; 6(9): e1008-18 5 Komajda M et al.: Physicians’ adherence to guideline-recommended medications in heart failure with reduced ejection fraction: data from the QUALIFY global survey. Eur J Heart Fail 2016; 18(5): 514-22 6 Ouwerkerk W et al.: Determinants and clinical outcome of uptitration of ACE-inhibitors and beta-blockers in patients with heart failure: a prospective European study. Eur Heart J 2017; 38(24): 1883-90 7 Felker GM et al.: Effect of natriuretic peptide–guided therapy on hospitalization or cardiovascular mortality in high-risk patients with heart failure and reduced ejection fraction: a randomized clinical trial. JAMA 2017; 318(8): 713-20 8 Malgie J et al.: Guideline-directed medical therapy for HFrEF: sequencing strategies and barriers for life-saving drug therapy. Heart Fail Rev 2023; 28(5): 1221r 9 Savarese G et al.: Physician perceptions, attitudes, and strategies towards implementing guideline-directed medical therapy in heart failure with reduced ejection fraction. A survey of the Heart Failure Association of the ESC and the ESC Council for Cardiology Practice. Eur J Heart Fail 2024; 26(6): 1408-18 10 Harrington J et al.: Medication-attributable adverse events in heart failure trials. JACC Heart Fail 2023; 11(4): 425-36 11 Mebazaa A et al.: Safety, tolerability and efficacy of up-titration of guideline-directed medical therapies for acute heart failure (STRONG-HF): a multinational, open-label, randomised, trial. Lancet 2022; 400(10367): 1938-52 12 Cotter G et al.: Optimization of evidence-based heart failure medications after an acute heart failure admission: A secondary analysis of the STRONG-HF randomized clinical trial. JAMA Cardiol 2024; 9(2): 114-24 13 Bassi NS et al.: Association of optimal implementation of sodium-glucose cotransporter 2 inhibitor therapy with outcome for patients with heart failure. JAMA Cardiol 2020; 5(8): 948-51 14 McDonagh TA et al.: 2023 focused update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023; 44(37): 3627-39
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
State of the Art Mitralklappen-therapie 2025
Bei Mitralklappenerkrankungen, allen voran der Mitralinsuffizienz (MI), stehen heute, durch die rasante Weiterentwicklung innovativer Therapieverfahren, fortschrittliche ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...