Bedeutende Fortschritte in der Therapie des kolorektalen Karzinoms
Autor:
Prof. Dr. med. Florian Otto
Tumor- und Brust Zentrum Ostschweiz
St. Gallen
E-Mail: florian.otto@tbz-ost.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Grosse Erfolge für immer kleinere Patientengruppen – so hat sich dieklinische Forschung in der Onkologie über die letzten Jahre entwickelt, nicht nur, aber auch im Bereich der kolorektalen Karzinome (KRK). In diesem Jahr lag der Fokus der «oral abstract session» auf zwei Themen: der Lokaltherapie von Metastasen und der systemischen Immuntherapie. Angereichert wurde der «gemischte Satz» durch Vorträge über die immunmodulatorische Wirkung eines Adenosin-Rezeptor-Antagonisten, das Auftreten von Genmutationen unter Therapie mit VEGF- und EGFR-Antikörpern sowie die Optimierung der Gabe eines EGFR-Antikörpers.
Keypoints
-
Resektion und Lokalablation zur Behandlung von Lebermetastasen bei mKRK sind gleichgut wirksam, die Ablation ist aber nebenwirkungsärmer.
-
«Debulking» ist keine sinnvolle Strategie in der Behandlung der mKRK.
-
Immuntherapie ist beim dMMR-KRK ausserordentlich gut wirksam.
Den Metastasen an den Kragen – OP, Ablation, Transplantation
Häufig ist die Metastasierung eines kolorektalen Karzinoms (KRK) – zumindest aus Sicht der Kliniker:innen – auf die Leber beschränkt. In dieser Situation kann die Erkrankung in einem Teil der Fälle durch Resektion oder Thermoablation aller vorhandenen Metastasen geheilt werden – aber welche der beiden Methoden ist besser? Kapselnahe Metastasen lassen sich meist nur chirurgisch angehen, zentral gelegene sind oft weder Ablation noch Resektion zugänglich. In den übrigen Fällen hat die von Martijn Meijerink aus Amsterdam vorgestellte COLLISION-Studie beide Methoden an 300 Patient:innen (max. 10 Metastasen, bis 3cm Durchmesser) verglichen. Unterschiede im Gesamtüberleben (OS) sowie im lokalen oder systemischen progressionsfreien Überleben (PFS) wurden nicht beobachtet, die Lokalablation führte jedoch zu weniger Komplikationen.
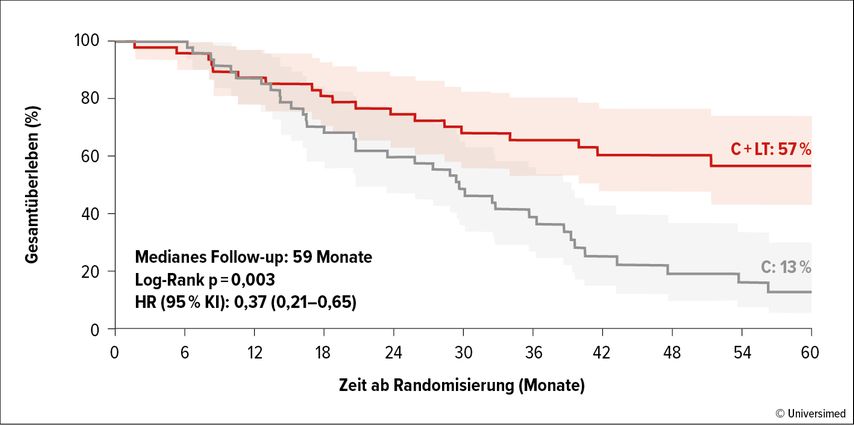
Ist die Lebermetastasierung weiter fortgeschritten und weder Resektion noch Ablation zugänglich, wäre eine Lebertransplantation eine potenziell kurative Therapie – wären da nicht die begrenzte Verfügbarkeit von Spenderorganen und Krankheitsrückfälle unter Immunsuppression. Trotzdem hat sich die französische randomisierte TransMet-Studie dieses Themas angenommen. René Adam aus Paris berichtete vom klinischen Verlauf der 36 hochselektierten Patient:innen (jünger als 65 Jahre, mindestens drei Monate stabile Erkrankung, CEA <80µg/l, keine BRAF-Mutation). Die OS-Rate der Transplantierten nach fünf Jahren lag bei 57% im Vergleich zu 13% bei den konventionell therapierten Patient:innen (Abb. 1). Trotz Krankheitsrezidiven (v.a. in der Lunge) bei 72% der Transplantierten waren 42% nach vier Jahren Nachbeobachtungszeit – und häufig erneuten Eingriffen – krankheitsfrei.
Abb. 1: Hepatisch metastasiertes KRK: Gesamtüberleben nach Lebertransplantation in der TransMet-Studie (modifiziert nach Adam R et al., 2024)
Geht die Metastasierung über die Leber hinaus, wird immer wieder ein maximales chirurgisches «Debulking» diskutiert. Nach drei Zyklen FOLFOX in der Erstlinie wurden 382 Patient:innen randomisiert und maximalem Debulking oder einer Kontrollgruppe zugewiesen, wenn mehr als 80% der Tumorläsionen einer Lokaltherapie (Resektion, Ablation, Strahlentherapie) zugänglich waren. Bezüglich OS und PFS zeigte sich keinerlei Unterschied zwischen den Gruppen, wie Elske Gootjes aus Nijmegen berichtete, als sie die Ergebnisse der ORCHESTRA-Studie vorstellte.
Schwachstellen des Tumors nutzen – Immuntherapie bei dMMR
Satelliteninstabile KRK, also Tumoren mit einem Defekt der DNA-Mismatch-Reparatur (dMMR), sind mit 15% aller primären KRK nicht selten. Da sie jedoch seltener metastasieren als KRK mit profizienter DNA-MMR (pMMR), machen sie lediglich 5% der metastasierten KRK (mKRK) aus. Drei Studien, die in der «oral abstract session» diskutiert wurden, befassten sich mit dieser Population.
In den Stadien II (Hochrisiko) und III führt eine neoadjuvante Therapie mit dem Anti-PD-1-Antikörper Pembrolizumab zu einer hohen Rate an kompletten Remissionen. Kai-Keen Shiu aus London berichtete über die Ergebnisse der NEOPRISM-CRC-Studie, in der 32 Patient:innen mit dMMR-CRC präoperativ mit drei Zyklen Pembrolizumab behandelt wurden. 41% der Tumoren wiesen eine BRAF-Mutation, 26% eine RAS-Mutation auf, fast alle hatten eine hohe »tumor mutational burden», ein Drittel der Patient:innen hatte ein Lynch-Syndrom. Trotz der relativ kurzen Vorbehandlung waren in 59% der Resektate keine vitalen Tumorzellen mehr nachweisbar.
Eine ähnliche Population (100 Patient:innen in den Stadien IIB und III, dMMR) wurde in einer randomisierten Phase-Ib-Studie entweder mit dem Anti-PD-1-Antikörper Sintilimab oder mit Sintilimab in Kombination mit dem Anti-CTLA-4-Antikörper IBI310 sechs Wochen lang therapiert. Während nach Behandlung mit Sintilimab 47% der Resektate keine vitalen Tumorzellen mehr aufwiesen, kam es nach Vorbehandlung mit der Kombination sogar zu 78% kompletten pathologischen Remissionen. Rui-Hua Xu aus Guangzhou erwähnte keine Fälle von Lokalkomplikationen.
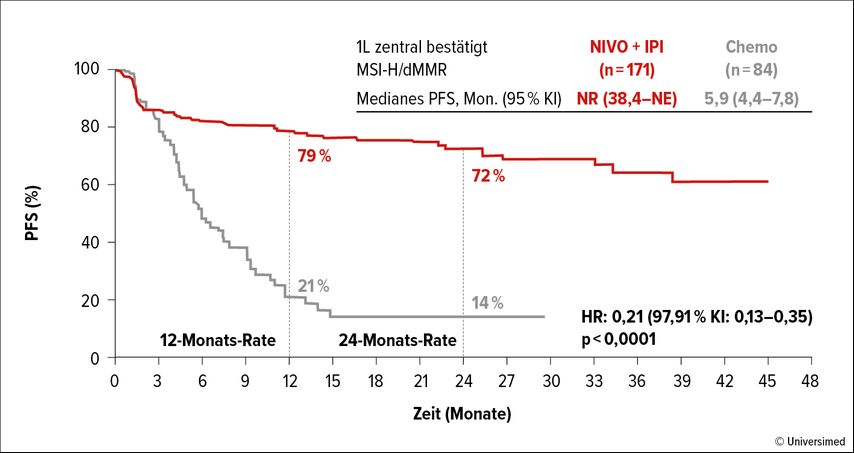
Eine andere Kombination, der Anti-PD-1-Antikörper Nivolumab zusammen mit dem Anti-CTLA-4-Antikörper Ipilimumab, wurde in der randomisierten Studie CheckMate 8HW gegen Standardchemotherapie in der ersten Behandlungslinie verglichen, allerdings bei etwa 300 Patient:innen mit metastasierter Erkrankung (dMMR-mKRK), wie Heinz-Josef Lenz aus Los Angeles berichtete. Die 24-Monate-PFS-Rate unter Immuntherapie erreichte 72%, unter Chemotherapie lediglich 14% (Abb. 2). Interessanterweise wirkte sich die vorangegangene Immuntherapie auch auf die Wirksamkeit der Zweitlinienbehandlung aus: So war die Rate des «PFS2» 24 Monate nach Start der Zweitlinientherapie 83% im Immuntherapiearm, jedoch nur 52% im Chemotherapiearm.
Abb. 2: Erstlinientherapie des dMMR-mKRK: progressionsfreies Überleben in der CheckMate-8HW-Studie (modifiziert nach Lenz HJ et al., 2024)
Adenosin-Rezeptor-Targeting, Panitumumab-Erhaltung und unter Therapie erworbene Genmutationen
KRK ohne Defekte in der DNA-Reparatur (pMMR) waren der Immuntherapie bisher kaum zugänglich. Adenosin wirkt immunsuppressiv über die Rezeptoren A2aR und A2bR. In der Phase-II-Studie ARC-9 wurde daher der Adenosin-Rezeptor-Antagonist Etrumadenant in der dritten Therapielinie in Kombination mit dem Anti-PD-L1-Antikörper Zimberelimab und einer «Standardtherapie» mit mFOLFOX6 und Bevacizumab an 75 Patient:innen im Vergleich zu Regorafenib (37 Patient:innen) erprobt. Das mittlere PFS wurde von zwei auf sechs Monate verlängert, das mOS von 9,5 auf 19,7 Monate. Aufgrund des eher schwachen Komparators sind die von Zev Wainberg aus Los Angeles präsentierten Ergebnisse allerdings schwierig zu interpretieren, sie könnten auch durch die FOLFOX-Rechallenge bedingt sein.
Nach sechs Zyklen einer Erstlinientherapie des RAS-Wildtyp-mKRK mit FOLFOX und dem Anti-EGFR-Antikörper Panitumumab wurde in der PANAMA-Studie, die von Dominik Modest aus Berlin vorgestellt wurde, zwischen einer FU/FA-basierten Erhaltungstherapie mit oder ohne Panitumumab randomisiert. Bei Krankheitsprogress in der Erhaltungsphase erfolgte die Reinduktion mit Panitumumab und FOLFOX. Zwar war eine kombinierte Erhaltungstherapie wirksamer, die Reinduktion nach kombinierter Erhaltung aber weniger effektiv, sodass sich die Zeit bis zum Versagen der Behandlungsstrategie zwischen der Studienarmen nicht unterschied.
Nicht weniger spannend als der Wirkmechanismus einer medikamentösen Tumortherapie sind die unter Therapie aktiv werdenden Resistenzmechanismen. Zum Teil beruhen diese Resistenzen auf Genmutationen im Tumorgewebe, die sich im Serum an der sogenannten «cell-free DNA» (cfDNA) nachweisen lassen. Solchen unter Therapie erworbenen Mutationen wurde in der PARADIGM-Studie nachgespürt, wie Hiroyuki Uetake aus Tokio berichtete. Vor und nach Therapie mit mFOLFOX6 und entweder dem Anti-EGFR-Antikörper Panitumumab oder dem Anti-VEGF-Antikörper Bevacizumab wurde nach Mutationen in der cfDNA gefahndet. Unter Therapie mit Panitumumab aufgetretene Mutationen im RTK/RAS-Signalweg waren mit Überleben nach Progression (PPS) und OS assoziiert. Unter Bevacizumab liessen sich Mutationen in Genen, die mit dem «CpG island methylator phenotype» (CIMP) in Verbindung stehen, mit kürzerem PPS und OS in Zusammenhang bringen.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...