Chemotherapie, Immuntherapie und Nebenwirkungsmanagement
Autor:
Priv.-Doz. Dr. Simon Peter Gampenrieder
Universitätsklinik für Innere Medizin III mit Hämatologie, internistischer Onkologie, Hämostaseologie, Infektiologie, Rheumatologie und Onkologisches Zentrum,
Paracelsus Medizinische Privatuniversität Salzburg
E-Mail: s.gampenrieder@salk.at
Neue Wege in der Brustkrebstherapie: Beim 47. San Antonio Breast Cancer Symposium wurden vielversprechende Ansätze für Chemotherapie, Immuntherapie und Nebenwirkungsmanagement vorgestellt. Von der Optimierung der adjuvanten Therapie bis hin zu effektiveren Maßnahmen gegen chemotherapieinduzierte Übelkeit – die präsentierten Studien bieten spannende Einblicke und richtungsweisende Impulse für die klinische Praxis.
Keypoints
-
Chemotherapieoptimierung: In der Studie TAILORx scheinen nur Patient:innen mit einem Oncotype-DX-Recurrence-Score ≥31 von einer adjuvanten anthrazyklinhaltigen Chemotherapie zu profitieren. In der Studie WSG-ADAPT waren acht Gaben wöchentlichen Nab-Paclitaxels tendenziell wirksamer als Paclitaxel alle zwei Wochen, jedoch ohne Signifikanz in Bezug auf das krankheitsfreie Überleben. In der Studie TRAIN-3 war eine verkürzte neoadjuvante Chemoimmuntherapie (drei oder sechs Zyklen) beim HER2-positiven Mammakarzinom ähnlich effektiv wie neun Zyklen, sofern eine streng definierte radiologische Komplettremission vorlag.
-
Immuntherapie beim frühen TNBC: Atezolizumab und Camrelizumab konnten die Rate an pathologischen Komplettremissionen in Kombination mit Chemotherapie steigern, zeigten jedoch keinen signifikanten Einfluss auf das ereignisfreie Überleben.
-
Nebenwirkungsmanagement: Olanzapin hat sich als überlegen gegenüber Prochlorperazin in der Behandlung refraktärer chemotherapieinduzierter Übelkeit erwiesen. Die Erhebung von PRO mittels Apps, kombiniert mit Alarmsystemen, verbessert nicht nur die Lebensqualität, sondern verlängert auch das Überleben von Brustkrebspatient:innen mit Metastasen.
Beim 47. San Antonio Breast Cancer Symposium wurden mehrere Studien vorgestellt, die darauf abzielten, die optimale adjuvante Chemotherapie für Patient:innen mit luminalen Mammakarzinomen zu definieren. Darüber hinaus wurden neue Erkenntnisse zu Immuncheckpoint-Inhibitoren beim frühen tripelnegativen Mammakarzinom (TNBC) präsentiert sowie Olanzapin als effektive Therapie gegen refraktäre, chemotherapieinduzierte Übelkeit bestätigt. Die bedeutendsten Studien zu den Themen Chemotherapie, Immuntherapie und Nebenwirkungsmanagement wurden beim 12. Post-SABCS der ABCSG am 10. Jänner 2025 in Wien vorgestellt und in diesem Artikel zusammengefasst.
Chemotherapie
TAILORx: Anthrazykline beihohem genomischem Risiko
Eine Post-hoc-Analyse der Studie TAILORx widmete sich der Frage, welche Patient:innen mit HR+/HER2– Mammakarzinom eine adjuvante, anthrazyklin-haltige Chemotherapie brauchen.1
In TAILORx wurden über 10000 Patient:innen auf Basis des Oncotype-DX-Recurrence-Scores (RS) mit oder ohne adjuvante Chemotherapie behandelt. Die Chemotherapie konnte anthrazyklinhaltig oder anthrazyklinfrei sein. In den verschiedenen Studienarmen erhielten insgesamt 2549 Patient:innen entweder Docetaxel/Cyclophosphamid (TC; n=2111) oder Doxorubicin, Cyclophosphamid und ein Taxan (T-AC; sequenziell oder simultan; n=438).
Patient:innen, die ein Anthrazyklin erhielten, hatten insgesamt etwas mehr Risikofaktoren für ein Rezidiv (etwas größere Tumoren, häufiger Grad 3 [G3] und höherer RS) und waren etwas jünger (medianes Alter 53 vs. 55 Jahre). Trotzdem schienen im Vergleich zu TC nur Patient:innen mit einem RS ≥31 von einem Anthrazyklin zu profitieren (HR: 0,32; p=0,009), während Patient:innen mit einem RS <31 keinen Vorteil von einem Anthrazyklin hatten (HR: 1,24; p=0,484).
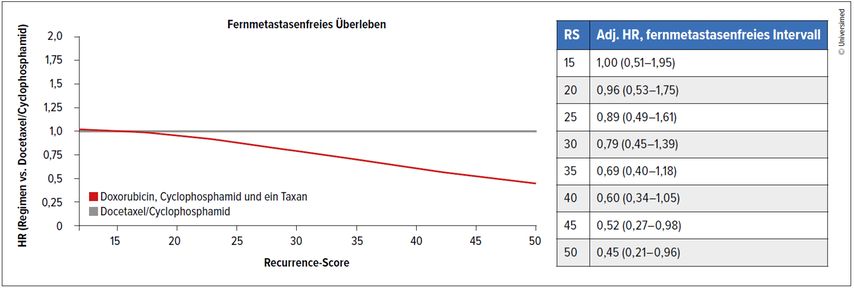
Der Zusammenhang zwischen RS und Anthrazyklin-Nutzen scheint linear zu sein: je höher der RS, desto größer der Benefit (Abb.1). In einer weiteren Subgruppenanalyse der Patient:innen mit RS ≥31 waren es nur Patient:innen mit Tumoren >2cm, die von einem Anthrazyklin profitierten. Diese Beobachtung stimmt mit jener aus dem FLEX-Register überein, wo nur Patient:innen mit einem MammaPrint high 2 (–1,000 bis –0,570) von dem Einsatz eines Anthrazyklins zu profitieren scheinen (3-Jahres-RFS [rezidivfreies Überleben]: +11,3% bei high 2 vs. –1,8% bei high 1).
Abb. 1: Zunehmender Vorteil von einem Anthrazyklin mit zunehmendem Oncotype-DX-Recurrence-Score (modifiziert nach Chen N et al.)1
WSG-ADAPT: Nab-Paclitaxel Q1Wvs. Paclitaxel Q2W
Mit der Wahl der Chemotherapie beschäftigte sich auch ein Subprotokoll der Chemotherapie-Studie ADAPT bei HR+/HER2– Brustkrebs der Westdeutschen Studiengruppe (WSG).2 Patient:innen mit hohem Rezidivrisiko erhielten entweder das klassische dosisdichte Therapieregime mit vier Gaben Paclitaxel 175mg/m2 alle zwei Wochen mit G-CSF-Support oder alternativ Nab-Paclitaxel 125mg/m2 wöchentlich für acht Gaben. Anschließend erhielten alle Patient:innen vier Zyklen dosisdichtes EC (Epirubicin/Cyclophosphamid).
Der experimentelle Arm mit Nac-Paclitaxel zeigte zwar eine höhere Rate pathologischer Komplettremission (pCR; 20,8% vs. 12,9%), allerdings übersetzte sich dies nicht in ein statistisch signifikant unterschiedliches krankheitsfreies Überleben (DFS).
Die Therapieabbrüche waren in beiden Studienarmen ungefähr gleich häufig (7,9% vs. 7,8%), allerdings wies Nab-Paclitaxel etwas mehr hämatologische Nebenwirkungen auf. Die Polyneuropathierate war insgesamt im Paclitaxel-Arm etwas höher (23,2% vs.20,8%), allerdings waren G3-Neuropathien häufiger im Nab-Paclitaxel-Arm (6,9% vs.3,6%).
Somit löst wöchentliches Nab-Paclitaxel das dosisdichte Regime mit Paclitaxel nicht als Standard ab, erweitert aber die Therapieauswahl für Patient:innen mit HR+/HER2– Mammakarzinom.
TRAIN-3: verkürzte neoadjuvante Therapie bei rCR
In der niederländischen Phase-II-Studie TRAIN-3 wurde eine Verkürzung der neoadjuvanten Chemotherapie von neun auf sechs oder sogar nur drei Zyklen untersucht, sofern die Patient:innen in der Zwischenuntersuchung eine radiologische Komplettremission hatten.3
Eingeschlossen wurden Patient:innen mit HER2-positivem Karzinom im Stadium II oder III. Sie erhielten eine neoadjuvante Therapie mit Paclitaxel, Carboplatin, Trastuzumab und Pertuzumab. Im Falle einer radiologischen Komplettremission wurde die Therapie von neun auf sechs oder drei Zyklen reduziert.
Ergänzend zur Mamma-MRT kamen zur Beurteilung der Remission auch Axilla-Ultraschall sowie eine Feinnadelpunktion bei initialem Lymphknotenbefall oder eine Vakuumaspirationsbiopsie der markierten Tumorregion bei HR-positiven Tumoren zum Einsatz. Dieses Vorgehen erwies sich als sicher: Der primäre Endpunkt wurde erreicht (wenig Ereignisse in der Gesamtkohorte) und Patient:innen mit verkürzten Regimen wiesen kein erhöhtes Rezidivrisiko auf (3-Jahres-EFS [ereignisfreies Überleben]: 96% in der HR–-Subgruppe und 97% in der HR+-Subgruppe).
Das Phase-II-Design und die aufwendige Definition einer radiologischen Komplettremission machen dieses Vorgehen allerdings noch nicht reif für den alltäglichen Einsatz.
Immuntherapie
NSABP B-59/GeparDouze: Atezolizumab +Chemotherapie beim eTNBC
Eine der wichtigsten Studien, die beim letztjährigen San Antonio Breast Cancer Symposium präsentiert wurden, war die NSABP-B-59- oder GeparDouze-Studie, ein Gemeinschaftsprojekt der USA und Deutschland.4 Es handelt sich dabei um eine multizentrische, doppelblinde, randomisierte, placebokontrollierte Phase-III-Studie für Patient:innen mit tripelnegativem frühem Mammakarzinom mit einer Tumorgröße von mehr als 2cm oder pathologischen Lymphknoten.
1550 Patient:innen erhielten entweder eine neoadjuvante Chemotherapie plus Placebo (Carboplatin plus Paclitaxel gefolgt von Doxorubicin oder Epirubicin plus Cyclophosphamid) oder in Kombination mit dem Anti-PD-L1-Antikörper Atezolizumab. Postoperativ erhielten Patient:innen Atezolizumab oder Placebo für insgesamt ein Jahr. Nach einem Amendment wurde bei fehlender pathologischer Komplettremission auch eine postneoadjuvante Therapie mit Capecitabin erlaubt, das knapp 50% der Patient:innen auch erhielten.
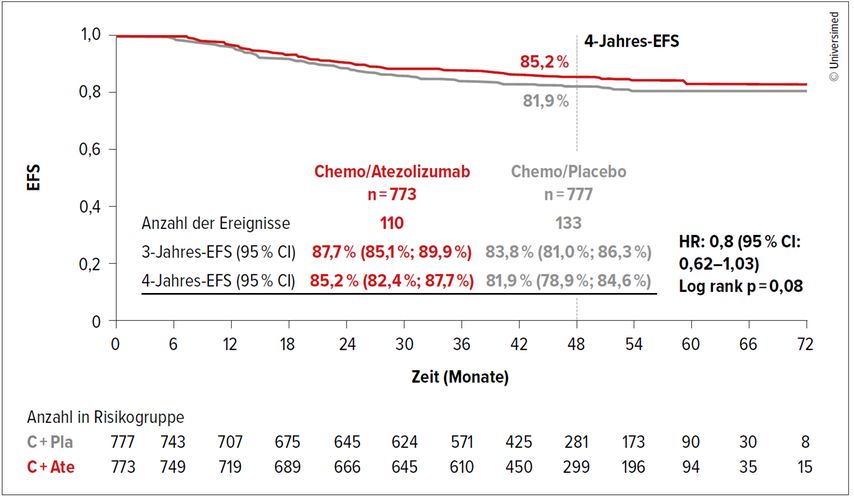
Die pCR-Rate konnte durch Atezolizumab zwar von 57,0% auf 63,3% gesteigert werden, der primäre Endpunkt EFS war jedoch nach einem medianen Follow-up von 49 Monaten nicht statistisch signifikant unterschiedlich zwischen den beiden Studienarmen (HR: 0,80; 95% CI: 0,62–1,03; p=0,08; Abb.2). Erwartungsgemäß war Atezolizumab mit immunvermittelten Nebenwirkungen assoziiert.
Abb. 2: Der primäre Endpunkt, das ereignisfreie Überleben (EFS), konnte in der NSABP-B-59/GeparDouze-Studie durch die Hinzunahme von Atezolizumab zur neoadjuvanten Chemotherapie nicht verlängert werden (modifiziert nach Geyer C et al.)4
Warum diese Studie im Gegensatz zur KEYNOTE-522-Studie keinen Vorteil durch die Hinzunahme der Immuntherapie zeigen konnte, bleibt letztlich unklar.5 Mögliche Erklärungen sind das etwas niedrigere Risikoprofil der Studienpopulation mit weniger nodal-positiven Patient:innen in der NSABP-Studie im Vergleich zur KEYNOTE-522-Studie (41% vs. 51%). Dies spiegelte sich auch in der besseren 3-Jahres-EFS-Rate der beiden Kontrollarme wider (84% vs. 77%). Zudem könnte die „bessere Chemotherapie“ (dosisdichtes AC oder EC bei 64% und Capecitabin adjuvant bei knapp 50%) den zusätzlichen Nutzen der Immuntherapie abgeschwächt haben. Schließlich kann aber auch eine unterschiedliche Wirksamkeit von Anti-PD-L1- und Anti-PD-1-Antikörper nicht ausgeschlossen werden.
Erwähnenswert ist in diesem Zusammenhang, dass in einer großen Biomarker-Analyse der KEYNOTE-522-Studie, die ebenso beim SABCS 2024 präsentiert wurde, weiterhin kein brauchbarer Biomarker für den Einsatz von Pembrolizumab identifiziert werden konnte. Weder vordefinierte Genexpressionssignaturen noch die Tumor-Mutationslast (TMB), die molekularen TNBC-Subtypen oder der HRD-Status zeigten einen prädiktiven Wert für die Immuntherapie.6
CamRelief: Camrelizumab +Chemotherapie beim eTNBC
Ganz ähnlich aufgebaut war die CamRelief-Studie, die die Wirksamkeit des in China hergestellten Anti-PD-1-Antikörpers Camrelizumab in einem chinesischen Patient:innenkollektiv mit tripelnegativem Brustkrebs untersuchte.7 Die Studie war allerdings deutlich kleiner (n=441) und der primäre Endpunkt die pCR-Rate, während das EFS nur einen sekundären Endpunkt darstellte. Weitere Unterschiede zu den vorhin genannten Studien waren der Einsatz von Nab-Paclitaxel (in Kombination mit Carboplatin) und ausschließlich dosisdichtem EC. Camrelizumab oder Placebo wurden alle zwei Wochen parallel zur Chemotherapie und anschließend für insgesamt ein Jahr verabreicht. Adjuvantes Capecitabin war erlaubt. Durch den Checkpoint-Inhibitor konnte die pCR-Rate signifikant von 44,7% auf 56,8% gesteigert werden (p=0,0038), allerdings zeigte sich kein statistisch signifikanter Unterschied im EFS (HR: 0,80; 95% CI: 0,46–1,42; p=0,224) oder im fernmetastasenfreien Überleben (DDFS; HR: 0,62; 95% CI: 0,29–1,33; p=0,107).
Nebenwirkungsmanagement
PRO-B: „patient-reported outcomes“ (PRO) mit App und Alarmsystem
Die Erhebung von „patient-reported outcomes“ (PRO), also Informationen über den Gesundheitszustand von Patient:innen, die von diesen selbst berichtet werden, haben bereits in mehreren Studien Vorteile für die Therapieadhärenz, für ungeplante Vorstellungen in der Notaufnahme, die Kommunikation zwischen Patient:in und Betreuungsteam und das Überleben von Krebspatient:innen gezeigt.
Die multizentrische randomisierte Studie PRO-B untersuchte, ob die wöchentliche Erhebung von PRO mittels App, verbunden mit einem Alarmsystem über das betreuende Brustzentrum, einen Einfluss auf die Fatigue bei Patient:innen mit metastasiertem Brustkrebs unter aktiver Tumortherapie hat.8 In der Kontrollgruppe wurden Symptome nur alle drei Monate und ohne Alarmsystem erfasst. Als weitere Endpunkte wurde der Einfluss auf das Gesamtüberleben nach einem Jahr sowie in der Subgruppe der tripelnegativen Mammakarzinome und von Patient:innen mit viszeralen Metastasen erfasst.
Nach sechs Monaten wiesen Patient:innen im experimentellen Arm signifikant weniger Fatigue auf. Zudem konnte das Gesamtüberleben nach zwölf Monaten signifikant verlängert werden (87,6% vs. 84,7%; HR: 0,71; 95% CI: 0,51–0,99; p=0,043). In der tripelnegativen Subgruppe zeigte sich ein ähnliches Ergebnis, allerdings war hier der Unterschied nicht signifikant (HR: 0,61; 95% CI: 0,24–1,53; p=0,289).
Olanzapin vs. Prochlorperazinbei refraktärer Übelkeit
In einer großen doppelblinden, placebo-kontrollierten Phase-III-Studie aus den USA wurde die Wirkung von Olanzapin mit jener von Prochlorperazin gegen refraktäre chemotherapieinduzierte Übelkeit untersucht.9 Eingeschlossen wurden 293 von insgesamt 1363 Patient:innen, die nach dem ersten Zyklus einer hochemetogenen Chemotherapie – trotz Guideline-konformer Prophylaxe – Übelkeit von Grad ≥3 auf einer 7-teiligen Skala aufwiesen.
Die Teilnehmenden wurden in drei Arme randomisiert: Placebo, Prochlorperazin 10mg oder Olanzapin 10mg jeweils an den Tagen 1–4 des zweiten Chemotherapiezyklus. Alle Patient:innen erhielten zusätzlich Netupitant, Palonosetron und Dexamethason. Sowohl Olanzapin als auch Prochlorperazin reduzierten signifikant die refraktäre Übelkeit, wobei Olanzapin sich als effektiver herausstellte (weniger maximale Übelkeit, weniger durchschnittliche Übelkeit, weniger Erbrechen als mit Prochlorperazin). Diese Studie bestätigt somit Olanzapin als wichtiges und wirksames Medikament gegen refraktäre chemotherapieinduzierte Übelkeit.
Literatur:
1 Chen N et al.: SABCS 2024; Abstr. #GS3-03
2 Kuemmel S et al.: SABCS 2024; Abstr. #GS3-04
3 Louis F et al.: SABCS 2024; Abstr. #RF1-03
4 Geyer C et al.: SABCS 2024; Abstr. #GS3-05
5 Schmid P et al.: N Engl J Med 2024; 391(21): 1981-91
6 O’Shaughnessy J et al.: SABCS 2024; Abstr. #LB1-07
7 Shao C-M et al.: SABCS 2024; Abstr. #GS3-06
8 Karsten MM et al.: SABCS 2024; Abstr. #GS1-06 9 Peppone L et al.: SABCS 2024; Abstr. #RF2-06
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...