Neue Fälle aus dem Tumorboard
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In dieser Ausgabe wird das Vorgehen bei primär nicht vollständig resezierbaren Lebermetastasen beschrieben. Außerdem werden zwei Patienten mit männlichem Mammakarzinom und eine Patientin mit multifokalem Lungenkarzinom vorgestellt.
Metastasiertes kolorektales Karzinom
Patient, 68 Jahre bei Erstvorstellung
Onkologische Anamnese
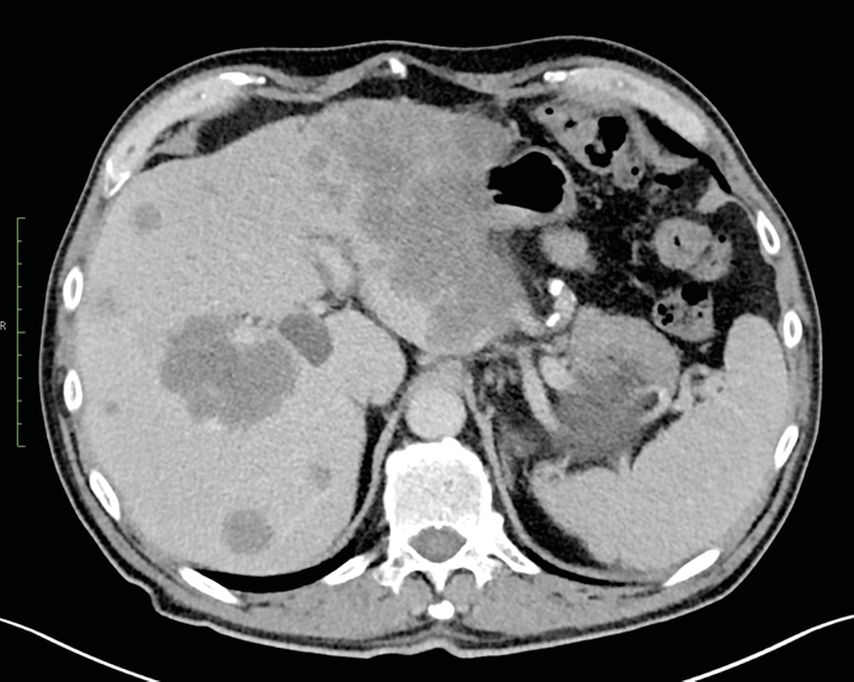
Im Juni 2023 wurde im Rahmen einer Koloskopie ein Tumor im Coecum diagnostiziert. Im anschließenden Staging mittels CT von Thorax, Leber und Abdomen wurden multiple (>30) bilobäre Lebermetastasen festgestellt (Abb. 1). Der Titer des Tumormarkers CEA lag >1000µg/l. In der molekularpathologischen Untersuchung zeigte sich keine RAS- oder BRAF-Mutation, und der Tumor war mikrosatellitenstabil. Abgesehen von einer medikamentös gut eingestellten Hypertonie hatte der Patient keine Begleiterkrankungen, war körperlich aktiv und in ausgezeichnetem Allgemeinzustand.
Tumorboardbesprechung zur Festlegung der initialen Strategie
Aufgrund der ungünstigen Verteilung der Metastasen mit Involvierung beider portaler Pedikel konnte initial aus technischen Gründen keine Operation angeboten werden. Die onkologische Ausgangssituation war wegen der synchronen Metastasierung, des hohen CEA-Werts und der hohen Tumorlast ungünstig. Daher wurde die Einleitung einer systemischen Therapie mit dem Ziel eines maximalen Ansprechens empfohlen. Aufgrund des im rechtsseitigen Kolon gelegenen Primärtumors riet das Tumorboard zu einer Triplet-Chemotherapie mit FOLFOXIRI (Folinsäure, 5-Fluorouracil, Oxaliplatin, Irinotecan) und dem Anti-VEGF-Antikörper Bevacizumab.
Um mit der bestmöglichen bildgebenden Methode alle vorhandenen Leberherde vor Einleitung der Chemotherapie darzustellen, wurde zu einer MRT der Leber mit leberspezifischem Kontrastmittel als Baseline-Untersuchung geraten.
Initialer Verlauf
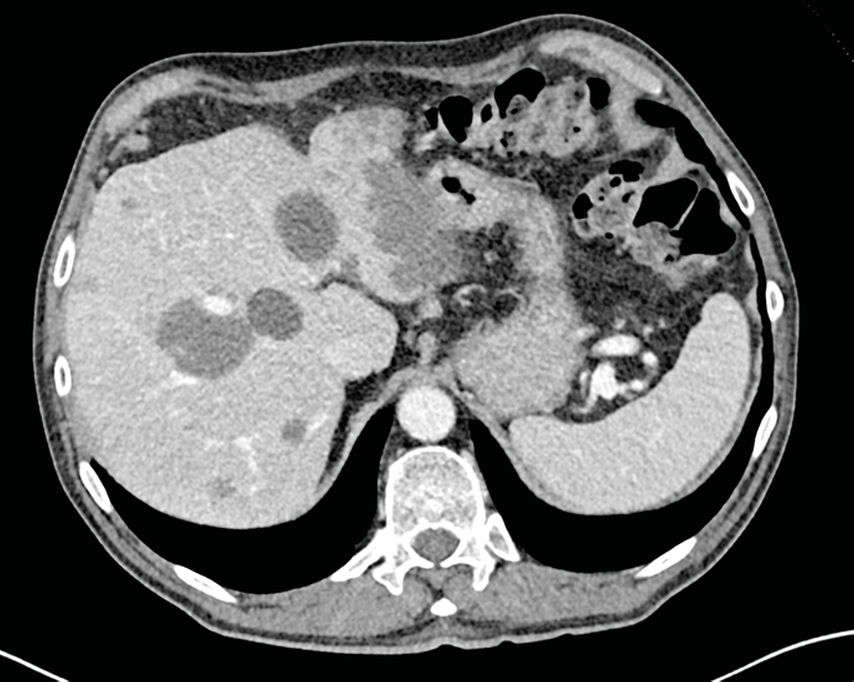
Bereits nach vier Zyklen FOLFOXIRI/Bevacizumab zeigte sich in der CT eine partielle Remission (Abb. 2); der Tumormarker CEA sank auf 46µg/l.
Erneute Tumorboardbesprechung
Eine komplette operative Entfernung sämtlicher Metastasen war nach zwei Monaten Therapie weiterhin nicht möglich. Allerdings erschien eine Entfernung der Metastasen am rechten Pfortaderpedikel bis auf eine zentrale Metastase direkt möglich. Es wurde daher im Sinne eines „Liver first“-Konzepts beschlossen, zunächst die Leber von Tumor zu befreien – und zwar in Form einer Kombination aus Resektionen, intraoperativen Mikrowellenablationen und stereotaktischer Bestrahlung der nicht operablen, etwa 5cm großen Metastase am rechten Pfortaderpedikel. Anschließend sollte der Primärtumor entfernt und danach die Chemotherapie fortgesetzt werden.
Weiterer Verlauf
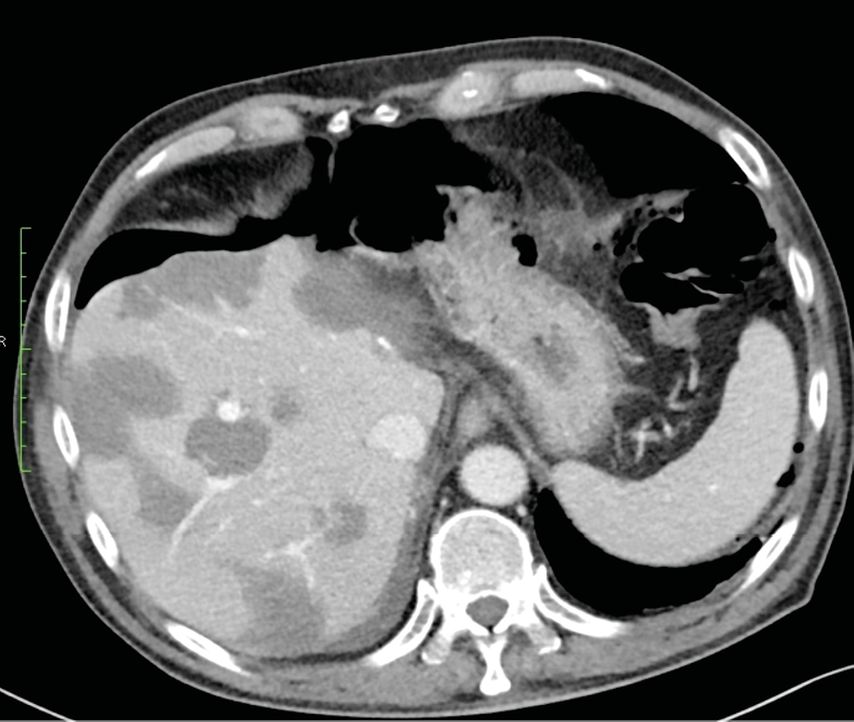
Es folgten die Resektion der linkslateralen Segmente 2 und 3, multiple parenchymsparende, atypische Resektionen sowie multiple intraoperative Mikrowellenablationen in der rechten Leber und im Segment 4. Damit konnten alle initial aus der MRT bekannten und intraoperativ zugänglichen Metastasen entfernt oder einer Ablation unterzogen werden. Die verbleibende große Metastase am rechten Pedikel wurde kurz nach der Leberoperation in elf Fraktionen mit insgesamt 55Gy stereotaktisch bestrahlt (Abb.3). Zwei Wochen danach wurde der Primärtumor mittels Hemikolektomie rechts entfernt.
Abb. 3: Postoperative CT nach linkslateraler Resektion, multiplen parenchymsparenden Resektionen und Mikrowellenablationen
Der gesamte Verlauf war frei von Komplikationen und die Chemotherapie konnte drei Wochen nach der Hemikolektomie fortgesetzt werden.
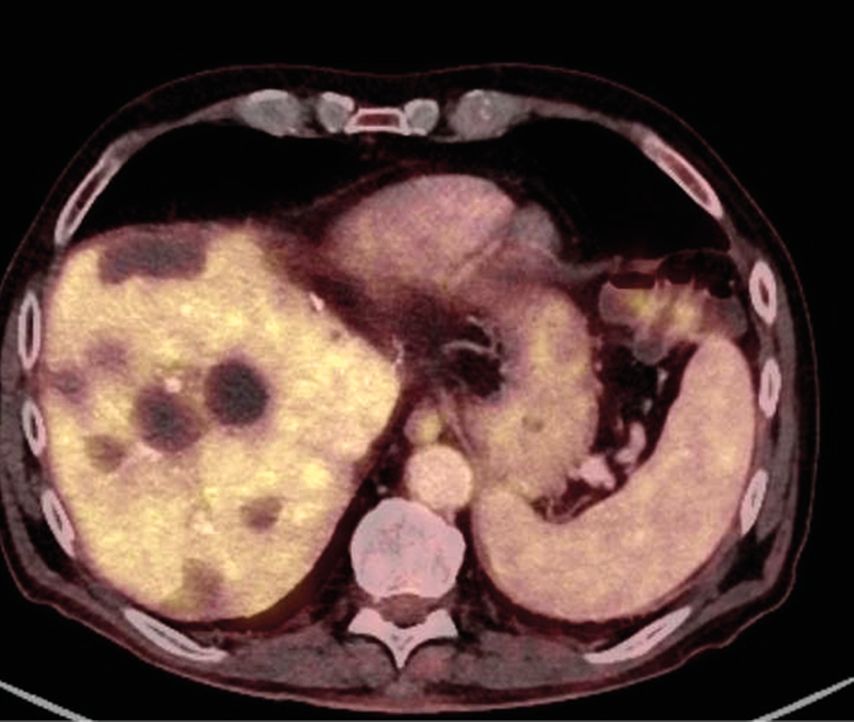
Drei Monate nach Abschluss der adjuvanten Chemotherapie mit FOLFOXIRI/Bevacizumab wurde eine FDG-PET/CT durchgeführt. Der Patient war dabei intraabdominell tumorfrei (Abb. 4). Es zeigten sich jedoch zwei kleine Lungenmetastasen, welche mittels Wedge-Resektionen reseziert werden konnten. Derzeit ist der Patient in Nachsorge und tumorfrei.
Abb. 4: FDG-PET drei Monate nach Abschluss der adjuvanten Chemotherapie mit FOLFOXIRI/Bevacizumab
Fazit
Die komplette Entfernung bzw. Destruktion aller Metastasen ist, wann immer möglich, das Therapieziel, da dadurch die beste Prognose erzielt werden kann. In den meisten Fällen erfolgt dies in Kombination mit perioperativer Chemotherapie. Im konkreten Fall konnten durch ein multimodales Vorgehen mit perioperativer Chemotherapie, ausgedehnter Leberresektion, intraoperativer Mikrowellenablation, stereotaktischer Bestrahlung sowie Lungenresektion alle Metastasen entfernt werden. Eine interdisziplinäre Besprechung der Ausgangssituation und der Restaging-Untersuchungen sollte immer erfolgen. Denn auch wenn bei der initialen Begutachtung eine Resektion nicht durchführbar erscheint, kann diese im Verlauf möglich werden. Die Beurteilung einer eventuellen Resektabilität sollte stets in Zusammenarbeit mit einem erfahrenen leberchirurgischen Zentrum erfolgen.
Autor:
Ao. Univ.-Prof. Dr. Klaus Kaczirek
Universitätsklinik für Allgemeinchirurgie
Medizinische Universität Wien
E-Mail:
klaus.kaczirek@meduniwien.ac.at
Multifokale Lungenkarzinome
Patientin, 76 Jahre bei Erstdiagnose
Onkologische Anamnese
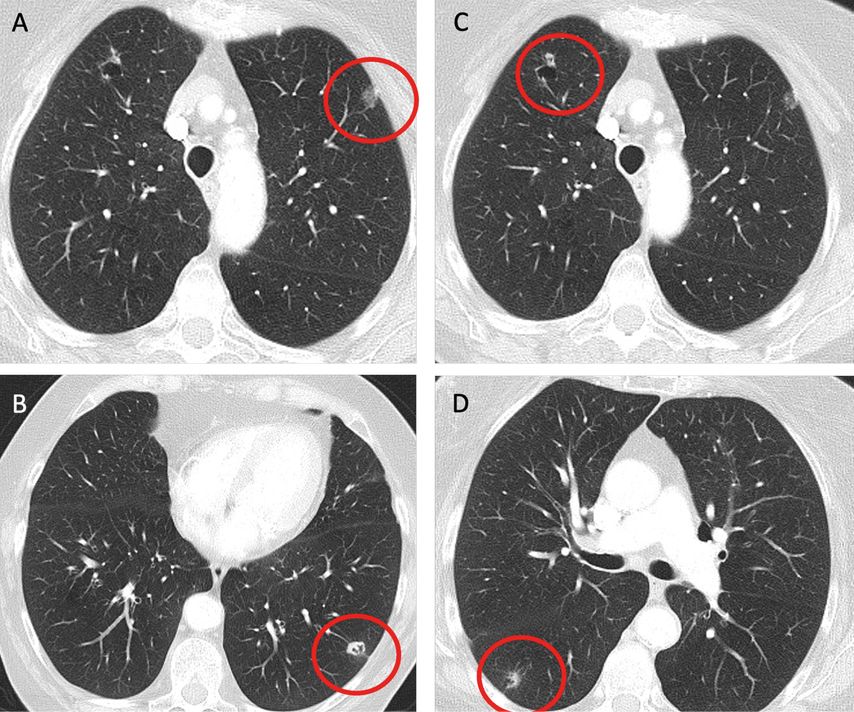
Die Patientin wurde erstmalig im September 2023 mit Verdacht auf multiple pulmonale Metastasen vorgestellt. Anamnestisch ist bei der Patientin ein Urothelkarzinom der linken Niere (St.p. offene Tumorresektion mittels modifizierter Nierenbeckenplastik links, Histologie: pT1 low grade, 09/2018) bekannt. Weiters besteht ein aktiver Nikotinabusus (55 „pack years“). In der Nachsorge-CT von Thorax und Abdomen mit Kontrastmittel zeigte sich kein Hinweis auf ein lokales Tumorrezidiv, allerdings waren pulmonal multiple subsolide Rundherde beidseits festzustellen (Abb. 1).
Abb. 1: Thorax-CT September 2023: suspekte Rundherde (rot eingekreist); A: linker Oberlappen, B: linker Unterlappen, C: rechter Oberlappen, D: rechter Unterlappen
Weitere Abklärung und Therapie
Radiomorphologisch zeigte sich ein hochsuspekter Befund. Differenzialdiagnostisch kamen am ehesten Metastasen oder ein nichtkleinzelliges Lungenkarzinom (NSCLC) in Betracht. Es wurde die Indikation zu einer diagnostischen videothorakoskopischen Operation im Sinne einer Keilresektion der Rundherde unter Durchleuchtung im linken Oberlappen und im linken Unterlappen gestellt. Zuvor wurden die Rundherde aufgrund der geringen Größe und der subsoliden Beschaffenheit CT-gezielt markiert. Eine alternative diagnostische CT-gezielte Biopsie wurde aufgrund der hohen Wahrscheinlichkeit eines inkonklusiven Befundes bei nur teilsoliden Tumoren nicht angestrebt.
Der histologische Befund ergab zwei unabhängige primäre Lungenkarzinome (linker Oberlappen: Adenokarzinom, G2, pT1a, pNX L1, V0, Pn0, R0; linker Unterlappen: rudimentär verhornendes Plattenepithelkarzinom, G2, pT1b, pNX, L0, V0, Pn0, R0). Im interdisziplinären Tumorboard wurde die Nachsorge und im Falle einer Größenprogredienz der Rundherde rechts eine neuerliche Operation nach zuvor durchgeführter kardiorespiratorischer funktioneller Abklärung empfohlen.
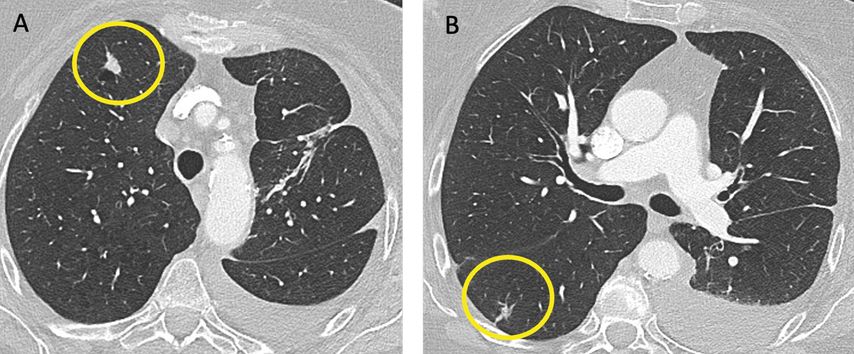
In der nachfolgenden CT des Thorax im Juli 2024 (Abb. 2) zeigten sich die Rundherde im rechten Oberlappen und Unterlappen gering größenprogredient, sodass eine neuerliche videoassistierte Thorakoskopie und parenchymsparende Keilresektionen der Rundherde vorgenommen wurden. Der histologische Befund ergab im rechten Oberlappen im Segment I ein wenig differenziertes, nicht verhornendes Plattenepithelkarzinom G3, pT1b, N0, R0, PD-L1 40%, im rechten Oberlappen, Segment II, keinen Hinweis auf Malignität und im rechten Unterlappen, Segment VI, ein minimal invasives Adenokarzinom, pT1a(mi), R0. Im Oncomine Focus Assay (DNA inkl. Genkopienanalyse/RNA) wurden keine Veränderungen detektiert.
Abb. 2: Thorax-CT Juli 2024: suspekte Rundherde (gelb eingekreist); A: rechter Oberlappen, B: rechter Unterlappen
Tumorboardempfehlung zurTherapie
Aufgrund des langsamen Wachstums sowie der unterschiedlichen Entitäten und Frühstadien aller Lungenkarzinome ist von einer Multifokalität und nicht von Metastasen auszugehen. Es wird daher die Tumornachsorge und keine adjuvante Therapie empfohlen.
Fazit
Die Einschätzung multipler pulmonaler Rundherde, besonders bei einer bekannten onkologischen Anamnese, ist alleine aufgrund der Bildgebung differenzialdiagnostisch häufig nicht eindeutig. Es sollte vor allem bei bekanntem Nikotinabusus immer auch an einen Primärtumor der Lunge gedacht und eine histologische Verifikation angestrebt werden. Eine Lokaltherapie ist die Behandlung der Wahl bei Patient:innen mit multifokalen Primärtumoren der Lunge ohne Metastasierung.
Autor:innen:
Dr. Katharina Sinn
Univ.-Prof. Dr. Clemens Aigner, MBA
Universitätsklinik für Thoraxchirurgie
Medizinische Universität Wien
E-Mail:
clemens.aigner@meduniwien.ac.at
Lokal fortgeschrittenes männliches Mammakarzinom
Patient 1, 58 Jahre bei Erstvorstellung
Onkologische Anamnese
Ein 58-jähriger Mann, wohnhaft in einer Pflegeeinrichtung, tastete im Mai 2023 erstmals eine Verhärtung der linken Mamille. Anamnestisch bestanden an Begleiterkrankungen Diabetes mellitus Typ 2, Vorhofflimmern, Nikotinabusus und eine PAVK IV mit St.p. Amputatio des linken Unterschenkels im November 2020 bei nässender Gangrän/Nekrose. Familienanamnese: Unterleibskrebserkrankung der Mutter im Alter von 37 Jahren.
Bei der Vorstellung in einem auswärtigen Brustzentrum im November 2023 ergab die Biopsie das Vorliegen eines invasiven Mammakarzinoms, NST, G3, ER 80% 3+, PgR 15% 2+, HER2 1+ neg., Ki67 70% im klinischen Stadium IIIB (cT4b [4,2cm] cN1 [bioptisch gesichert]). Die genetische Beratung und Testung erbrachten keinen Hinweis auf das Vorliegen einer ursächlichen Keimbahnmutation. Eine primäre Metastasierung konnte mittels CT von Thorax und Abdomen sowie Ganzkörperknochenszintigrafie ausgeschlossen werden.
Der Patient wurde zur Evaluierung der Möglichkeit einer neoadjuvanten Chemotherapie an der klinischen Abteilung für Onkologie der Universitätsklinik für Innere Medizin 1/AKH Wien vorstellig. In Anbetracht des Allgemeinzustandes des Patienten erschien diese jedoch nicht zielführend. Somit erfolgte die Zuweisung an die Universitätsklinik für Chirurgie, wo am 26. Jänner 2024 eine erste Begutachtung stattfand.
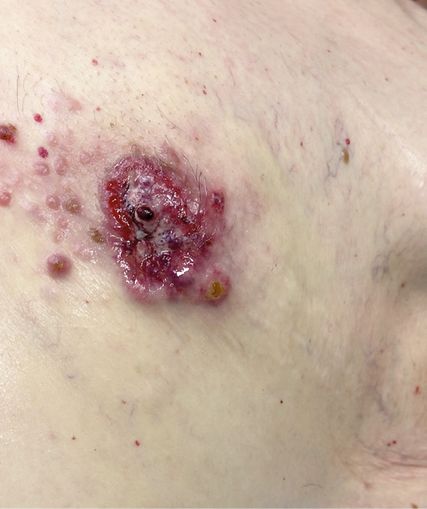
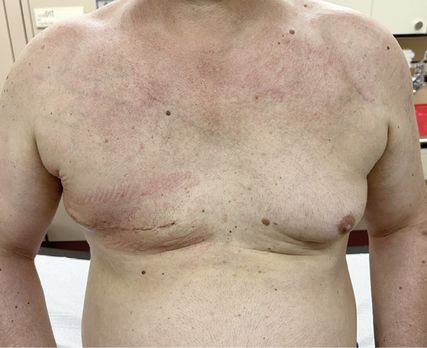
Hier zeigte sich die linke Brustwarze exulzeriert und aufgebraucht, die Haut in einer Ausdehnung von ca. 5cm gerötet mit kleinen kutanen Satellitenläsionen kaudomedial (Abb. 1); in der linken Axilla waren mehrere derbe Lymphknoten palpabel.
Therapie und weiteres Vorgehen
Am 6. Februar 2024 erfolgte eine modifiziert radikale Mastektomie mit axillärer Dissektion. Der finale histologische Befund ergab als Diagnose ein invasives, niedrig differenziertes Mammakarzinom NST vom Luminal-B-/HER2-negativen Subtyp, G3, mit Ulzeration und Satellitenknoten im Bereich der umgebenden Haut (im Gesunden entfernt), mit Lymphgefäßeinbrüchen und ausgedehnter axillärer Lymphknotenmetastasierung, pT4b, pN3a (30/33), L1, V-, R0, ER 90%, PR 20%, HER2 1+ neg., Ki67 80%. Der stationäre Aufenthalt dauerte 15 Tage, die Drainage wurde am 14. Tag entfernt.
Am 15. Februar 2024 empfahl das Tumorboard eine endokrine Therapie und die Evaluierung eines CDK4/6-Inhibitors sowie eine Strahlentherapie. Die klare Kontraindikation gegen Chemotherapie bestand weiterhin.
Weiterer Verlauf
Am 26. März 2024 wurde der Patient aufgrund der Verschlechterung seines Allgemeinzustandes mit Verdacht auf Pneumonie in einem auswärtigen Spital aufgenommen. Anamnestisch war seit zwei Wochen keine orale Nahrungszufuhr erfolgt, dementsprechend imponierte ein Gewichtsverlust von rund 15kg. Im Aufnahmelabor waren neben einer deutlichen CRP-Auslenkung ein akutes Nierenversagen sowie ein massiver Anstieg der LDH auffällig.
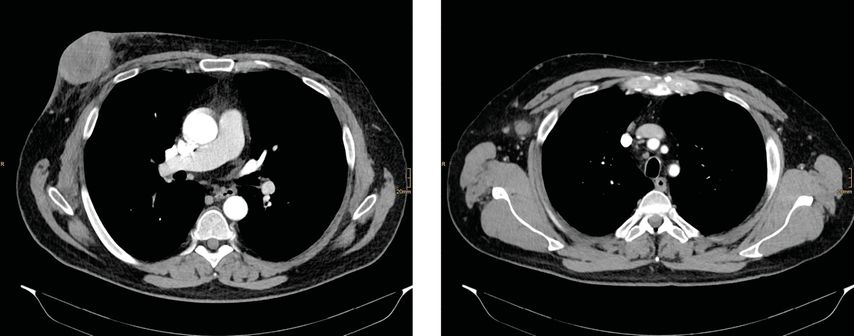
Eine CT von Thorax und Abdomen, die zur weiterführenden Abklärung veranlasst worden war, erbrachte eine spindelige, etwa 3x1cm große Retention an der linken Thoraxwand, in erster Linie einem postoperativen Hämatoserom entsprechend. Darüber hinaus waren eine ausgedehnte Pneumonie im rechten Lungenflügel sowie erstmals eine diffuse, vorwiegend osteoplastische Metastasierung des gesamten Achsenskeletts und multiple Herde im omentalen und mesenterialen Fettgewebe wie bei einer Peritonealkarzinose auffällig.
Nach antibiotischer Therapie, Flüssigkeits- und Elektrolytsubstitution sowie Kostaufbau konnte der Patient am 15. April wieder in die Pflegeeinrichtung entlassen werden.
Bei Wiedervorstellung an der Abteilung für Onkologie am 22. April 2024 zeigte sich zusätzlich zum Tumorprogress ein großflächiger Dekubitus, sodass der Patient auf eine Palliativstation transferiert wurde; er verstarb am 28. April 2024.
Patient 2, 55 Jahre bei Erstvorstellung
Onkologische Anamnese
Ein anderer Patient stellte sich am 2.Februar 2024 erstmals in unserer chirurgischen Ambulanz vor. Er war vom Hausarzt bei Verdacht auf Abszess über sechs Wochen behandelt worden.
Der 55-jährige adipöse Patient gab an, täglich Wein und Schnaps zu konsumieren. Lokal fand sich eine Verhärtung der rechten Mamma/Mamille von ca. 8x8cm Größe, livide verfärbt und nässend und ohne Druckdolenz. Ein Lymphknotenpaket war in der rechten Axilla palpabel.
Die Biopsie ergab ebenfalls als Diagnose ein Mammakarzinom vom Subtyp Luminal B/HER2-negativ, radiologisch cT4b (8cm), cN2: invasiv NST, G3; B5b, ER: 7, PR: 8, HER2: negativ (0%); Ki67: 70%.
Der Befund der genetischen Testung und das Staging erbrachten keinen Hinweis auf das Vorliegen einer familiären Hochrisikosituation bzw. einer primären Metastasierung.
Therapie und weiterer Verlauf
Es wurde darauf eine neoadjuvante Chemotherapie mit 12xPaclitaxel wöchentlich und 4xEC eingeleitet, die unter Alkoholkarenz gut toleriert wurde. Klinisch imponierte ein deutliches Ansprechen. Am 20. August 2024 wurde eine modifiziert radikale Mastektomie ausgeführt. Der histologische Befund ergab ein invasives Mammakarzinom NST, G3, ypT1c (15mm), L1, V0, R0; ER: 80%, PR: 80%, HER2: 1+ neg., Ki67: 10%. In der Axilla fand sich nur noch ein tumorbesiedelter Lymphknoten, entsprechend ypN1a (1/14).
Adjuvant erfolgt nun eine Strahlentherapie der Thoraxwand und des Lymphabflusses. Des Weiteren sind eine endokrine Therapie und eine Behandlung mit einem CDK-4/6-Inhibitor geplant.
Fazit
-
Etwa 1% der Mammakarzinome tritt bei Männern auf. Die Behandlung erfolgt analog dem weiblichen Mammakarzinom.
-
Risikofaktoren für das Auftreten eines Mammakarzinoms beim Mann sind neben einer familiären Disposition (Keimbahn-BRCA2-Mutation) fortgeschrittenes Alter, Alkoholabusus, Adipositas, und Rauchen.
-
Aufgrund geringer Awareness aufseiten der Betroffenen, der Pflegekräfte und Ärzt:innen erfolgt die Diagnose oft erst in einem fortgeschrittenen Stadium.
-
Zum Zeitpunkt der Diagnose besteht bereits bei 30–40% der Patienten eine Lymphknotenmetastasierung.
-
Awareness und Enttabuisierung bleiben eine Herausforderung, doch es gibt bereits Selbsthilfegruppen, Internetseiten der Krebshilfe usw.
-
Wie in der Falldiskussion gezeigt, kann es bei multimorbiden Patienten durch einen Zentrumswechsel zu einem relevanten Zeitverlust vor einer Behandlung kommen.
-
Möglicherweise kann durch die nun bessere Verfügbarkeit von PET-CTs mit speziellen Tracern wie 18F-Fluoroestradiol (FES) eine Metastasierung rascher diagnostiziert werden.
Autor:innen:
Assoc. Prof. Dr. Ruth Exner
Klinische Abteilung für Viszeralchirurgie
Universitätsklinik für Allgemeinchirurgie
Medizinische Universität Wien
E-Mail:
ruth.exner@meduniwien.ac.at
Priv.-Doz. Dr. Maximilian Marhold, PhD
Assoc. Prof. Rupert Bartsch
Klinische Abteilung für Onkologie
Universitätsklinik für Innere Medizin 1 Medizinische Universität Wien
Dr. Fredrik Waneck
Abteilung für Kardiovaskuläre und Interventionelle Radiologie
Universitätsklinik für Radiologie und Nuklearmedizin
Medizinische Universität Wien
Literatur:
1 ESMO Guidelines: Ann Oncol 2024; 35(2): 159-1 2 Lin AP et al.: Br J Surg 2021; 108(9): 1034-42 3 O‘Brien SR et al.: Radiographics 2023; 43(3): e220143
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...