Wechselwirkung und Polypharmazie in der Onkologie
Autorin:
Mag. Katharina Lindner
Anstaltsapotheke
Allgemeines Krankenhaus der Stadt Wien
E-Mail: katharina.lindner@akhwien.at
In der Onkologie gilt es oft, nicht nur die Primärerkrankung – den Krebs – zu behandeln, sondern auch die mit der Erkrankung und den Therapien einhergehenden Komorbiditäten. Mit der Anzahl der Medikationen steigt jedoch das Risiko für unerwünschte Neben- und Wechselwirkungen. Im folgenden Artikel finden Sie eine Übersicht dazu, worauf medizinisches Personal in der Onkologie diesbezüglich besonders achten sollte.
Definition von Arzneimittelinteraktionen und Polypharmazie
Arzneimittelwechselwirkungen (auch Arzneimittelinteraktionen) treten bei gleichzeitiger Einnahme mehrerer Arzneimittel auf. Werden mehr als fünf Arzneimittel eingenommen, spricht man von einer sogenannten Polymedikation. Sind es mehr als 15 Arzneimittel, liegt eine sogenannte exzessive Polymedikation vor. Die durch das Arzneimittel intendierte erwünschte pharmakologische Wirkung kann so mitunter entfallen, abgeschwächt oder unter Umständen sogar verstärkt werden.
Anzumerken ist, dass klinische Effekte von Arzneimittelinteraktionen nicht zwangsläufig bei jedem Patienten auftreten müssen. Zudem sind Ausmaß und Intensität von Patient zu Patient unterschiedlich.1 Grundsätzlich sind Interaktionen bereits vor der Applikation zu beachten. Sinnvoll wäre es daher bei Interaktionen aufgrund von Enzyminhibitionen, zuerst mit einer konservativen Dosis zu beginnen und die Reaktion des Organismus zu beobachten.2
Unerwünschte Arzneimittelwirkungen und Wechselwirkungen
Die Wahrscheinlichkeit für unerwünschte Arzneimittelwirkungen (UAW, Nebenwirkungen) steigt mit der Anzahl der eingenommenen Medikamente drastisch an. Im Allgemeinen muss aufgrund von Arzneimittelwechselwirkungen mit gänzlich unerwarteten pharmakologischen Wirkungen gerechnet werden. Wirkungs- wie auch Nebenwirkungsprofil der einzelnen Medikamente sind zum Teil nicht mehr nachvollziehbar. So muss gegebenenfalls ebenso mit einem Fehlen der erhofften Wirkung gerechnet werden.
Auch das Risiko für das Auftreten von Wechselwirkungen wird mit der Anzahl der eingenommenen Arzneimittel deutlich höher. Bei Anwendung von zwei Arzneimitteln liegt dieses bei ca. 13%, bei sieben gleichzeitig verabreichten Arzneimitteln bereits bei 82%.3 Werden Medikamente oder auch Nahrungsergänzungsmittel von Ärzten verschiedener Fachrichtungen verordnet und liegen zusätzlich nicht genügend wechselseitige Informationen vor, steigt das Risiko für Wechselwirkungen ebenfalls enorm.4
Entscheidend für die Bewertung sind Dauer und Schwere der Interaktion, die Darreichungsform sowie die therapeutische Breite der betroffenen Wirkstoffe.
Nahrungsmittel als eskalierender Faktor
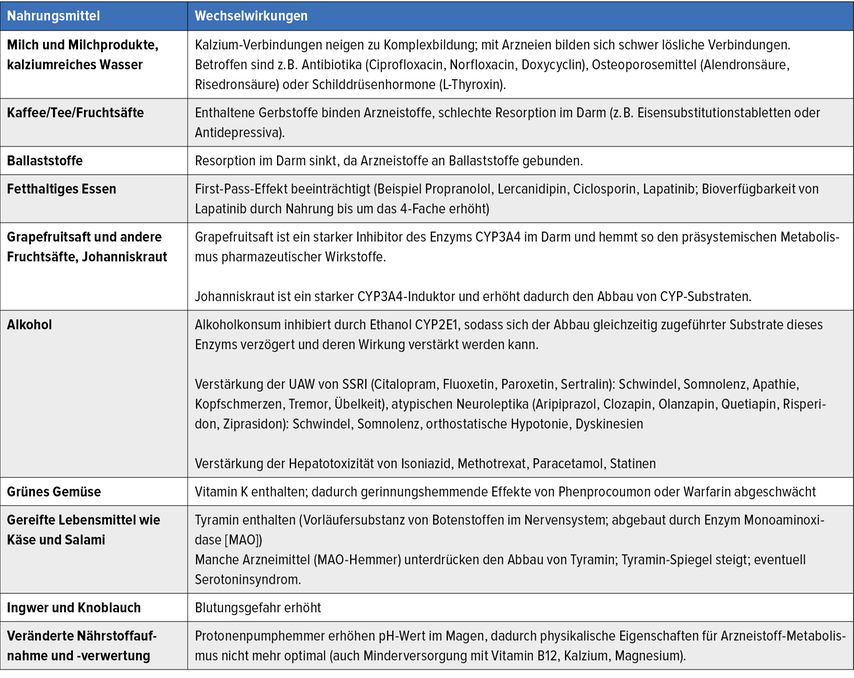
Bereits am vorgeschriebenen Einnahmemodus lässt sich erkennen, wie unterschiedlich Arzneimittel auf Nahrungsmittel reagieren können (Tab. 1). Faktoren wie die Einnahme auf nüchternen Magen, mit einer Mahlzeit, eine Stunde vor dem Essen, zur oder kurz nach einer Mahlzeit können entscheidend für den Therapieerfolg sein.
Ein weiteres Thema sind Flüssigkeiten, mit denen orale Arzneimittel eingenommen werden können. Ein Negativbeispiel dafür sind kalziumreiche Nahrungsmittel wie Milch und Milchprodukte, kalziumangereicherte Fruchtsäfte und kalziumreiche Mineralwässer. Diese können die Wirkungen von Medikamenten durch Komplexbildung (Chelatbildung) durch Ionen mit Bisphosphonaten (z.B. Alendronat, Risedronat), Eisensalzen, Fluoridverbindungen und Strontiumderivaten (z.B. Strontiumranelat) massiv beeinflussen.5
Genetische Polymorphismen
Auch genetische Polymorphismen spielen eine Rolle im Metabolismus. Manche Menschen metabolisieren Arzneistoffe sehr schnell („ultra-rapid metabolizer“), während andere Personen bestimmte Arzneistoffe nur in geringem Ausmaß und sehr langsam umsetzen können („slow metabolizer“).2
Eine Hürde: der Schluckakt
Der Schluckakt ist ein immer wiederkehrendes Thema, das sich stark limitierend auf therapeutische Möglichkeiten im onkologischen Bereich auswirkt. Ist der Schluckvorgang durch Raumforderungen oder das Fehlen der motorischen Bedingungen nicht möglich, muss zwischen parenteraler und enteraler Ernährung entschieden werden. Wird eine Magensonde eingesetzt, werden alle benötigten Medikamente auf ihre Sondengängigkeit bzw. Mörserbarkeit überprüft und gegebenenfalls wird auf andere Präparate umgestellt.
Die onkologische Therapie
Orale Zytostatika sind zum Teil sehr kostenintensive Therapien, die je nach therapeutischem Ansatz bis zum Progress der Erkrankung oder zum Auftreten nicht tolerierbarer Nebenwirkungen zum Einsatz kommen. Sie weisen oft eine sehr schmale therapeutische Breite auf. Das erhebliche Neben- und Wechselwirkungsprofil in Verbindung mit teils komplexen Einnahmevorschriften erschwert die eigenverantwortliche Therapie der onkologischen Patienten und trägt zu einer schlechteren Adhärenz bei.
Eine optimale Therapie kann nur dann erfolgen, wenn Arzneimittel genau nach Vorschrift eingenommen werden. Für viele Menschen, vor allem ältere Personen, ist es nicht leicht, den Überblick über all ihre Arzneien zu behalten. Zudem werden auch häufig Nahrungsergänzungsmittel eingenommen. Viele Patienten bedenken bzw. wissen nicht, dass Arzneimittel durch andere Arzneimittel, Nahrungsergänzungsmittel oder Nahrung in ihrer Wirkung beeinflusst werden können. Hier ist eine umfassende Aufklärung vonnöten.
Im Gegensatz zu einer intravenös verabreichten Chemotherapie, die in Dosierung und Zusammensetzung genau auf die Parameter des Patienten (Allgemeinzustand, Gewicht, Nierenfunktion etc.) abgestimmt wird, erfolgt die Dosierung oraler Onkologika relativ „ungestützt“ von derartigen Informationen bzw. sind die Informationen bei Zulassung hinsichtlich der Pharmakokinetik und deren Abhängigkeit z.B. von der Ernährung oft sehr dürftig.
Dadurch kann es dazu kommen, dass Medikamente entweder in zu hohen oder in nicht adäquaten Mengen in der Blutbahn vorliegen. Die Resorption ist von Mensch zu Mensch unterschiedlich und hängt unter anderem vom individuellen Lebensstil des Patienten ab. Ein repräsentatives Beispiel dafür stellt Lapatinib dar. Die Bioverfügbarkeit ist in Abhängigkeit von der Art der Nahrung um etwa das Zwei- bis Dreifache höher, wenn Lapatinib eine Stunde nach einer Mahlzeit im Vergleich zu einer Stunde vor der ersten Tagesmahlzeit eingenommen wird.
Viele orale Zytostatika werden über CYP-Isoenzyme (besonders CYP3A4) metabolisiert. Auch für Angehörige medizinischer Fachkreise ist es oftmals schwierig, den Überblick zu behalten. Die teilweise recht unübersichtliche Fachinformation hilft hier auch nicht weiter.
Komorbiditäten im onkologischen Setting
Patienten, die in einem onkologischen Setting therapiert werden, leiden zum Teil an unterschiedlichen Komorbiditäten. Da nicht nur geriatrische Patienten, sondern Menschen in allen Lebensabschnitten betroffen sein können, variieren potenzielle Komorbiditäten entsprechend. Die Zusatzerkrankung stellt ein eigenes, diagnostisch abgrenzbares Krankheitsbild dar, das nicht selten kausal mit der Grunderkrankung zusammenhängt. Die Zusatzerkrankung kann aber auch unabhängig von der Grunderkrankung sein.
Psychiatrische Zusatzmedikation
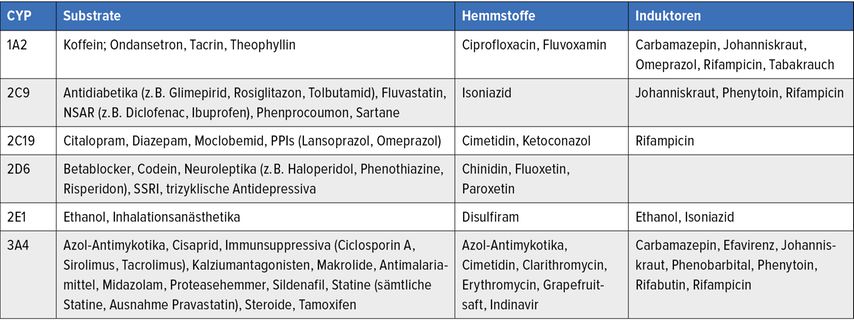
Ein wichtiger Punkt sind die durch die Krebserkrankung hervorgerufenen therapiebedürftigen psychischen Belastungen und Angstzustände. Viele Psychopharmaka werden über CYP-Enzyme in der Leber metabolisiert. Eine für den Arzneistoffmetabolismus verantwortliche wichtige Enzymgruppe stellen die Cytochrom-P450(CYP450)-Isoenzyme dar. Ihre Aufgabe besteht darin, eine Vielzahl von Wirkstoffen (z.B. Warfarin, Phenytoin, Chinidin, Tolbutamid und Cyclosporin) zu oxidieren (Tab. 2).6
Tab. 2: Die für den Arzneimittelmetabolismus wichtigsten CYP450-Enzyme, die von ihnen verstoffwechselten Arzneistoffe (Substrate), ihre Hemmstoffe und Induktoren (Beispiele). Modifiziert nach Tatro SD2 & Goldberg RM et al.3
Das wohl bekannteste Isoenzym der CYP-Familie ist jedoch CYP3A4. Etwa ein Drittel aller Leberenzyme gehört zu diesem Subtyp und ca. 40% aller Arzneistoffe werden hier über den Phasen-Metabolismus umgewandelt bzw. abgebaut. Werden Medikamente hier blockiert (Enzyminhibition) oder zu schnell abgebaut (Enzyminduktion), kann es zu fehlender Wirkung oder vermehrten unerwünschten (Neben-)Wirkungen kommen.
Wirkstoffinteraktionen auf dieser Ebene kommen also durch Inhibition oder Induktion dieser Isoenzyme zustande. Wird ein CYP-Isoenzym inhibiert, so wird die Metabolisierung des Wirkstoffes gedrosselt, der das Substrat dieses CYP-Enzyms ist, weshalb es in der Folge zu einem erhöhten Serumspiegel des Wirkstoffes (des Substrates) kommt.2
Umgekehrt ist es bei einer Induktion des CYP-Enzyms. Wird dieses induziert, so metabolisiert es sein Substrat vermehrt, was eine Senkung des Substrat-Wirkstoff-Spiegels zur Folge hat. Dies kann mithilfe von Carbamazepin veranschaulicht werden. Carbamazepin induziert CYP2C9, weshalb die Phenytoin-Serumkonzentration aufgrund des vermehrten Metabolismus gesenkt wird. Als Beispiele für weitere Enzyminduktoren gelten Phenobarbital, Phenytoin und Rifampicin.
Liegt daher eine Therapie mit einem Wirkstoff vor, der ein CYP-Substrat darstellt, und wird nun ein weiterer Wirkstoff zur Therapie hinzugefügt, der ein Induktor des CYP-Isoenzyms ist, so sollte man die Dosis des Substrat-Wirkstoffs so anpassen, dass die enzyminduzierende Wirkung des anderen Wirkstoffs berücksichtigt wird. Nach Absetzen des Induktors muss ebenfalls die Dosis des Wirkstoffs adaptiert werden.2
Ebenso darf nicht außer Acht gelassen werden, dass es zu Variationen der Affinität eines Enzyms zum Substrat kommen kann. Bei den CYP2D6-Inhibitoren sinkt die Affinität beispielsweise: Fluoxetin >Sertralin > Fluvoxamin. Auch bei CYP2C19 kann die Affinität bei bestimmten Wirkstoffen variieren: Fluvoxamin > Fluoxetin > Sertralin.2
Ein weiteres Beispiel für Arzneimittelinteraktion durch Enzyminduktion/-inhibition ist der Verzehr von Grapefruits bzw. Grapefruitsaft. Zwar erfolgen 95% der Arzneistoffmetabolisierung durch CYP-Enzyme in der Leber, doch auch in der Mukosa des Dünndarms sind CYP-Enzyme lokalisiert, die Xenobiotika bereits vor dem Übertritt in den Pfortaderkreislauf metabolisieren und somit den Organismus und insbesondere die Leber vor möglichen Schäden durch mit der Nahrung aufgenommene Fremdstoffe schützen. Der Haupteffekt der Grapefruitinhaltsstoffe besteht in der irreversiblen Hemmung dieser intestinalen CYP3A4-Enzyme. P-Glykoproteine (P-gp) und organische Anionentransporter des Typs 1A2 (OAT 1A2) werden ebenfalls gehemmt.7
Die intestinalen CYP3A4-Enzyme bewirken eine präsystemische Metabolisierung bestimmter Arzneistoffe bereits in den Enterozyten des Darms. Die CYP3A4-Hemmung führt so zur Wirkungsverstärkung von Arzneistoffen, die sonst durch CYP3A4 normalerweise bereits in der Darmmukosa inaktiviert und damit nicht in vollem Umfang bioverfügbar werden. Umgekehrt führt die CYP3A4-Hemmung durch Grapefruitinhaltsstoffe bei Prodrugs (z.B. Felodipin), die erst durch CYP3A4 bioaktiviert werden, zur Wirkungsabschwächung.
Entscheidend ist hierbei die Tatsache, dass bei lebensmittelüblichen Zufuhrmengen von Grapefruitprodukten nur die intestinalen CYP3A4-Enzyme gehemmt werden, während die hepatischen CYP3A4-Enzyme erst bei exzessivem Grapefruitkonsum jenseits der üblichen Verzehrgewohnheiten betroffen sind.
Da es sich bei der CYP3A4-Inhibition um eine irreversible Suizidhemmunghandelt, ist der Effekt bereits kurz nach dem Verzehr üblicher Grapefruitmengen voll ausgeprägt und hält bis zu drei Tage an. Erst durch die sukzessive Neusynthese des Enzyms wird die Hemmung aufgehoben. Daher muss der Patient während der gesamten Therapiedauer mit Arzneistoffen, für die diese Art der Interaktion relevant ist, auf Grapefruitprodukte verzichten. Eine zeitversetzte Einnahme bietet keinen ausreichenden Schutz.
Hämatologische Komorbiditäten
Komorbiditäten ergeben sich beispielsweise auch durch ein nicht intaktes Blutbild. Fehlen Granulozyten, ist das Abwehrsystem des Körpers geschwächt und es kann eine antibiotische und antimykotische Abschirmungsprophylaxe erforderlich sein. Ein schwankender Thrombozytenwert und das Fehlen von körperlicher Bewegung verursachen in Kombination mit der onkologischen Grunderkrankung veränderte Gerinnungsparameter, die regelmäßig kontrolliert und gegebenenfalls therapiert werden müssen.
Nicht nur eingenommene Arzneimittel, sondern auch z.B. Vitamin-K-haltige Nahrungsmittel (wie Spinat) beeinflussen orale Antikoagulanzien vom Cumarin-Typ (z.B. Phenprocoumon, Acenocoumarol, Warfarin) und führen durch die verstärkte Vitamin-K-Zufuhr zu einer Wirkungsabschwächung. Ärzte und Patienten sollten sich auch der Möglichkeit einer Wechselwirkung von Vitamin-K-Antagonisten und Bestandteilen moderner Ernährung („Superfood“) wie z.B. Goji-Beeren bewusst sein.8 Bei Patienten, die Vitamin-K-Antagonisten in Kombination mit Goji-Beeren zu sich nahmen, wurden eine INR-Erhöhung (Verlängerung der Gerinnungsdauer) und eine damit verbundene Blutungsneigung verzeichnet.
Bei 90% der kommerziell verfügbaren Goji-Beeren handelt es sich um Früchte von Lycium barbarum aus der Familie der Nachtschattengewächse. Die Beeren finden seit langer Zeit Verwendung in der traditionellen chinesischen Medizin – aufgrund der ihnen nachgesagten „gesundheitsfördernden“ Wirkung werden sie auch in Europa zunehmend in unterschiedlichen Formulierungen vermarktet (Tabletten, Tee, Säfte, Konzentrate etc.). Fallberichte, die durch das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) vorgestellt wurden, deuten darauf hin, dass auch die Inhaltsstoffe von Goji-Beeren, vermutlich über eine Blockade von CYP2C9, die Plasmaspiegel der Cumarine steigern.
Der genaue Mechanismus ist nicht bekannt. Patienten, die Vitamin-K-Antagonisten einnehmen, sollten Zubereitungen vermeiden, die Goji-Beeren enthalten, wie z.B. Tees, Marmeladen etc.9
Übelkeit und Erbrechen bei Krebstherapie
Antiemetika sind ein nicht wegzudenkender Teil der onkologischen Therapie. Übelkeit und Erbrechen gehören zu den am stärksten belastenden Nebenwirkungen medikamentöser Tumortherapie. Intensität und Dauer der Symptomatik sind abhängig von der Art der antineoplastischen Behandlung, der Kombination mit anderen Medikamenten und von patientenindividuellen Faktoren. Unterschieden werden akute und verzögerte Symptomatik sowie antizipatorisches Erbrechen.
Die antiemetische Prophylaxe richtet sich nach dem emetogenen Potenzial der Therapie. 5-HT3-Rezeptor-Antagonisten sind sehr wirksam in der Prophylaxe von akuter Emesis. Eine häufig beschriebene Nebenwirkung ist zum Beispiel Obstipation. Hierbei kann es zu EKG-Veränderungen kommen, was wiederum eine engmaschige Kontrolle bei möglicher Kombination mit LQTS-fördernden Wirkstoffen erforderlich macht.
Auch NK1-Rezeptor-Antagonisten werden zur antiemetischen Therapie eingesetzt. Diese werden mit Dexamethason kombiniert und sind in der Regel gut verträglich. Die Vertreter Aprepitant, Fosaprepitant und Netupitant sind moderate Inhibitoren von CYP3A4. Daher ist bei kombinierter Anwendung mit Dexamethason, welches ebenfalls über CYP3A4 metabolisiert wird, die Dosis von Dexamethason zu halbieren. Diese Empfehlung trifft jedoch ausschließlich auf die 20mg-Dexamethason-Dosierung zu, nicht aber auf die Dexamethason-Gaben in Höhe von 8mg oder 12mg.
Bisher existieren jedoch nur Daten zu Aprepitant. Vermutete Interaktionen von Aprepitantmit Zytostatika wie Docetaxel, Vincristin oder Etoposid konnten bisher nicht bestätigt werden. Rolapitant ist ein moderater Inhibitor von CYP2D6. Kortikosteroide sind indiziert in der Prophylaxe von verzögerter Emesis.
Wechselwirkungen bei Analgesie
Ein weiterer zentraler Punkt ist die Schmerztherapie bei onkologischen Patienten. NSAR (nichtsteroidale Antirheumatika) sind aus der Arzneimitteltherapie nicht mehr wegzudenken. Das Interaktionspotenzial wird jedoch oft unterschätzt. Zusammen mit ACE-Inhibitoren gegeben, steigt die Gefahr des akuten Nierenversagens. Die Anwendung gemeinsam mit ß-Blockern, Diuretika, ACE-Inhibitoren oder Sartanen fördert die Blutdrucksenkung, erhöht aber gleichzeitig auch das Risiko für eine Hyperkaliämie. Die Kombinationstherapie mit Antidepressiva, Diuretika oder Antikonvulsiva erhöht das Risiko für das Auftreten einer Hyponatriämie (über das Syndrom inadäquater ADH-Sekretion [SIADH]).
Das Blutungsrisiko im gastrointestinalen Bereich steigt bei gleichzeitiger Einnahme von NSAR mit SSRI (selektive Serotonin-Wiederaufnahme-Hemmer, z.B. Fluoxetin), oralen Antikoagulanzien, Acetylsalicylsäure oder Kortikoiden an. Eine Anamnese muss demnach regelmäßig und sorgfältig durchgeführt werden, um möglichst viele Aspekte im Sinne einer potenziellen Arzneimittelinteraktion zu berücksichtigen.
Ein weiteres Risiko stellt die oftmals vorkommende Kombination von einem SSRI und Tramadol dar. Beide Substanzen weisen ein unterschiedlich starkes proserotonerges Potenzial auf, wodurch das Risiko für eine Serotonin-Toxizität in Kombination erhöht wird. Zudem können beide Arzneimittel dosisabhängig das QT-Intervall verlängern.
Wird diese Kombination eingesetzt, sollten vor allem bei höheren Dosierungen und Risikokonstellationen EKG-Kontrollen und bei relevanter QTc-Verlängerung Blutuntersuchungen (Kalium, Magnesium) durchgeführt werden. Zudem kann Fluoxetin die Metabolisierung von Tramadol in den aktiven Metaboliten O-Desmethyltramadol in relevantem Maße hemmen, was zu einer verminderten analgetischen Wirkung führen kann.
Insgesamt scheint eine derartige Kombination daher nicht empfehlenswert. Alternativ wird dazu geraten, ein anderes nicht proserotonerges Opioid oder allenfalls ein anderes Antidepressivum (nicht SSRI oder zumindest keinen CYP2D6-Inhibitor in Kombination) zu verwenden. Man muss auch beachten, dass die Inhibition des CYP2D6 durch Fluoxetin aufgrund der langen Halbwertszeit seines Metaboliten (Norfluoxetin) bis zu 2–3 Wochen nach Absetzen andauern kann.
Medikamente auf Interaktionen prüfen
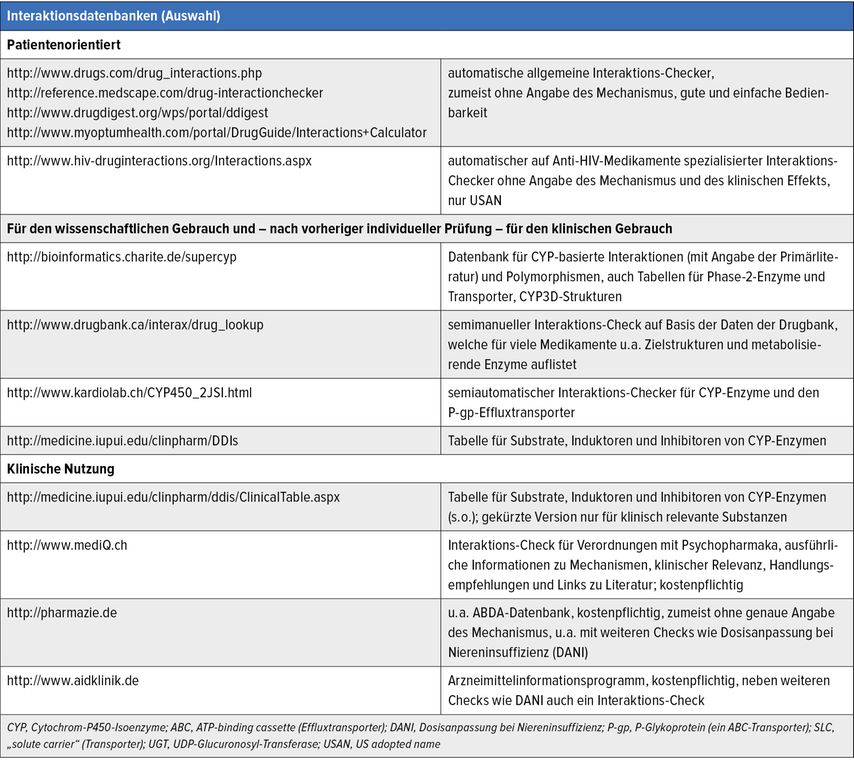
In Tab. 3 sind wichtige und praktikable Werkzeuge und Informationsressourcen zusammengestellt. Je nach den individuellen Anforderungen und nach dem therapeutischen Fachbereich gibt es Schwerpunkte und Limitationen dieser Tools.
Schlussfolgerung
Arzneimittelinteraktionen aufgrund von Komorbiditäten und Polypharmazie sollten im klinischen Alltag nicht unterschätzt werden, sind diese doch mit steigender Morbidität und einer erhöhten Mortalitäts- und Hospitalisierungsrate verbunden. Einer US-amerikanischen Studiezufolge wird rund ein Viertel der vermeidbaren Krankenhausaufnahmen durch Arzneimittelwechselwirkungen verursacht.10,7
Grundsätzlich zeigt die Vielzahl an Publikationen zum Thema Arzneimittelinteraktion die große Bedeutung einer gut durchdachten Kombination von Medikamenten in Bezug auf eine erfolgreiche Therapie.
Im klinischen Alltag ist es wichtig, bei jeder Änderung einer bestehenden Arzneimitteltherapie (d.h. Absetzen eines Wirkstoffes, Neuverordnung einer Therapie und Dosisveränderungen) an die Möglichkeit des Auftretens von Arzneimittelwechselwirkungen zu denken. Für die schnelle Informationsbereitstellung eignen sich am besten Kitteltaschenfolder bzw. Cytochromtabellen mit den wichtigsten Wechselwirkungen.
Datenbankgestützte Wechselwirkungsprogramme ermöglichen es, einen schnellen Überblick über komplexe Polymedikationsverschreibungen zu erlangen, wobei man sich der Grenzen dieser Hilfestellungen durchaus bewusst sein muss (z.B. Overalerting, fragwürdige klinische Relevanz, mangelnde Sensitivität und Spezifität). Aus Sicht der Autorin kann eine elektronische Datenbankprüfung auf Wechselwirkungen die individuelle Fall-zu-Fall-Beurteilung der klinischen Relevanz von Interaktionen durch Arzneimitteltherapieexperten, wie z.B. klinische Pharmazeuten und Arzneimittelinformationsapotheker, nicht ersetzen.
In den meisten Zentren ist eine derartige Beratungsleistung über die jeweilige Krankenhausapotheke konsiliarisch verfügbar. Die Integration dieser Expertise in multiprofessionelle Behandlungsteams ist essenziell, damit sich alle Gesundheitsberufe bei immer komplexer werdenden Therapien auf spezifische Fragestellungen fokussieren können.
Literatur:
1 Van Roon EN et al.: Clinical relevance of drug-drug interactions: a structured assessment procedure. Drug Saf 2005; 28(12): 1131-9 2 Tatro SD: Drug Interaction Facts 2011: the Authority on Drug Interactions. Saint Louis: Wolters Kluwer Health/Facts & Comparisons, 2011. Seiten xvii-xxxiii-xxxiv 3 Goldberg RM et al.: Drug-drug and drug-disease interactions in the ED: analysis of a high-risk population. Am J Emerg Med 1996; 14(5): 447-50 4 Bjerrum L et al.: Risk factors for potential drug interactions in general practice. Eur J Gen Pract 2008; 14: 23-9 5 Aktories K et al.: Allgemeine und spezielle Pharmakologie und Toxikologie. 11. Auflage. München: Elsevier, 2013 6 Biesalski HK et al.: Ernährungsmedizin. 4. Auflage. Stuttgart: Thieme Verlag, 2010 7 McDonnell PJ et al.: Hospital admissions resulting from preventable adverse drug reactions. Ann Pharmacother 2002; 36(9): 1331-6 8 Okafor HU et al.: Therapeutic efficacy and effect on gametocyte carriage of an artemisinin and a non-based combination treatment in children with uncomplicated P. falciparum malaria, living in an area with high-level chloroquine resistance. J Trop Pediatr 2010; 56(6): 398-406 9 BULLETIN ZUR ARZNEIMITTELSICHERHEIT, Informationen aus BfArM und PEI, Ausgabe 03/2013 10 Dechanont S et al.: Hospital admissions/visits associated with drug–drug interactions: a systematic review and meta-analysis. Pharmacoepidemiol Drug Saf 2014; 23(5): 489-97 11 Fernandez N et al.: Effects of dietary factors on levodopa pharmacokinetics. Expert Opin Drug Metab Toxicol 2010; 6(5): 633-42
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...