Revisionsmöglichkeiten nach arthroskopischer Rotatorenmanschettenrekonstruktion
Autor:innen:
Dr. Angelika Schwarz
Prim. Dr. Michael Plecko
Unfallkrankenhaus Steiermark
Graz
E-Mail: angelika.schwarz@auva.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Notwendigkeit einer Revision nach arthroskopischer Rotatorenmanschettenrekonstruktion stellt eine klinische Herausforderung dar, insbesondere bei Patient:innen mit Rezidivrupturen.
Keypoints
-
Der Muskelstatus und patientenspezifische Faktoren sind entscheidend für den Erfolg einer Revisionsoperation.
-
MRT und/oder Arthro-MRT sind entscheidend, um die richtige Revisionsstrategie festzulegen.
-
Bei jüngeren aktiven Patient- :innen gibt es eine Vielzahl an Therapieoptionen, sowohl als arthroskopische als auch als offene Verfahren.
-
Die inverse Schultertotalendoprothese ist eine effektive Therapieoption mit einer niedrigen Schwankungsbreite in den Ergebnissen.
-
Die inverse Schultertotalendoprothese ist die Methode der Wahl bei Cuff-Arthropathien – auch in der Revision.
Rotatorenmanschettenrupturen gehören zu den häufigsten Verletzungen, die in der Orthopädie und Traumatologie behandelt werden und sind die häufigste Ursache für den Funktionsverlust und Schmerzen in der Schulter. Rotatorenmanschettenverletzungen, die von Tendinopathien über partielle bis hin zu vollständigen Rissen reichen, nehmen mit dem Alter deutlich zu. Während sie bei Patient:innen unter 30 Jahren nur in 10% der Fälle auftreten, steigt die Häufigkeit bei über 80-Jährigen auf über 60%; unabhängig davon, ob Symptome vorhanden sind.1 Während jüngere Patient:innen häufiger von traumatischen Rupturen betroffen sind, dominieren im Alter degenerative Schäden.2
Rotatorenmanschettenrekonstruktionen wurden erstmals 1911 von Codman beschrieben.3 Seitdem haben fortschrittliche arthroskopische Techniken dieses Verfahren grundlegend verändert und gelten als das Standardverfahren. Obwohl die arthroskopische Rotatorenmanschettenrekonstruktion im Vergleich zu vielen anderen orthopädischen Eingriffen mit einer geringen Morbidität einhergeht, treten dennoch Komplikationen auf, die für die Patient:innen langfristige Folgen haben können. Die Notwendigkeit einer Revision nach arthroskopischer Rotatorenmanschettenrekonstruktion stellt eine klinische Herausforderung dar, insbesondere bei Patient:innen mit Rezidivrupturen.
Fortschritte in der Arthroskopie, Prothetik und Pathoanatomie haben neue Behandlungsansätze eröffnet. Dieser Artikel beleuchtet die klinischen Implikationen von Rerupturen und deren optimale Behandlungsmöglichkeiten sowie weitere spezielle Revisionsgründe.
Revisionsgründe
Fehlgeschlagene Rotatorenmanschettenrekonstruktionen können auf verschiedene Faktoren zurückgeführt werden.
-
Es handelt sich generell entweder um ein strukturelles Versagen – Reruptur –
-
oder ein funktionelles Versagen – Pseudoparalyse oder Funktionsdefizit.
Insgesamt treten Komplikationen bei arthroskopischen und offenen Verfahren in vergleichbarer Häufigkeit auf. Mansat et al. diskutierten eine Metaanalyse hinsichtlich offener Repairs und berichteten über eine Gesamt-Komplikationsrate von 10,5%.4 Bei arthroskopischen Eingriffen an der Schulter wurden im Literaturkorpus ähnliche Gesamt-Komplikationsraten mit 10,6% berichtet.5–7
Reruptur
Rerupturen nach einer Rotatorenmanschettenrekonstruktion sind häufig und wurden mit Raten von 13 bis 94% dokumentiert, obwohl die klinischen Ergebnisse nach der Operation in vielen Fällen zufriedenstellend sind.8 Die aktuelle Studienlage berichtet über inhomogene Rerupturraten von 10 bis zu 57%.9–15 Eine Rezidivruptur der Rotatorenmanschette ist ein komplexer, multifaktorieller Prozess. Zu den Risikofaktoren zählen Patientenmerkmale, die Morphologie der Ruptur und der Schulter, die gewählte Rekonstruktionstechnik sowie die Rehabilitationsstrategien.12,15–18 Insbesondere die Größe des Defektes und das Alter der Patient:innen gelten als zentrale Prädiktoren. Mit zunehmendem Alter zeigt sich ein linearer Anstieg der Rezidivrate um etwa 5% pro Dekade, wobei ab dem 70. Lebensjahr ein deutliches Risiko und ein deutlicher Anstieg für erneute (Re)Rupturen besteht.12,15
Der Double-Row-Repair führt zu strukturell besseren Ergebnissen mit geringeren Rerupturraten. Allerdings zeigen Studien keine signifikanten Unterschiede im klinischen Outcome zwischen der Single-Row- und der Double-Row-Versorgung.19–23 Typische Versagensmodi nach verschiedenen Repair-Techniken umfassen bei allen Techniken den „failure in continuity“. Bei der Single-Row-Technik tritt häufig eine laterale Reruptur oder ein „failure to heal“ am Footprint auf. Die Double-Row-Technik ist anfällig für lokale Rerupturen am medialen Anker, die durch das Durchschneiden der Fäden verursacht werden („medial cuff failure“). Bei der Suture-Bridge-Technik kann es ebenso zu einem „medial cuff failure“ kommen, wobei das Sehnengewebe am Footprint intakt bleibt. Darüber hinaus tritt gelegentlich ein lateraler Fixationsverlust der Suture-Bridge auf.15, 24, 25
Pseudoparalyse
Die Pseudoparalyse ist definiert als die Unfähigkeit, den Arm aktiv – trotz vollständiger passiver Beweglichkeit – über 90° anzuheben. Funktionsstörungen des Musculus subscapularis und Musculus supraspinatus oder von drei Rotatorenmanschettenmuskeln stellen wesentliche Risikofaktoren dar.26 Beim primären arthroskopischen Rotatorenmanschetten-Repair kann bei 90% der Patient:innen eine Rückbildung der Pseudoparalyse erreicht werden, während die Erfolgsrate bei Revisionseingriffen lediglich 43% beträgt.27
Spezielle Revisionsgründe
Die Rolle der Nervus-suprascapularis-Neuropathie bei Rerupturen wird kontrovers diskutiert. Mediale Retraktionen posterosuperiorer Rupturen könnten theoretisch den Nervus suprascapularis übermäßig belasten, wenngleich keine eindeutige Evidenz für eine routinemäßige Freilegung des Nervus suprascapularis vorliegt. Zudem ist die Diagnose schwierig – da Symptome wie Schmerz, Schwäche und Atrophie nicht eindeutig vom klinischen Bild einer Reruptur unterscheidbar sind.28
Seltenere chirurgische Komplikationen nach Rotatorenmanschettenrekonstruktionen umfassen zudem eine Musculus-deltoideus-Insuffizienz, Chondrolyse oder Osteonekrose, Fremdkörperreaktionen, Implantatversagen oder -dislokation und intraoperative Frakturen.4, 5, 29 Infektionen treten selten auf und variieren je nach Verfahren mit einer Rate von 0,27% bis 1,9% bei Mini-open-Verfahren und 0,23–0,4% bei arthroskopischen Eingriffen.15, 29, 30 Postoperative Komplikationen wie eine „captured shoulder“ – eine Verklebung der Rotatorenmanschette am Akromion31 – sowie neurologische Komplikationen (neben dem oben genannten Nervus suprascapularis besonders der Nervus axillaris und Nervus musculocutaneus)4,7,29 sind ebenfalls zu benennen. Sensorische Neuropathien oder das CRPS32 sollten ebenfalls berücksichtigt werden.
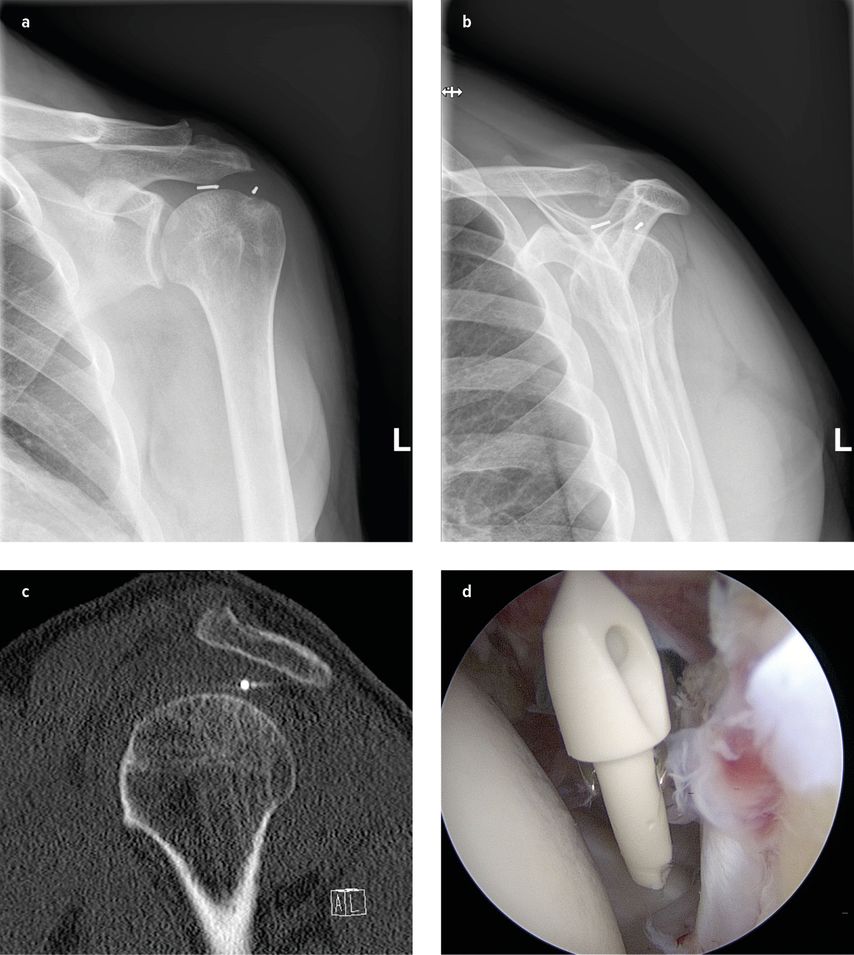
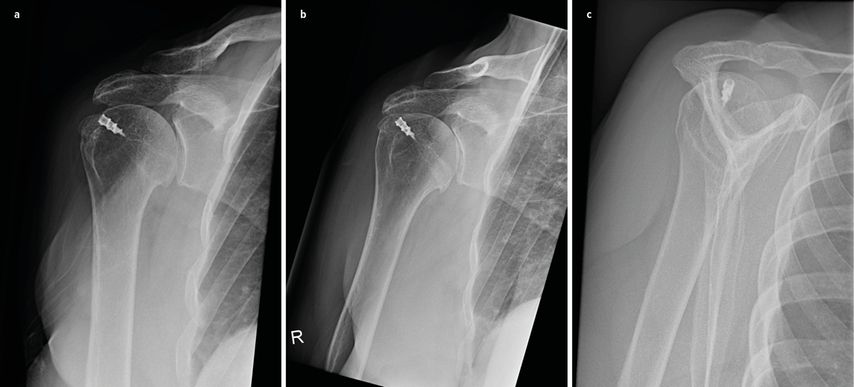
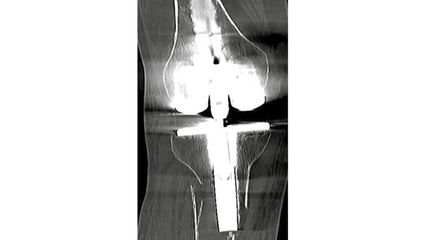
Abb. 1:Röntgen in 2 Ebenen und CT einer Reruptur mit disloziertem Anker und intraoperativer arthroskopischer Implantatentfernung
Diagnostik und Bildgebung
Die präzise Analyse der zugrunde liegenden Pathologie ist entscheidend für die Planung eines erfolgreichen Revisionseingriffs nach Rotatorenmanschettenrekonstruktion. Eine umfassende Diagnostik umfasst eine detaillierte Anamnese, eine gründliche klinische Untersuchung sowie den gezielten Einsatz bildgebender Verfahren.33, 34 Das Vorliegen einer Pseudoparese weist klinisch häufig auf eine Reruptur hin.
-
Röntgenaufnahmen: Standardmäßig werden Röntgenaufnahmen der Schulter in drei Ebenen angefertigt, um den knöchernen Zustand, die Gelenkskongruenz sowie das Vorhandensein und die Position des Implantats zu bewerten.
-
Eine Erweiterung erfolgt gegebenenfalls per Computertomografie (CT) oder CT-Arthrografie.
-
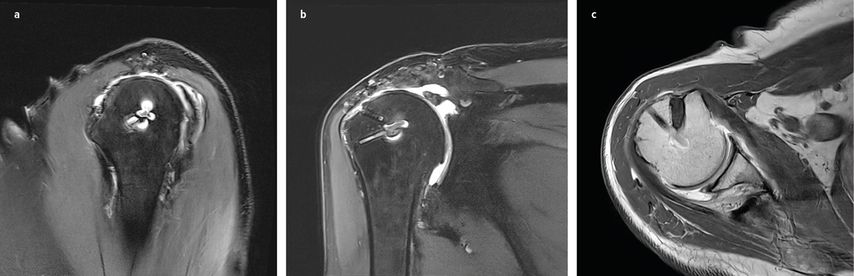
Magnetresonanztomografie (MRT): Das MRT, häufig auch als hochauflösende MRT-Arthrografie, spielt eine zentrale Rolle in der Diagnostik. Nach operativen Eingriffen kann die Aussagekraft jedoch durch Metallartefakte oder Narbengewebe eingeschränkt sein, was die Interpretation erschweren kann. Bei der Interpretation des MRTs muss berücksichtigt werden, dass sich die Rotatorenmanschette auch nach bis zu 12 Monaten noch in der Heilungsphase befinden kann. Areale mit Signalanstieg können einer Reruptur ähneln. Rerupturen sind am deutlichsten in den T2- und PD-gewichteten Schichten beurteilbar.25
-
Sonografie: Obwohl die Genauigkeit der Sonografie stark von der Erfahrung des Untersuchers abhängt, bietet sie den Vorteil, dynamisch eingesetzt werden zu können.
Eine gezielte Auswahl und Kombination dieser diagnostischen Verfahren gewährleistet eine optimale Beurteilung der zugrunde liegenden Pathologie und bildet die Grundlage für die Planung einer adäquaten Revisionsstrategie.35–37
Der Muskelstatus ist entscheidend für den Erfolg der Revisionschirurgie und wird durch die Goutallier-Klassifikation hinsichtlich der fettigen Infiltration beurteilt. Eine geringe Infiltration (Grad 0–1) ist vielversprechend für eine erfolgreiche Rekonstruktion, während eine höhere Infiltration (Grad 2–4) das Risiko für eine (Re)Reruptur und progrediente Muskeldegeneration erhöht. Goutallier et al. zeigten mit einer klinischen Folgestudie nach Index- Beschreibung der Klassifikation im CT 1994, dass präoperative Atrophien mit höheren Rerupturraten assoziiert sind, insbesondere im fortgeschrittenen Stadium. Besonders die fettige Infiltration wurde als wichtiger negativer Prognosefaktor identifiziert.38
In der Gruppe der Rerupturen konnte außerdem eine Progression der strukturellen Veränderungen – auch im angelagerten Muskel (ISP bei SSP-Reruptur) – gezeigt werden. Diese fettige Degeneration korreliert dabei signifikant mit dem klinischen Outcome.39 Die Klassifikation von Rotatorenmanschetten-Rerupturen erfolgt typischerweise nach Sugaya und unterscheidet fünf Typen (Tab. 1).40
Revisionsmöglichkeiten
Die Wahl der Revisionsstrategie hängt von Sehnenzustand, Defektausmaß, Gewebequalität und patientenspezifischen Merkmalen ab. Technische und biologische Herausforderungen wie minderwertiges Gewebe, Narbenbildung, Atrophie und fettige Infiltration erschweren die Versorgung.24, 41–43 Begleitpathologien treten häufig auf, im Rahmen von Rerupturen sind selbige in bis zu 45% der Fälle nachweisbar. Zudem sollten alle möglichen Ursachen für anhaltende Schmerzen oder Faktoren, die die Refixation gefährden, adressiert werden. Schmerzursachen wie die lange Bizepssehne, das Akromioklavikulargelenk, der Gelenksknorpel, eine adhäsive Kapsulitis und Neuropathie des Nervus suprascapularis sollten identifiziert und entsprechend therapiert werden.42
Für junge Patient:innen und manuell arbeitende, aktive Patient:innen mit einer irreparablen Rotatorenmanschetten-Reruptur kann ein Sehnentransfer eine vielversprechende Behandlungsoption sein.44,45 Hingegen stellt bei Patient:innen mit symptomatischer, massiver Rotatorenmanschetten-Reruptur und begleitender glenohumeraler Arthrose die inverse Schultertotalendoprothese den idealen Therapieansatz dar.46, 47
Rerupturen können kleiner als der ursprüngliche Defekt sein, weshalb heilende Sehnenbereiche erhalten bleiben sollten. Dennoch treten in einem wesentlichen Anteil bei Rerupturen auch massive Rotatorenmanschettenrupturen auf. Rotatorenmanschettenmassenrupturen machen etwa 20% aller Rupturen der Rotatorenmanschette und 80% der Rerupturen aus. Hier ist der Zeitraum neben den biologischen und mechanischen Aspekten ein entscheidender Faktor.42
Verschiedene Ansätze wurden zur Klassifikation von Rotatorenmanschettendefekten verwendet, wobei jeder Ansatz seine eigenen Begrenzungen hat und eine einheitliche Definition fehlt. Cofield et al. betrachteten eine Ruptur als massiv, wenn der Durchmesser mindestens 5cm beträgt.43 Zumstein et al. definierten eine Ruptur als massiv, wenn zwei oder mehrere Sehnen vollständig rupturiert waren.48
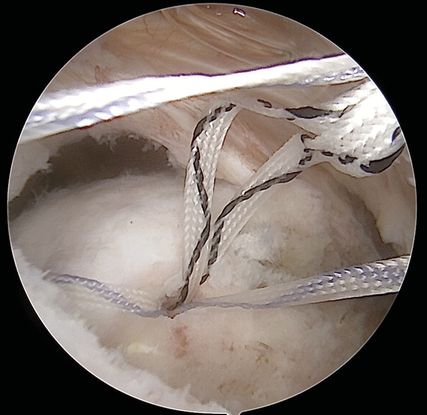
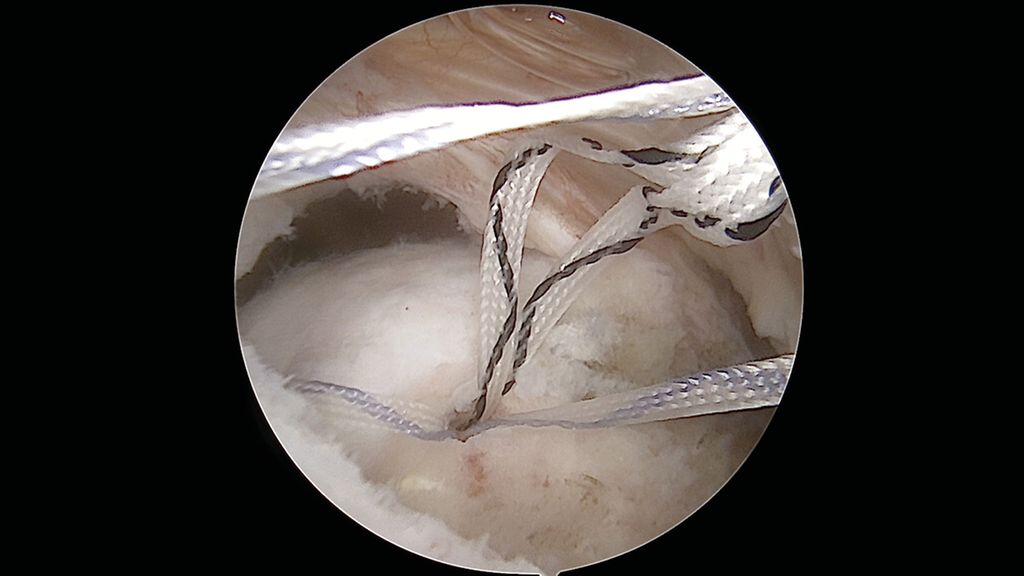
Abb. 3: Arthroskopische Revisionsoperation nach erneuter arthroskopischer Ankerplatzierung
Die Definition einer irreparablen Rotatorenmanschettenruptur variiert erheblich. Einige Chirurgen sind der Ansicht, dass alle Risse reparabel sind; während andere Rupturen mit einer chronischen akromiohumeralen Distanz (AHD) von weniger als 7mm49 oder einer Atrophie über Grad 250 als irreparabel betrachten. Zudem hat sich mit den Fortschritten in Bezug auf Anker, Nahtfestigkeit, Fixierungen51 und „interval slides“26 die Definition von „irreparabel“ weiterentwickelt.
Es ist generell allerdings anzuerkennen, dass einige Läsionen irreparabel sind oder nicht rekonstruiert werden sollten. Der wichtigste prognostische Faktor für das Ergebnis ist wie oben genannt die nicht funktionale Muskulatur, insbesondere bei einer fettigen Infiltration Grad 3 oder 4.38
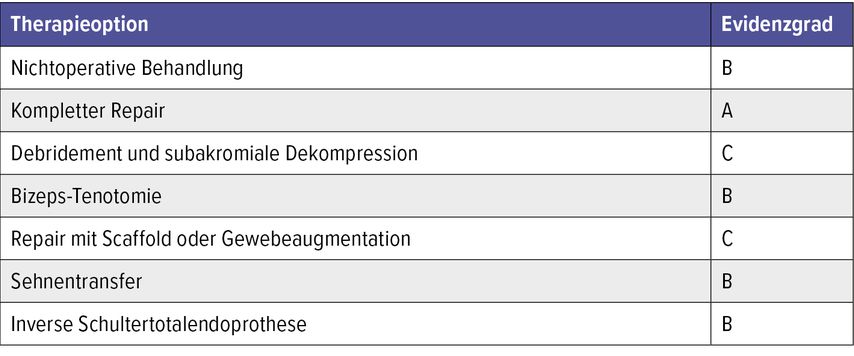
Tabelle 2 zeigt die Übersicht der essenziellen Therapieoptionen bei Rezidiven oder Rotatorenmanschetten-Sehnendefekten.
Tab. 2: Essenzielle Therapieoptionen bei Rezidiven oder Rotatorenmanschetten-Sehnendefekten, um die bestmögliche Behandlungsstrategie auf Grundlage der aktuellen wissenschaftlichen Erkenntnisse auszuwählen (basierend auf der verfügbaren Evidenz). A: Gute Evidenz aus Level-I-Studien, um eine Intervention zu empfehlen oder abzulehnen. B: Mäßige Evidenz aus Level-II- oder -III-Studien, um eine Intervention zu empfehlen oder abzulehnen. C: Schwache Evidenz aus Level-IV- oder -V-Studien, um eine Intervention zu empfehlen oder abzulehnen
(Partial) Repair und Gewebsmobilisation
Das Ziel eines Repairs – auch wenn es nur teilweise ist – sind die Wiederherstellung der Kraftkoppelungen und die Stabilisierung für die normale Schulterkinematik. Als Ansatz sollte generell gelten, alle Teile der Rotatorenmanschette, die ohne übermäßige Spannung an den Footprint gebracht werden können, zu refixieren.42 Komplexe Repair- und Mobilisationstechniken variieren je nach Art der Läsion und beinhalten unter anderem die „margin convergence“52 oder „interval slides“.26
Bei der einfachen Revisionstechnik kommt es meist zur inkompletten Heilung ohne Sehnendefekt bei insuffizienter Sehnendicke, knöchernen Läsionen durch Mikrobewegungen der Anker oder den klassischen Versagensmustern. Bei der komplexen Revisionstechnik wird ein Double-Row-Repair angestrebt. Hier sollten partiell geheilte Sehnen geschont werden und defektes (Naht-)Material entfernt werden. Der Footprint kann leicht medialisiert werden und „Margin convergence“-Nähte52 verkleinern den Defekt. Das tiefe Blatt insbesondere der Infraspinatussehne sollte in den Repair integriert werden. Es ist wichtig, auf die Delamination der Sehnen (in etwa 80% der Fälle) zu achten.19, 23, 53
Sehnentransfer
Bei jüngeren und aktiven Patient:innen ohne Arthrose kann ein Sehnentransfer eine Option sein, insbesondere zur Verbesserung der Rotation. Allerdings sind diese Methoden bei Pseudoparalyse nicht geeignet, da sie keine aktive Bewegung in Elevation und Abduktion wiederherstellen können.44, 45
Anteriore Rotatorenmanschetteninsuffizienz
Der Pectoralis-major-Transfer ist der am häufigsten eingesetzte Muskeltransfer bei Subscapularis-Defiziten. Durch seine Zugrichtung kann er die Innenrotation und die transversale Kraftkoppelung wiederherstellen und eine anterosuperiore Migration des Humeruskopfes verhindern. Dabei wird der Sehnenansatz des Musculus pectoralis major auf das Tuberculum minus verlagert. Zwar wird der Schmerz häufig reduziert, jedoch bleibt die funktionelle Wiederherstellung oft unzureichend.54, 55
Der anteriore Latissimus-dorsi-Transfer (LDT) kann auch eine sinnvolle Behandlungsoption darstellen. Die meisten Patient:innen zeigen eine Verbesserung der Symptome der Subscapularis-Insuffizienz, einschließlich der anterosuperioren Migration und einer besseren Schulterfunktion.55, 56
Posteriore Rotatorenmanschetteninsuffizienz
Bei posteriorer Rotatorenmanschetteninsuffizienz wird häufig ein posteriorer Latissimus-dorsi-Transfer (LDT) durchgeführt. Die Technik gilt insbesondere bei Patient:innen mit aktiver Schulterbewegung, aber fehlender Kontrolle der Außenrotation als vielversprechend. Gute Ergebnisse werden bei intakter M.-subscapularis- und M.-teres-minor-Sehne erzielt. Beim Latissimus-dorsi-Transfer wird der M. latissimus dorsi mobilisiert und an den Ansatz des M. infraspinatus umgeleitet.57 Langzeitstudien zeigen zwar klinische Verbesserungen, jedoch keinen klaren Vorteil gegenüber dem partiellen Repair.57–59
Der Lower-Trapezius-Transfer (LTT) wird aktuell bei irreparablen Defekten der hinteren Rotatorenmanschette propagiert. Der Hauptfokus liegt auf der Wiederherstellung der Außenrotation und der Stabilität der Schulter. Dabei wird der untere Trapezius mithilfe eines Sehnenallografts an das Tuberculum majus verlagert.60 Ideal ist das Verfahren für Patient:innen mit erhaltener aktiver Elevation, stabiler Schulterstruktur und intaktem M. subscapularis. Studien berichten über gute funktionelle Ergebnisse, insbesondere in der Wiederherstellung der Außenrotation und Reduktion von Schmerzen.60–62
Augmentation durch biologische oder mechanische Scaffolds
Die Wahl des Scaffolds hängt von mechanischen Eigenschaften, Gewebereaktion und Gewebeintegration ab. Augmentationen oder Interpositionen bieten mechanische Unterstützung und können das Zellwachstum fördern, was die Heilung der Sehne am Knochen verbessern soll. Wachstumsfaktoren im plättchenreichen Plasma (PRP) wirken zudem positiv regenerativ auf die Heilung vom Weichgewebe, zeigen jedoch keine relevant positiven klinischen Ergebnisse. Biologische Grafts oder Autografts63 werden in der Regel bevorzugt, moderne Grafts zeigen vielversprechende erste Ergebnisse.64, 65
Bei stark degenerierten Sehnen kann eine Augmentation mit biologischen Patches wie Amnionpatches sinnvoll sein.64,66 Bei größeren Defekten oder „medial cuff failure“ kann eine komplexe Technik mit Patch-Augmentation angewandt werden. Patch-Augmentationen senken die Rerupturraten auf 17 bis 45% und verbessern die Sehnenheilung, jedoch bleiben das postoperative Outcome und Komplikationen wie Infektionen problematisch.67
Für irreparable Rerupturen kommt auch die „superior capsular reconstruction“ (SCR) ins Spiel. Aufgrund der begrenzten Anzahl hochwertiger Studien kann der tatsächliche Stellenwert in der klinischen Praxis jedoch nicht vollständig bestätigt werden.68
Alternative Verfahren
Verschiedene Faktoren wie die Patient:innenablehnung, biologische Gegebenheiten oder die Eigenschaften der Ruptur können eine Rekonstruktion unmöglich machen. In solchen Fällen werden alternative Ansätze wie Physiotherapie69, subakromiale Dekompression und palliative Bizepstenotomie (plus subakromiale Dekompression)70 empfohlen.
Der subakromiale Balloon-Spacer ist ein kontrovers diskutierter Ansatz. Es ist nicht klar, ob die kurzzeitigen klinischen Verbesserungen durch Placeboeffekte oder durch echte biomechanische Veränderungen bedingt sind. Die retrospektive Level-III-Studie von Lafosse et al. zeigte, dass der Einsatz dieses Implantats weder zu einer signifikanten Reduktion der Rerupturrate noch zu einer nachhaltigen Verbesserung der klinischen Ergebnisse nach einem Jahr führt.71
Inverse Schultertotalendoprothese
Defektarthropathien stellen ein häufiges klinisches Problem bei älteren Patient:innen dar. Die inverse Schultertotalendoprothese ist eine bewährte Methode zur Behandlung von Patient:innen mit irreparabler Rotatorenmanschetten-(Re)Ruptur und einer damit verbundenen Arthropathie. Dabei werden die biomechanischen Hebelverhältnisse verändert, um die Funktion des Musculus deltoideus zu optimieren.72
Die inverse Schultertotalendoprothese wurde von Paul Grammont 1985 für nicht rekonstruierbare Rotatorenmanschettenmassendefekte entwickelt.72–75 Stetige Weiterentwicklungen des Prothesendesigns optimieren die sehr guten klinischen Ergebnisse. Patient:innen erreichen generell eine gute Schmerzreduktion und sehr gute Funktionsverbesserung mit geringer Schwankungsbreite bei hoher Patient:innenzufriedenheit.46, 76–78
Die Fähigkeit zur Außenrotation spielt eine entscheidende Rolle für die Funktion der Schulter. Ein traditioneller Ansatz zur Verbesserung der Außenrotation bei massiven Rotatorenmanschettendefekten ist die Kombination einer inversen Schultertotalendoprothese mit einem Muskeltransfer. Durch die Weiterentwicklung moderner Prothesendesigns hat diese Technik jedoch an Bedeutung verloren. Sie bleibt jedoch eine Option für Patient:innen mit erheblichen Defiziten der primären Außenrotatoren, insbesondere wenn der Musculus teres minor ebenso irreparabel geschädigt oder funktionsunfähig ist. In solchen Fällen wurden vielversprechende klinische Ergebnisse aufgezeigt.79
Moderne Prothesendesigns weisen ein höheres glenoidales Offset auf. Die Lateralisierung ist eine effektive Strategie, um das Adduktionsnotching zu reduzieren und gleichzeitig die Fähigkeit zur Außenrotation zu verbessern. Dieses Design zeigt eine sehr gute Verbesserung der Rotation mit dem Vorteil, ein eventuelles Innenrotationsdefizit zu verhindern. Die Lateralisierung kann sowohl auf der glenoidalen als auch auf der humeralen Seite mit unterschiedlichen Auswirkungen erfolgen.80
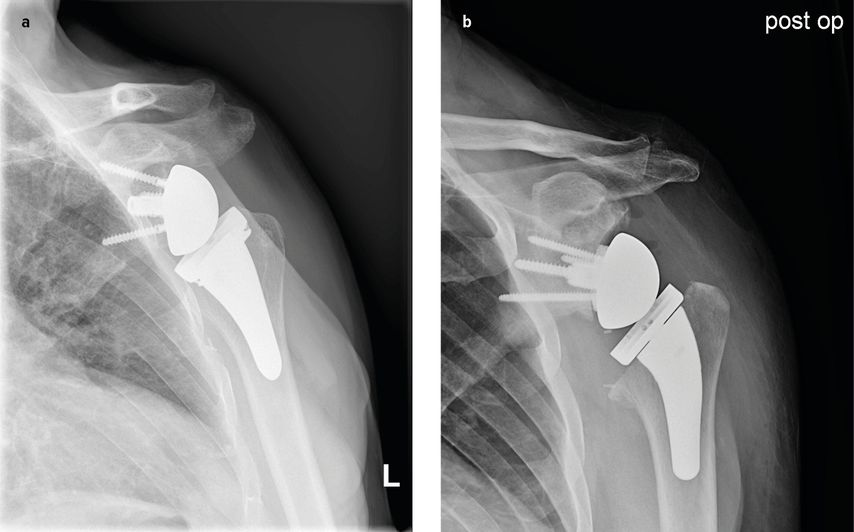
Abb. 5: 5a: Inverse Schultertotalendoprothese mit 2 verschiedenen Implantaten, 5b: zusätzliche knöcherne Metallaugmentation am Glenoid bei knöchernem Defekt
Zusammenfassung
Rezidivrupturen nach arthroskopischer Rotatorenmanschettenrekonstruktion treten häufig auf und werden durch verschiedene patientenspezifische Faktoren und die Größe des Risses beeinflusst. Die Behandlung von Rerupturen kann durch verschiedene chirurgische Ansätze erfolgen, je nach Zustand des Gewebes und der beteiligten Sehnen. Diese Ansätze umfassen sowohl einfache als auch komplexe Techniken wie Sehnentransfers oder den Einsatz von Augmentationen/Interpositionen und biologische Add-ons. Ein (Partial) Repair wird, wenn sinnvoll und indiziert, angestrebt.
Eine etablierte Behandlungsmöglichkeit ist die inverse Schultertotalendoprothese für Low-demand-Patient:innen und/oder Patient:innen mit begleitender Arthrose. Hinsichtlich des klinischen Outcomes wurden gute klinische Ergebnisse mit niedriger Schwankungsbreite dargelegt.
Seltene chirurgische Indikationen für eine operative Revision nach arthroskopischer Rotatorenmanschettenrekonstruktion beinhalten unter anderem fakultative Muskelinsuffizienzen, Infektionen, spezifische Nervenläsionen und postoperative Vernarbungen bis hin zur adhäsiven Kapsulitis; wobei die Inzidenz dieser Komplikationen relativ niedrig ist.
Für die Behandlung wird eine evidenzbasierte Vorgehensweise empfohlen, wobei die Wahl der Therapie auf dem Zustand der Sehne, dem Ausmaß des Defekts und dem individuellen Bild der Pathologie basiert. Die verfügbaren Optionen müssen anhand des Literaturkorpus mit unterschiedlich starker Evidenz bewertet werden.
Literatur:
1 Codding JL, Keener JD: Current Reviews in Musculoskeletal Medicine 2018; 11: 77-85 2 Teunis T et al.: J Shoulder Elbow Surg 2014; 23: 1913-21 3 Codman EA: J Shoulder Elbow Surg 2011; 20: 347-9 4 Mansat P et al.: Orthopedic Clinics of North America 1997; 28: 205-13 5 Weber SC et al.: Arthroscopy 2002; 18: 88-95 6 Shin JJ et al.: J Am Acad Orthop Surg Glob Res Rev 2018; 2(12): e093.7 7 Brislin KJ et al.: Arthroscopy 2007; 23: 124-8 8 Jost B et al.: J Bone Joint Surg Am 2006; 88(3): 472-9 9 Hug K et al.: Knee Surg Sports Traumatol Arthrosc 2015; 23: 2628-34 10 Le BTN et al.: Am J Sports Med 2014; 42: 1134-42 11 Kim HM et al.: J Bone Joint Surg Am 2014; 96: 106-12 12 Diebold G et al.: J Bone Joint Surg Am 2017; 99: 198-205 13 Lapner PLC et al.: J Bone Joint Surg Am 2012; 94(14): 1249-57 14 Iijima Y et al.: J Shoulder Elbow Surg 2019; 28: 1562-67 15 Lee S et al.: Arthroscopy 2020; 36: 2080-88 16 Li H et al.: Am J Sports Med 2018; 46: 1892-1900 17 Shimokobe H et al.: JOrthop Surg Res 2017; 12 18 Saltzman BM et al.: J Shoulder Elbow Surg 2017; 26: 1681-1691 19 Millett PJ et al.: JShoulder Elbow Surg 2014; 23: 586-597 20 Franceschi F et al.: Am J Sports Med 2007 (8): 1254-60 21 Aydin N et al.: J Shoulder Elbow Surg 2010; 19: 722-25 22 Burks RT et al.: Am J Sports Med 2009; 37: 674-82 23 Sheibani-Rad S et al.: Arthroscopy 2013; 29: 343-8 24 Cho NS et al.: Am J Sports Med 2010; 38: 664-71 25 Kim YK et al.: Am J Sports Med 2013; 41: 2270-7 26 Lo IKY et al.: Arthroscopy 2004; 20(1): 22-33 27 Denard PJ et al.: Arthroscopy 2012; 28: 1214-9 28 Collin P et al.: J Shoulder Elbow Surg 2014; 23: 28-34 29 Parada SA et al.: Curr Rev Musculoskelet Med 2015; 8: 40-52 30 Hughes JD et al.: Orthop J Sports Med 2017; 5(7): 2325967117715416 31 Mormino MA et al.: Arthroscopy 1996; (4): 457-61 32 Borgeat A et al.: Anesthesiology 2001; 95(4): 875-80 33 Lenza M et al.: Cochrane Database Syst Rev 2013; 9: CD009020 34 Oh JH et al.: J Shoulder Elbow Surg 2010; 19: 14-20 35 Nazarian LN et al.: Radiology 2013; 267: 589-95 36 Rhee RB et al.: Semin Musculoskelet Radiol 2012; 16: 3-14 37 Yubran AP et al.: Insights Imaging 2024; 15(1): 61 38 Goutallier D et al.: JShoulder Elbow Surg 2003; 12: 550-554 39 Jost B et al.: J Bone Joint Surg Am 2000; 82(3): 304-14 40 Sugaya H et al.: Arthroscopy 2005; 21: 1307-16 41 Khazzam M et al.: JSES Int 2020; 4: 625-31 42 Lädermann A et al.: Int Orthop 2015; 39: 2403-14 43 DeOrio JK et al.: J Bone Joint Surg Am 1984; 66(4): 563-7 44 Merolla G et al.: Muscles Ligaments Tendons J 2015; 4(4): 425-32 45 Adam JR et al.: J Clin Orthop Trauma 2021; 17: 254-260 46 Boileau P et al.: J Shoulder Elbow Surg 2009; 18: 600-606 47 Drake GN et al.: Clin Orthop Relat Res 2010; 468: 1526-33 48 Zumstein MA et al.: J Bone Joint Surg 2008; 90: 2423-2431 49 Nové-Josserand L et al.: Clin Orthop Relat Res 2005; 433: 90-6 50 Warner JJP et al.: J Shoulder Elbow Surg 2001; 10: 37-46 51 Burkhart SS et al.: Am J Sports Med 2014; 42: 457-462 52 Lall AC et al.: Arthrosc Tech 2018; 7: e823-e827 53 Cha SW et al.: J Orthop Surg Res 2016; 11(1): 75 54 Gavriilidis I et al.: Int Orthop 2010; 34: 689-94 55 Burnier M et al.: Curr Rev Musculoskelet Med 2020; 13: 725-33 56 Elhassan BT et al.: J Shoulder Elbow Surg 2020; 29: 2128-34 57 Gerber C et al.: J Bone Joint Surg 2013; 95: 1920-6 58 Weening AA et al.: Int Orthop 2010; 34: 1239-44 59 Zafra M et al.: Int Orthop 2009; 33: 457-62 60 Elhassan BT et al.: Arthrosc Tech 2016; 5: e981-8 61 Elhassan BT et al.: J Shoulder Elbow Surg 2016; 25: 1346-53 62 Elhassan BT et al.: J Shoulder Elbow Surg 2020; 29: 2135-42 63 Endell D et al.: Arthrosc Tech 2023; 12: e383-6 64 Suroto H et al.: J Biomim Biomater Biomed Eng 2018; 39: 98-102 65 Russo M et al.: J Clin Med 2024; 13(17): 5066 66 Wang JT et al.: Chin J Traumatol 2024; doi: 10.1016/j.cjtee.2024.04.001. Online ahead of print 67 Russo M et al.: J Clin Med 2024; doi: 10.3390/jcm13175066. Online ahead of print 68 Werthel JD et al.: Orthop Traumatol Surg Res 2021; doi: 10.1016/j.otsr.2021.103072. Epub 2021 Sep 22 69 Collin PG et al.: Orthop Traumatol Surg Res 2015; 101: 203-5 70 Walch G et al.: J Shoulder Elbow Surg 2005; 14: 238-46 71 Minarro JC et al.: Arthroscopy 2024; 40: 242-8 72 Baulot E et al.: Clin Orthop Relat Res 2011; 469: 2425-31 73 Boileau P et al.: JShoulder Elbow Surg 2005; 14: 147-61 74 Grammont PM et al.: Clin Orthop Relat Res 2011; 469(9): 2424 75 Grammont PM et al.: Etude et réalisation d’une nouvelle prothèse d’épaule. Rhumatologie 1987 (Aix-les-Bains) 39: 407-418 76 Werner CML et al.: J Bone Joint Surg Am 2005; 87(7): 1476-86 77 Nolan BM et al.: Clin Orthop Relat Res 2011; 469: 2476-82 78 Schwarz AM et al.: BMC Musculoskelet Disord 2021; 22(1): 48 79 Monir JG et al.: JSES Rev Rep Tech 2024; 4: 607-14 80 Liu B et al.: J Shoulder Elbow Surg 2023; 32: 1662-72
Das könnte Sie auch interessieren:
Schenkelhalsfrakturen bei Menschen mit Demenz
Patienten mit Hüftfraktur sollten zeitnah operiert werden, wenn es die Indikation zulässt – auch im Falle einer Demenz. Denn ein konservatives Vorgehen geht vor allem bei Kopf-Hals- ...
«Auch Patienten mit Demenz profitieren von einer chirurgischen Stabilisierung»
Patienten mit Hüftfraktur und einer leichten, mittelschweren oder schweren Demenz haben ein geringeres Risiko zu sterben, wenn sie operiert werden – vor allem wenn es sich um Kopf-Hals- ...
Management periprothetischer Frakturen am Kniegelenk
Mit steigenden Versorgungszahlen der Knieendoprothetik und dem höheren Lebensalter entsprechend der Alterspyramide nimmt auch die Zahl der periprothetischen Frakturen zu und stellt die ...