COPD: State of the Art
Bericht:
Mag. Andrea Fallent
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Vom reaktiven zum proaktiven Management – Präventivmaßnahmen werden in der Versorgung von COPD-Patient:innen immer wichtiger. Das unterstreichen auch die Aktualisierungen im GOLD-Report 2025: Sie betreffen u.a. den Fokus auf Prä-COPD bzw. PRISm, die Evaluierung von häufigen Komorbiditäten, das Einbeziehen von Umweltfaktoren und das Detektieren spezieller Phänotypen, für die Biologika im Behandlungsverlauf eine mögliche Therapieoption darstellen.
Prim. Ao. Univ.-Prof. Dr. Judith Löffler-Ragg, Landeskrankenhaus Hochzirl – Natters, präsentierte in ihrem Vortrag beim 12. Pneumo Aktuell neue Erkenntnisse zu den obstruktiven Atemwegserkrankungen Asthma und COPD. Aufgrund der erheblichen Heterogenität dieser Erkrankungen und ihrer unspezifischen Symptome wie Atembeschwerden, Husten und Auswurf ist die Differenzierung im klinischen Alltag nicht immer einfach, aktuelle Studiendaten und Konzepte ermöglichen jedoch eine zunehmend präzisere Diagnosestellung und Therapieanpassung.
In der neuen Definition der COPD im GOLD-Report 20251 wird auf die anhaltende, oft fortschreitende Behinderung des Atemflusses bei COPD hingewiesen, während bei Asthma von einer variablen Atemflusslimitation gesprochen wird (GINA-Report 2024)2. Die Atemflusslimitation bei COPD kann mit den bekannten Kriterien durch Spirometrie bestimmt werden, das weitere Management erfasst aber noch andere Aspekte: „Aufgrund der heterogenen Erkrankungsbilder kommen wir nur weiter, wenn wir bei unseren Patient:innen gut phänotypisieren und das Konzept der ,treatable traits‘ anwenden“, betonte Löffler-Ragg. Konkret gemeint sind jene Parameter in Hinblick auf klinische Phänotypen, Biomarker und Ätiologie, die klinisch relevant sind, objektiv gemessen werden können und nicht zuletzt auch beeinflussbar sind.
Frühe Formen der COPD
Ab dem 40. Lebensjahr ist jeder zehnte. Österreicher von COPD betroffen, ab 70 jeder vierte.3 Wichtig ist das konsequente Management von Anfang an, um sowohl Symptomatik als auch Sterberisiko zu reduzieren. Hier gilt es, verstärkt die frühen Formen der COPD in Betracht zu ziehen: die Prä-COPD („early COPD“) bzw. den PRISm(„preserved ratio impaired spiro-metry“)-Phänotyp. Dazu zählen Personen mit Risikofaktoren und Symptomen, die aber in der Lungenfunktionsmessung (noch) keine Atemflusslimitation zeigen. Die frühe Detektion ist u.a. deshalb von Bedeutung, da Studien eine erhöhte Prävalenz von kardiovaskulären Erkrankungen und Diabetes sowie eine höhere Mortalität bei Personen mit Prä-COPD oder PRISm zeigen.4 Weiters konnte festgestellt werden, dass schon in dieser Gruppe entzündliche Veränderungen der peripheren Atemwege („small airways disease“) auftreten und die Wahrscheinlichkeit eines Übergangs in eine COPD wahrscheinlich ist.5 Spezifische Befunde wie Pathologien im CT (Emphysem) oder DLCO-Reduktion sollten berücksichtigt werden, um die Chance für frühe Interventionen, wie beispielsweise die Reduktion progressions-treibender Risikofaktoren, zu nützen, so Löffler-Ragg. Bei der Einteilung hat sich seit dem GOLD-Report 2024 nichts geändert: Das Grading anhand von Lungenfunktion, Symptomen (mMRC und CAT) und Exazerbationen in die Gruppen A, B und E bleibt gleich.1
Neue Aspekte zur Therapie
Einsatz von ICS
In der Gruppe B bzw. E besteht die initiale pharmakologische Therapie aus lang wirksamen Anticholinergika (LAMA) und lang wirksamen β2-Sympathomimetika (LABA). Die Anzahl der Exazerbationen und der Eosinophilen im Blut (≥300/μl) ist ein Wegweiser für den Einsatz der Triple-Therapie (Zusatz von inhalativen Kortikosteroiden; ICS). Metaanalysen von mehr als 60 Studien zeigen einen Benefit, wenn bei mehr als 200 Zellen/μl und Exazerbationen auf eine inhalative Triple-Therapie gewechselt wird.6,7
Gleichzeitig wird vor einem Übergebrauch von ICS gewarnt, weshalb Kontraindikationen unbedingt berücksichtigt werden müssen. Die Abbildung 1 zeigt die Faktoren, die bei einer Addition von ICS zu berücksichtigen sind. Für die negativen Auswirkungen von ICS u.a. auf das Mikrobiom der Atemwege gibt es immer mehr Evidenz.1,8,9 Löffler-Ragg zitierte in diesem Zusammenhang eine aktuelle Übersichtsarbeit zu Nebenniereninsuffizienz durch ICS: Ein erhöhtes Risiko besteht u.a. bei Verwendung von Fluticasonpropionat, bei Personen mit niedrigem BMI sowie bei der Therapie mit Inhibitoren von Cytochrom P450 3A4 wie Ritonavir.10
Abb. 1: Parameter, die bei der Ergänzung von inhalativen Kortikosteroiden (ICS) zu lang wirksamen Bronchodilatatoren zu berücksichtigen sind (modifiziert nach Augusti A et al. 2018)8
Behandlungsoptionen mit Dupilumab und Ensifentrin
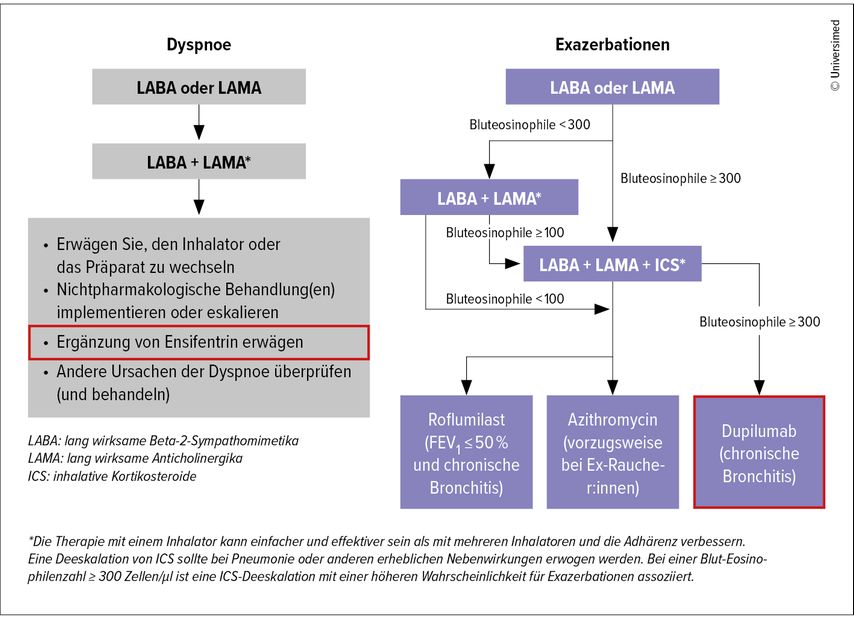
Eine Neuerung im GOLD-Report 2025 betrifft die Einführung von Dupilumab und Ensifentrin im Behandlungsverlauf (Abb. 2). Ensifentrin ist ein inhalativer Inhibitor der Phosphodiesterasen PDE3 und PDE4, der antiinflammatorisch und bronchienerweiternd wirkt und auch die Zilienmotilität positiv beeinflusst.11 Ensifentrin wurde im Juni 2024 von der US-amerikanischen Food and Drug Administration (FDA) zugelassen, in Europa wurde noch keine Zulassung beantragt (Stand 6.2.2025). Der Einsatz von Ensifentrin ist im GOLD-Report 2025 in der pharmakologischen Therapie zusätzlich zur LABA/LAMA-Kombination vorgesehen, falls die Dyspnoe trotz der dualen Therapie anhält.1 Der Interleukin(IL)-4-Rezeptor-Antikörper Dupilumab wird bei der Therapie von Exazerbationen als Therapieeskalation vorgeschlagen, wenn trotz inhalativer Triple-Therapie weitere Exazerbationen auftreten und der Nachweis einer Typ-2-Inflammation vorliegt (Bluteosinophile ≥300μl). Dazu liegen Daten aus zwei Studien mit mehr als 900 COPD-Patient:innen mit eosinophiler Signatur vor, die eine Reduktion der Exazerbationen um mehr als 30% dokumentieren.12,13
Abb. 2: Der Einsatz von Dupilumab und Ensifentrin im Behandlungsverlauf (modifiziert nach GOLD-Report 2025)1
COPD und kardiovaskuläres Risiko
Mit COPD ist die Prävalenz von kardiovaskulären Erkrankungen (CVD) grundsätzlich erhöht. Kardiovaskuläre Ereignisse sind eine häufige Todesursache. Allerdings bleiben kardiovaskuläre Erkrankungen oft unbemerkt und daher unbehandelt. Die „Big 4“ arterielle Hypertonie, koronare Herzkrankheit (KHK), Herzinsuffizienz und Arrhythmien sollten daher regelmäßig eruiert werden: „Und zwar in Ruhe, bei klinisch stabilen Patient:innen und nicht erst bei exazerbierter COPD“, so Löffler-Ragg. Die Empfehlung gemäß GOLD-Report 2025 lautet daher: Alle COPD-Patient:innen sollten auf CVD gescreent werden und eine leitliniengerechte Therapie erhalten. Durch eine Exazerbation (ECOPD) steigen das Risiko für ein akutes kardiovaskuläres Ereignis und die Mortalität, insbesondere in den ersten 7 Tagen nach einer schweren Exazerbation, sie bleiben bis zu 12 Monate lang erhöht.1,14 Dies könnte auf Risikofaktoren zurückzuführen sein, die sowohl bei COPD als auch bei kardiovaskulären Erkrankungen auftreten, wie systemische Entzündung, abnormalen Gasaustausch in der Lunge und Hyperinflation. Die aktuelle Empfehlung lautet, Exazerbationen nicht mehr nach dem Ort der Behandlung (ambulant vs. stationär) zu klassifizieren, sondern Parameter wie die mögliche Ätiologie, systemische Entzündung und Schwere der Ateminsuffizienz miteinzubeziehen – wie initial im Rome Proposal vorgeschlagen.1,15 Zusätzlich stehen bereits Algorithmen zur Verfügung, die Biomarker, klinischen Status und pathophysiologische Mechanismen kombinieren, um die Abklärung möglicher Differenzialdiagnosen zu ECOPD (u.a. akutes Herzversagen, Lungenembolie, Pneumonie) bzw. von Komorbiditäten im akuten Setting zu erleichtern.1,16
COPD und pulmonale Hypertonie
Der aktuelle GOLD-Report behandelt auch die Diagnose der pulmonalen Hypertonie (PH), definiert durch einen mittleren pulmonalarteriellen Druck von mehr als 20mmHg. Hervorgehoben wird, dass die beiden Erkrankungen häufig nebeneinander bestehen. Alle fünf PH-Gruppen können bei COPD auftreten: Etwa 25 bis 30% der COPD-Patient:innen haben eine milde Form, etwa 5% entwickeln eine schwere PH (pulmonaler Gefäßwiderstand [PVR]>5 Wood-Einheiten [WU]. Bei der schweren PH wurde ein spezifischer pulmonal-vaskulärer Phänotyp identifiziert, der mit einer mäßigen Atemflusslimitation, keiner oder milder Hyperkapnie, aber einer deutlichen DLCO-Einschränkung (<45%) einhergeht. Patient:innen mit PH-COPD sollten an ein spezialisiertes Zentrum überwiesen werden.1 Eine Register-Studie gibt erste Hinweise darauf, dass die Therapie mit Phosphodiesterase-5-Hemmern einen Überlebensvorteil bringen könnte.17
Nichtpharmakologische Maßnahmen und Klima
Neben Medikamenten spielen auch nichtpharmakologische Maßnahmen eine entscheidende Rolle im Management der COPD. Dazu zählen Rauchentwöhnung, Rehabilitation, nichtinvasive Beatmung und Impfungen, die nachweislich einen positiven Einfluss auf die Mortalität haben. Die RSV-Impfung hat im GOLD-Report mittlerweile den Evidenzgrad A, weiters gibt es Updates zur Pneumokokken- und Influenza-Impfung. Auch der Klimawandel beeinflusst COPD-Patient:innen erheblich, daher wurde dazu ein Kapitel mit aktualisierten Empfehlungen eingefügt.
Populationsstudien in England haben ein erhöhtes Sterberisiko für Patient:innen nach Hitze- oder Kälteeinwirkung nachgewiesen sowie ein erhöhtes Risiko für Exazerbationen bei sehr hohen bzw. sehr niedrigenAußentemperaturen. Der Bericht empfiehlt, dass Patient:innen mit COPD die Temperatur im Schlafzimmer bei kaltem Wetter über 18°C halten sollten und bei Hitzewellen möglichst unter 24°C, entsprechend den Empfehlungen der WHO.1
Mucus-Plugs als neuer Therapieansatz
Ein vielversprechendes Forschungsfeld ist die Schleimproduktion bei COPD. Aktuelle Studiendaten zeigen, dass 30% der COPD-Patient:innen – auch ohne subjektiv empfundenen Auswurf – Schleimretentionen (Mucus-Plugs) in der Lunge haben, die mit einer schlechteren Prognose aufgrund von reduzierter Ventilation mit Hypoxämie, verminderter Lungenfunktion und Leistung assoziiert sind.18 Forschungserkenntnisse über die Entstehung und Konsistenz der Mucus-Plugs könnten eine wichtige Rolle für Therapieansätze zur Beeinflussung der Schleimsekretion spielen.19 Ein weiterer interessanter Ansatz ist die gezielte Modulation der Entzündungskaskade, insbesondere von Interleukin (IL) 13, das eine Hyperplasie der Becherzellen induziert.
Einsatz von Biologika
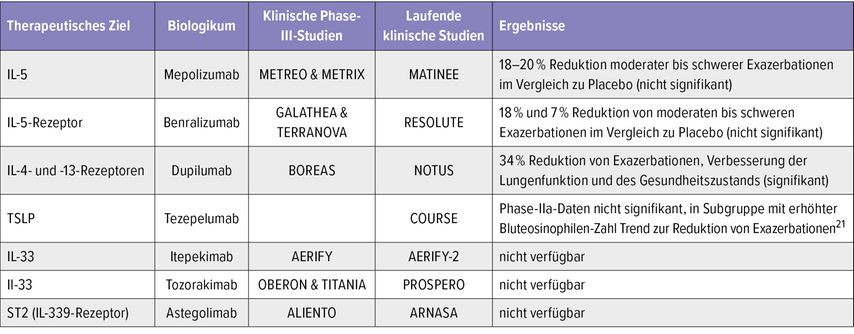
Bei der Therapie von schwerem Asthma mit Typ-2-Inflammation punkten monoklonale Antikörper durch die Reduktion von Exazerbationen und die Verbesserung der Lungenfunktion. Auch in der COPD gibt es entsprechende Ansatzpunkte für Biologika (Tab. 1). Frühere Studien zu Anti-IL-5-Antikörpern (Mepolizumab, Benralizumab) zeigten zwar keine signifikanten Ergebnisse, aber sehr wohl einen möglichen Benefit in Subgruppenanalysen. Signifikante Studiendaten bei COPD mit Typ-2-Inflammation gibt es wie erwähnt zu Dupilumab. Interessant ist auch das Targeting von Alarminen wie TSLP („thymic stromal lymphopoietin“) und IL-33, zu dem die Resultate von Phase-III-Studien noch nicht vorliegen.
Tab. 1: Mögliche therapeutische Ziele für die Biologikabehandlung von COPD und laufende klinische Studien (modifiziert nach Kersul AL, Cosio BG 2024)24
Erwartet wird die Publikation mit den Ergebnissen der Phase-III-Folgestudie zu Mepolizumab (MATINEE) in einem adaptierten Studiendesign, nachdem die bisherigen Studien METREO und METRIX ihren Endpunkt nicht erreicht haben. In MATINEE konnte gezeigt werden, dass die Therapie bei COPD-Patient:innen mit einem eosinophilen Phänotyp zur signifikanten Reduktion von Exazerbationen führte.20
Kürzlich wurden die Ergebnisse einer Phase-IIa-Studie mit dem Anti-TSLP-Antikörper Tezepelumab publiziert: COPD-Patient:innen mit vorhergegangenen Exazerbationen trotz inhalativer Triple-Therapie erhielten Tezepelumab in der Dosis von 420mg s.c. alle 4 Wochen oder Placebo.21 Die Ergebnisse waren bezüglich der Reduktion von Exazerbationen zwar insgesamt nicht signifikant, die Studie konnte aber einen Rückgang der Exazerbationen bei Proband:innen mit erhöhten Baseline-Bluteosinophilen zeigen.
Im Bereich des breiten Spektrums der Biologikatherapien werden noch weitere große Beweisstudien benötigt, so Löffler-Ragg. Vielversprechende Real-World-Daten zum Einsatz verschiedener Biologika zur Exazerbationsreduktion bei Patient:innen mit Asthma und COPD gibt es von Lommatzsch et al. Die Therapien bewirkten Exazerbationsreduktionen, eine bessere klinische Kontrolle und haben zum Teil Effekte auf die Lungenfunktion.22
Die „treatable traits“ bei COPD und detaillierte Arztbriefe
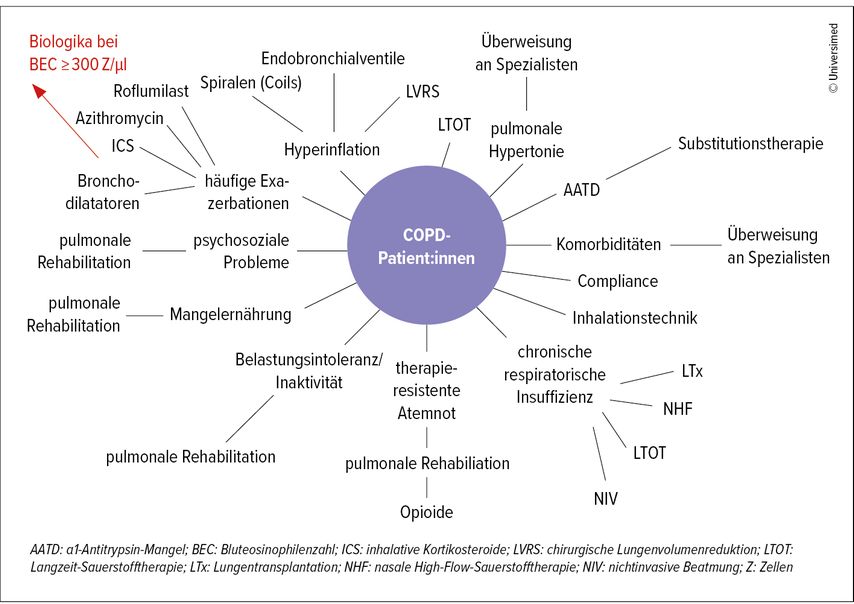
Abbildung 3 zeigt orientierend die „treatable traits“23 bei schwerer COPD, die es zu berücksichtigen gilt und auf die Löffler-Ragg abschließend hinwies: „Wir haben viel abzuarbeiten: Klinik, Lungenfunktion, Biomarker und Bildgebung, unter anderem auch auf einen Alpha-1-Antitrypsin(AAT)-Mangel zu schauen und auf die Optionen bei Hyperinflation. Darüber hinaus müssen wir prüfen, ob die Dyspnoe nicht psychosozial überlagert ist, ob der Rehabilitationsstatus und die Inhalationstechnik passen.“ Bleiben trotz all dieser Maßnahmen Patient:innen mit häufigen Exazerbationen übrig, kommt die inhalative Triple-Therapie zum Einsatz bzw. sind bei bronchitischem Phänotyp auch Roflumilast oder Azithromycin zu erwägen.
Abb. 3: Überblick über die „treatable traits“ bei fortgeschrittener COPD mit den Behandlungsoptionen inkl. Biologika für eine sehr selektionierte Subgruppe (modifiziert nach van Dijk M et al. 2020)23
Neben dieser Eskalation stellen Biologika eine weitere Option dar. In diesem Zusammenhang forderte Löffler-Ragg ein ausführlicheres Reporting im Diagnosekopf von Arztbriefen mit mehr Details zu Ätiologie (z.B. AAT-Mangel, „pack years“, andere Exposition) und Endotyp (Biomarker: Eosinophile, FeNO, IgE), mit CT-Befunden (emphysematös, bronchitisch, Mucus-Plugs), Komorbiditäten, Reha- und Impfstatus, anstatt nur „COPD IVE“ zu schreiben. Das sei wichtig, um Informationsverluste zu vermeiden und einen multimodalen Therapieplan (pulmonal/extrapulmonal) zu ermöglichen.
Zusammenfassung
Die Behandlung der COPD befindet sich im Wandel. Während in der Vergangenheit eine rein symptomorientierte Therapie dominierte, entwickeln sich zunehmend individualisierte Ansätze, die Ätiologie, Biomarker, klinische und radiologische Phänotypisierung zur Gestaltung multimodaler Therapiepläne einbeziehen. Die wichtigsten Handlungsempfehlungen lauten:
-
Früherkennung und Prävention: Früherkennung von Prä-COPD und PRISm mit Reduktion von Risikofaktoren könnte das Fortschreiten der Krankheit verhindern.
-
Regelhafte kardiovaskuläre Abklärung inkl. PH bei allen Schweregraden der COPD
-
Multimodales Management: Kombination aus pharmakologischen und nichtpharmakologischen Strategien
-
Optimierte Pharmakotherapie: Neue Medikamente wie Ensifentrin und Dupilumab bzw. andere Biologika erweitern künftig das therapeutische Spektrum für selektionierte Phänotypen.
-
Proaktive Medizin: Der Übergang von einer reaktiven zu einer proaktiven Behandlungsstrategie verbessert die langfristige Prognose.
Quelle:
„State of the Art COPD & Asthma“, Vortrag von Prim. Ao. Univ.-Prof. Dr. Judith Löffler-Ragg, Natters, im Rahmen des 12. Pneumo Aktuell am 25. Jänner 2025 in Wien
Literatur:
1 Global Initiative for Chronic Obstructive Lung Disease (GOLD): Global strategy for prevention, diagnosis and management of COPD: 2025 Report. https://goldcopd.org/2025-gold-report/ ; zuletzt aufgerufen am 30.1.2025 2 Global Initiative for Asthma: GINA Main Report 2024. https://ginasthma.org/2024-report/ ; zuletzt aufgerufen am 30.1.2025 3 Studnicka M et al.: COPD prevalence in Salzburg, Austria. Chest 2007; 131(1): 29-36 4 Wijnant SRA et al.: Trajectory and mortality of preserved ratio impaired spirometry: the Rotterdam Study. Eur Respir J 2020; 55: 1901217 5 Tanabe N: Increase attention to computed tomography findings of emphysema without airflow limitation: small airway disease is already there. Am J Respir Crit Care Med 2024; 209(6): 619-21 6 Chen H et al.: Association of inhaled corticosteroids with all-cause mortality risk in patients with COPD: a meta-analysis of 60 randomized controlled trials. Chest 2023; 163(1): 100-14 7 Quint JK et al.: Rational use of inhaled corticosteroids for the treatment of COPD. NPJ Prim Care Respir Med 2023; 33(1): 27 8 Augusti A et al.: Inhaled corticosteroids in COPD: friend or foe? Eur Respir J 2018; 52(6): 1801219 9 Lea S et al.: How inhaled corticosteroids target inflammation in COPD. Eur Respir Rev 2023; 32: 230084 10 Beuschlein F et al.: European Society of Endocrinology and Endocrine Society Joint Clinical Guideline: Diagnosis and therapy of glucocorticoid-induced adrenal insufficiency. Eur J Endocrinol 2024; 190(5): G25-G51 11 Anzueto A et al.: Ensifentrine, a novel phosphodiesterase 3 and 4 inhibitor for the treatment of chronic obstructive pulmonary disease: randomized, double-blind, placebo-controlled, multicenter phase III trials (the ENHANCE Trials). Am J Respir Crit Care Med 2023; 208(4): 406-16 12 Bhatt SP et al.: Dupilumab for COPD with type 2 inflammation indicated by eosinophil counts. N Engl J Med 2023; 389(3): 205-14 13 Bhatt SP et al.: Dupilumab for COPD with blood eosinophil evidence of type 2 inflammation. N Engl J Med 2024; 390(24): 2274-83 14 Graul EL et al.: Temporal risk of nonfatal cardiovascular events after chronic obstructive pulmonary disease exacerbation: a population-based study. Am J Respir Crit Care Med 2024; 209(8): 960-72 15 Celli BR et al.: An updated definition and severity classification of chronic obstructive pulmonary disease exacerbations: the Rome Proposal. Am J Respir Crit Care Med 2021; 204(11): 1251-8 16 Celli BR et al.: Differential diagnosis of suspected chronic obstructive pulmonary disease exacerbations in the acute care setting: best practice. Am J Respir Crit Care Med 2023; 207(9): 1134-44 17 Tello K et al.: Association of phosphodiesterase-5 inhibitor treatment with improved survival in pulmonary hypertension associated with COPD in the Pulmonary Vascular Research Institute GoDeep Meta-Registry. Chest 2025; 167(1): 224-40 18 Mettler SK et al.: Silent airway mucus plugs in COPD and clinical implications. Chest 2024; 166(5): 1010-9 19 Arima M et al.: Eosinophilic mucus diseases. Allergol Int 2024; 73(3): 362-74 20 GSK-Presseinformation: www.gsk.com/media/11545/matinee-press-release-060924.pdf ; zuletzt aufgerufen am 4.2.2025 21 Singh D et al.: Efficacy and safety of tezepelumab versus placebo in adults with moderate to very severe chronic obstructive pulmonary disease (COURSE): a randomised, placebo-controlled, phase 2a trial. Lancet Respir Med 2025; 13(1): 47-58 22 Lommatzsch M et al.: Response to various biologics in patients with both asthma and chronic obstructive pulmonary disease. Respiration 2023; 102(12): 986-90 23 van Dijk M et al.: Treatment of severe stable COPD: the multidimensional approach of treatable traits. ERJ Open Res 2020; 6(3): 00322-2019 24 Kersul AL, Cosio BG: Biologics in COPD. Open Respir Arch 2024; 6(2): 100306
Das könnte Sie auch interessieren:
Telemonitoring bei CPAP-Patienten:Begleitung von Anfang an
Inder Therapie schlafbezogener Atmungsstörungen bietet Telemonitoring (TM) die Möglichkeit, Probleme insbesondere in der Gewöhnungsphase, aber auch später auftretende Therapieprobleme ...
Pathobiologie und Genetik der pulmonalen Hypertonie
Für die 7. Weltkonferenz für pulmonale Hypertonie (World Symposium on Pulmonary Hypertension; WSPH) 2024 beschäftigten sich zwei Task-Forces aus 17 internationalen Experten allein mit ...