Die optimale Prostatastanzbiopsie – wo stehen wir?
Autoren:
Dr. Conrad Leitsmann
Priv.-Doz. DDr. Johannes Mischinger
Universitätsklinik für Urologie,
Medizinische Universität Graz
E-Mail:
Der breite Einsatz der multiparametrischen Magnetresonanztomografie (mpMRT) bei Patienten mit einem Verdacht auf ein Prostatakarzinom (PCa) hat die traditionelle Landschaft der Prostatabiopsie tiefgreifend verändert. Darüber hinaus konfrontiert uns die zunehmende kritische Anwendung von Antibiotika im periinterventionellen Einsatz mit neuen Herausforderungen.
Keypoints
-
Die perineale MRT-TRUS-Fusionsbiopsie entwickelt sich immer mehr zur Standardbiopsietechnik.
-
Eine Antibiotikagabe, vor allem bei einer transrektalen Biopsie, sollte kritisch und gezielt durchgeführt werden.
-
Der Stellenwert der antibiotischen Prophylaxe im transperinealen Setting zur Prävention symptomatischer Harnwegsinfekte muss überprüft werden.
-
Neue Techniken wie Mikroultraschall sind vielversprechend, jedoch fehlen noch umfangreichere Daten, welche die Möglichkeiten und potenziellen Probleme adressieren.
-
KI hat großes Potenzial, die Zuverlässigkeit der Bildgebung und Biopsie zu erhöhen.
Fortschritt in der Detektion eines klinisch signifikanten PCa
In der Erstdiagnostik des PCa hat die mpMRT des Beckens und der Prostata in letzter Zeit zunehmend an Bedeutung gewonnen. Läsionen in der mpMRT sollten gemäß der PI-RADS-Klassifikation Version 2.1 eingestuft werden.1 Eine PI-RADS-Läsion ≥3 gilt als verdächtig im Hinblick auf eine Malignität und sollte biopsiert werden.2 Die auf die mpMRT-Bildgebung gestützte Prostatabiopsie (MRT-PBx) hat eine deutliche Verbesserung bei der Detektion eines Prostatakarzinomgrades ≥2 gemäß ISUP (Gleason ≥7a) im Vergleich zur systematischen konventionellen Ultraschall-gestützten PBx gezeigt.3,4 Die Genauigkeit bei der Identifizierung der signifikanten PCa-Indexläsion korreliert mit bis zu 90% mit dem Präparat nach radikaler Prostatektomie (RP).5 Die Korrelation mit Proben aus radikalen Prostatektomien bestätigt somit, dass die MRT der Prostata eine gute Sensitivität für die Erkennung und Lokalisierung eines PCa mit einem ISUP-Grad ≥2 hat, insbesondere wenn der Durchmesser der Läsion größer als 10mm ist.6
Diese Erkenntnisse führten unter anderem dazu, dass die Leitlinie der Europäischen Fachgesellschaft (EAU) heute die Durchführung einer mpMRT vor einer PBx empfiehlt.2 Der transperineale Zugang und die Entwicklung neuer Sonografiegeräte werfen aktuell die Frage nach der optimalen Biopsietechnik auf.
Zugangswege der Fusionsbiopsie
Eine mpMRT-PBx kann entweder perineal oder transrektal durchgeführt werden. Beide Zugangsweisen sind technisch gut durchführbar und bieten eine hohe Bildqualität für eine effektive Fusionsbiopsie. Jedoch unterscheiden sich die beiden Methoden hinsichtlich ihrer potenziellen Risiken und der diagnostischen Effizienz. In jüngster Zeit hat der perineale Zugang aufgrund einiger Vorteile zunehmend an Bedeutung gewonnen.2 Zahlreiche randomisierte Studien zeigen, dass der perineale Zugang nicht nur eine bessere Detektionsrate für klinisch signifikante Tumoren bietet, sondern auch mit einer signifikant niedrigeren Rate an Infektionen und Sepsis verbunden ist.7,8
Eine dieser Studien von Tu et al. unterstreicht die Effektivität des perinealen Ansatzes besonders in der Identifizierung von signifikanten Tumoren, die eine sofortige therapeutische Intervention erfordern.9 Eine weitere Studie zeigte, dass die Infektionsrate beim perinealen Zugang im Vergleich zum transrektalen Zugang signifikant niedriger war. Die Sepsisrate lag bei Patienten, die perineal biopsiert wurden, nahezu bei null, während diejenigen, die transrektal biopsiert wurden, eine höhere Komplikationsrate in Bezug auf Infektionen aufwiesen.10 Die Ergebnisse sind besonders relevant in Zeiten zunehmender Antibiotikaresistenzen, da jede Reduktion von infektionsbedingten Komplikationen und die damit verbundene Vermeidung einer antibiotischen Behandlung von Bedeutung sind.11
Verzicht auf antibiotische Prophylaxe
Der perineale Zugang ermöglicht die Durchführung des Eingriffs mit minimaler Antibiotikagabe(„single shot“) oder gar ohne eine solche.8 Die EAU-Leitlinie befürwortet klar den perinealen Zugang zur Reduktion von Antibiotikagaben und zur Minimierung von Infektionskomplikationen.2 Im Gegensatz dazu erfordert der transrektale Zugang aufgrund des höheren Risikos für eine bakterielle Kontamination strengere präventive Maßnahmen. Hier wird empfohlen, vor der Biopsie einen rektalen Abstrich durchzuführen und eine prophylaktische Behandlung mit zwei verschiedenen Antibiotikaklassen zu initiieren.2 Der Einsatz von Fluorchinolonen ist dabei aufgrund erhöhter Risiken nicht mehr für die Prophylaxe bei der PBx empfohlen,12was die urologische Community seitdem bezüglich der Wahl eines geeigneten Antibiotikums im Unklaren lässt. Dies unterstreicht die Bedeutung des perinealen Zugangs als sicherere und antibiotikasparende Alternative in der modernen PCa-Diagnostik. Das Sepsisrisiko ist bei der transperinealen PBx so gering, dass letztlich in einer randomisierten Studie nur evaluiert werden kann, ob die antibiotische Prophylaxe notwendig ist, um einen symptomatischen Harnwegsinfekt zu verhindern.
Durchführung unter Lokalanästhesie
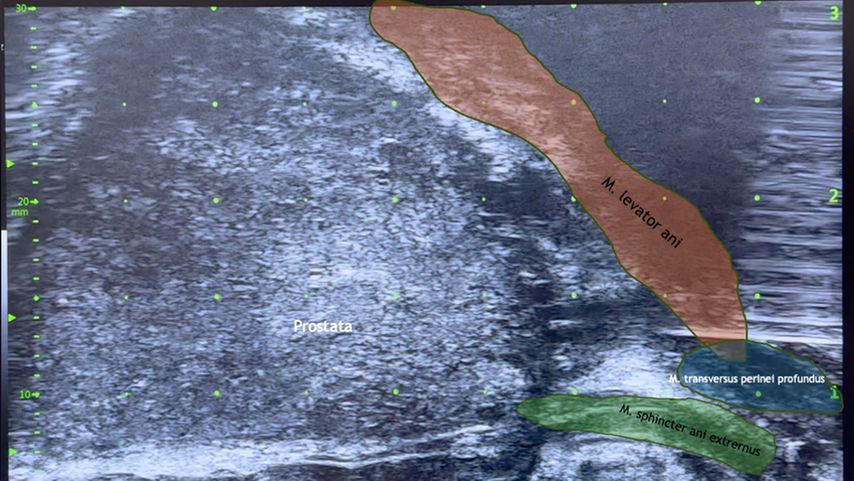
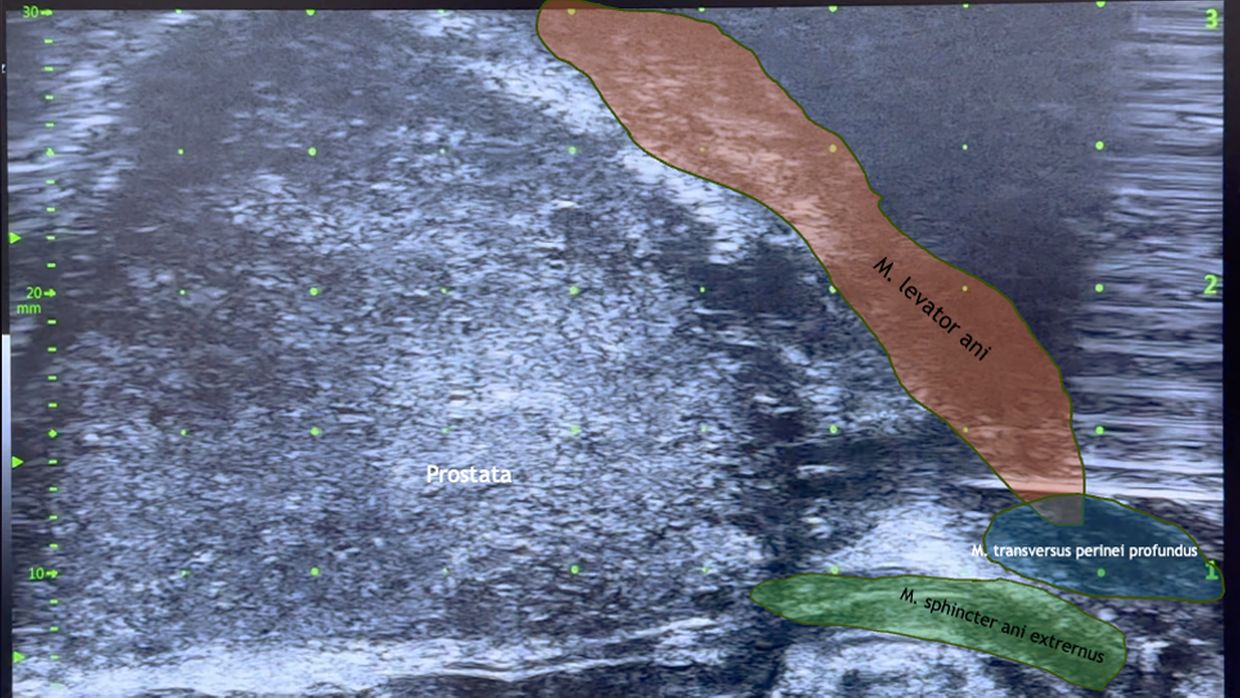
Der perineale Zugang für die PBx (Abb. 1) bietet nicht nur größere diagnostische und infektiologische Vorteile, sondern ist auch in Bezug auf den Patientenkomfort effektiv. Diese Methode kann zunehmend erfolgreich unter lokaler Betäubung durchgeführt werden. Die lokale Betäubung minimiert das Unbehagen und die Schmerzen während des Eingriffs erheblich und macht den perinealen Zugang für die Patienten gut tolerierbar. Zudem werden die schon begrenzten Ressourcen unserer Gesundheitseinrichtungen nicht zusätzlich belastet. Die Patienten berichten häufig von einer schnellen Erholung und geringen postoperativen Beschwerden – ein weiterer Pluspunkt als bevorzugte PBx-Option.13
Abb. 1: Perinealer Zugang für die Prostatabiopsie mit den wichtigsten Leitstrukturen
Ausschlaggebend ist die Erfahrung des Operateurs
Auf dem Markt existieren zahlreiche Systeme zur Durchführung einer MRT-PBx, die von verschiedenen Herstellern angeboten werden. Ein direkter Vergleich dieser Systeme würde es Urologenermöglichen, die jeweiligen Vor- und Nachteile gegeneinander abzuwägen. Jedoch gibt es diesen bis dato nicht. Interessanterweise zeigen Studien bei vorbiopsierten Patienten,8 die kognitive Biopsien (bei denen der Arzt visuell MR-Bilder mit Ultraschallbildern während des Eingriffs abgleicht) mit echten Fusionsbiopsien (bei denen eine Software die Bildfusion automatisch vornimmt) vergleichen, keinen signifikanten Unterschied in Bezug auf die Genauigkeit der Tumordetektion.14 Dies deutet darauf hin, dass die Wahl des Systems weniger von der Technologie als vielmehr von der Erfahrung und dem Können des ausführenden Urologen abhängt.15
Neue Technologien
Der Mikroultraschall der Prostata, eine innovative Technologie in der Prostatabildgebung, nutzt beispielsweise hochauflösenden Ultraschall mit einer Frequenz von 29MHz, um besonders detaillierte Bilder zu erzeugen. Diese ermöglicht eine exzellente Auflösung, um verdächtige Areale zu identifizieren, insbesondere der peripheren Zone. Für die Beurteilung der Ultraschallbilder wird der PRI-MUS-Score verwendet, der sich am PIRADS-Score für MRT-Befunde orientiert.16 Erste Studien weisen darauf hin, dass die Detektionsraten mittels Mikroultraschall vergleichbar mit denen der mpMRT sind, was ihn zu einem vielversprechenden Ansatz macht und möglicherweise zukünftig Biopsien ohne vorhergehende MRT ermöglicht. Allerdings sind weitere Untersuchungen erforderlich, um die Effektivität und Sicherheit von Mikroultraschall-gestützten PBx vollständig zu validieren.17
Aktuelle Studien wurden zwar teilweise verblindet durchgeführt, jedoch fehlt derzeit ein echter Vergleich der Detektionsraten in einem komplett verblindeten Verfahren zwischen der mpMRT-PBx und der ausschließlich auf Mikroultraschall basierenden PBx mit einer großen Anzahl von Patienten.18 Somit wird Mikroultraschall hauptsächlich ergänzend zum mpMRT verwendet und es bestehen weiterhin Herausforderungen, insbesondere auch die fehlende Beurteilung der Transitionalzone, die noch adressiert werden müssen, um die Methode als eigenständige diagnostische Option zu etablieren2,18
Auch im Bereich der Prostatakrebsdiagnostik spielt das Thema künstliche Intelligenz (KI) eine zunehmende Rolle. Erste Untersuchungen zur Nutzung von KI in der Befundung des mpMRT deuten darauf hin, dass hier Potenzial besteht, die Genauigkeit der Diagnose zu verbessern. KI-Anwendungen in der Fusionsbiopsie, wo sie zur präziseren Detektion des PCa beitragen könnten, sind dabei besonders vielversprechend, befinden sich jedoch größtenteils noch im experimentellen Stadium. Um ihre Wirksamkeit und Anwendbarkeit im klinischen Alltag zu bestimmen, sind weitere umfassende Studien notwendig. Die Integration von KI könnte zukünftig eine bedeutende Rolle in der Optimierung der Krebsdiagnostik spielen, indem sie die Zuverlässigkeit der Bildgebung und Biopsie erhöht und somit zu effektiveren und zielgerichteteren Behandlungsstrategien führt.2,19
Einfluss auf die Behandlungstrategie
Die mpMRT-PBx zeigt im Weiteren auch einen bedeutenden Einfluss auf die Behandlungsstrategien und deren Ergebnisse. Insbesondere verbessert sie die Verlaufskontrolle bei der aktiven Überwachung des PCa und ermöglicht durch die höhere Detektionsrate eine präzisere Überwachung der Krankheitsentwicklung, was zu einer gezielteren und bedarfsgerechten Behandlung führt.20 Diese genauere Diagnostik führt auch nach RP zu besseren funktionellen und onkologischen Ergebnissen, da eine präzise Lokalisierung und Charakterisierung des Tumors vor der Operation eine optimierte chirurgische Planung ermöglichen.21 Somit trägt die verbesserte Qualität der Biopsie durch die mpMRT-PBx nicht nur zur genaueren Diagnose bei, sondern beeinflusst maßgeblich die gesamte therapeutische Vorgehensweise und verbessert langfristig die Prognose der Patienten.
Fazit
Zusammenfassend ist festzuhalten, dass die perineale mpMRT-PBx ohne Antibiotikagabe oder mit einem Single-Shot-Antibiotikum heute das Mittel der Wahlist. Weitere technische Entwicklungen bleiben abzuwarten.
Literatur:
1 Oerther B et al.: Cancer detection rates of the PI-RADSv2.1 assessment categories: systematic review and meta-analysis on lesion level and patient level. Prostate Cancer Prostatic Dis 2022; 25(2): 256-63 2 Mottet N et al.: Guidelines on Prostate Cancer, EAU Guidelines. Edn. presented at the EAU Annual Congress Paris 2024. ISBN 978-94-92671-23-3 3 Drost FH et al.: Prostate MRI, with or without MRI-targeted biopsy, and systematic biopsy for detecting prostate cancer. Cochrane Database Syst Rev 2019; 25(4): CD012663 4 Kasivisvanathan V et al.: MRI-targeted or standard biopsy for prostate-cancer diagnosis. N Engl J Med 2018; 378(19): 1767-77 5 Radtke JP et al.: Multiparametric magnetic resonance imaging (MRI) and MRI-transrectal ultrasound fusion biopsy for index tumor detection: correlation with radical prostatectomy specimen. Eur Urol 2016; 70(5): 846-53 6 Bratan F et al.: Influence of imaging and histological factors on prostate cancer detection and localisation on multiparametric MRI: a prospective study. Eur Radiol 2013; 23(7): 2019-29 7 Berry B et al.: Comparison of complications after transrectal and transperineal prostate biopsy: a national population-based study. BJU Int 2020; 126(1): 97-103 8 Wegelin O et al.: The FUTURE Trial: A multicenter randomised controlled trial on target biopsy techniques based on magnetic resonance imaging in the diagnosis of prostate cancer in patients with prior negative biopsies. Eur Urol 2019; 75(4): 582-90 9 Tu X et al.: Transperineal magnetic resonance imaging-targeted biopsy may perform better than transrectal route in the detection of clinically significant prostate cancer: systematic review and meta-analysis. Clin Genitourin Cancer 2019; 17(5): e860-e70 10 Hu JC et al.: Transperineal versus transrectal magnetic resonance imaging-targeted and systematic prostate biopsy to prevent infectious complications: the PREVENT randomized trial. Eur Urol 2024; S0302-2838(23)03342-0 11 Bennett HY et al.: The global burden of major infectious complications following prostate biopsy. Epidemiol Infect 2016; 144(8): 1784-91 12 Bundesinstitut für Arzneimittel und Medizinprodukte: Rote-Hand-Brief zu Fluorchinolon-Antibiotika, 8. April 2019 13 Bulusu A et al.: Current perceptions, practice patterns, and barriers to adoption of transperineal prostate biopsy under local anesthesia. Urology. 2024; S0090-4295(24)00292-9 14 Pirola GM et al.: Transperineal US-MRI fusion-guided biopsy for the detection of clinical significant prostate cancer: asystematic review and meta-analysis comparing cognitive and software-assisted technique. Cancers (Basel) 2023; 15(13): 3443 15 Lenfant L et al.: Learning curve for fusion magnetic resonance imaging targeted prostate biopsy and three-dimensional transrectal ultrasonography segmentation. BJU Int 2024; 133(6): 709-16 16 Sountoulides P et al.: Micro-ultrasound-guided vs multiparametric magnetic resonance imaging-targeted biopsy in the detection of prostate cancer: asystematic review and meta-analysis. J Urol 2021; 205(5): 1254-62 17 Ghai S et al.: Comparison of micro-US and multiparametric MRI for prostate cancer detection in biopsy-naive men. Radiology 2022; 305(2): 390-8 18 Klotz L et al.: Optimization of prostate biopsy - micro-ultrasound versus MRI (OPTIMUM): A 3-arm randomized controlled trial evaluating the role of 29 MHz micro-ultrasound in guiding prostate biopsy in men with clinical suspicion of prostate cancer. Contemp Clin Trials 2022; 112: 106618 19 Kim H et al.: The role of AI in prostate MRI quality and interpretation: Opportunities and challenges. Eur J Radiol 2023; 165: 110887 20 Valentin B et al.: Magnetic resonance imaging-guided active surveillance without annual rebiopsy in patients with grade group 1 or 2 prostate cancer: the prospective PROMM-AS study. Eur Urol Open Sci 2024; 59: 30-8 21 Leitsmann C et al.: Impact of multiparametric magnetic resonance imaging targeted biopsy on functional outcomes in patients following robot-assisted laparoscopic radical prostatectomy. Front Surg 2023; 10: 1305365
Das könnte Sie auch interessieren:
Prostatakarzinom: Screening, Diagnostik, Bildgebung, Biopsie und Optionen im lokalisierten und metastasierten Setting
Im April 2024 wurde ein Bericht der Lancet Commission on prostate cancer veröffentlicht, in welchem ein Anstieg der Prostatakarzinominzidenz von 1,4 Millionen 2020 auf 2,9 Millionen im ...
Nierenzellkarzinom: Update zu Diagnostik, Therapie und translationaler Forschung
Am diesjährigen EAU-Kongress in Paris fanden zahlreiche Sitzungen, Vorträge und Diskussionen zum Nierenzellkarzinom (RCC) statt. Es wurden Kontroversen in der initialen Diagnostik sowie ...
Fortschritte & Deeskalationsstrategien in der Therapie von Hoden- & Penistumoren
Am EAU-Kongress 2024 in Paris waren in den Vorträgen zur Therapie des Hoden- und Peniskarzinoms Langzeittoxizität und Deeskalation zwei der häufigsten Stichwörter. U.a. wurden mögliche ...