Point-of-Care-Ultraschall (POCUS): das moderne Stethoskop?
Autoren:
Dr. med. Mark Kirsch
Dr. med. Marius Treusch
Klinik Innere Medizin
Universitätsspital Basel
Petersgraben 4
4031 Basel
E-Mail: mark.kirsch@usb.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der technische Fortschritt hat kleinere «Pocket size»-Ultraschallgeräte mit guter Bildqualität hervorgebracht. Ultraschall steht somit als schnelle bettseitige Untersuchung auch jedem Hausarzt und Internisten zur Verfügung. Wie wird dieser POCUS eingesetzt, wo hat er sich bewährt, welche Vor-, aber auch Nachteile könnte er in der Patientenbehandlung bringen? Wird Point-of-Care-Ultraschall das Stethoskop und die klinische Untersuchung nicht nur komplettieren, sondern in manchen Bereichen sogar ersetzen?
Keypoints
-
Die Integration des Point-of-Care-Ultraschalls (POCUS) in Anamnese und klinische Untersuchung führt zu einer signifikanten Verbesserung der Patientenversorgung.
-
Die Stärke des POCUS liegt darin, dass anamnestische, klinische und sonografische Befunde direkt am Bett des Patienten zusammengeführt werden können.
-
Seit Januar 2022 ist die POCUS-Basis-Notfallsonografie in der Schweiz Bestandteil der Weiterbildung in Allgemeiner Innerer Medizin.
Die Erfindung des Stethoskops führt man auf den Lungenfacharzt René Théophile Hyacinthe Laënnec zu Beginn des 19. Jahrhunderts zurück. Es wird berichtet, dass er nicht mehr sein Ohr direkt auf Brust und Rücken seiner Patientinnen und Patienten legen wollte. Eine Zeitungsrolle soll ihm beim Auskultieren geholfen und ihn auf die Idee der Entwicklung eines Stethoskops gebracht haben. Als er im Jahr 1826 an Tuberkulose starb, war der Ultraschall in seiner klinischen Anwendung noch lange nicht erfunden worden.1
Auch wenn schon Ende des 19. Jahrhunderts der piezoelektrische Effekt als grundlegendes technisches Prinzip des heutigen Ultraschalls von den Gebrüdern Curie entdeckt worden und im Ersten Weltkrieg das Echolot zur Ortung von feindlichen U-Booten zu trauriger Berühmtheit gekommen war, so dauerte es doch noch bis in die 1940er-Jahre, bis das Ultraschallverfahren seine ersten klinisch diagnostischen Anwendungen fand.2
Die interessante Parallele der beiden «Auskultationstechniken» ist, auch wenn die Bezeichnung Stethoskop von den griechischen Begriffen «stethos» (Brust) und «skopein» (schauen) abgeleitet ist und wir auf unserem Ultraschallgerät faszinierende Bilder betrachten, dass beide Techniken doch eigentlich in die Patienten hineinhören und die Bilder aus Schallwellen einmal im Kopf des Arztes und einmal im Computer entstehen.
Nun scheint es auf den ersten Blick so zu sein, dass beide Verfahren – die klinische Untersuchung und der bettseitige Ultraschall – um die Zeit am Patienten konkurrieren, und Stimmen werden laut, dass der Ultraschall in vielen Bereichen die tradierte klinische Untersuchung nicht nur ergänzen, sondern sogar ersetzen könnte. Die Wertigkeit des POCUS im klinischen Alltag im Vergleich zur klinischen Untersuchung mit dem Stethoskop soll in diesem Artikel unter verschiedenen Gesichtspunkten gezielt unter die Lupe genommen werden.
Einfluss des Ultraschalls auf die Arzt-Patienten-Beziehung
Dass eine ausgiebige klinische Untersuchung das Arzt-Patienten-Verhältnis positiv beeinflusst, konnte einmal mehr durch Duan et al. gezeigt werden. Die Gruppe fand heraus, dass die Patientenzufriedenheit steigt, je mehr Komponenten die klinische Untersuchung umfasst.3 Allerdings scheint auch der Einsatz des bettseitigen Ultraschalls die positive Wahrnehmung der Kompetenz des Arztes zu fördern, wie durch Howard et al. in einer Untersuchung bei Patienten, die auf die Notfallstation aufgenommen wurden, gezeigt werden konnte. Hier war nicht nur die Bewertung der Diagnosefindung mittels Ultraschall, sondern auch die Wahrnehmung des medizinischen Personals und der Gesamteindruck der Notaufnahme positiver bei den Patienten, die eine Ultraschalluntersuchung erfahren hatten.4
Lungenultraschall versus pulmonale Auskultation/Untersuchung
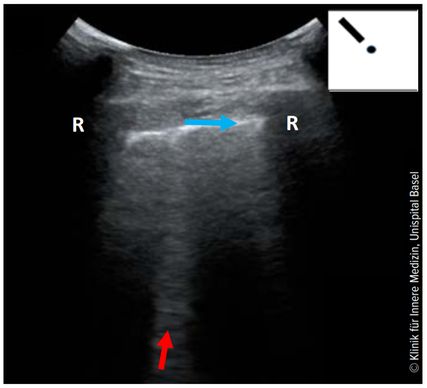
Abb. 1: B-Linie (stationärer POCUS; oben rechts Piktogramm schematisch). R: Rippe mit dorsaler Schallauslöschung; Pfeil (blau): Pleuraspalt; Pfeil (rot): B-Linie
Abb. 2: Kostodiaphragmaler Winkel rechts mit basaler Pneumonie und Randwinkelerguss von dorsal (stationärer POCUS; oben rechts Piktogramm schematisch). LU: Lunge; LE: Leber; R: Rippenschatten; P: Pneumonie; Pfeil (rot): Randwinkelerguss; Pfeil (blau): gefangene Luft
Abb. 3: Zirrhotische Leber mit Aszites hepatopetal durchflossener Pfortader im Color-Doppler (stationärer POCUS; oben rechts Piktogramm schematisch). LE: Leber; DA: Darm; AS: Aszites; Pfeil (blau): V. cava; Pfeil (rot): noch normaler hepatopetaler portaler Fluss im Color-Doppler
Bei der Auskultation der Lungen können für die verschiedenen Untersuchungsqualitäten unterschiedliche Sensitivitäten und Spezifitäten beschrieben und denen der bettseitigen POCUS-Untersuchung entgegengestellt werden (Tab. 1). Wenn es nach Dr. Daniel Lichtenstein, einem der Pioniere des Lungenultraschalls und Erstbeschreiber der B-Linien als Zeichen der vermehrten interstitiellen pulmonalen Flüssigkeit und der A-Linien als mögliches Zeichen eines Pneumothorax5 (Abb.1, typische B-Linie), geht, dann ist der Lungenultraschall der klinischen Untersuchung in Bezug auf die Sensitivität bei der Pneumonie, dem Pleuraerguss (Abb.2, basale Pneumonie mit Begleiterguss), dem Pneumothorax und auch beim interstitiellen Syndrom mit vergleichbarer Spezifität weit überlegen. Dies kann in weiteren Studien in der Grundaussage bestätigt werden, wenn auch die hohe Spezifität z.B. bei der Pneumonie in vielen Studien nicht erreicht wird und die Sensitivität der klinischen Diagnose der Pneumonie von Lichtenstein wahrscheinlich unterschätzt wird. Bei der bettseitigen Diagnose eines symptomatischen Pneumothorax ist zu erwähnen, dass die klinische Diagnose der sonografischen am wenigsten unterlegen zu sein scheint. Erwähnt werden muss jedoch, dass die Angaben der klinischen Untersuchung hier in der Metaanalyse von Arts vor allem Patienten nach stattgehabtem Trauma einschliesst. Bei der Diagnose von Pleuraergüssen würde sich die Wertigkeit der klinischen Diagnose nach unserer Meinung ebenfalls derjenigen der sonografischen stark annähern, wenn nur klinisch relevante grossvolumige Pleuraergüsse zugrunde lägen. Bei der Diagnostik des interstitiellen Syndroms, z.B. im Rahmen einer kardialen Insuffizienz, scheint der Lungenultraschall in den letzten Jahren vermehrt breite Anwendung zu finden. Dies liegt nach unserer Meinung in der unkomplizierten repetitiven Anwendung im klinischen Alltag und der Überlegenheit der Methode im Vergleich zum konventionellen Thoraxröntgen begründet (s. auch Abschnitt zur Herzinsuffizienz). Einmal mehr zeigt sich die Nützlichkeit einer bettseitigen sonografischen pulmonalen Bildgebung beim isolierten Patienten in der Zeit von Covid-196 oder bei instabilen Intensivpatienten.7
Herzsonografie versus kardiale Auskultation/Untersuchung
Die Auskultation der Herzklappen kann lediglich die Klappenbeteiligung und den Mechanismus (Stenose versus Insuffizienz) und allenfalls sehr eingeschränkt eine Graduierung des Schweregrads erfassen. Der Goldstandard ist hier die Echokardiografie durch den Kardiologen. Hier stellt sich nicht die Frage der Überlegenheit der Sonografie gegenüber der klinischen Untersuchung, sondern ob der Herz-POCUS bei einfacheren Fragestellungen auch vom weniger geübten Hausarzt oder Internisten verlässlich durchgeführt werden kann. Hier konnte in mehreren Studien gezeigt werden, dass eine hochgradig eingeschränkte linksventrikuläre Pumpfunktion des Herzens von Internisten mit hoher Treffsicherheit erkannt wird.8,9 In bis zu 97% der Fälle wurde die linksventrikuläre Funktion des Herzens richtig beurteilt.9 Wird die Beurteilung differenzierter, leidet die Zuverlässigkeit und wichtige Befunde können übersehen oder falsch eingeschätzt werden. So fand man in einer retrospektiven Untersuchung im Vergleich von bettseitig durchgeführten Herzsonografien mit kardiologischen Echokardiografien nur noch in 70% übereinstimmende Ergebnisse.10 Zusammenfassend reicht die Qualität der bettseitigen Herzsonografie aber aus, um dem Hausarzt und dem Internisten im klinischen Alltag von Nutzen zu sein, wie in Abschnitten zur Akutmedizin und zur Herzinsuffizienz noch näher ausgeführt wird.
Abdomenultraschall versus abdominelle Auskultation/Untersuchung
Abb. 4: Wenig freie Flüssigkeit (stationärer POCUS; oben rechts Piktogramm schematisch). BL: Blase; U: Uterus; Pfeil (rot): freie Flüssigkeit
Abb. 5: Gestaute Niere rechts, Grad 2–3 (stationärer POCUS; oben rechts Piktogramm schematisch). Pfeil (rot): aufgeweitete Kelchhälse

Abb. 6: Harnleiterstein mit Twinkling-Phänomen kurz vor Austritt in Blase (stationärer POCUS; oben rechts Piktogramm schematisch). BL: Blase; Pfeil (rot): Twinkling-Phänomen
Abb. 7: Abflussbehinderung in Blasenkatheter durch Hämatom (stationärer POCUS; oben rechts Piktogramm schematisch). KB: Katheterballon; Pfeil (rot): Hämatom umgibt kappenartig den Ballon
Abb. 8: Cholezystitis (stationärer POCUS; oben rechts Piktogramm schematisch). GB: Gallenblase; Pfeil (blau): Stein; Pfeil (rot): Flüssigkeit im Gallenblasenbett
Abb. 9: Gallenblase mit verdickter Wand bei Aszites (stationärer POCUS; oben rechts Piktogramm schematisch). AS: Aszites; DA: Darm; GB: Gallenblase
Abb. 10: Teilthrombosiertes infrarenales Bauchaortenaneurysma (stationärer POCUS; oben rechts Piktogramm schematisch). Balken (rot): Durchmesser der Aorta; Balken (blau): Durchmesser des durchflossenen Lumens
Abb. 11: Appendizitis (stationärer POCUS; oben rechts Piktogramm schematisch). Pfeil (blau): Übergang laterale Bauchmuskulatur in Rektusscheide; Pfeil (rot): im Power-Doppler gesteigerte Durchblutung des aufgeweiteten Appendix
Abb. 12: Dünndarmwandödem bei paralytischem Dünndarmileus (stationärer POCUS; oben rechts Piktogramm schematisch). Pfeil (rot): Kerckring-Falten; Balken (blau): verdickte Wand
Auch bei der klinischen Untersuchung und Auskultation des Abdomens kann in vielen Punkten bereits der Vergleich mit dem POCUS erfolgen (Tab. 2).
Die klinische Untersuchung einer Milzvergrösserung kann beim kleinen Organ unter dem linken Rippenbogen nicht sehr sensitiv sein und der POCUS muss hier in der Sensitivität klar überlegen sein. Dennoch gilt es auch hier natürlich, weitere Informationen wie die Körpergrösse, die Form der Milz und den klinischen Kontext in die Interpretation zu integrieren, um eine ausreichende Spezifität zu gewährleisten. Bei der Diagnose einer Hepatomegalie scheint die Ultraschalluntersuchung der klinischen Untersuchung etwas weniger überlegen zu sein, auch wenn in der als Referenz angegebenen Arbeit von Arora et al. die Fähigkeit von Medizinstudenten untersucht wurde. Zum einen sind die sonografischen Messpunkte der Leberausmessung und die maximalen Messparameter immer noch in Diskussion, zum anderen ist eine vergrösserte Leber unter dem rechten Rippenbogen auch der klinischen Untersuchung gut zugänglich. Von entscheidender klinischer Bedeutung ist oft aber nicht die Lebergrösse, sondern vielmehr die Organbeschaffenheit (Verfettung/Fibrose/Zirrhose), wobei die Evaluation mittels Sonografie selbstverständlich entscheidende Vorteile bietet (Abb.3, Leberzirrhose mit Aszites).
Mit dem Ultraschall lassen sich geringste Flüssigkeitsmengen mit hoher Sensitivität zuverlässig bestimmen11 (s. auch Abschnitt zur Akutmedizin sowie Abb.4, geringe intraabdominale Flüssigkeit). Hier erscheint uns die angegebene Sensitivität des POCUS bezüglich sonografischer Detektion von Aszites in der Publikation von Arora et al. mit 77% nicht repräsentativ. Wie bereits erwähnt untersucht diese Arbeit die Fähigkeiten von Medizinstudenten. Die niedrige Sensitivität des POCUS in dieser Untersuchung zeigt wahrscheinlich die Notwendigkeit eines intensiveren Ultraschalltrainings.
Die Evaluation einer postrenalen Komponente beim akuten Nierenversagen ist eine häufige Fragestellung im klinischen Alltag. Neben dem Aspekt, dass einseitige Obstruktionen in der klinischen Untersuchung nicht gut erfasst werden können, scheint auch die klinische Untersuchung einer gefüllten Blase – in der angegebenen Referenz erfolgte die Untersuchung durch das Pflegepersonal – erneut von geringer Sensitivität (Abb.5, Nierenstau Grad III; Abb.6, prävesikaler Harnleiterstein). Es konnte mehrfach gezeigt werden, dass das Blasenvolumen mit geringer Abweichung valide mit der zugrunde liegenden Volumenformel eines Ellipsoids (HöhexBreitexLängex0,5) bestimmt werden kann.12 Automatisierte sog. «Bladder-Scanner» stehen für die einfache Frage des Restharns zur Verfügung. Tragbare Systeme für den ambulanten Bereich sind in Entwicklung13 (Abb.7, Harnblasenkatheter mit Obstruktion durch Blutkoagel).
Bei der Diagnose der Cholezystitis ist der POCUS neben der Klinik die Methode der Wahl. Das Auffinden von Gallensteinen erhöht die Vortestwahrscheinlichkeit für eine Cholezystitis signifikant. Die sonografisch bestimmte Wandverdickung kann nicht losgelöst vom klinischen Kontext betrachtet werden, da sie unspezifisch ist14 (Abb.8, Cholezystitis bei Cholezystolithiasis; Abb.9, Gallenblasenwandverdickung bei Aszites). Ein Hauptbestandteil der klinischen, aber auch der sonografischen Beurteilung ist das sog. Murphy-Zeichen. Hier bringt die genaue Lokalisation der Gallenblase in der Sonografie eine signifikante Steigerung der Sensitivität. In der Bewertung des sonografischen Murphy-Zeichens vermischen sich klinische und sonografische Erfahrung. Der behandelnde Arzt am Bett scheint hier sensitiver zu sein als der «entfernte» Spezialist oder nicht ärztliche technische Mitarbeiter.15 Unter diesem Aspekt kann auch über die bessere Bildgebung bei Cholezystitis (Computertomografie versus POCUS) bezüglich Sensitivität und Spezifität diskutiert werden.16,17 Unbestritten ist, dass in den meisten Fällen die klinische Untersuchung kombiniert mit dem POCUS die Diagnose der Cholezystitis erbringen kann.
Der POCUS hat in vielen nationalen Leitlinien in der Screening-Untersuchung des Bauchaortenaneurysmas Einzug gehalten.18 Bei einer Sensitivität des Palpierens einer «pulsierenden Masse» von 47,1% ist es nicht erstaunlich, dass der POCUS von weit grösserem Nutzen in der Diagnose eines akut rupturierten Bauchaortenaneurysmas ist als die klinische Untersuchung (Abb.10, teilthrombosiertes infrarenales Bauchaortenaneurysma).
Bei der primär klinischen Diagnose der Appendizitis hat der Unterbauchschmerz eine gute Sensitivität. Durch Kombination verschiedener klinischer Parameter kann die Genauigkeit der klinischen Diagnose weiter gesteigert werden (z.B. Alvarado-Score19). Dennoch hat sich der POCUS als zusätzliche Bildgebung bewährt. Hier kann z.B. die Darstellung eines Appendikolithen von entscheidender Bedeutung sein, um das weitere Vorgehen festzulegen. Dem POCUS wird in geübten Händen eine mit der Abdomen-CT vergleichbare Treffsicherheit in der Diagnose der Appendizitis zugeschrieben20 (Abb.11, entzündlich veränderter Appendix).
In der klinischen Untersuchung zur Beurteilung des Darms allgemein wurde gezeigt, dass ein Darmverschluss oder der Grad einer postoperativen Passagestörung durch die Auskultation nur schlecht beurteilt werden kann.21,22 Vor diesem Hintergrund scheint auch die Entwicklung des POCUS des Darms vielversprechend. Auch wenn sich der Darmultraschall meist nur dem erfahrenen Sonografeur erschliesst, konnte seine Wertigkeit doch im Follow-up von chronisch-entzündlichen Darmerkrankungen und in der Diagnostik von weiteren Darmpathologien bereits gezeigt werden23,24 (Abb.12, entzündlich verdickte Dünndarmschleimhaut bei paralytischem Ileus).
Implementierung des Ultraschalls bei Punktionen
Es besteht mittlerweile ein hoher Grad an Evidenz, dass die ultraschallgesteuerte Punktion sicherer ist als eine anatomisch orientierte Punktion. Sei es bei der Aszitespunktion25,26, der Pleurapunktion27 oder z.B. beim Einlegen zentralvenöser Katheter28. Es wird auch diskutiert, ob die Sonografie nicht das postinterventionelle Thoraxröntgen nach Einlage eines zentralvenösen Katheters ersetzen könnte.29
Implementierung von Ultraschallalgorithmen in der Akutmedizin
Historisch gesehen hat der POCUS seit dem Jahrtausendwechsel zunächst in der Akutmedizin Einzug gehalten. Es hat sich eine Vielzahl von fixen Ultraschallalgorithmen z.B. im Rahmen einer kardiopulmonalen Reanimation30, eines unklaren Schockgeschehens (RUSH-Protokoll)31 oder beim polytraumatisierten Patienten (eFAST) etabliert.32,33 Eindrücklich ist z.B. auch die wachsende Evidenz für den Lungenultraschall in der differenzialdiagnostischen Abklärung der akuten Dyspnoe. Hier konnten beispielsweise Pivetta et al. zeigen, dass Lungenultraschall zusätzlich zur klinischen Untersuchung, inklusive Thoraxröntgen und BNP-Bestimmung, in 8 von 100 Fällen dazu führt, dass die ursächliche Zuordnung der Dyspnoe revidiert werden musste.34 In der Abklärung akuter pulmonaler Pathologien hat das sog. BLUE-Protokoll Verbreitung gefunden.35
Implementierung des Ultraschalls bei der Behandlung von herzinsuffizienten Patienten
Ein 3. oder 4. Herzton, ein verbreiterter Herzspitzenstoss, indirekte Zeichen der hydropischen Dekompensation wie Beinödeme, gestaute Halsvenen oder pulmonale Rasselgeräusche können eine Herzinsuffizienz nur mit einer geringen Sensitivität erfassen. Es sei aber angemerkt, dass hier erhobene pathologische Befunde eine hohe Spezifität aufweisen und somit im Prozess der klinischen Diagnosefindung ihren Stellenwert behalten.36
In den letzten 20 Jahren wurde die klinische Untersuchung durch sonografische Methoden ergänzt. Neben der Bestimmung des Diameters von V.cava und V.jugularis und von dessen inspiratorischer Atemvariabilität sind hier auch der Lungenultraschall mit dem Nachweis von vermehrten B-Linien sowie seit ein paar Jahren der Nachweis eines pathologisch veränderten Flussmusters in der Leber- , Nieren- oder Portalvene zu nennen. Der zusätzliche Nutzen einer sonografischen Beurteilung des Volumenstatus kombiniert mit der klinischen Untersuchung konnte bereits eindrücklich aufgezeigt werden. So konnten Pellicori et al. mit der sonografischen Beurteilung der V.cava, der Jugularvenen und der Lungen zeigen, dass in etwa der Hälfte der herzinsuffizienten Patienten ohne klinische Zeichen noch sonografische Zeichen der Hypervolämie gefunden werden können.37 Flussparameter in der Pfortader, der Leber- und Nierenvenen wurden zusätzlich zum Diameter der V.cava in Kombination mit dem sog. VEXUS-Score erfolgreich evaluiert, um ein akutes perioperatives Nierenversagen im Rahmen von kardiochirurgischen Eingriffen mit hoher Spezifität vorherzusagen.38,39
Sehr eindrücklich sind die in den letzten Jahren publizierten Ergebnisse zum ambulanten Management von herzinsuffizienten Patienten unter der Hinzunahme des Lungenultraschalls. Marini et al. sprechen gar von einer «number needed to treat» von 8,4Patienten, um mittels zusätzlichen Ultraschalls eine stationäre Wiederaufnahme zu vermeiden.40 Auch wenn diese Ergebnisse in einer Metaanalyse von Mhanna et al. relativiert werden41 und die Lungenultraschall-basierte Anpassung der Diuretikatherapie noch unscharf umrissen ist, so scheint der Lungenultraschall bei herzinsuffizienten Patienten im ambulanten Setting doch vielversprechend zu sein.
Fazit
Die Sonografie ist fester Bestandteil der modernen Medizin. Die Stärke des POCUS liegt in der bettseitigen Zusammenführung der sonografischen Befunde mit der Anamnese, der klinischen Untersuchung und anderen erhobenen Befunden. So selbstverständlich wie die klinische Untersuchung mit dem Stethoskop zum medizinischen Alltag gehört, so selbstverständlich muss der POCUS integriert werden. In der Ausbildung können sich POCUS und klinische Untersuchung gegenseitig unterstützen.42 Durch die Implementierung der POCUS-Basis-Notfallsonografie in die Weiterbildung für Allgemeine Innere Medizin in der Schweiz seit Januar 2022 wurde diesem wichtigen Aspekt Rechnung getragen. Vor diesem Hintergrund gilt es, die Ausbildungsstrukturen im regen Austausch mit den verantwortlichen Institutionen und Ausbildungsstätten weiter auszubauen. Hier können wir von ersten Erfahrungen am eigenen Standort berichten43 und man kann auch bereits auf internationale Erfahrungen der POCUS-Ausbildung zurückgreifen.44–46 Der Ausbildungsaufwand ist nicht zu unterschätzen, sollte aber aufgrund der hier geschilderten Vorteile für die Patientenversorgung in Angriff genommen werden.
Literatur:
1 The centennial of the stethoscope. JAMA 2016; 315: 2738 2 Newman PG, Rozycki GS: Surg Clin North Am 1998; 78: 179-95 3 Duan L et al.: Postgrad Med 2020; 132: 102-8 4 Howard ZD et al.: J Emerg Med 2014; 46: 46-53 5 Lichtenstein D, Mezière G: Intensive Care Med 1998; 24: 1331-4 6 Kameda T et al.: J Med Ultrason 2021; 48: 31-43 7Brogi E et al.: Crit Care 2017; 21: 325 8 Razi R et al.: J Am Soc Echocardiogr 2011; 24: 1319-24 9 Mjølstad OC et al.: Eur Heart J Cardiovasc Imaging 2013; 14: 1195-202 10 Maxwell AG, Jardine DL: Intern Med J 2019; 49: 1025-8 11 Keil-Ríos D et al.: Intern Emerg Med 2016; 11: 461-6 12Padilha JF et al.: Int Urogynecol J 2020; 31: 973-9 13 Jo HG et al.: Sensors 2021; 21: 5445 14 Runner GJ et al.: AJR Am J Roentgenol 2014; 202: W1-12 15 Noble VE et al.: Eur J Emerg Med 2010; 17: 80-3 16 Wertz JR et al.: AJR Am J Roentgenol 2018; 211: W92-7 17 Gruber H, Loizides A: AJR Am J Roentgenol 2019; 212: W43 18 Benson RA et al.: Br J Radiol 2018; 91: 20170306 19 Alvarado AA: Ann Emerg Med 1986; 15: 557-64 20 Hwang ME: Radiol Technol 2018; 89: 224-37 21 Felder S et al.: J Surg Educ 2014; 71: 768-73 22 Read TE et al.: Dis Colon Rectum 2017; 60: 608-13 23Allocca M et al.: J Crohns Colitis 2021; 15: 143-51 24 Wale A, Pilcher J: Semin Ultrasound CT MR 2016; 37: 301-12 25 Ennis J et al.: Int J Clin Med 2014; 5: 1277-93 26 Millington SJ, Koenig S: Chest 2018; 154: 177-84 27 Peris A et al.: N Engl J Med 2018; 378: e19 28 Saugel B et al.: Crit Care 2017; 21: 225 29 Ablordeppey EA et al.: AEM Educ Train 2021; 5: e10530 30 Blanco P, Martínez Buendía C: J Ultrasound 2017; 20: 193-8 31 Keikha M et al.: Bull Emerg Trauma 2018; 6: 271-8 32 Canelli R et al.: N Engl J Med 2022; 386: e23 33 Netherton S et al.: CJEM 2019; 21: 727-38 34 Pivetta E et al.: Eur J Heart Fail 2019; 21: 754-66 35 Bekgoz B et al.: Am J Emerg Med 2019; 37: 2020-7 36 Watson RD et al.: BMJ 2000; 320: 236-9 37 Pellicori P et al.: Eur J Heart Fail 2019; 21: 904-16 38 Beaubien-Souligny W et al.: J Am Heart Assoc 2018; 7: e009961 39Beaubien-Souligny W et al.: Ultrasound J 2020; 12: 16 40 Marini C et al.: Lung ultrasound-guided therapy reduces acute decompensation events in chronic heart failure. Heart 2020; 106: 1934-9 41 Mhanna M et al.: Heart Fail Rev 2022; 27: 821-6 42 Wong CK et al.: Postgrad Med J 2021; 97: 10-5 43 Arpagaus Armona GF et al.: Prim Hosp Care Allg Inn Med 2022; 22: 42-4 44 Blans MJ et al.: Neth J Med 2020; 78: 116-24 45 Mellor TE et al.: Mil Med 2019; 184: 901-6 46 LoPresti CM et al.: Am J Med 2019; 132: 1356-60 47Arts L et al.: Sci Rep 2020; 10: 7347 48 Lichtenstein D et al.: Anesthesiology 2004; 100: 9-15 49 Ye X et al.: PLoS One 2015; 10: e0130066 50 Xirouchaki N et al.: Intensive Care Med 2011; 37: 1488-93 51Lichtenstein DA et al.: Crit Care Med 2005; 33: 1231-8 52 Arora S et al.: J Ultrasound 2017; 20: 199-204 53 Gosink BB, Leymaster CE: J Clin Ultrasound 1981; 9: 37-44 54 Olson APJ et al.: Crit Ultrasound J 2015; 7: 13 55 Ceratti RDN, Beghetto MG: Rev Gaucha Enferm 2021; 42: e20200014 56 Daurat A et al.: Anesth Analg 2015; 120: 1033-8 57 Jain A et al.: Acad Emerg Med 2017; 24: 281-97 58 Sharif S et al.: CJEM 2021; 23: 626-30 59 Fernando SM et al.: Acad Emerg Med 2022; 29: 486-96 60 Benabbas R et al.: Acad Emerg Med 2017; 24: 523-51
Das könnte Sie auch interessieren:
Management of chronic insomnia according to the latest European guidelines
Insomnia is among the most prevalent sleep disorders, affecting up to one third of adults and 6–10% with chronic forms. The 2023 European Insomnia Guidelines1 emphasize that insomnia is ...
Kognitive und soziale Folgen eines Schlaganfalls
Jährlich erleiden in der Schweiz rund 249 von 100000 Menschen einen Schlaganfall, dessen Folgen weit über die akute medizinische Versorgung hinausreichen. Neben motorischen ...
Gesundheitsbelastungen und Gefährdungen durch Schicht- und Nachtarbeit
Schicht- und Nachtarbeit führen durch Schlafverlust und zirkadiane Desynchronisation zu einem erhöhten Risiko für vielfältige Gesundheitsprobleme. Dazu gehören verbreitete somatische ...