Traitement pharmacologique de l’obésité aujourd’hui et demain
Auteurs:
Dr méd. Lukas Burget1,2
Dr méd. Stefan Fischli1
1Abteilung Endokrinologie/Diabetologie,
Luzerner Kantonsspital
2Adipositaszentrum Zentralschweiz, Luzerner Kantonsspital und Kantonsspital Nidwalden
E-mail: lukas.burget@luks.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le traitement pharmacologique de l’obésité prend de plus en plus d’importance ces dernières années et devrait à l’avenir combler le fossé entre les modifications du mode de vie et la chirurgie bariatrique. Nous présentons dans cet article les différentes options pharmacologiques en détail. Certains de ces médicaments sont déjà autorisés ou en passe de l’être.
L’obésité est devenue une maladie à prendre au sérieux et d’ampleur pandémique ces dernières décennies, le nombre de personnes souffrant d’obésité ayant quintuplé rien qu’en Europe au cours des 50 dernières années. Aux États-Unis, 70% des adultes ont désormais un IMC ≥25kg/m2 et 40% des adultes souffrent d’obésité.1 En Suisse, 42% de la population est en surpoids ou souffre d’obésité et le pourcentage de personnes souffrant d’obésité (IMC ≥30kg/m2) s’élève à 11%. Il est inquiétant de constater que 15% des enfants et des adolescents en Suisse sont déjà en surpoids ou souffrent d’obésité.2
Comorbidités et mortalité liées à l’obésité
Outre une multitude de complications secondaires sévères, telles que le diabète, l’hypertension artérielle, la dyslipidémie, le syndrome d’apnées obstructives du sommeil, les différentes manifestations de la stéatose hépatique, mais aussi les dépressions et les tumeurs, l’obésité contribue ainsi de manière significative à une augmentation de la morbidité et de la mortalité3 — un IMC de 40kg/m2 se traduit par une réduction moyenne de l’espérance de vie pouvant atteindre jusqu’14 ans.4,5 Une perte de poids comprise entre 5 et 15% permet toutefois déjà d’obtenir des améliorations significatives en ce qui concerne les facteurs de risque cardiovasculaires ainsi que les critères d’évaluation «durs», tels que l’infarctus du myocarde et l’AVC.6–8
Étiologie de l’obésité et mécanismes de régulation de l’appétit
Les causes de l’obésité, qui doit être considérée comme une maladie chronique, sont multifactorielles. Un aspect important est certainement notre système d’appétit et métabolique, déterminé en grande partie génétiquement, qui est confronté pour la première fois depuis moins d’un siècle à un excès calorique constant. La régulation de l’appétit elle-même est extrêmement complexe et régulée par un grand nombre de processus métaboliques périphériques et nerveux centraux.
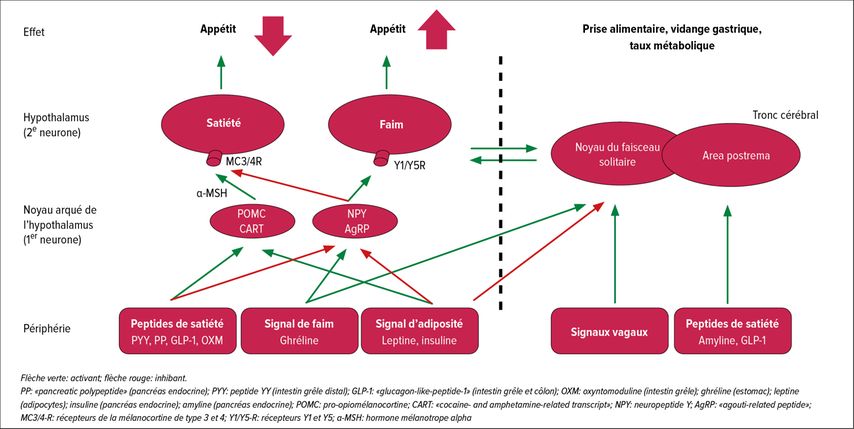
De nombreuses hormones, principalement gastro-intestinales, telles que la ghréline, le «glucagon-like peptide-1» (GLP-1) ou le «glucose-dependent insulinotropic polypeptide» (GIP), mais aussi la leptine, qui provient des adipocytes, exercent leurs effets modulateurs de l’appétit par l’intermédiaire de récepteurs spécifiques dans le «centre de l’appétit», le noyau arqué de l’hypothalamus.9 Elles y influencent la synthèse et la sécrétion de différents neuropeptides qui ont à leur tour des propriétés directes augmentant (orexigène) ou diminuant (anorexigène) l’appétit (Fig. 1).10 La prise alimentaire est ainsi contrôlée en interaction avec différents mécanismes de l’appétit issus de la zone du «centre de récompense» mésolimbique (alimentation hédoniste) ainsi qu’avec les habitudes alimentaires acquises au fil des années.11
Fig. 1: Représentation schématique du système d’appétit et de satiété principalement basé sur les incrétines
Toute perte de poids significative étant interprétée par l’organisme comme une «urgence calorique», celui-ci tente de retrouver son poids initial en augmentant sa prise alimentaire et en réduisant sa dépense énergétique. Les fluctuations de poids qui en résultent, avec des pertes puis des prises de poids, sont décrites de manière assez pertinente dans le langage courant comme «l’effet yo-yo».12
Objectifs thérapeutiques, options thérapeutiques et «Diabesity»
Une option thérapeutique doit donc non seulement conduire à une perte de poids significative, mais aussi permettre de maintenir ce poids. Tout traitement devrait toujours inclure des mesures de modification du mode de vie, y compris une augmentation de la dépense énergétique (activité physique et sport) et une réduction constante de l’apport calorique quotidien (changement d’alimentation). Cela ne permet toutefois qu’une perte de poids durable de 5 à 10% maximum.13 Désormais bien établies, les opérations bariatriques permettent en revanche d’atteindre des pertes de poids initiales allant jusqu’à 40%, voire jusqu’à 30% à long terme. Les effets bénéfiques en termes de complications secondaires et de réduction de la mortalité ont désormais également été démontrés.14,15 Depuis quelques années, les médicaments spécifiques à l’obésité gagnent également en importance et devraient à l’avenir combler le vide thérapeutique entre la modification stricte du mode de vie et l’opération bariatrique.
La plupart des substances autorisées ou en passe de l’être sont déjà utilisées depuis longtemps comme antidiabétiques extrêmement puissants ou étaient destinées à cette utilisation dès leur première autorisation, avant l’élargissement de l’horizon thérapeutique. Bien que l’effet pharmacodynamique soit différent, la quasi-totalité de ces substances appartiennent au groupe des analogues des incrétines, les incrétines («hormones intestinales») exerçant principalement leur effet sur l’appétit et la graisse corporelle dans les régions de l’hypothalamus et du tronc cérébral.16 En raison de leur effet antihyperglycémiant significatif et extrêmement précieux sur le plan clinique, d’un profil d’effets secondaires bien connus et relativement légers, ainsi que de leur effet protecteur sur le plan cardiovasculaire, ces préparations sont déjà largement utilisées depuis un certain temps en diabétologie et sont bien connues dans ce domaine. En ce sens, il convient de noter que l’obésité et le diabète de type 2 (DT2) sont étroitement liés: près de la moitié des cas de diabète sont étiologiquement basés sur une obésité préexistante et 90% des personnes atteintes de DT2 sont en surpoids ou souffrent d’obésité. Le terme «Diabesity», souvent utilisé aux États-Unis, décrit ainsi très bien cette situation.17,18
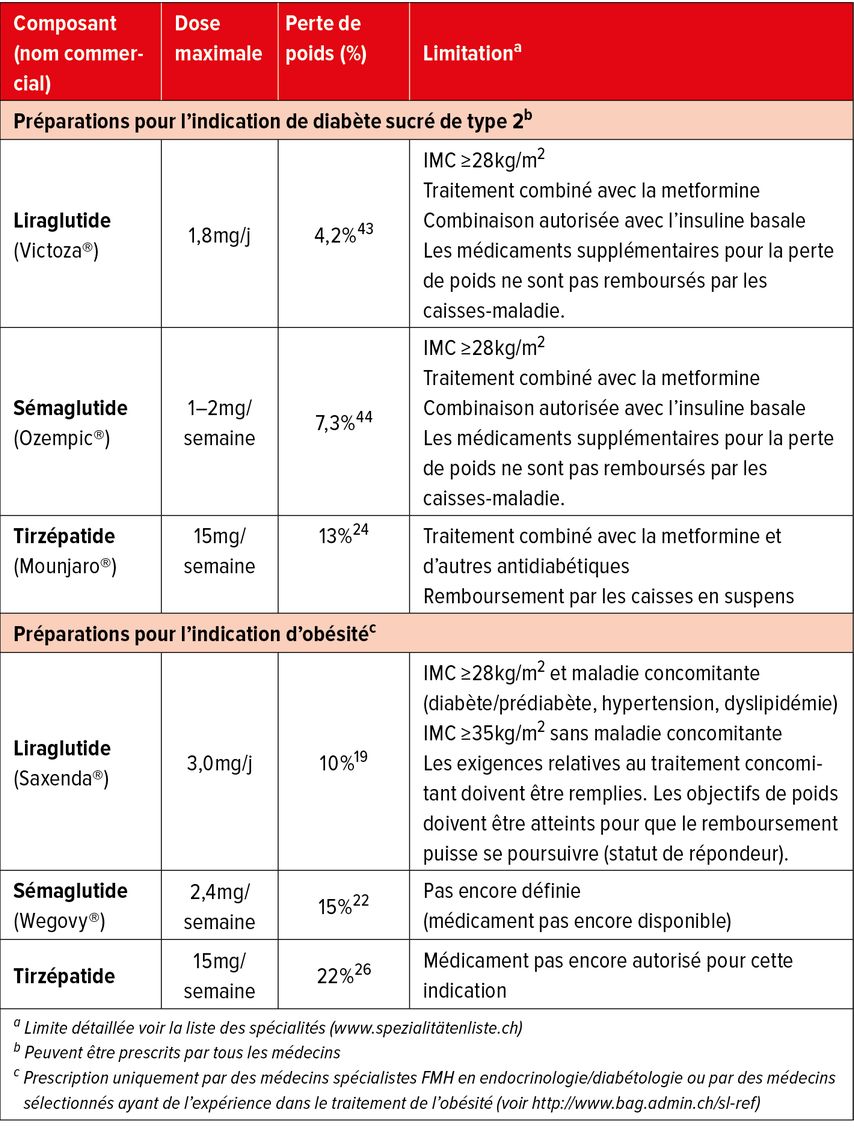
Le tableau 1 donne un aperçu des produits thérapeutiques déjà autorisés en Suisse et de ceux dont l’autorisation et la mise sur le marché sont attendues prochainement. Les composants sont autorisés pour les indications (DT2 ou surpoids/obésité) sous différents noms commerciaux. Il faut en tenir compte, car les préparations avec l’indication «surpoids/obésité» peuvent uniquement être prescrites par des médecins spécialistes FMH en endocrinologie/diabétologie ou par des médecins sélectionnés expérimentés dans le traitement de l’obésité.
Tab. 1: Aperçu des traitements basés sur les incrétines (agonistes des récepteurs du GLP-1, agonistes des récepteurs du GIP/GLP-1) pour le traitement du diabète sucré de type 2 et du surpoids/de l’obésité
Mono-agonistes
Agonistes des récepteurs du GLP-1
Le GLP-1 natif appartient à la classe d’hormones appelées incrétines. Il est synthétisé dans l’intestin grêle et le côlon, et agit par l’intermédiaire de ses récepteurs au niveau du pancréas endocrine, où il entraîne une augmentation de la libération d’insuline en fonction des repas et une inhibition de la sécrétion de glucagon, tout en retardant le transit intestinal. Dans le «centre de l’appétit» hypothalamique, le GLP-1 induit une diminution de la cascade de signalisation des voies orexigènes, de l’appétit et de la prise alimentaire.19 L’un des premiers agonistes des récepteurs du GLP-1 (GLP-1-RA) synthétisés, à savoir le liraglutide 3,0mg (Saxenda®), est utilisé avec succès depuis plusieurs années dans le traitement des patient·es souffrant d’obésité ou en fort surpoids et des complications secondaires. L’étude d’autorisation a permis d’obtenir une perte de poids de près de 10%, sachant que les non-répondeurs, c’est-à-dire les patient·es n’ayant pas perdu de poids, ont également été pris en compte dans le calcul (30%). Les super-répondeurs ayant enregistré des pertes de poids >15% représentaient tout de même 15% dans ce groupe.20 Des pertes de poids nettement plus importantes (>20%) sont également observées dans des cas isolés dans notre clinique. Elles constituent toutefois une exception.
Le potentiel d’effets secondaires de ce principe actif bien connu en diabétologie et, entre-temps, dans le traitement de l’obésité, est faible; il comprend principalement des troubles gastro-intestinaux tels que des nausées et des ballonnements, qui surviennent en particulier pendant la phase de dosage. Initialement suspectée, la survenue fréquente de pancréatites, de goitres, de carcinomes thyroïdiens ou de néoplasies, en particulier de carcinomes pancréatiques, n’a pas été observée dans l’étude d’autorisation ni dans les études ultérieures. La survenue un peu plus fréquente d’une cholélithiase n’est probablement pas uniquement spécifique à la substance, puisque ce phénomène est observé avec pratiquement toutes les méthodes conduisant à une perte de poids efficace et rapide.21,22 Cependant, des modifications spécifiques à la substance sont également discutées, comme une modification du péristaltisme de la vésicule biliaire induite par le GLP-1.
Depuis son inscription sur la liste des spécialités et sa prise en charge par les caisses-maladie, ce traitement est disponible en Suisse pour pratiquement toutes les personnes répondant aux critères de remboursement et peut être prescrit par des médecins spécialistes en endocrinologie/diabétologie ou des médecins expérimentés dans le traitement de l’obésité. Les conditions de remboursement sont un IMC ≥28kg/m2 et la présence de complications secondaires (hypertension artérielle ou dyslipidémie ou prédiabète/DT2) ou un IMC ≥35kg/m2 sans complications secondaires. En ce qui concerne les garanties de remboursement des coûts induits, des pertes de poids définies doivent être obtenues au cours des 10 premiers mois afin que le traitement soit également remboursé pour la période actuellement limitée à trois ans.
Le sémaglutide 2,4mg (Wegovy®), qui ne doit être administré qu’une fois par semaine, a déjà été autorisé par Swissmedic et est sur le point d’être mis sur le marché en Suisse. Ce principe actif, lui aussi déjà bien connu en diabétologie (sémaglutide 1,0mg = Ozempic®), entraîne une perte de poids de 15% en moyenne chez les patient·es non diabétiques et de 7% chez les patient·es diabétiques à la dose spécifique de 2,4mg par semaine.23,24 Chez un tiers des participant·es à l’étude, on a même pu obtenir une perte de poids de 20%. Le potentiel d’effets secondaires est très similaire à celui de Saxenda®. Les modalités de prescription et de remboursement par les caisses-maladie font actuellement l’objet de négociations. Un coup d’œil aux États-Unis, où Wegovy® est déjà utilisé, montre toutefois que Saxenda® sera remplacé par ce nouveau médicament contre l’obésité. D’une manière générale, il convient de noter que la perte de poids induite par les GLP-1-RA est plus importante dans les populations en surpoids non atteintes de DT2 que dans celles atteintes de diabète. Les raisons ne sont pas claires.
La réduction significative de différents facteurs de risque cardiovasculaires obtenue grâce à ces traitements, y compris une baisse de l’HbA1c pouvant atteindre 2% chez les patient·es atteint·es de «Diabesity», est pertinente d’un point de vue holistique et mentionnée par souci d’exhaustivité.
Doubles agonistes
Agonistes des récepteurs du GLP-1/GIP
La régulation endocrinienne et neuronale de l’appétit à plusieurs voies, du niveau périphérique au niveau nerveux central, ayant désormais été étudiée de manière approfondie, ce n’était qu’une question de temps avant que les multi-agonistes ne soient également découverts. Les «twincrétines», ou doubles agonistes des récepteurs du GLP-1/GIP, décrites pour la première fois il y a 10 ans, constituent actuellement la classe la plus intéressante de ces agonistes multirécepteurs.25
Le représentant le plus en vue des «twincrétines» est le tirzépatide, une combinaison d’agonistes des récepteurs du GIP/GLP-1 dans un rapport de 5:1. Comme les GLP-1-RA, le tirzépatide est autorisé et déjà utilisé sur le plan clinique comme antidiabétique sous le nom de Mounjaro®. Dans ce groupe de patient·es atteint·es de DT2, l’accent est mis sur une réduction de l’HbA1c d’environ 2,5% ainsi que sur une perte de poids de 13% en moyenne.26 Dans l’étude d’autorisation pour l’indication d’obésité, les données sont toutefois un peu plus impressionnantes en ce qui concerne le poids, avec des pertes de 22% en moyenne, ce qui place ce traitement dans la catégorie des opérations bariatriques en termes d’efficacité.27 Le potentiel d’effets secondaires du tirzépatide est comparable à celui des GLP-1-RA et est dominé par les troubles gastro-intestinaux. La comparaison des études d’autorisation suggère certes une tolérance légèrement meilleure, mais les différentes populations étudiées ne peuvent pas être comparées directement entre elles et il reste spéculatif de savoir si la tolérance éventuellement meilleure en comparaison peut s’expliquer par la proportion de GIP.
GLP-1-RA en combinaison avecl’amyline synthétique ou les agonistes des récepteurs glucagon
D’autres doubles agonistes ne sont encore prêts à être autorisés ni mis sur le marché. Il convient de mentionner ici la combinaison du sémaglutide, un GLP-1-RA déjà bien connu, et du cagrilintide, une amyline pancréatogène de synthèse qui, outre son effet renforçant l’action de l’insuline, possède également des propriétés de satiété. Le cotadutide, un double agoniste des récepteurs du GLP-1/glucagon, est un autre représentant de ces doubles substances endocrines, qui ont été découvertes dès 2009.28 Les profils des études menées jusqu’à présent diffèrent de ceux des substances déjà autorisées mentionnées et sont parfois nettement plus courts. Des pertes de poids comprises entre 15 et 20% semblent toutefois réalistes, même si les études sur le cotadutide se concentrent majoritairement sur la NAFLD et la NASH.29,30
Triples agonistes et agonistes des récepteurs de la mélanocortinede type 4
Agonistes des récepteurs du GLP-1/GIP/glucagon
Le développement de médicaments contre l’obésité encore plus puissants ne s’arrête pas là. La combinaison d’agonistes des récepteurs du GLP-1/GIP/glucagon permet d’associer trois classes d’hormones favorisant la perte de poids.31 Les pertes de poids de 30% et plus obtenues dans le modèle de souris pourraient également être atteintes dans des groupes de patients souffrant d’obésité: les premières études menées sur des diabétiques souffrant d’obésité montrent une perte de poids moyenne de 10kg après moins de 3mois.32,33 Cela correspond à l’effet de Saxenda®, qui n’a toutefois été atteint qu’au bout de 12 mois dans le cadre de l’étude réalisée à l’époque. Dans une étude de phase II portant sur retratutide, un triple agoniste du GLP-1/GIP/glucagon, publiée récemment, une perte de poids de 24% a été observée après 48 semaines; le poids a continué à diminuer vers la fin de l’étude et une perte supplémentaire semble envisageable en cas de poursuite du traitement.34
Setmélanotide (Imcivree®)
Une obésité monogénique (mutation d’un seul gène) doit être envisagée pour les formes d’obésité sévères et, en particulier, l’obésité apparue dans la petite enfance. Une cause monogénique est identifiée chez jusqu’à 7% de ces patient·es. L’une des mutations les plus fréquentes concerne le récepteur de la mélanocortine de type 4, qui joue un rôle central dans le circuit hypothalamique de régulation de l’appétit.35,36 Avec le setmélanotide (Imcivree®), les autorités de réglementation américaine (FDA) et européenne (EMA) ont désormais autorisé un agoniste des récepteurs de la mélanocortine de type 4 qui permet d’obtenir une réduction de l’hyperphagie et une perte de poids significatives chez les personnes concernées.37,38
Résumé et perspectives
Dans l’ensemble, une nouvelle fenêtre thérapeutique semble s’être ouverte, en particulier pour les patient·es souffrant d’obésité dont l’IMC se situe entre 30 et 40kg/m2. Il est tout à fait envisageable que la combinaison de différents agonistes des récepteurs ou un traitement séquentiel avec alternance des différentes substances constituent le standard thérapeutique dans cette population. L’obésité devant être considérée comme une maladie chronique, à l’instar du diabète, de l’hypertension artérielle ou de l’ostéoporose, un traitement à vie est probablement nécessaire. Contrairement à la chirurgie bariatrique, le traitement pharmacologique est réversible et peut être arrêté ou changé, le cas échéant. Ces traitements ne doivent pas seulement se concentrer sur le poids, mais aussi sur les différentes complications secondaires, les comorbidités et, en fin de compte, la mortalité totale spécifique à l’obésité. Des données d’études valables sont encore attendues, en particulier en ce qui concerne la mortalité. Compte tenu des données sur les critères d’évaluation «durs», telles qu’elles ont déjà été publiées pour les GLP-1-RA chez les diabétiques,39,40 on peut supposer que ces données pourront également être générées à moyen et long terme dans des groupes de patient·es souffrant d’obésité. Dans un communiqué de presse publié récemment, NovoNordisk a communiqué les premiers résultats de l’étude SELECT avec une réduction significative de MACE chez des patients obèses sous 2,4mg de semaglutide.41 Il est important de noter pour les soins de base qu’il existe actuellement des difficultés de livraison pour le sémaglutide 1,0mg (Ozempic®) et qu’un nombre considérable de patient·es diabétiques traité·es par cette préparation doivent passer, au moins temporairement, à d’autres substances. L’une des raisons est probablement une augmentation massive de l’utilisation du sémaglutide dans la vie courante. La promotion de cette tendance sur les médias sociaux par des personnalités comme Elon Musk n’a certainement pas freiné cette évolution.42
Littérature:
1 NCD Risk Factor Collaboration (NCD-RisC): Lancet 2017; 390: 2627-42 2 https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/determinanten/uebergewicht.html 3 Abdelaal M et al.: Ann Transl Med 2017; 5: 161 4 Berrington de Gonzalez A et al.: N Engl J Med 2010; 363: 2211-9 5 Kitahara CM et al.: PLoS Med 2014; 11: e1001673 6 Look AHEAD Research Group; Gregg EW et al.: Lancet Diabetes Endocrinol 2016; 4: 913-21 7 Sundström J et al.: Circulation 2017; 135: 1577-85 8 Lean ME et al.: Lancet 2018; 391: 541-51 9 Clemmensen C et al.: Cell 2017; 168: 758-74 10 Valassi E et al.: Neuroendocrine control of food intake. Nutr Metab Cardiovasc Dis 2008; 18: 158-68 11 Berthoud HR et al.: Gas-troenterology 2017; 152: 1728-38 12 Sumithran P et al.: N Engl J Med 2011; 365: 1597-604 13 Lv N et al.: Prev Med 2017; 100:180-93 14 Alkhalifah N et al.: Surg Endosc 2018; 32: 3024-31 15 Adams TD et al.: N Engl J Med 2017; 377: 1143-55 16 Grandl G et al.: Compr Physiol 2019; 10: 99-124 17 Blüher M: Nat Rev Endocrinol 2019; 15: 288-98 18 Tinajero MG, Malik VS: Endocrinol Metab Clin North Am 2021; 50: 337-55 19 Drucker DJ: Cell Metab 2018; 27: 740-56 20 Pi-Sunyer X et al.; SCALE Obesity and Prediabetes NN8022-1839 Study Group: N Engl J Med 2015; 373: 11-22 21 Funch D et al.: R Diabetes Metab Syndr Obes 2021; 14: 2619-29 22 Kristensen SL et al.: Lancet Diabetes Endocrinol 2019; 7: 776-85 23 Wilding JPH et al.:N Engl J Med 2021; 384: 989-1002 24 Rubino DM et al.: STEP 8 Investigators:JAMA 2022; 327: 138-50 25 Finan B et al.: Sci Transl Med 2013; 5: 209ra151 26 Frías JP et al.: SURPASS-2 Investigators: N Engl J Med 2021; 385: 503-15 27 Jastreboff AM et al.: SURMOUNT-1 Investigators: N Engl J Med 2022; 387: 205-16 28 Day JW et al.: Nat Chem Biol 2009; 5: 749-57 29 Enebo LB et al.: Lancet 2021; 397: 1736-48 30 Nahra R et al.: Diabetes Care 2021; 44: 1433-42 31 Finan B et al.: Nat Med 2015; 21: 27-36 32 Urva S et al.: Lancet 2022; 400: 1869-81 33 Coskun T et al.: Cell Metab 2022; 34: 1234-47.e9 34 Jastreboff AM et al.; Retatrutide Phase 2 Obesity Trial Investigators: Triple-hormone-receptor agonist retatrutide for obesity - a phase 2 trial. N Engl J Med 2023 [epub ahead of print] 35 Malhotra S et al.: Pediatr Genet 2021; 10: 194-204 36 Farooqi IS: Handb Clin Neurol 2021; 181: 301-10 37 Collet TH et al.: Mol Metab 2017; 6: 1321-9 38 Markham A: Drugs 2021; 81: 397-403 39 Marso SP et al.; LEADER Steering Committee: N Engl J Med 2016; 375: 311-22 40 Marso SP et al.; SUSTAIN-6 Investigators: N Engl J Med 2016; 375: 1834-44 41 https://www.novonordisk.com/news-and-media/news-and-ir-materials/news-details.html?id=166301#:~:text=Novo%20Nordisk%20A%2FS%3A%20Semaglutide,the%20SELECT%20cardiovascular%20outcomes%20trial 42 Musk E: Twitter, Oktober 2022 43 Nauck M et al.: Diabetes Care 2016; 39: 1501-9 44 Pratley RE et al.; SUSTAIN 7 investigators: Lancet Diabetes Endocrinol 2018; 6: 275-86
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...