Carcinome hépatocellulaire
Auteur:
Prof. Dr méd. Markus H. Heim
Chefarzt Hepatologie
Clarunis – Universitäres Bauchzentrum Basel
E-mail:
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le carcinome hépatocellulaire (CHC) survient souvent dans le cadre d’une maladie hépatique avancée. Le pronostic n’est donc pas seulement déterminé par le stade de la tumeur, mais aussi, dans une large mesure, par le degré de sévérité de la maladie hépatique. Ces dernières années, des progrès importants ont été réalisés dans le traitement du CHC. Cette revue a pour but de fournir un aperçu actuel de l’épidémiologie, de l’évaluation et du traitement du CHC.
Keypoints
-
Les patients atteints de maladie hépatique avancée, notamment en présence d’une cirrhose, présentent un risque nettement accru de survenue de CHC et doivent être surveillés par échographie tous les 6 mois.
-
Le choix du traitement dépend à la fois du stade de la tumeur et de la fonction hépatique.
-
Aux stades précoces du CHC, des traitements à visée curative sont utilisés: résection chirurgicale, transplantation, ablation percutanée et radiothérapie interne sélective.
-
Au stade intermédiaire, les traitements locorégionaux par voie transartérielle sont au premier plan.
-
Les immunothérapies sont le premier choix en termes de traitement systémique.
Bien que le carcinome hépatocellulaire n’occupe que la 14e place en termes d’incidence en Suisse, il est la sixième cause de décès par cancer.1 La grande majorité des CHC (>90%) surviennent en présence d’une maladie hépatique chronique, telle que l’hépatite C chronique ou l’hépatite B chronique, la maladie hépatique liée à l’alcool et la stéatose hépatique non alcoolique (NAFLD), actuellement rebaptisée MASLD («metabolic dysfunction-associated steatotic liver disease»).2 En Europe occidentale, l’hépatite C chronique et la maladie hépatique liée à l’alcool sont les causes les plus fréquentes.3 La MASLD a toutefois considérablement gagné en importance ces dernières années.4
Indépendamment de l’étiologie de la maladie hépatique sous-jacente, la cirrhose du foie est le principal facteur de risque de survenue de CHC. L’incidence annuelle du CHC en cas de cirrhose s’élève entre 1 et 8%.
Surveillance et diagnostic
L’identification des patients atteints de maladies hépatiques chroniques relève en grande partie du médecin de premier recours. La détermination des valeurs hépatiques dans le cadre des examens de contrôle y contribue grandement. De nombreuses maladies hépatiques peuvent aujourd’hui être guéries, ce qui permet d’éviter la survenue d’une cirrhose. Pour déterminer le stade de la maladie hépatique (stade de fibrose), des tests simples, tels que FIB-4 (score de fibrose 4), mais aussi l’âge, l’aspartate aminotransférase [ASAT], l’alanine aminotransférase [ALAT] et la numération plaquettaire peuvent être utilisés en médecine générale.5 Le stade de fibrose peut être déterminé plus précisément par élastographie impulsionnelle (Fibroscan®), élastographie ultrasonique, élastographie par résonance magnétique (MRE) et biopsie hépatique. En présence d’une cirrhose, les personnes concernées doivent être informées du risque accru de carcinome hépatique et de l’éventualité d’une surveillance. L’European Association for the Study of the Liver (EASL) et la Swiss Association for the Study of the Liver (SASL) recommandent à cet effet une échographie hépatique tous les 6 mois.6,7 En cas de conditions échographiques difficiles, le contrôle peut sinon être effectué par tomodensitométrie (TDM) ou par imagerie par résonance magnétique (IRM) chez les patients concernés. Si un ou plusieurs foyers suspects sont détectés lors d’un examen de contrôle, l’évaluation se poursuit en utilisant des techniques d’imagerie multiphasique avec produit de contraste, telles que la TDM et l’IRM, ou l’échographie avec produit de contraste (CEUS), si possible dans un centre de référence. Si des critères bien définis sont remplis lors de ces examens, le diagnostic de CHC peut également être posé sans confirmation par biopsie.8 Le diagnostic histologique par biopsie tumorale reste toutefois la référence.
Traitement
Une particularité importante du CHC est que le pronostic n’est pas seulement déterminé par le stade de la tumeur, mais aussi par celui de la maladie hépatique sous-jacente. Le cas échéant, l’évaluation et le traitement des patients atteints de CHC doivent être effectués dans un centre disposant d’une grande expertise multidisciplinaire, y compris en hépatologie et en chirurgie hépatique. Au stade précoce du CHC, il convient de mettre en œuvre un traitement à visée curative. Il s’agit notamment de la résection chirurgicale, de la transplantation hépatique, de l’ablation percutanée (par micro-ondes ou radiofréquence) et, pour des patients sélectionnés, de la radiothérapie externe ainsi que de la radiothérapie interne sélective (SIRT, «selective internal radiation therapy») par segmentectomie par SIRT.7,9 Au stade intermédiaire, la tumeur est traitée par voie transartérielle. La chimio-embolisation transartérielle (TACE, «transarterial chemoembolization»), qui a fait ses preuves, est de plus en plus souvent remplacée par la SIRT, plus récente.10 Au stade avancé, la SIRT ou les traitements systémiques peuvent être utilisés si la tumeur se limite encore au foie. En cas de CHC métastasé, le traitement systémique palliatif est au premier plan. Des progrès ont été réalisés dans ce domaine ces dernières années avec l’introduction de l’immunothérapie.11,12 L’allocation correcte de ces options thérapeutiques requiert une classification («staging») minutieuse. Le système de classification «Barcelona Clinic Liver Cancer» (BCLC)13 est très répandu et également recommandé, avec quelques modifications, dans l’«Expert Opinion Statement» (EOS) de la SASL (Fig.1).7
Fig. 1: Système de classification «Barcelona Clinic Liver Cancer» (BCLC) modifié (adapté selon Goossens et al., 2020)7
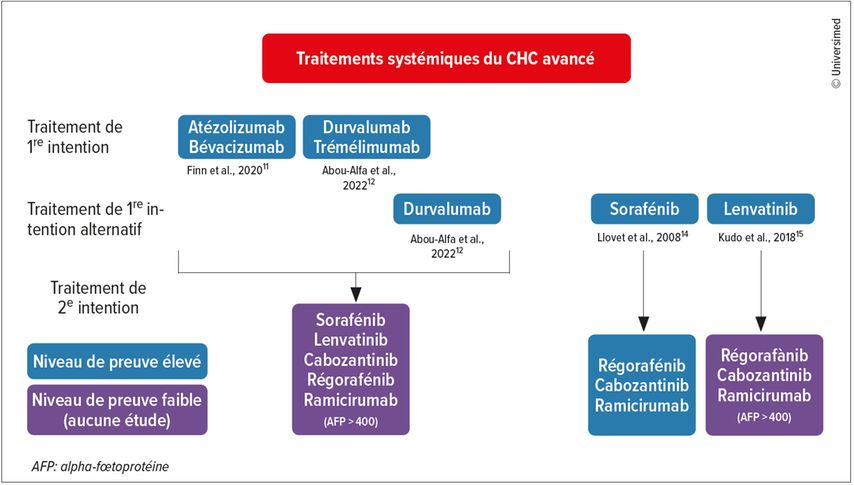
Les préférences actuelles dans le choix des traitements systémiques palliatifs sont illustrées dans la Figure 2, qui se base sur les recommandations internationales.13 En Suisse, les traitements de première intention autorisés sont l’atézolizumab (Tecentriq®) en association avec le bévacizumab (Avastin®), ainsi que les inhibiteurs multikinases sorafénib (Nexavar®) et lenvatinib (Lenvima®). L’association d’immunothérapies durvalumab (Infinzi®) et trémélimumab (Imjudo®) a été récemment autorisée par Swissmedic, et devrait être disponible en Suisse dans les prochains mois.
Perspectives
Après des années de stagnation des options thérapeutiques pour les patients atteints de CHC, des progrès importants ont été réalisés ces dernières années. En chirurgie, des procédures mini-invasives ont été développées, permettant d’opérer des patients atteints de maladie hépatique avancée sélectionnés, car le risque de décompensation de la fonction hépatique a été considérablement réduit. En radiologie interventionnelle, des progrès significatifs dans la radiothérapie interne sélective (SIRT) ont été documentés, conjointement avec la médecine nucléaire, dans des études randomisées contrôlées prospectives. Pour le CHC avancé, l’introduction des immunothérapies constitue un véritable changement de paradigme. Dans tous ces domaines, le développement clinique de nouvelles procédures et de nouveaux médicaments se poursuit avec une grande intensité. Il faut espérer que la mortalité du CHC pourra enfin être réduite dans un avenir proche.
Littérature:
1 NICER: Cancer data extracted from the Swiss national dataset managed by the Foundation National Institute for Cancer Epidemiology and Registration (NICER). http://www.nicer.org/en/statistics-atlas/cancer-incidence/ 2 Rinella ME et al.: A multisociety Delphi consensus statement on new fatty liver disease nomenclature. J Hepatol 2023; 79: 1542-56 3 Singal AG et al.: Epidemiology and surveillance for hepatocellular carcinoma: new trends. J Hepatol 2020; 72: 250-61 4 Huang DQ et al.: Global epidemiology of NAFLD-related HCC: trends, predictions, risk factors and prevention. Nat Rev Gastroenterol Hepatol 2021; 18: 223-38 5 Sterling RK et al.: Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection. Hepatol 2006; 43: 1317-25 6 EASL Clinical Practice Guidelines: management of hepatocellular carcinoma. J Hepatol 2018; 69: 182-236 7 Goossens N et al.: Management of hepatocellular carcinoma: SASL expert opinion statement. Swiss Med Wkly 2020; 150: w20296 8 Bruix J et al.: Clinical management of hepatocellular carcinoma. Conclusions of the Barcelona-2000 EASL conference. European Association for the Study of the Liver. J Hepatol 2021; 35: 421-30 9 Salem R et al.: Yttrium-90 radioembolization for the treatment of solitary, unresectable HCC: the LEGACY study. Hepatol 2021; 74: 2342-52 10 Dhondt E et al.: (90)Y radioembolization versus drug-eluting bead chemoembolization for unresectable hepatocellular carcinoma: results from the TRACE phase II randomized controlled trial. Radiol 2022; 303: 699-710 11 Finn RS et al.: Atezolizumab plus Bevacizumab in unresectable hepatocellular carcinoma. N Engl J Med 2020; 382: 1894-905 12 Abou-Alfa GK et al.: Tremelimumab plus Durvalumab in unresectable hepatocellular carcinoma. NEJM Evid 2022; 1: doi:10.1056/EVIDoa2100070 13 Reig M et al.: BCLC strategy for prognosis prediction and treatment recommendation: the 2022 update. J Hepatol 2022; 76: 681-93 14 Llovet JM; SHARP Investigators Study Group.: Sorafenib in advanced hepatocellular carcinoma. N Engl J Med 2008; 359: 378-90 15 Kudo M et al.: Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomised phase 3 non-inferiority trial. Lancet 2018; 391: 1163-73
Das könnte Sie auch interessieren:
Diabète de type 1: recherche de stratégies cardio- et néphroprotectrices
Malgré tous les succès obtenus dans la prise en charge de cette maladie au cours des décennies, les patients souffrant de diabète de type 1 (DT1) continuent d’enregistrer une mortalité ...
Étude GDAC: la personnalisation du taux d’HbA1c se concrétise
Le taux d’HbA1c, mesure de la charge glycémique à long terme, est largement accepté et a été associé au risque de complications du diabète il y a plus de 30 ans déjà.1 Cependant, la ...
Psychologie clinique dans le cadre de la réadaptation cardiovasculaire: approches de mise en pratique
Les patient·es atteint·es de maladies cardiovasculaires souffrent souvent de troubles psychiques. Cela peut avoir un impact considérable sur la qualité de vie et le pronostic. Grâce à un ...