Management von Patientinnen und Patienten mit Refluxerkrankung und Barrett-Ösophagus
Autor:
Dr. med. Matthias Sauter
Leiter Gastroenterologie, Leitender Arzt
Klinik für Innere Medizin
Spital Zollikerberg
8125 Zollikerberg
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die gastroösophageale Refluxerkrankung (GERD) stellt nach wie vor die häufigste gutartige Erkrankung des oberen Gastrointestinaltrakts in der westlichen Welt dar; an Refluxbeschwerden leiden 10−20% der westlichen Bevölkerung, dies führt zu hohen Kosten im Gesundheitssystem und zu vielen Abwesenheiten vom Arbeitsplatz. Dieser Artikel beschreibt die Diagnostik und Therapie bei GERD und das Vorgehen bei therapieresistenten Beschwerden. Des Weiteren finden Sie einen Überblick über das Management bei Barrett-Ösophagus. Es existieren verschiedene Leitlinien; der vorliegende Übersichtsartikel folgt zum grössten Teil den deutschen Leitlinien der DGVS (Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten)1,2 und den endoskopischen Guidelines der ESGE (European Society of Gastrointestinal Endoscopy)3.
Keypoints
-
Bei Patienten mit einer Refluxerkrankung wird je nach Vorliegen von Alarmsymptomen und Risikofaktoren für einen Barrett-Ösophagus zwischen einer probatorischen Therapie und einer primären Diagnostik mittels Endoskopie unterschieden.
-
Eine PPI-Therapie ist sicher und effizient, sollte aber (mit Ausnahmen) zeitlich begrenzt und in der niedrigstmöglichen Dosierung eingesetzt werden.
-
Neben der PPI-Therapie kommen zur Therapie der Refluxerkrankung Allgemeinmassnahmen/Lifestyle-Änderungen und andere Medikamente zum Einsatz.
-
Bei persistierenden Beschwerden und hohem Leidensdruck ist nach einmaligem PPI-Wechsel und Überprüfen der Compliance eine funktionsdiagnostische Untersuchung mittels Ösophagusmanometrie und 24h-Impedanz-pH-Metrie indiziert.
-
Der Barrett-Ösophagus als Komplikation einer GERD stellt eine fakultative Präkanzerose für ein Ösophaguskarzinom dar; je nach Länge des Segments und der Gesamtsituation ist eine PPI-Therapie sinnvoll und eine Surveillance indiziert.
Man unterscheidet typische Symptome (Sodbrennen/saures Aufstossen) von atypischen Symptomen (Laryngitis, chronischer Husten, Asthma) (Tab.1).
Auch bei Gesunden findet sich ein physiologischer saurer und nicht saurer Reflux in der 24h-pH-Metrie. Von einer gastroösophagealen Refluxerkrankung («gastroesophageal reflux disease», GERD) spricht man dann, wenn der Reflux entweder störende Symptome (2x/Woche milde oder 1x/Woche mittelgradige Symptome) verursacht oder wenn es zu Komplikationen wie Strikturen oder einem Barrett-Ösophagus kommt (Montreal-Klassifikation).
Heutzutage werden unter dem Sammelbegriff GERD subsummiert:4
-
Erosive Refluxösophagitis
-
Nicht erosive Refluxkrankheit (NERD)
-
Refluxhypersensitivität/hypersensitiver Ösophagus
-
Funktionelle Refluxbeschwerden/funktionelles Sodbrennen
-
Extraösophageale Manifestationen
Komplikationen der GERD inkl. Barrett-Ösophagus
Zu den Risikofaktoren für eine Refluxerkrankung zählen Übergewicht, genetische Prädisposition, das Alter, das Vorliegen einer Hiatushernie, Nikotinabusus, Schwangerschaft und das Vorliegen einer Kollagenose/Sklerodermie.
Diagnostik
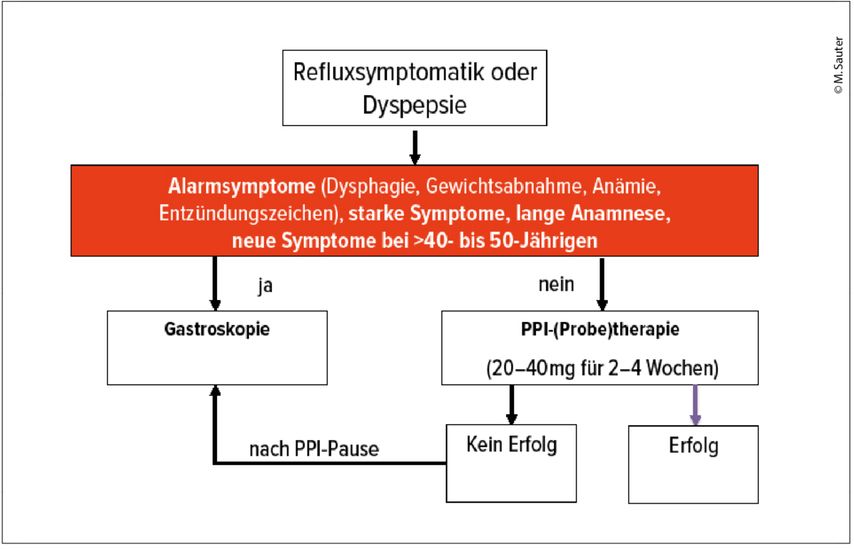
Die initiale Anamnese entscheidet darüber, ob eine probatorische Therapie oder primär eine Diagnostik erfolgen soll (Abb.1). Bei Fehlen von Alarmsymptomen kann eine zeitlich begrenzte probatorische Therapie mit Protonenpumpeninhibitoren (PPI) in Standarddosis erfolgen. Hierbei ist wichtig zu wissen, dass die diagnostische Wertigkeit der «probatorischen» primären PPI-Therapie begrenzt ist (Sensitivität circa 70%, Spezifität circa 45% im Vergleich zu «Endoskopie plus pH-Metrie»). Wenn nach Ansprechen auf eine primäre Therapie eine hohe PPI-Dosis als Erhaltungstherapie notwendig ist, um beschwerdefrei zu sein (z.B. 1 ganze Tablette pro Tag), wird eine Endoskopie empfohlen. Bei Vorhandensein von Alarmsymptomen wird direkt eine primäre Endoskopie durchgeführt (auch wenn lange nicht bei jedem Patienten mit Alarmsymptomen eine andere Diagnose gefunden wird).
Auch bei Patienten mit chronischen Refluxbeschwerden ohne andere Alarmsymptome ist in gewissen Fällen eine primäre Gastroskopie indiziert, sofern gewisse Risikofaktoren für einen Barrett-Ösophagus bestehen (s.u. und Tab.2).
Findet sich in der Endoskopie eine Refluxösophagitis, ist die Diagnose gesichert; das Ausmass der Entzündung sollte dokumentiert werden, z.B. mittels der Los-Angeles-Klassifikation. Ist die Endoskopie bland, liegt entweder eine nicht erosive Refluxerkrankung oder eine andere Diagnose vor (z.B. Refluxhypersensitivität, funktionelles Sodbrennen). Eine weiterführende Diagnostik (d.h. eine Ösophagusmanometrie/pH-Metrie) ist Patienten mit therapierefraktären Symptomen oder mit persistierender Entzündung in der Endoskopie unter korrekt angewendeter PPI-Therapie vorbehalten (s.u.).
Therapie
Die Therapie der Refluxerkrankung umfasst 4 Standbeine:
Allgemeinmassnahmen inkl. Gewichtsreduktion
PPI/H2-Rezeptor-Antagonisten
Andere Medikamente
Operative/endoskopische Therapiemassnahmen
Allgemeinmassnahmen
Zu den Allgemeinmassnahmen zählen (Tab.3):
-
Gewichtsreduktion: Das Vorhandensein von Übergewicht verdoppelt das Risiko für eine GERD. Bei Übergewichtigen reduziert die Gewichtsreduktion die Symptome und die ösophageale Säureexposition. Auch wenn die Gewichtsabnahme im klinischen Alltag ein schwieriges Thema ist, stellt sie nach wie vor die primäre Empfehlung der Lifestyle-Modifikationen dar.
-
Hochlagern des Oberkörpers/frühes Abendessen: Diese Massnahmen sind vor allem bei nächtlichen Beschwerden zu empfehlen und es gibt eine gewisse Evidenz für ihre Wirksamkeit.
-
Ernährung: Es besteht eine allgemeine Empfehlung zur Vermeidung von zu üppigen und fetthaltigen Mahlzeiten. Der totale Verzicht z.B. auf Kaffee oder scharfe Speisen für alle Patienten zeigt in Studien jedoch keine Evidenz. Vielmehr sollten individuelle «Triggerfoods» ermittelt und dann vermieden werden (Zitrusfrüchte, saure Nahrungsmittel wie z.B. Tomaten). Hier ist bei hohem Leidensdruck und Symptompersistenz unter Therapie gelegentlich eine Ernährungsberatung sinnvoll.
PPI/H2-Rezeptor-Antagonisten
Die Einführung der PPI Ende der 1980er-Jahre hat die Therapie der Refluxerkrankung wie auch der Ulkuskrankheit fundamental verändert. In den letzten Jahren sind die PPI jedoch in Verruf geraten aufgrund einer Fülle von Studien über unerwünschte Langzeiteffekte (Tab.4). Es handelt sich dabei jedoch oft um Beobachtungsstudien aus grossen Kohorten mit möglichen Störvariablen und z.T. widersprüchlichen Ergebnissen. Das Risiko für eine C.-difficile-Infektion scheint leicht erhöht zu sein, und dies sollte bei Patienten mit stattgehabter Infektion berücksichtigt werden. Für andere postulierte Risiken wie z.B. eine Demenz gibt es keine guten Daten. Zusammenfassend gilt weiterhin, dass der Nutzen der PPI-Therapie bei guter Indikation das potenzielle Risiko überwiegt. Dennoch sollte die PPI-Therapie in möglichst niedriger Dosierung und für eine möglichst kurze Dauer eingesetzt werden; bei einer Dauertherapie muss die Indikation hinterfragt werden. Der «Magenschutz» mit PPI bei Polypharmazie ist klar obsolet.
Effekt der PPI
PPI sind hocheffizient in der Heilung der Ösophagitis; der Effekt auf die Symptome ist ebenfalls gut, hängt jedoch stark von der Art des Symptoms ab (60−80% für Sodbrennen, 50% für Regurgitation, 20% oder weniger für vermuteten Reflux-assoziierten Husten/Heiserkeit).5 Dies muss bei Therapiebeginn berücksichtigt und mit dem Patienten besprochen werden. Welcher der einzelnen PPI-Wirkstoffe die höchste Effizienz hat, ist nicht ganz klar und es kann an dieser Stelle keine klare Präferenz gegeben werden. Vorteile haben Esomeprazol (da ein Enantiomer von Omeprazol mit vermutlich besserer pharmakologischer Wirkung) und Dexlansoprazol (keine zwingende präprandiale Einnahme notwendig).
Die Dosierung soll in Standarddosis begonnen werden mit einer begrenzten Dauer und anschliessendem Auslassversuch (Ausnahme schwere Ösophagitis, s.u.).
H2-Rezeptor-Antagonisten
H2-Rezeptor-Antagonisten, welche im Vergleich mit PPI in Studien zwar eine geringere Effektivität haben, bieten eine gute Alternative bei PPI-Unverträglichkeit oder bei leichten Symptomen, wobei das Präparat Ranitidin in der letzten Zeit lange nicht verfügbar war.
Andere Medikamente
Antazida wie Magaldrat (Riopan®) oder Magnesium-/Aluminiumhydroxid (Alucol®) binden Säure und können bei leichten Symptomen alleine oder bei persistierenden Beschwerden unter PPI zusätzlich eingenommen werden, primär postprandial. Eine weitere Option stellt das Alginat Gaviscon® dar, das Salz der Alginsäure (aus der Zellwand gewisser Algen), welches bei Kontakt mit Säure präzipitiert. Es hat den Vorteil, die auf der Speise schwimmende Säure (auch «acid pocket» oder «acid layer» genannt) zu binden und eine Schutzschicht gegen oben zu bilden, um so Refluxepisoden und die ösophageale Säureexposition zu reduzieren.6
Bei erwiesener Refluxerkrankung und persistierenden Symptomen werden gelegentlich andere Medikamente mit allerdings geringerer Evidenz eingesetzt, wie z.B. Ziverel® (Natriumhyaluronat, Chondroitinsulfat), welches die Ösophagus-Mukosa schützen soll.
Operative Therapien
Die etablierte operative Therapie ist die laparoskopisch durchgeführte Fundoplicatio, ggf. mit Hiatusraffung. Es gibt verschiedene Fundoplicatio-Varianten (nach Thal, Toupet, Dor). Die Operation sollte immer erst nach einer funktionsdiagnostischen Untersuchung durchgeführt werden (Ösophagusmanometrie/24h-Impedanz-pH-Metrie), bei welcher der Reflux nachgewiesen und andere Erkrankungen (wie eine Achalasie, Ösophagusspasmen oder funktionelle Erkrankungen wie eine Rumination) ausgeschlossen werden können.
Am wirksamsten ist die operative Therapie bei Patienten mit einer Hiatushernie und mit klassischen Refluxbeschwerden inkl. Volumenregurgitation (Aufstossen von Flüssigkeit in den Mund, z.B. beim Vornüberbeugen). Auch wirkt die Operation besser bei Patienten, bei denen das Sodbrennen gut auf eine PPI-Therapie anspricht. Bei Patienten mit atypischen Beschwerden wie Husten oder auch Thoraxschmerzen ist der Effekt deutlich geringer. Somit ist sie nur bei einem kleinen Teil aller Refluxpatienten auch wirklich sinnvoll. Zu den Risiken/Nachteilen gehört eine postoperative Dysphagie und Meteorismus. Auch muss dem Patienten bewusst sein, dass die Volumenregurgitation durch die Operation effizient reduziert wird, dass aber in bis zu 20% der Fälle aufgrund persistierender anderer Refluxbeschwerden weiterhin PPI eingenommen werden müssen, um beschwerdefrei zu sein.
Zu den noch nicht etablierten operativen Verfahren gehören unter anderem das Linx®- (mechanischer Verschluss des gastroösophagealen Überganges durch operativ eingesetzte Magnete) und das Endostim®-Verfahren (Elektrostimulation des Schliessmuskels durch Implantation eines Schrittmachers nahe des unteren Ösophagussphinkters).
Zu den endoskopischen, ebenfalls noch nicht etablierten Verfahren gehören unter anderem Stretta (endoskopische Radiofrequenzablation im Bereich des gastroösophagealen Übergangs) und die Anti-Reflux-Mukosektomie, die beide das Ziel haben, durch eine Narbenbildung im Bereich des unten Ösophagussphinkters die Refluxbarriere zu stärken.7
Auch wenn diese Optionen rein pathomechanisch interessant sind, sind sie alle nach wie vor als experimentell zu bezeichnen. Sie haben in den Guidelines noch keinen Platz gefunden und sollten nur in Studien/Kohorten durchgeführt werden.
Weiterführendes Management/Therapieversagen
Finden sich in der Endoskopie ausgeprägte Erosionen (Los-Angeles-Klassifikation der Ösophagitis C und D) oder ein Ulkus, erfolgt eine endoskopische Abheilungskontrolle unter PPI nach 8 Wochen, auch um ein darunterliegendes Karzinom auszuschliessen. Bei diesen Befunden oder bei Auftreten einer Striktur ist formal eine Erhaltungstherapie indiziert. Bei allen anderen Fällen wird die Therapie nach (4−)8 Wochen sistiert und bei Wiederauftreten der Beschwerden (neben den Allgemeinmassnahmen) in der niedrigstmöglichen Dosierung bedarfsadaptiert fortgesetzt.
Therapieversagen
Je nach primärem Symptom ist das Ansprechen auf die Therapie unterschiedlich (s.o.). Studien haben zudem gezeigt, dass in bis zu 40% der Fälle eine medikamentöse Malcompliance besteht. Zudem werden PPI oft auch falsch verschrieben (nicht primär vor dem Frühstück). Daneben spielen andere Mechanismen eine Rolle:
-
Persistierender Volumenreflux aufgrund einer stark insuffizienten Refluxbarriere mit grosser Hiatushernie, bei welcher PPI eine begrenzte Wirkung haben (ggf. operatives Vorgehen, s.o.)
-
Erhöhte Perzeption im Ösophagus auf gering sauren oder nicht sauren Reflux (Refluxhypersensitivität) → Einsatz von Antazida, evtl. trizyklischen Antidepressiva (z.B. Amitryptilin) in der Indikation eines «viszeralen Analgetikums»
-
Ösophageale Hypomotilität (z.B. im Rahmen einer systemischen Sklerose) → keine direkte medikamentöse Einflussnahme möglich
-
«Rapid Metabolizer» des Cytochrom-P450-Isoenzyms 2C19 → Wechsel auf ein anderes PPI-Präparat wie z.B. Esomeprazol, Rabeprazol
Funktionsdiagnostik
Um unter anderem die erwähnten Faktoren zu beurteilen, ist (evtl. nach Dosis-Teilung/Erhöhung/Wechsel auf ein anderes Präparat) eine funktionsdiagnostische Abklärung mittels hochauflösender Ösophagusmanometrie und 24h-Impedanz-pH-Metrie (oder alternativ drahtloser pH-Metrie «Bravokapsel») indiziert. Diese Untersuchungen dienen u.a. dazu, im Falle einer Endoskopie ohne Erosionen eine nicht erosive Refluxerkrankung oder eine Hypersensitivität nachzuweisen: Deshalb sollte bei unauffälliger Endoskopie die anschliessende pH-Metrie nach 2-wöchiger PPI-Pause durchgeführt werden. Des Weiteren wird mittels Manometrie der untere Ösophagussphinkter beurteilt, und es wird nach Motilitätsstörungen gesucht (welche bei bis zu 10% der Patienten mit persistierenden Refluxsymptomen unter PPI bestehen). Wichtig ist dabei, dass der Patient während der Manometrie nicht nur Wasser, sondern auch feste Speisen schluckt, da dies die Sensitivität der Untersuchung erhöht. Auch kann mit der Funktionsdiagnostik eine Rumination und ein Syndrom der Aerophagie mit «supra-gastric belching» gesucht werden: Bei der Rumination handelt sich um eine funktionelle Erkrankung, bei der durch vom Patienten unbemerkte, aber willkürliche Kontraktion der Bauchwandmuskulatur Nahrung nach oben in den Mund gestossen wird. Bei der Aerophagie mit «supra-gastric belching» wird Luft geschluckt und anschliessend wieder aufgestossen, von aussen als repetitives Rülpsen sichtbar. Sowohl bei der Rumination als auch bei der Aerophagie wird als Therapie eine spezifische Physiotherapie mit Atemübungen durchgeführt. Verschiedene Massnahmen bei anderen therapierefraktären Symptomen sind in Tabelle 5 zusammengefasst.
Barrett-Ösophagus
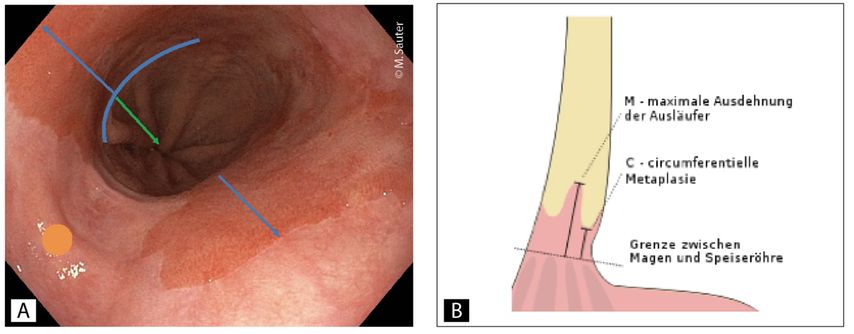
Abb. 2: Barrett-Ösophagus. A) exemplarisches Foto eines Barrett-Ösophagus (blaue Linie: Ende der Magenfalten = gastroösophagealer Übergang; grüner Pfeil: Hiatushernie; blaue Pfeile: Barrett-Zunge; oranger Punkt: plattenepitheliale Schleimhaut der Speiseröhre); B) Ausmass der Barrett-Schleimhaut gemäss Prag-Klassifikation
Beim Barrett-Ösophagus handelt es sich um eine intestinale Metaplasie im distalen Ösophagus.
Der Barrett-Ösophagus stellt eine fakultative Präkanzerose für ein Adenokarzinom (sog. Barrett-Karzinom) dar. Die histologische Definition war in der Vergangenheit je nach Land/Region unterschiedlich, was man beim Studium der Literatur beachten sollte. Die Refluxerkrankung spielt bei der Entstehung des Barrett-Ösophagus eine wichtige Rolle, wobei jedoch nicht jeder Refluxpatient einen Barrett-Ösophagus entwickelt. Die Risikofaktoren dafür sind in Tabelle 2 erwähnt, protektive Faktoren sind möglicherweise u.a. eine Statintherapie.
Bei der Endoskopie ist es wichtig, das Ausmass des Barrett-Ösophagus genau zu beschreiben (in der sog. Prag-Klassfikation, Abb.2); auch muss die Region (möglichst ohne Entzündung) genau inspiziert werden, am besten mit Darstellung unter Blaulicht («narrow band imaging») und/oder nach Applikation von Essigsäure, da damit Regionen mit Atypien besser erkannt und beurteilt werden können.
Das Risiko für eine Progression zu einer Dysplasie und dann zu einem Karzinom hängt von der Länge des Barrett-Segments und den gleichen Risikofaktoren (Tab.2) ab. Das Risiko ist wahrscheinlich niedriger als angenommen und beträgt je nach Barrett-Länge und Vorliegen der erwähnten Barrett-Risikofaktoren bis 3% pro Jahr, wobei neuere Studien niedrigere Progressionsraten von ca. 0,4% pro Jahr dokumentiert haben. Obwohl das Risiko für ein Ösophaguskarzinom bei einem Patienten mit Barrett-Ösophagus 30-mal höher ist als in der Normalbevölkerung, scheint das absolute Risiko für einen individuellen Patienten mit Barrett-Ösophagus niedrig zu sein.
Je nach Länge des Segments und der Gesamtsituation (Lebenserwartung/Komorbiditäten) wird eine PPI-Therapie empfohlen und es wird eine Surveillance durchgeführt. Eine PPI-Therapie scheint bis zu einem gewissen Mass vor einer Progression zu einem Karzinom zu schützen.
Abb. 3: Die gastroösophageale Refluxerkrankung (GERD) ist die häufigste gutartige Erkrankung des oberen Gastrointestinaltrakts in der westlichen Welt. 10−20% der westlichen Bevölkerung leiden an Refluxbeschwerden
Die Surveillance erfolgt gemäss ESGE-Guidelines folgendermassen:3
-
Wenn die Endoskopie nicht nach dem o.g. Standard durchgeführt wurde (genaue Inspektion, Biopsien, ggf. Färbung) → Wiederholung der Endoskopie
-
Barrett <1cm ohne Dysplasien: keine Nachsorge
-
Barrett 1−3cm lang ohne Dysplasien: Kontrolle in 5 Jahren
-
Barrett 3−10cm lang ohne Dysplasien: Kontrolle in 3 Jahren
>10cm Länge: Zuweisung ans Zentrum
Dysplasien im Barrett-Ösophagus gehören in erfahrene Hände (sowohl hinsichtlich der Endoskopie als auch der pathologischen Beurteilung). Im Falle einer Dysplasie und sichtbarer Läsion sollte eine endoskopische Resektion (Mukosektomie) erfolgen; im Falle einer «Low grade»-Dysplasie ohne visuelle Auffälligkeiten erfolgt eine endoskopische Kontrolle nach 6 Monaten an einem Zentrum mit grosser Erfahrung. Bei Vorliegen einer «High grade»-Dysplasie soll in jedem Fall eine Therapie erfolgen (endoskopische Resektion +/– Radiofrequenzablation [RFA]). Nach einer solchen Therapie ist eine weitere Surveillance indiziert.
Literatur:
1 Koop H et al.: S2k guideline: gastroesophageal reflux disease guided by the German Society of Gastroenterology: AWMF register no. 021-013. Z Gastroenterol 2014; 52: 1299-346 2 Porschen R et al.: S3-Leitlinie – Diagnostik und Therapie der Plattenepithelkarzinome und Adenokarzinome des Ösophagus. Z Gastroenterol 2019; 57: e120 3 Weusten B et al.: Endoscopic management of Barrett’s esophagus: European Society of Gastrointestinal Endoscopy (ESGE) Position Statement. Endoscopy 2017; 49: 191-8 4 Vakil N et al.: The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus. Am J Gastroenterol 2006, 101: 1900-20 5 Kahrilas PJ et al.: Management of the patient with incomplete response to PPI therapy. Best Pract Res Clin Gastroenterol 2013, 27: 401-14 6 Sauter M, Fox MR: [The acid pocket – a novel target for the treatment of gastro-esophageal reflux disease.] Z Gastroenterol 2018; 56: 1276-82 7 Rettura F et al.: Refractory gastroesophageal reflux disease: a management update. Front Med 2021; 8: 765061
Das könnte Sie auch interessieren:
Aktuelle Studien und Poster
Vom 13. bis 14. September trafen sich die Schweizer Gastroenterolog:innen und Hepatolog:innen in Interlaken zu ihrem Jahreskongress 2024. Im Folgenden stellen wir Ihnen einige der in ...
Künstliche Intelligenz in der Gastroenterologie und Hepatologie
Die Digitalisierung der Medizin und zunehmende Anwendungsmöglichkeiten AI(«artificial intelligence»)-assistierter Medizinprodukte in Diagnostik und Therapie gastrointestinaler ...
Target-Mikrobiome in der Behandlung gastrointestinaler Erkrankungen
Das Mikrobiom kann durch unterschiedliche Parameter wie Ernährung, Antibiotika und Krankheiten beeinflusst werden. Veränderungen der Zusammensetzung sind mit zahlreichen ...