Akute Toxizitäten von bispezifischen Antikörpern und CAR-T-Zell-Therapien
Autor:
Matthias Hellberg-Naegele, MSc
Pflegeexperte APN Netzwerk Onkologie
Entwicklung und Qualitätsmanagement, Kantonsspital St. Gallen
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Behandlungsoptionen in der Hämatologie entwickeln sich rasant. So gibt es neben den CAR-T-Zell-Therapien, die sich in den letzten Jahren etabliert haben, nun auch eine Reihe von bispezifischen Antikörpern, die in der Behandlung vor allem von Leukämien, Lymphomen und dem multiplen Myelom zum Einsatz kommen. Die schwerwiegendsten Akuttoxizitäten beider Therapieformen sind das Zytokinfreisetzungssyndrom (CRS) und das Immuneffektorzell-assoziierte Neurotoxizitätssyndrom (ICANS). Pflegefachkräften kommt hier eine tragende Rolle bei der Früherkennung der zugehörigen Symptome zu.
Bei CAR(Chimeric antigen receptor)-T-Zellen handelt es sich um gentechnisch modifizierte T-Zellen, die Rezeptoren für die Zielantigene der Tumorzelle exprimieren. Unter den derzeit kommerziell erhältlichen Therapien gibt es diese gegen das Oberflächenantigen CD19, zugelassen für verschiedene Lymphome und die akute lymphatische Leukämie (ALL), und gegen BCMA, ein Oberflächenantigen auf den Myelomzellen.
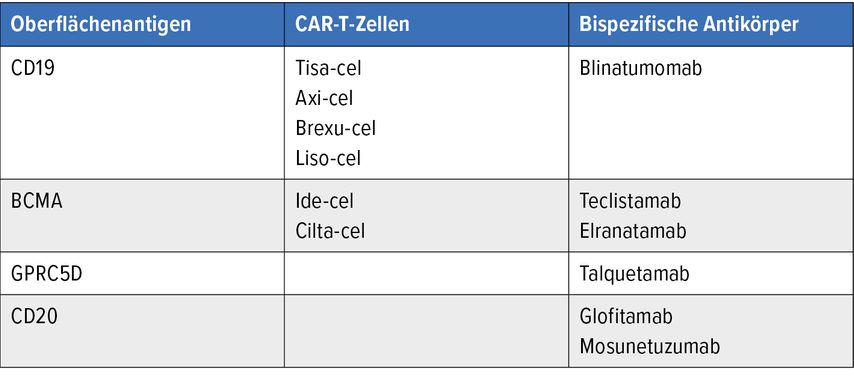
Bispezifische Antikörper hingegen haben neben ihrer Bindungsstelle an den Tumorzellen eine zweite Bindungsstelle an den T-Zellen (CD3). So werden Tumorzelle und T-Zelle zueinandergebracht und die T-Zelle kann die Tumorzelle zerstören. Für CD19 ist hier schon seit vielen Jahren Blinatumomab in der Behandlung der ALL etabliert, für BCMA gibt es neu Teclistamab und Elranatamab. Darüber hinaus zielen Talquetamab auf GPRC5D auf den Myelomzellen und Glofitamab und Mosunetuzumab auf CD20 auf den Lymphomzellen (Tab. 1).
Zytokinfreisetzungssyndrom
Das CRS äussert sich durch Fieber nicht-infektiöser Ursache, grippeähnliche Symptome, Hypotonie und Hypoxie. Das Auftreten eines CRS nach einer CAR-T-Zell-Therapie ist unmittelbar in den ersten Tagen nach der Reinfusion der CAR-T-Zellen häufig.1 Auch bei den bispezifischen Antikörpern tritt das CRS häufig in den ersten Tagen während der Step-up-Gaben auf.2
Als zentraler Mediator für die Entstehung eines CRS betrachtet man das Interleukin 6 (IL6). Entsprechend ist der frühzeitige Einsatz von Tocilizumab mit bis zu vier Gaben die Therapie der Wahl.3 Tocilizumab ist ein monoklonaler Antikörper gegen IL6-Rezeptoren. Zur Früherkennung des CRS sind regelmässige Kontrollen von Blutdruck, Puls, Temperatur und Sauerstoffsättigung empfohlen. Wichtig sind das frühzeitige Erkennen von Fieber und der Ausschluss von Infektionen bzw. einer Sepsis. Vor allem die Patient:innen unter einer CAR-T-Zell-Therapie können zum Zeitpunkt des Auftretens von Fieber als Folge der lymphodepletierenden Chemotherapie neutropen sein.3
Immuneffektorzell-assoziiertes Neurotoxizitätssyndrom
ICANS äussert sich sehr heterogen mit unterschiedlichen neurologischen Symptomen (z.B. Vigilanzminderung, kognitive Beeinträchtigungen, Aphasie und Krampfanfälle) in unterschiedlicher Ausprägung und tritt häufig erst fünf bis sechs Tage nach der CAR-T-Zell-Reinfusion auf.1
Zur schnelleren Erkennung von ICANS hat sich die mehrmals tägliche Erhebung des Immuneffektorzell-assoziierten Enzephalopathie-Scores (ICE) etabliert. Im Rahmen des ICE-Scores werden die Orientierung (Jahr, Monat, Stadt, Ort), das Benennen von drei Gegenständen, eine Schriftprobe, die Konzentration (von 100 in 10er-Schritten rückwärts zählen) und, durch Durchführen einer Geste, die Fähigkeit des Befolgens getestet.4
Mittel der Wahl zur Behandlung eines ICANS wäre der Einsatz von Steroiden, bei gemeinsamem Auftreten mit einem CRS auch Tocilizumab.1–3 Bei hochgradigem ICANS kann das Pflegekonzept der Basalen Stimulation® helfen, über Sinneswahrnehmungen Ängste bei den Betroffenen zu reduzieren.5
CRS & ICANS: Häufigkeit und Prophylaxe
CRS und ICANS können zwar sowohl bei CAR-T-Zell-Therapien als auch bei bispezifischen Antikörpern auftreten, allerdings sind die Häufigkeit und Stärke unter den beiden Therapieformen, aber auch unter den einzelnen Produkten recht unterschiedlich verteilt. So liegt die Häufigkeit des Auftretens von CRS jeden Grades bei CAR-T-Zell-Therapien bei den meisten Produkten bei über 90% und bei schweren Formen ≥Grad 3 vor allem bei Brexu-cel und Tisa-cel je nach Indikation bei über 20%.6–8
Um das Risiko eines CRS zu minimieren, werden die Dosen der bispezifischen Antikörper mit einer Step-up-Dosierung schrittweise bis zur therapeutischen Dosisgesteigert. Das kann über einen Zeitraum von einer Woche bis zu wenigen Wochen passieren. Dies reduziert das Risiko vor allem eines CRS von ≥Grad3 auf unter 5%. Dennoch liegt die Wahrscheinlichkeit eines CRS jeden Grades bei den bispezifischen Antikörpern für Myelome und Lymphome zwischen 40 und 80%.9–12
Ähnlich verhält es sich mit ICANS. Auch diese sind bei CAR-T-Zell-Therapien häufig. Vor allem bei Axi-cel und Brexu-cel liegt ihr Auftreten bei über 50%.6,13–16 Für Axi-cel gibt es zwischenzeitlich ein Update bezüglich des Managements zur Reduktion von CRS und ICANS. So konnte bei der Kohorte 6 durch den prophylaktischen Einsatz von Kortikosteroiden und Levetiracetam plus frühzeitigen Einsatz von Kortikosteroiden und Tocilizumab bei Auftreten von Symptomen die Inzidenz von CRS und ICANS deutlich reduziert werden.17 Bei bispezifischen Antikörpern liegt das Auftreten von ICANS bzw. neurologischen Symptomen jeden Grades mit Ausnahme von Blinatumomab18,19 bei unter 15%, ≥Grad3 liegt unter 2%.
Akuttoxizität bei Talquetamab
Bezüglich Akuttoxizität besonders hervorzuheben ist der bispezifische Antikörper Talquetamab, der neben den oben erwähnten Symptomen noch Haut- und Nageltoxizitäten sowie Mundtrockenheit und schwere Geschmacksstörungen auslösen kann.20,21 Diese Symptome können sehr herausfordernd für Patient:innen sein.
So können Mundtrockenheit und Geschmacksverlust schon in den ersten Wochen zu einer deutlichen Reduktion der Nahrungsaufnahme und zum Gewichtsverlust führen. Gegen die Hauttrockenheit wird starke Feuchtigkeitszufuhr empfohlen, an Händen und Füssen Ammoniumlactat-haltige Lotionen (12%). An den Nägeln können Nagelhärter eingesetzt werden. Gegen die Mundtrockenheit empfehlen sich Mundbefeuchtung und der Einsatz von Speichelersatzprodukten. Sinnvoll ist auch eine Ernährungsberatung.21
Unterstützung durch Advanced Practice Nurses
In vielen Spitälern in der Schweiz werden Advanced Practice Nurses (APN)22 in der Begleitung von Patient:innen mit einer CAR-T-Zell-Therapie eingesetzt. Ihr Beitrag erstreckt sich über verschiedene Phasen der Therapie und umfasst eine Vielzahl von Aufgaben und Verantwortlichkeiten.23 Ihr Einsatz ist auch bei einer Therapie mit bispezifischen Antikörpern sinnvoll.
Die Aufgaben der APN umfassen:
-
Aufklärung und Beratung von Patient:innen und deren Familien. APN helfen, Ängste und Unsicherheiten zu reduzieren und unterstützen dabei, informierte Entscheidungen zu treffen.
-
Koordination der Versorgung: APN fungieren als zentrale Ansprechpartner:innen und koordinieren die verschiedenen Aspekte der Behandlung.
-
Unterstützung der Pflegeteams bei Überwachung und Management von CRS und ICANS.
-
Unterstützung während des gesamten Behandlungsverlaufs: APN bieten Kontinuität während der gesamten Behandlungsphase, von der Vorbereitung durch die Therapie bis zur Nachsorge.
-
Patient:innenschulung zum Selbstmanagement: APN schulen Patient:innen und deren Familien in Bezug auf Selbstmanagementstrategien, die notwendig sind, um die Behandlung zu Hause fortzusetzen und Komplikationen zu vermeiden.
-
Forschung und evidenzbasierte Praxis: APN beteiligen sich an Forschungsprojekten, die darauf abzielen, die Wirksamkeit und Sicherheit der CAR-T-Zell-Therapie zu verbessern. Sie wenden evidenzbasierte Praktiken an und tragen zur Weiterentwicklung des Pflegewissens in diesem spezialisierten Bereich bei.
-
Psychosoziale Unterstützung: APN unterstützen Patient:innen und Familien auch in psychosozialer Hinsicht, indem sie emotionale Unterstützung bieten, Zugang zu Unterstützungsdiensten vermitteln und bei der Bewältigung der mit der Therapie verbundenen Belastungen helfen.
Fazit
Sowohl die CAR-T-Zell-Therapie als auch bispezifische Antikörper sind sehr effektive und vielversprechende neue Behandlungsformen in der Hämatologie. Ihre Akuttoxizitäten erfordern eine hohe Expertise der Pflegefachkräfte und eine aufeinander abgestimmte multiprofessionelle Zusammenarbeit. APN tragen durch ihre umfassende Betreuung und ihr Fachwissen wesentlich zur Verbesserung der Patient:innenergebnisse und zur Optimierung der Versorgungsqualität bei.
Literatur:
1 Bücklein VL et al.: CAR-T Zellen: Management von Nebenwirkungen. Online unter https://www.onkopedia.com/de/onkopedia/guidelines/car-t-zellen-management-von-nebenwirkungen . Abgerufen am 27.6.2024 2 Crombie JL et al.: Consensus recommendations on the management of toxicity associated with CD3×CD20 bispecific antibody therapy. Blood 2024; 143(16): 1565-75 3 Hayden PJ et al.: Management of adults and children receiving CAR T-cell therapy: 2021 best practice recommendations of the European Society for Blood and Marrow Transplantation (EBMT) and the Joint Accreditation Committee of ISCT and EBMT (JACIE) and the European Haematology Association (EHA). Ann Oncol 2022; 33(3): 259-75 4 Ellard R et al.: The EBMT immune effector cell nursing guidelines on CAR-T therapy: a framework for patient care and managing common toxicities. Clin Hematol Int 2022; 4(3): 75-88 5 Rizzi CC, Naegele M: Basale Stimulation bei CAR-T-Zell-Therapie. Anwendung des Konzepts und ganzheitliche Erfassung bei ICANS. Onkologiepflege 2024; 10(2): 36-7 6 Shah BD et al.: KTE-X19 for relapsed or refractory adult B-cell acute lymphoblastic leukaemia: phase 2 results of the single-arm, open-label, multicentre ZUMA-3 study. Lancet 2021; 398(10299): 491-502 7 Schuster SJ et al.: Tisagenlecleucel in adult relapsed or refractory diffuse large B-cell lymphoma. N Engl J Med 2019; 380(1): 45-56 8 Maude SL et al.: Tisagenlecleucel in children and young adults with B-cell lymphoblastic leukemia. N Engl J Med 2018; 378(5): 439-48 9 Chari A et al.: Talquetamab, a G protein-coupled receptor family C group 5 member D x CD3 bispecific antibody, in patients with relapsed/refractory multiple myeloma (RRMM): phase 1/2 results from monumenTAL-1. Blood 2022; 140(Suppl. 1): 384-87 10 Moreau P et al.: Teclistamab in relapsed or refractory multiple myeloma. N Engl J Med 2022; 387(6): 495-505 11 Dickinson MJ et al.: Glofitamab for relapsed or refractory diffuse large B-cell lymphoma. N Engl J Med 2022; 387(24): 2220-31 12 Budde LE et al.: Safety and efficacy of mosunetuzumab, a bispecific antibody, in patients with relapsed or refractory follicular lymphoma: a single-arm, multicentre, phase 2 study. Lancet Oncol 2022; 23(8): 1055-65 13 Wang M et al.: KTE-X19 CAR T-cell therapy in relapsed or refractory mantle-cell lymphoma. N Engl J Med 2020; 382(14): 1331-42 14 Jacobson CA et al.: Axicabtagene ciloleucel in relapsed or refractory indolent non-Hodgkin lymphoma (ZUMA-5): a single-arm, multicentre, phase 2 trial. Lancet Oncol 2022; 23(1): 91-103 15 Neelapu SS et al.: Axicabtagene ciloleucel CAR T-cell therapy in refractory large B-cell lymphoma. N Engl J Med 2017; 377(26): 2531-44 16 Locke FL et al.: Axicabtagene ciloleucel as second-line therapy for large B-cell lymphoma. N Engl J Med 2022; 386(7): 640-54 17 Oluwole OO et al.: Prophylactic corticosteroid use in patients receiving axicabtagene ciloleucel for large B-cell lymphoma. Br J Haematol 2021; 194(4): 690-700 18 Kantarjian HM et al.: Blinatumomab versus chemotherapy for advanced acute lymphoblastic leukemia. N Engl J Med 2017; 376(9): 836-47 19 Gökbuget N et al.: Blinatumomab for minimal residual disease in adults with B-cell precursor acute lymphoblastic leukemia. Blood 2018; 131(14): 1522-31 20 Laheij AMGA, van de Donk NWCJ: Characterization of dysgeusia and xerostomia in patients with multiple myeloma treated with the T-cell redirecting GPRC5D bispecific antibody talquetamab. Support Care Cancer 2024; 32(1): 20 21 Mancia SS et al.: Characterization and management of oral and dermatological toxicities in patients receiving the CD3 X GPRC5D bispecific antibody talquetamab (JNJ-64407564) for the treatment of relapsed and/or refractory multiple myeloma. Blood 2021; 138(Suppl. 1): 1658 22 Naegele M: Advanced Nursing Practice in der klinischen Praxis. Leading Opinions Hämatologie & Onkologie 2022; 18(8): 26-28 23 Kisielewski D, Naegele M: Advanced practice nursing and CAR-T cell therapy: opportunities, challenges and future directions. Semin Oncol Nurs 2024; 40(3): 151628