ESTRO 2024: SBRT, TNT und neue Lösungen mit künstlicher Intelligenz
Autor:innen:
OÄ Dr. med. Elena Riggenbach
OA Dr. med. Hossein Hemmatazad
PD Dr. med. Mohamed Shelan
OÄ Dr. med. Ekin Ermiş
Radioonkologie
Universitätsspital Bern, Inselspital
Korrespondenz:
E-Mail: elena.riggenbach@insel.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der grösste europäische Kongress in der Radioonkologie fand dieses Jahr in Glasgow statt. Ein vielseitiges Programm mit Highlights zu einem breiten Spektrum von Tumorentitäten und Fachbereichen zeigte, in welche Richtung die strahlentherapeutische Zukunft gehen kann. Ausgewählte Studienergebnisse werden im folgenden Artikel zusammengefasst.
Keypoints
-
Die erste randomisierte Evidenz zu Operation vs. Radiotherapie (RT) bei Oropharynxkarzinomen zeigt, dass die RT sowohl hinsichtlich Nebenwirkungen als auch Tumorkontrolle mindestens gleichwertig ist.
-
Die Patient:innenselektion für den intendierten Organerhalt beim fortgeschrittenen Rektumkarzinom ist entscheidend, damit die Vorteile der Induktionschemotherapie (höhere Komplettremissions- und Organerhaltungsrate) die Mehrtoxizität aufwiegen.
-
Mit interstitieller Brachytherapie könnten zukünftige adjuvante Radiotherapiekonzepte von nur 2–3 Tagen für das Mammakarzinom im Frühstadium zum Standard werden.
Kopf-Hals-Tumoren: randomisierte Evidenz OP vs. RT
Die ORATOR-Studie war eine randomisierte Phase-II-Studie, die die primär operative mit der primär strahlentherapeutischen Therapie (OP-Arm vs. RT-Arm) bei Patient:innen mit Oropharynxkarzinomen verglich. Erste Studienresultate wurden bereits hochrangig im Lancet1 und im Journal of Clinical Oncology2 publiziert. Die finalen 5-Jahres-Daten wurden nun auf dem ESTRO-Kongress 2024 vorgestellt.3
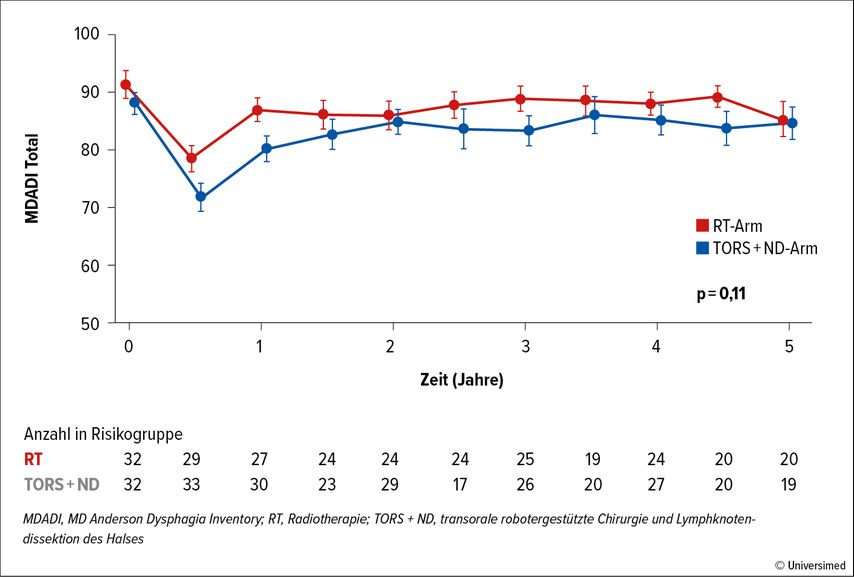
Der primäre Endpunkt, die Schluckfunktion, gemessen anhand des MD Anderson Dysphagia Inventory (MDADI), unterschied sich während des gesamten Nachbeobachtungszeitraumes in den Gruppen nicht statistisch signifikant, wenngleich er zu allen Zeitpunkten zugunsten der primären Radio(chemo)therapie verschoben war (Abb. 1). Es fanden sich keine Unterschiede im progressionsfreien (PFS) oder Gesamtüberleben (OS; 5-Jahres-OS-Rate: 84% im RT-Arm vs. 85% im OP-Arm; p=0,92; 5-Jahres-PFS-Rate: 84% vs. 82%; p=0,83).
Abb. 1: Veränderung der Schluckfunktion (gemessen anhand des MDADI-Lebensqualitätsscore) im Zeitverlauf nach Behandlungsarm (modifiziert nach Palma DA et al.)3
Die kanadische Gruppe um David Palma stellte zudem die reifen OS-Daten der heiss diskutierten ORATOR2-Studie vor.4 Diese leicht modifizierte Nachfolgerstudie schloss einzig Patient:innen mit HPV-positiven Oropharynxkarzinomen ein (cT1–2, cN0–2 ohne extrakapsuläres Wachstum, cM0) und untersuchte für diese prognostisch günstigeren Tumoren eine Therapiedeeskalation im Sinne einer Dosisreduktion der Radiotherapie (RT).
Patient:innen erhielten randomisiert entweder eine primäre, dosisreduzierte RT (RT-Arm: 60Gy auf Makrotumoranteile und 48–54Gy auf Lymphabflusswege in 30 Fraktionen, mit wöchentlichem Cisplatin bei nodaler Positivität) oder eine transorale laser- oder robotergestützte Resektion mit Neck-Dissektion ± adjuvanter RT (OP-Arm). Es war bereits bekannt, dass die Studie vorzeitig bei 61 Patient:innen aufgrund von vorherigen Todesfällen im OP-Arm (zwei davon therapieassoziiert) abgebrochen werden musste.5
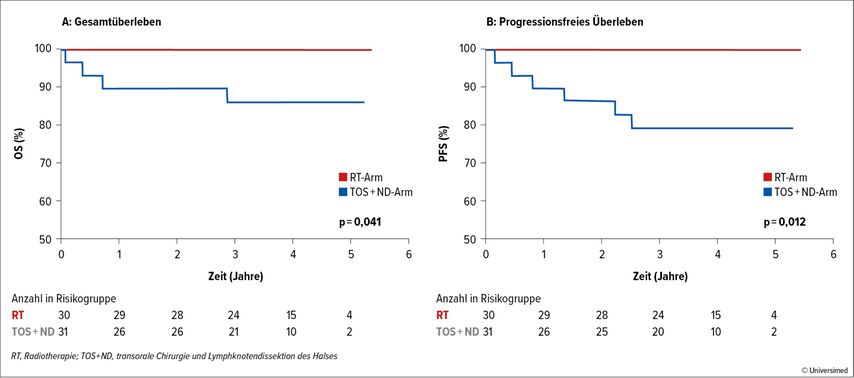
Der primäre Endpunkt der Verlängerung des Gesamtüberlebens nach zwei Jahren im Vergleich zu einer historischen Kontrolle wurde nach einem medianen Follow-up von 3,7 Jahren im RT-Arm erreicht (2-Jahres-OS-Rate: 100%; p=0,006), nicht jedoch im OP-Arm (2-Jahres-OS-Rate: 90%; p=0,296). Der OP-Arm war hinsichtlich OS zudem signifikant schlechter als der RT-Arm (p=0,041; Abb. 2). Das gleiche Muster zeigte sich beim 2-Jahres-PFS (100% vs. 86%; p=0,012).
Abb. 2: Gesamtüberleben (A) und progressionsfreies Überleben (B) stratifiziert nach Behandlungsarm (modifiziert nach Palma DA et al.)4
Der Anteil an Patient:innen mit keinerlei funktioneller Einschränkung bei der Nahrungsaufnahme war deutlich zugunsten des RT-Armes verschoben (81% vs. 38%; p=0,05). Patient:innenberichtete Endpunkte der Lebensqualität waren vergleichbar in beiden Behandlungsarmen, ebenso die Schluckfunktion gemäss MDADI.
Auch wenn von onkochirurgischer Seite bezüglich dieser Studie wiederholt auf die unerwartet hohe Mortalität im OP-Arm hingewiesen wird (und die gewählte Technik, ein zu grosser chirurgischer Sicherheitsabstand oder der Zufall als Erklärung gesucht werden), muss jegliche Rate an Grad-5-Toxizitäten im Kontext potenzieller Deeskalation der Therapie HPV-positiver Oropharynxkarzinome äusserst kritisch eingeordnet werden.
Prostatakarzinom
Die moderate Hypofraktionierung (mit leicht erhöhter Einzeldosis von 3Gy über vier Wochen) ist für viele Patient:innen, die mit lokalisiertem Prostatakarzinom (PC) geheilt werden können, der radiotherapeutische Standard. Eine weitere Verkürzung des Behandlungsschemas mit noch höherer Einzeldosis (≥5Gy) wird dank präziser, bildgeführter Positionierungstechnik möglich («stereotactic body radiotherapy», SBRT) und zeigte sich in der PACE-B-Studie für Menschen mit PC im mehrheitlich intermediären Risikostadium (IR) als sicher.6 Deutlich weniger Daten liegen für das Stadium mit hohem Risiko (HR) und das häufig eingesetzte SBRT-Regime von fünf Bestrahlungssitzungen vor.7
In der grossen Phase-III-Studie PACE-C erhielten 1208 Patient:innen mit IR oder HR PC randomisiert entweder eine moderat hypofraktionierte Bestrahlung (MHRT: 60Gy/20 Fraktionen über vier Wochen) oder eine SBRT (36,25Gy/fünf Fraktionen über ein bis zwei Wochen).8 Ergänzend erhielten alle Patient:innen eine antihormonelle Therapie über sechs bis zwölf Monate. Da bei höherem Risikoprofil auch die Bestrahlungsregion durch Einschluss von mehr Samenblasenvolumen grösser sein kann, sind die vorgestellten Akuttoxizitätsdaten relevant.
Etwa ein Drittel der eingeschlossenen Patient:innen waren HR, 28% im SBRT-Arm hatten ein Tumorstadium T3a, erhielten also ein etwas grösseres Bestrahlungsvolumen. Trotz akzelerierter Behandlung zeigten sich keine Unterschiede in Bezug auf die Häufigkeit irritativer oder obstruktiver Beschwerden der Harnblase. Die mit CTCAE und EPIC-26 gemessene Beeinträchtigung der Darmfunktion trat hingegen nach SBRT statistisch signifikant häufiger auf. Hochgradige Nebenwirkungen (Grad 3) waren äusserst selten und vergleichbar in beiden Armen (<1%). Die Spättoxizitäts- und Effizienzdaten der PACE-C-Studie bleiben abzuwarten, damit die SBRT auch für dieses Patient:innenkollektiv mit höchster Evidenz gestützt werden kann.
Die Autor:innen einer deutlich kleineren Phase-II-Studie haben am diesjährigen Kongress bereits ihre 5-Jahres-Daten vorgestellt. In der hypo-FLAME-Studie wurde bei 100 Patient:innen mit PC (75% HR, 25% IR) die SBRT mit integrierter Dosiseskalation auf den im MRI sichtbaren Makrotumor untersucht (fünf Sitzungen, 1x/Woche). Die 5-Jahres-Daten legen nun ein mit der MHRT vergleichbares, akzeptables Toxizitätsprofil bei guter biochemischer Kontrollrate nahe (von 93% nach fünf Jahren).9
Rektumkarzinom: Organerhalt nachInduktions-TNT
Die totale neoadjuvante Therapie (TNT) ist der neue Standard für lokal fortgeschrittene Hochrisiko-Rektumkarzinome. Mit ihr werden pathologische Komplettremissionsraten um 30% erzielt. Die französische GRECCAR12-Studie ist die erste Phase-III-Studie, die die TNT mit Induktionsregime zur Erhöhung des intendierten Organerhalts untersucht.10 Sie wurde mit dem Preis für das «Best Clinical Paper» ausgezeichnet. Im Unterschied zum Organerhalt durch den «Watch and wait»-Ansatz erlaubt der hier gewählte Organerhalt inklusive lokaler Exzision der Narbe bzw. des Tumorresiduums (LE) die pathologische Bestätigung des Ansprechens.
Insgesamt 213 Patient:innen mit fortgeschrittenem Rektumkarzinom (cT2T3 N0–1 M0, Tumorgrösse ≤4cm und ≤10cm von der Anokutanlinie) erhielten im experimentellen Arm eine Induktionstherapie mit vier Zyklen FOLFIRINOX (Folinsäure, 5-Fluorouracil, Irinotecan und Oxaliplatin) gefolgt von Radio-Chemotherapie (50Gy, konkomitierend Capecitabin) oder im Kontrollarm die alleinige Radio-Chemotherapie.
Das Ansprechen wurde klinisch und mittels MRI acht bis zehn Wochen nach Ende der neoadjuvanten Therapie kontrolliert. Bei gutem Ansprechen wurde die LE angeboten, mit komplettierender totaler mesorektaler Exzision (TME) einzig im Falle eines histopathologischen Stadiums ypT3 oder ypT2cN1. Patient:innen mit ungenügendem Ansprechen erhielten direkt eine TME.
Die Adhärenz bei der Induktionschemotherapie war hoch, jedoch traten bei 29% der Patient:innen Nebenwirkungen von Grad ≥3 auf (v.a. Diarrhö oder Neutropenie). Die Toleranz der nachgeschalteten Radio-/Chemotherapie und die perioperative Morbidität waren vergleichbar in beiden Armen. Der primäre Endpunkt der Organerhaltungsrate ein Jahr nach LE war statistisch knapp nicht signifikant, wenngleich er mit 72% nach Induktionschemotherapie vs. 63% mit alleiniger Radio-Chemotherapie als möglicherweise klinisch relevant eingestuft werden kann (HR: 1,88; 95% CI: 0,99–3,57). Die pathologische Komplettremission war höher im experimentellen Arm (45% vs. 28%; OR: 2,13; 95% CI: 1,16–3,91). Weitere sekundäre Endpunkte des OS und rezidivfreien Überlebens blieben nach drei Jahren ohne Unterschied.
Interessanterweise zeigten die Subgruppen der initialen TME (also jene Patient:innen mit ungenügend eingestuftem Ansprechen) in beiden Armen einen hohen Anteil an ypT0 (41% vs. 25%), sodass die korrekte Patient:innenselektion als grosse Herausforderung in der Strategie des Organerhaltes bleibt.
Zervixkarzinom, Mammakarzinom und interventionelle Radiotherapie
Die multizentrischen prospektiven EMBRACE-Studien legen den Standard der bildgestützten Brachytherapie und der individualisierten Dosisplanung für die Behandlung des fortgeschrittenen Zervixkarzinoms im klinischen Alltag fest.
Welche entscheidenden Vorteile die Implementierung moderner Technik und standardisierter Dosisvorgaben hinsichtlich lokaler Kontrolle, Gesamtüberleben und Toxizitätsreduktion erbringt, ist von den Langzeitdaten der Studie EMBRACE-I bereits bekannt. Nun wurde eine relevante Zusatzuntersuchung derselben Studiengruppe zur konkomitierenden Chemotherapie präsentiert.11 Sie untersuchte den Einfluss der kumulativen Cisplatin-Dosis während der definitiven Radio-Chemotherapie des Zervixkarzinoms auf die Entwicklung von Fernmetastasen. Das konkomitierende Cisplatin wurde wöchentlich in bis zu sieben Zyklen und in einer Dosis von 40mg/m2 oder dosisreduziert 30mg/m2 appliziert. Die EMBRACE-I-Kohorte wurde hierfür in vier Dosislevel unterteilt, abhängig von der kumulativ erhaltenen Cisplatindosis (≤80, 90–160, 170–200, >200mg/m2). Zudem wurden die 1318 Patient:innen basierend auf zwei Risikofaktoren, der nichtplattenepithelialen Histologie oder der nodalen Positivität, in «high-risk» (Vorliegen von mindestens einem Risikofaktor) und «low-risk» (kein Risikofaktor) eingeteilt.
Während bei «Low-risk»-Patient:innen das Fernmetastasierungsrisiko nicht von der Cisplatindosis abhing, war eine solche Korrelation bei «High-risk»-Patient:innen vorhanden: Der Vorteil war bei einer kumulativen Cisplatindosis von 170–200mg/m2 am deutlichsten. Kein zusätzlicher Benefit war für das Dosislevel >200mg/m2 zu sehen. Ob dieser Vorteil auch in der sich verändernden Therapielandschaft mit Pembrolizumab gilt, ist unklar.
In der Entität des Mammakarzinoms waren Deeskalationsstrategien der Teilbrustbestrahlung («partial breast irradiation», PBI) im Fokus. Von der bisher grössten Studie zur akzelerierten Teilbrustbestrahlung (APBI) in der konventionellen Bestrahlungstechnik (3D-CRT) wurde der primäre Endpunkt präsentiert.12 Die IRMA-Studie war eine randomisierte Phase-III-Nichtunterlegenheits-Studie, in deren Rahmen 3309 Patient:innen mit Mammakarzinom und günstigem Risikoprofil (Alter ≥49 Jahre, <3cm Tumorgrösse, pN0–1) entweder die adjuvante APBI in 3D-CRT (38,5Gy/10 Fraktionen, 2x täglich) oder die Ganzbrustbestrahlung («whole breast irradiation», WBI) erhielten. Der primäre Endpunkt des ipsilateralen Lokalrezidivs nach fünf Jahren zeigte sich nicht unterlegen (0,9% nach APBI vs. 0,7% nach WBI, n.s.).
Einen Schritt weiter geht die Technik der interstitiellen Brachytherapie, für die zunehmend der modernere Begriff der interventionellen Radiotherapie verwendet wird. Sie erlaubt dank hoher Konformität und steilem Dosisgradienten im Setting der PBI kürzeste Behandlungskonzepte. Level-I-Evidenz für die Nichtunterlegenheit der einwöchigen Behandlung gegenüber der Ganzbrustbestrahlung lag für diese Technik längst vor.
Die nun vorgestellten 5-Jahres-Daten der «Very Accelerated Partial Breast Irradiation»(VAPBI)-Studie sind vielversprechend.13 In dieser Phase-I/II-Studie erhielten 81 Patient:innen mit «Low-risk»-Mammakarzinom eine adjuvante VAPBI mittels interventioneller Radiotherapie. Hierbei wurden drei Fraktionen von 7,45Gy oder vier Fraktionen von 6,25Gy über eine Gesamtbehandlungszeit von zwei bis drei Tagen appliziert.
Bei leicht höherem Auftreten moderater Fibrosierung (22% Grad 1, 9% Grad 2) und sehr gutem kosmetischem Resultat wurden vergleichbare Lokalkontrollraten berichtet.
Palliation und Oligometastasierung: Mehrwert durch SBRT?
Im Bereich der Palliation wurde die Phase-III-Studie DOSIS vom neuen ESTRO-Präsidenten Prof. Dr. med. Matthias Guckenberger vorgestellt.14 Sie musste aufgrund schlechter Rekrutierung vorzeitig beendet werden, erreichte aber dennoch ihren primären Endpunkt.
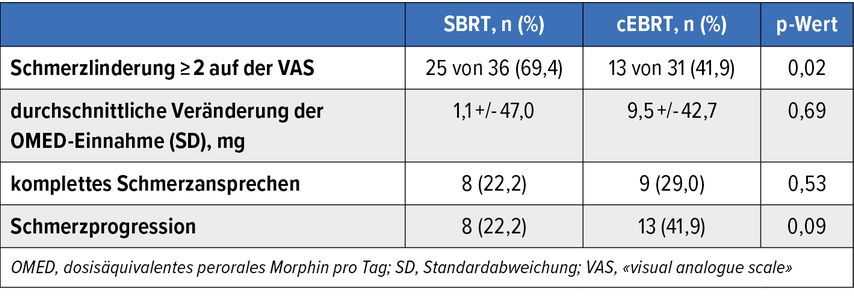
63 Patient:innen mit schmerzhafte, spinaler Knochenmetastase erhielten randomisiert entweder eine dosisintensivierte SBRT (40Gy/5 Fraktionen oder 48,5Gy/10) oder eine konventionelle externe Radiotherapie (cEBRT; 30Gy/10 oder 20Gy/5). Die Schmerzlinderung um ≥2 Punkte gemessen auf der «visual analogue scale» (VAS) war nach sechs Monaten signifikant höher nach SBRT verglichen mit der cEBRT (69% vs. 42%; p=0,02). Nicht alle erfassten Schmerzparameter zeigten jedoch einen Vorteil (Tab.1),14 sodass auch hier die Optimierung der korrekten Patient:innenselektion angestrebt werden sollte.
Tab. 1: Schmerzansprechen sechs Monate nach stereotaktischer Radiotherapie (SBRT) oder konventioneller Radiotherapie (cEBRT) in der Intention-to-treat-Analyse (modifiziert nach Guckenberger M et al.)14
Zudem wurden finale Daten der einarmigen Phase-II-Studie ETOP-CHESS vorgestellt.15 Sie untersuchte bei Patien:innen mit oligometastasiertem NSCLC und maximal drei Metastasen, die drei Monate nach Standard-Systemtherapie progressionsfrei blieben, Sicherheit und Effizienz der zusätzlichen Lokaltherapien (SBRT der Metastasen sowie definitive Radiotherapie oder Operation des Primärtumors).
Mit einer 1-Jahres-PFS-Rate von 45% wurde der primäre Endpunkt nicht erreicht. Die Progressionen waren mehrheitlich distant und ausserhalb der lokal behandelten Regionen. Die multimodale Therapie zeigte ein günstiges Sicherheitsprofil, was als Basis für die nächste Kohorte genommen wurde, für die bereits rekrutiert wird und bei der die Resultate durch Intensivierung mit dualer Immuncheckpoint-Blockade weiter verbessert werden sollen.
Künstliche Intelligenz in der Strahlentherapie
Die künstliche Intelligenz (KI) ist im radioonkologischen Klinikalltag angekommen und wird unser Fachgebiet in den nächsten Jahren nachhaltig verändern, was an zahlreichen Beiträgen auf diesem Kongress deutlich wurde.
Die personalisierte RT setzt die Abgrenzung von Zielvolumen und angrenzenden Risikoorganen (sog. Konturierung) voraus. KI-unterstützte Automatisierungen könnten Effizienz, Genauigkeit und Konsistenz dieser arbeits- und zeitintensiven Aufgabe erhöhen. KI-basierte Segmentierungslösungen für Risikoorgane sind in vielen Kliniken bereits im Einsatz, die Konturierung von Zielvolumen hingegen bleibt eine grosse Herausforderung.
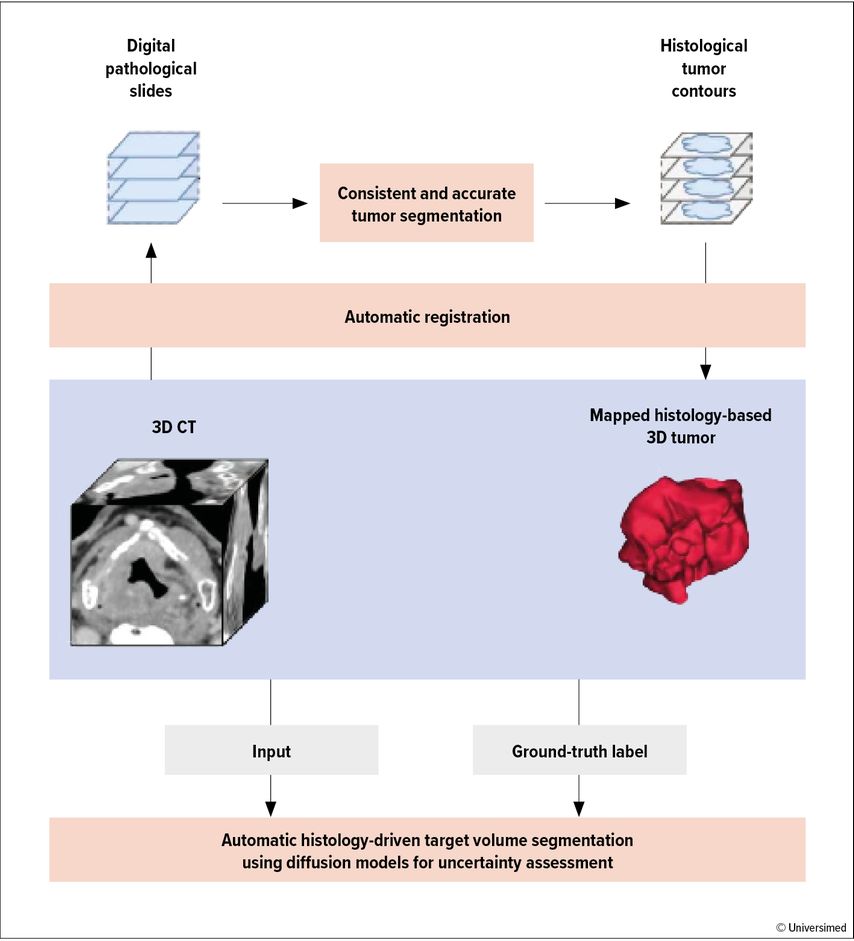
Eine französische Gruppe hat einen innovativen Ansatz vorgestellt, der den histologischen Goldstandard in die Autokonturierung von Zielvolumen implementiert.16 Ein Datensatz von 180 Patient:innen mit Kopf-Hals-Tumoren mit jeweils präoperativem CT und fünf bis zwölf digitalisierten Histologieschnitten von reseziertem, tumortragendem Larynxgewebe wurde als Input für die Generierung eines Deep-Learning-Autosegmentierungsmodells von Zielvolumen verwendet (Abb. 3). Eine bereits validierte, multimodale Registrierungsmethode wurde dabei verwendet, um die Tumorkonturen der digitalisierten Histologieschnitte auf die (präoperative) Planungs-CT zu übertragen. An einer Testkohorte von 20 Fällen war die automatisiert erstellte Zielvolumenkontur näher am Goldstandard als die manuellen Konturen von Expert:innen.
Abb. 3: Pipeline automatisierter Zielvolumenkonturierung unter Verwendung der Histologie. Exakte Tumorausdehnung digitalisierter Histologieschnitte wird auf die Planungs-CT transferiert («deformable mapping»). Konturen von beiden Modalitäten werden in das Deep-Learning-Autosegmentierungsmodell eingespeist (modifiziert nach Leroy A et al.)16
Richtig eingesetzt haben solche Ansätze das Potenzial, die Therapieplanung grundlegend zu verändern und die Behandlungsqualität der RT weiter zu verbessern.
Literatur:
1 Nichols AC et al.: Radiotherapy versus transoral robotic surgery and neck dissection for oropharyngeal squamous cell carcinoma (ORATOR): an open-label, phase 2, randomised trial. Lancet Oncol 2019; 20: 1349-59 2 Nichols AC et al.: Randomized trial of radiotherapy versus transoral robotic surgery for oropharyngeal squamous cell carcinoma: long-term results of the ORATOR trial. J Clin Oncol 2022; 40: 866-75 3 Palma DA et al.: Radiation vs transoral robotic surgery for oropharyngeal cancer: final results of the ORATOR trial. ESTRO 2024; Abstr. #1421 4 Palma DA et al.: Radiotherapy vs. trans-oral surgery for treatment de-escalation in HPV-associated oropharyngeal squamous cell carcinoma: primary analysis of the ORATOR2 trial. ESTRO 2024; Abstr. #3409 5 Palma DA et al.: Assessment of toxic effects and survival in treatment deescalation with radiotherapy vs transoral surgery for HPV-associated oropharyngeal squamous cell carcinoma: the ORATOR2 phase 2 randomized clinical trial. JAMA Oncol 2022; 8: 1-7 6 Tree AC et al.: Intensity-modulated radiotherapy versus stereotactic body radiotherapy for prostate cancer (PACE-B): 2-year toxicity results from an open-label, randomised, phase 3, non-inferiority trial. Lancet Oncol 2022; 23: 1308-20 7 Fransson P et al.: Ultra-hypofractionated versus conventionally fractionated radiotherapy for prostate cancer (HYPO-RT-PC): patient-reported quality-of-life outcomes of a randomised, controlled, non-inferiority, phase 3 trial. Lancet Oncol 2021; 22: 235-45 8 Tree A et al.: Acute toxicity from PACE-C comparing Stereotactic Body Radiotherapy (SBRT) with moderate hypofractionation (MHRT). ESTRO 2024; Abstr. #3395 9 Draulans C et al.: Focal boost SBRT in men with intermediate- and high-risk PCa: 5-year results of the hypo-FLAME trial. ESTRO 2024; Abstr. #3396 10 Vendrely V et al.: Organ preservation in rectal cancer: the GRECCAR12 randomized phase 3 trial (NCT02514278). ESTRO 2024; Abstr. #1929 11 Knoth J et al.: Impact of cumulative cisplatin-dose on distant metastasis after chemoradiation of cervical cancer. ESTRO 2024; Abstr. #890 12 Meduri B et al.: APBI with 3D-CRT vs. WBI: primary endpoint results of the prospective randomised phase 3 IRMA trial. ESTRO 2024; Abstr. #3520 13 JL Guinot et al.: Five-year results of Very Accelerated Partial Breast Irradiation VAPBI phase I-II GEC-ESTRO trial. ESTRO 2024; Abstr. #2246 14 Guckenberger M et al.: Dose-intensified stereotactic body radiotherapy for painful vertebral metastases: a randomized phase 3 trial. Cancer 2024 15 Guckenberger M et al.: Multimodality treatment in synchronous oligometastatic NSCLC: final analysis of the ETOP CHESS trial. ESTRO 2024; Abstr. #178 16 Leroy A et al.: Histology to CT transfer for HNC target volume auto-segmentation with deep-learning diffusion models. ESTRO 2024; Abstr. #1334
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...