Die Rolle der Bildgebung bei der kardialen Sarkoidose
Autor:
Prof. Dr. Dr. med. Christoph Gräni
Leiter Kardiale Bildgebung
Universitätsklinik für Kardiologie
Inselspital, Universitätsspital Bern
E-Mail: christoph.graeni@insel.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die kardiale Sarkoidose ist eine seltene, jedoch bedeutende entzündliche Erkrankung des Herzens. Die klinische Präsentation kann sehr unterschiedlich sein und reicht von subklinischen Manifestationen bis hin zu thorakalen Beschwerden, Dyspnoe, Rhythmusstörungen und plötzlichem Herztod. Neben der Biopsie spielt die kardiale Bildgebung, namentlich die Echokardiografie, das Herz-MRI und die Positronenemissionstomografie (PET) eine entscheidende Rolle in der Diagnostik. Herz-MRI und PET sind zudem nützliche Methoden zur Risikostratifizierung und erlauben das Monitoring der Patienten unter Therapie.
Keypoints
-
Die kardiale Sarkoidose ist sehr selten und kann isoliert oder in Kombination mit dem Befall von mehreren Organen auftreten.
-
Die Symptome der kardialen Sarkoidose sind unspezifisch und umfassen neben Thoraxschmerzen unter anderem Herzrhythmusstörungen und Herzinsuffizienz.
-
Die Echokardiografie kann Hinweise für eine kardiale Sarkoidose liefern mit Vorhandensein einer Verdickung oder Ausdünnung der Herzwände, welche nicht einer Koronarversorgung zuordenbar sind, eine Aneurysmabildung und eine verminderte linkventrikuläre Ejektionsfraktion.
-
Herz-MRI und FDG-PET sind wichtige Verfahren zur Erkennung von Entzündung und Myokardnarben und können die Herzbeteiligung der Sarkoidose dokumentieren.
-
Die Therapie umfasst eine medikamentöse Behandlung mittels Herzinsuffizienz- und Rhythmustherapie, Immunsuppression und gegebenenfalls eine Herztransplantation.
-
Das Monitoring der Entzündung mittels Herz-MRI und PET ermöglicht eine präzise Verlaufskontrolle und Risikostratifizierung.
Die Sarkoidose ist eine entzündliche, granulomatöse Systemerkrankung, deren genaue Ursache unklar ist. Sie betrifft in erster Linie die Lunge und die Lymphknoten, kann aber auch andere Organe wie Leber, Haut, Augen, zentrales Nervensystem und Herz betreffen.1 Die genaue Prävalenz der kardialen Sarkoidose ist schwierig zu bestimmen, da viele Fälle unentdeckt bleiben oder fehldiagnostiziert werden. Es wird geschätzt, dass etwa 5–25% der Patienten mit systemischer Sarkoidose eine Herzmanifestation aufweisen. Die isolierte kardiale Sarkoidose, bei der das Herz die einzige betroffene Region ist, tritt seltener auf und macht etwa 2–5% der Fälle aus.2
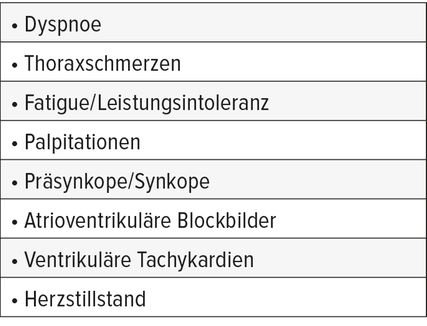
Generell können bei der kardialen Sarkoidose alle Strukturen des Herzens von der Bildung von Granulomen betroffen sein, jedoch sind am häufigsten das linksventrikuläre Myokard und das Reizleitungssystem betroffen. Die kardiale Sarkoidose stellt eine Herausforderung dar, weil sie wegen ihrer variablen klinischen Präsentation schwierig zu diagnostizieren ist. Das klinische Spektrum reicht von subklinischer Manifestation als Zufallsfund bis zu Thoraxschmerzen, Palpitationen, Dyspnoe, Leistungsintoleranz, Müdigkeit, Synkope und Schwindel (Tab. 1). Selten ist der plötzliche Herztod die Erstmanifestation bei der kardialen Sarkoidose.
Im Elektrokardiogramm (EKG) und der Ergometrie können Erregungsleitungsstörungen wie atrioventrikuläre Blockbilder oder eine Brady- oder Tachykardie Hinweise geben. Labortests können erhöhte Entzündungsmarker wie C-reaktives Protein und Leukozyten sowie erhöhte Herzenzyme wie Troponin aufweisen, welche jedoch weder sensitiv noch spezifisch sind. Erhöhte Laborparameter wie das NT-pro-BNP oder BNP können auf eine Herzinsuffizienz hindeuten, sind aber nicht immer zwingend vorhanden.2 Die Biopsie gilt als Goldstandard, jedoch wird gerade bei der isolierten kardialen Sarkoidose die Diagnose oft verpasst. Deshalb sind die kardialen Bildgebungsverfahren, namentlich die Echokardiografie, die kardiale Magnetresonanztomografie (MRI), FDG(Fluorodeoxyglucose)-Positronenemissionstomografie (PET) besonders wichtig bei Verdacht auf eine kardiale Sarkoidose.3
Diagnostik
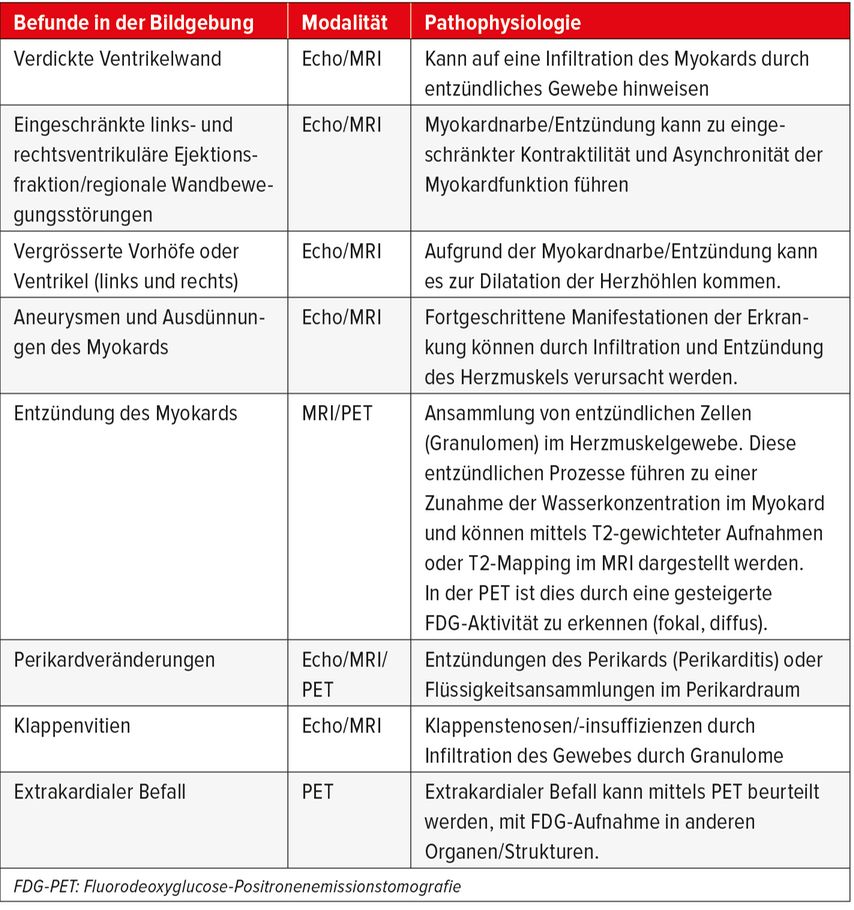
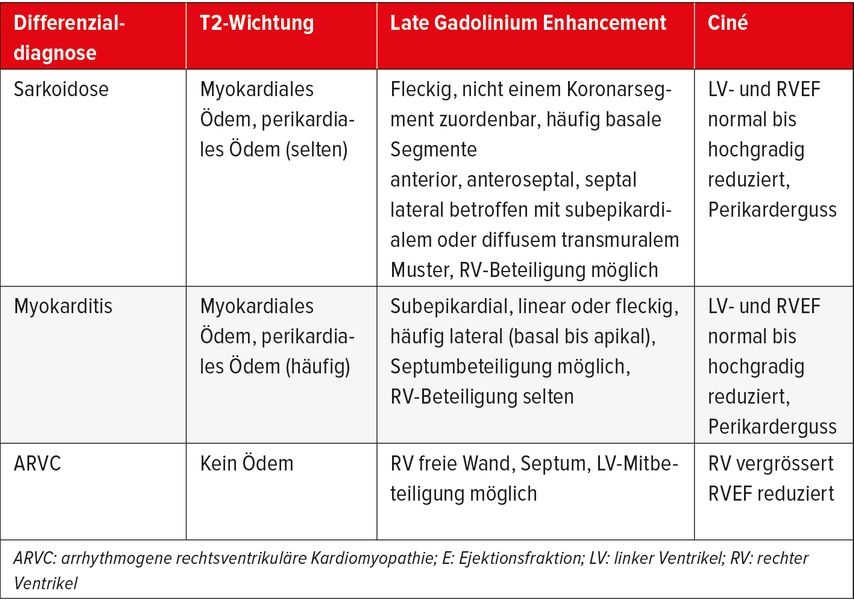
Bei kardialer Sarkoidose können folgende echokardiografische Befunde eruiert werden: eine Verdickung der Herzwände durch das Ödem im Rahmen einer aktiven Sarkoidose, Wandbewegungsstörungen und ausgedünnte Herzwände bei Narben, nicht einer koronaren Versorgung zuordenbar, mit konsekutiver eingeschränkter Pumpfunktion und allenfalls Perikarderguss (Tab. 2). Eine mögliche Sarkoidose-assoziierte pulmonale Hypertension ist selten, sollte aber in der echokardiografischen Beurteilung nicht vergessen werden. Falls der Verdacht einer kardialen Sarkoidose aufgrund von klinischen und echokardiografischen Befunden vorliegt, ist das Herz-MRI im nächsten Schritt eine optimale Methode zur Differenzierung von der koronaren Herzkrankheit, einer arrhythmogenen rechtsventrikulären Kardiomyopathie, dilatativen und restriktiven Kardiomyopathien sowie einer akuten oder chronischen Myokarditis4 (Tab. 3).
Das Herz-MRI repräsentiert eine hochauflösende Bildgebungstechnik, die detaillierte Informationen über die Gewebestruktur und -funktion liefert. Es kann entzündliche Veränderungen, Narbenbildung und Verdickungen des Herzmuskels nachweisen. Typische Befunde sind ein diffuses oder fleckiges Late Gadolinium Enhancement im linken, aber auch rechten Ventrikel, nicht einem Koronarversorgungsgebiet zuordenbar sowie ein Myokardödem mit eingeschränkter Funktion und möglicher Dilatation des Ventrikels. Die FDG-PET spielt mittlerweile eine wichtige Rolle und ist auch in den drei internationalen Guidelines – der Heart Rhythm Society (HRS), der World Association of Sarcoidosis and Other Granulomatous Disorders Sarcoidosis Organ (WASOG) und der Japanese Ministry of Health & Welfare (JMHW) – bezüglich der diagnostischen Kriterien für eine kardiale Sarkoidose verankert.5 Bei der kardialen Sarkoidose zeigt die FDG-PET typischerweise eine erhöhte Aktivität in den betroffenen Myokardregionen an und kann auch dabei helfen, andere Organe zu identifizieren, die von der Sarkoidose betroffen sein können.
Obwohl die definitive Diagnose einer kardialen Sarkoidose nur mittels einer endomyokardialen Biopsie (EMB) gestellt werden kann, ist in hochsuggestiven Situationen auch die Kombination von nichtinvasiven Kriterien genügend5 (Abb. 1). Zu beachten ist, dass die Sensitivität der EMB aufgrund falsch negativer Befunde (sogenannte «Sampling Errors») relativ niedrig ist – dies aufgrund des häufig fleckigen Befalls des Herzmuskels. Die Bildgebung kann dabei in gewissen Situationen hilfreich sein, um eine EMB optimal zu steuern. Unabhängig davon sollte bei Patienten mit extrakardialer Sarkoidose zunächst eine histologische Bestätigung, zum Beispiel aus Lymphknoten oder durch Lungenbiopsie, angestrebt werden, da dies mit einer höheren diagnostischen Aussagekraft verbunden ist. Wenn eine extrakardiale Sarkoidose bioptisch gesichert werden kann, ist die Herz-MRI- und/oder FDG-PET-Bildgebung häufig auch ausreichend, um eine aktive kardiale Beteiligung der Sarkoidose auch ohne EMB zu diagnostizieren.5 Wenn jedoch der Ansatz der extrakardialen Biopsie nicht erfolgreich ist oder eine isolierte kardiale Sarkoidose vermutet wird und nichtinvasiv nicht gestellt werden kann, sollte anschliessend neben der Bildgebung eine EMB in Betracht gezogen werden. Die EMB sollte insbesondere bei Patienten mit einem raschen, sich verschlechternden Verlauf mit Herzinsuffizienz, fehlendem Ansprechen auf eine Herzinsuffizienztherapie oder bei therapierefraktären Arrhythmien durchgeführt werden.
Abb. 1: Herz-MRI und FDG-PET einer 49-jährigen Patientin, die sich mit Dyspnoe, erhöhtem NT-proBNP und Kammertachykardie im Langzeit-EKG vorstellte. Das Herz-MRI bestätigte die Echokardiografie mit Dilatation des linken Ventrikels sowie inferiorer Hypo- bis Akinesie (gelbe Pfeile) bei Abwesenheit einer koronaren Herzkrankheit in diesem Versorgungsgebiet. Zudem zeigte sich im Herz-MRI eine Hypertrophie des Septums mit 17mm (weisser Doppelpfeil) und eine inferiore Ausdünnung des Myokards (gelbe Pfeile), eine LVEF von 39%, Ödem (schwarze Pfeile) im T2-Mapping mit 57ms (Norm <50ms) sowie ein ausgeprägtes, fleckiges und diffuses Late Gadolinium Enhancement (rote Pfeile) anterior, septal, inferior und im rechten Ventrikel. Die FDG-PET zeigte eine z. T. fokale und diffuse gesteigerte metabolische Aktivität (weisser Pfeil) im linken Myokard und teilweise im rechten Myokard. Aufgrund der Befunde konnte somit die Diagnose einer isolierten kardialen Sarkoidose gestellt werden (LVEF: linksventrikuläre Ejektionsfraktion; FDG-PET: Fluorodeoxyglucose-Positronenemissionstomografie)
Fallstricke bei der FDG-PET-Bildgebung und der EMB
Im Gegensatz zur Viabilitätsprüfung oder Tumorsuche ist bei der FDG-PET zur Inflammationssuche eine besondere Diät-Vorbereitung nötig.6 Die empfohlene kohlenhydratfreie (oder kohlenhydratarme), protein- und fettreiche Diät vor einer FDG-PET-Untersuchung bei Sarkoidose basiert auf der Pathophysiologie des Glukosestoffwechsels und der FDG-Aufnahme im Körper. Die Entzündungsherde bei der Sarkoidose weisen eine erhöhte Stoffwechselaktivität auf, die zu einer erhöhten Glukoseaufnahme führt. FDG ist ein radioaktives Glukoseanalogon, das in den Entzündungsherden akkumuliert und somit die Entdeckung und Lokalisierung der betroffenen Gewebe ermöglicht. Durch die kohlenhydratfreie (oder kohlenhydratarme) Diät vor der FDG-PET-Untersuchung wird das Myokard auf einen Fettsäurestoffwechsel umgestellt, wodurch eine bessere Unterscheidung zwischen den Entzündungsherden und dem normalen Myokardgewebe ermöglicht wird. Wichtig zu wissen: Es können auch andere kardiale und extrakardiale Strukturen wie die physiologische Stoffwechselaktivität von aktiviertem Skelettmuskel, Tumoren, Infektionen, Thrombus oder Plaques zu einer erhöhten FDG-Aufnahme führen.
Therapieansätze
Die interdisziplinäre Behandlung der kardialen Sarkoidose zielt darauf ab, die Entzündung zu reduzieren, die Symptome zu lindern, die Herzfunktion zu verbessern und Rhythmusstörungen und deren bedrohliche Folgen zu vermeiden. In leichten Fällen kann eine medikamentöse Therapie mit entzündungshemmenden Medikamenten wie Kortikosteroiden ausreichen. In schwereren Fällen können Immunsuppressiva oder andere immunmodulierende Medikamente eingesetzt werden. Selten ist sogar eine Herztransplantation erforderlich.5
Verlauf, Prognose, Therapiemonitoring
Der klinische Verlauf und die Prognose der Sarkoidose sind sehr variabel. Während die Mehrheit der Sarkoidosepatienten einen kurzen, selbstlimitierenden Verlauf der Erkrankung mit vollständiger Genesung zeigen, tritt bei einer signifikanten Anzahl von Fällen ein chronischer oder chronisch-rezidivierender Verlauf auf. Bis zu 10% der Patienten entwickeln schwerwiegende Komplikationen wie eine terminale Lungenfibrose oder eine fortschreitende Beteiligung des Herzens mit Herzinsuffizienz oder malignen Herzrhythmusstörungen. Das regelmässige Monitoring der kardialen Sarkoidose ist von grosser Bedeutung, um den Verlauf der Erkrankung zu überwachen und die Therapie anzupassen. Bildgebende Verfahren wie das Herz-MRI und die FDG-PET spielen dabei eine entscheidende Rolle. Sie ermöglichen es, Veränderungen im Herzen zu erkennen, den Therapieerfolg zu bewerten und das Risiko für Komplikationen abzuschätzen.7
Fazit
Die kardiale Sarkoidose ist eine komplexe Herzerkrankung, die eine genaue Diagnosestellung, eine angemessene Therapie und ein regelmässiges Monitoring erfordert. Bildgebende Verfahren wie die Echokardiografie, das Herz-MRI und die FDG-PET sind von entscheidender Bedeutung, um die Diagnose zu bestätigen, das Risiko abzuschätzen und den Therapieerfolg zu dokumentieren. Die interdisziplinäre Betreuung der Sarkoidosepatienten ist äusserst wichtig, um ein optimales Management zu gewährleisten.
Literatur:
1 Franzen DP et al.: Sarcoidosis – a multisystem disease. Swiss Med Wkly 2022; 152: w30049 2 Sohn DW, Park JB: Cardiac sarcoidosis. Heart 2023; doi:10.1136/heartjnl-2022-321379 3 Greulich S et al.: Hybrid cardiac magnetic resonance/fluorodeoxyglucose positron emission tomography to differentiate active from chronic cardiac sarcoidosis. JACC Cardiovasc Imaging 2022; 15: 445-56 4 Gräni C: How cardiac magnetic resonance is changing the management of myocarditis. Eur Heart J 2023; 44: 909-11 5 Ueberham L et al.: Pathophysiological gaps, diagnostic challenges, and uncertainties in cardiac sarcoidosis. J Am Heart Assoc 2023; 12: e027971 6 Hutt E et al.: Novel dietary protocol prior to 18F-fluorodeoxyglucose positron emission tomography to evaluate for cardiac sarcoidosis. J Nucl Cardiol 2021; 28: 2190-3 7 Adhaduk M et al.: Comparison of cardiac magnetic resonance imaging and fluorodeoxyglucose positron emission tomography in the assessment of cardiac sarcoidosis: Meta-analysis and systematic review. J Nucl Cardiol 2022; doi:10.1007/s12350-022-03129-8r
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...