Endokarditis nach TAVI
Autorin:
PD Dr. med. Anna Conen, MSc
Klinik für Infektiologie und Infektionsprävention
Kantonsspital Aarau
Tellstrasse 25
5001 Aarau
E-Mail: anna.conen@ksa.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die infektiöse Endokarditis (IE) ist eine bekannte Komplikation nach chirurgischem oder interventionellem Aortenklappenersatz (AKE). Auch wenn die Inzidenz der IE bei beiden Formen des AKE ähnlich zu sein scheint, so gibt es doch bedeutende Unterschiede zwischen diesen beiden Krankheitsbildern. Die TAVI-assoziierte IE scheint besonders häufig sehr früh nach Einlage aufzutreten und dann vor allem durch Enterokokken verursacht zu sein. Diese Tatsache, aber auch die hohe Morbidität und Mortalität, die mit der TAVI-assoziierten IE verbunden sind, rechtfertigen optimierte peri- und postinter-ventionelle Hygiene- und Präventionsmassnahmen. Im Folgenden sollen Daten aus dem Schweizerischen TAVI-Endokarditis-Register vorgestellt werden.
Keypoints
-
Eine Mengenausweitung der TAVI ist zu erwarten, da zunehmend auch Patienten mit intermediärem und niedrigem perioperativem Risiko behandelt werden.
-
Die Inzidenz der infektiösen Endokarditis (IE) nach TAVI beträgt 1,0/100Personenjahre und ist damit etwa gleich wie nach chirurgischem Aortenklappenersatz. Die höchste Inzidenz findet sich sehr früh nach TAVI (<100 Tage).
-
Das Erregerspektrum der IE nach TAVI unterscheidet sich je nach Zeitpunkt des Auftretens der IE: Sehr früh (<100 Tage nach TAVI) dominieren Enterokokken, spät (>1 Jahr nach TAVI) S.aureus und vergrünende Streptokokken.
-
Die Komplikationsrate bei Patienten mit einer TAVI-assoziierten IE ist hoch, so besteht ein 4-fach erhöhtes Schlaganfall- und ein 6,5-fach erhöhtes Sterberisiko.
-
Deswegen ist die Prävention der Endokarditis wesentlich.
Im Jahr 2002 wurde erstmals bei einem Patienten mit symptomatischer Aortenklappenstenose eine Aortenklappe über einen Herzkatheter implantiert (Transkatheter-Aortenklappenimplantation, TAVI). Seither ist diese Methode zu einer Standardbehandlung der schweren symptomatischen Aortenklappenstenose geworden. Während initial vor allem Patienten mit einem hohen perioperativen Risiko mittels TAVI behandelt wurden, hat sich die TAVI auch bei Patienten mit einem intermediären und niedrigen perioperativen Risiko als effektiv und mindestens gleichwertig wie der chirurgische Aortenklappenersatz (AKE) erwiesen.1–3 Aufgrund dieser günstigen Studienergebnisse, aber auch der technischen Fortschritte und der vereinfachten Prozeduren hat sich die TAVI zu einer breit akzeptierten Behandlungsmethode der symptomatischen Aortenklappenstenose entwickelt, was sich in deutlich steigenden Fallzahlen widerspiegelt.
Eine bekannte Komplikation nach chirurgischem AKE, aber auch nach einer TAVI, ist die infektiöse Endokarditis (IE), welche einen relevanten Einfluss auf Morbidität, Mortalität und Gesundheitskosten hat.4 Erstmals wurde die IE nach TAVI im Jahr 2010 beschrieben.5 Die Inzidenz der IE nach TAVI wird in einer grossen, internationalen Registerstudie (20006 Patienten mit TAVI, davon 250 Patienten mit IE) mit 1,1/100Personenjahre (95% CI: 1,1–1,4) angegeben.6 Damit ist die Inzidenz vergleichbar mit derjenigen nach chirurgischem AKE, und dies, obwohl viele TAVI-Interventionen im Katheterlabor und nicht im Operationssaal durchgeführt werden, was Unterschiede in infektionspräventiven Massnahmen bedeuten könnte. Andererseits sind die Interventionsdauer und die Wundfläche beim chirurgischen AKE bedeutend grösser, was eine höhere Infektionsrate begünstigen könnte.1,3,7–9 Relevante Unterschiede bestehen allerdings im Erregerspektrum zwischen der IE nach chirurgischem AKE (v.a. Staphylokokken) und nach TAVI (mehrheitlich Enterokokken). Diese können unter anderem damit erklärt werden, dass TAVI-Patienten deutlich älter und polymorbider sind, mehr Kontakte zum Gesundheitswesen und somit eine veränderte Hautkolonisation aufweisen, aber auch durch die Interventionstechnik. Die TAVI wird mehrheitlich über einen Leistenzugang eingelegt, wobei sich die Leistenflora von der Hautflora im Thoraxbereich, die beim chirurgischen AKE relevant ist, unterscheidet.7,10–14
Prävention
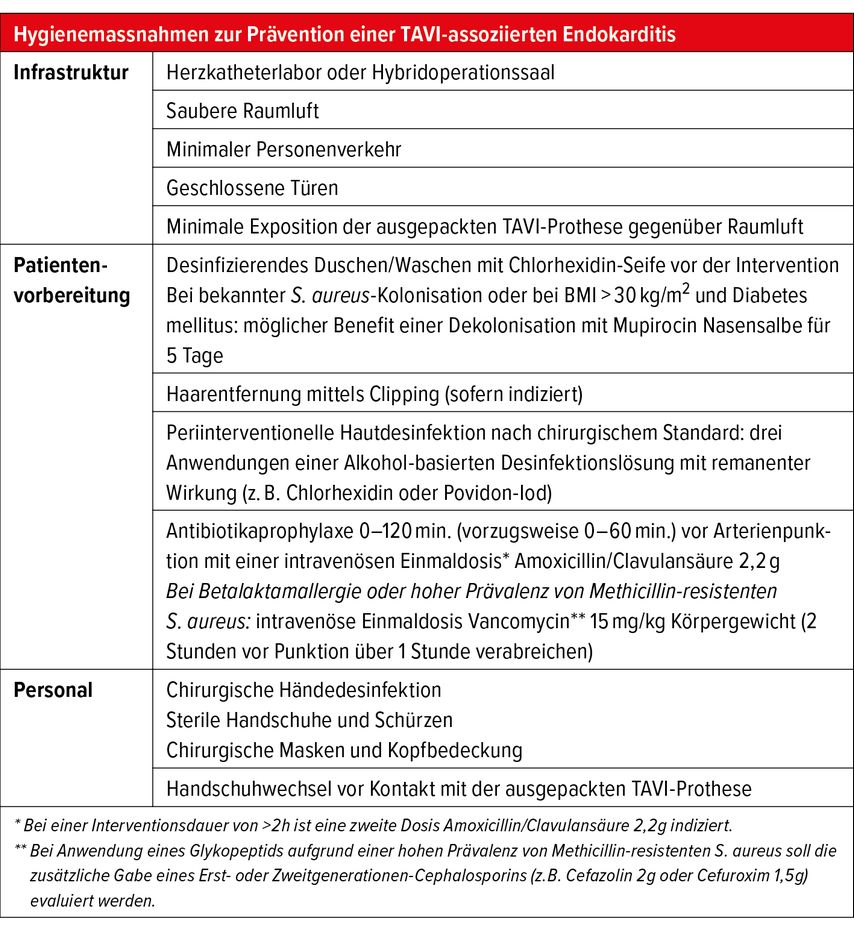
Im Gegensatz zum chirurgischen AKE, bei welchem die WHO und medizinische Fachgesellschaften Empfehlungen zur Prävention der IE publiziert haben, gab es bis vor Kurzem keine solchen für Patienten mit einer TAVI.15–17 Erst im Jahr 2021 wurden in Zusammenarbeit mit der internationalen Gesellschaft für kardiovaskuläre Infektionen (ISCVID) Empfehlungen zu infektionspräventiven Aspekten rund um die Infrastruktur (Katheterlabor oder Hybridoperationssaal), Patientenvorbereitung und Massnahmen beim Personal publiziert.18 Erwähnenswert ist die adaptierte Antibiotikaprophylaxe, welche die oben erwähnten, häufigen Erreger (inklusive Enterokokken) berücksichtigt (Tab.1). Diese optimierten Präventionsbemühungen sind gerade vor dem Hintergrund wesentlich, dass die TAVI-assoziierte IE eine der höchsten Mortalitätsraten überhaupt nach IE aufweist, welche im Spital mit 30–40% angegeben wird.6,8,11,19
Schweizerisches TAVI-Endo-karditis-Register
In der Schweiz werden seit 2007 TAVI Prozeduren durchgeführt. Seit 2011 werden alle Patienten gemäss Beschluss des Bundesamtes für Gesundheit zur Qualitätskontrolle und für die finanzielle Abgeltung in eine nationale, multizentrische, prospektive Kohortenstudie (Swiss TAVI Registry) eingeschlossen. Die Datenerhebung erfolgt elektronisch und klinische Ereignisse, einschliesslich der IE, werden durch ein definiertes Event-Komitee validiert. Erste Ergebnisse des Schweizerischen TAVI-Endokarditis-Registers, ein Unterregister des Swiss TAVI Registry, sollen hier präsentiert werden.20
Studienpopulation und Definitionen
Zwischen 02/2011 und 07/2018 wurden insgesamt 7203 Patienten von 15 Spitälern ins Swiss TAVI Registry eingeschlossen. Dabei erfüllten Patienten die Definition einer IE, wenn diese nach Duke entweder als definitive IE oder aber als mögliche IE, die als IE behandelt wurde, klassifiziert wurde.21 Die Einteilung erfolgte nach dem Zeitpunkt des Auftretens in periprozedurale (<100 Tage nach TAVI), verzögerte (≥100 Tage, aber <12 Monate nach TAVI) und späte IE (≥12 Monate nach TAVI). Die periprozedurale und verzögerte IE wurden als frühe IE zusammengefasst.
Resultate
Insgesamt erlitten 149 Patienten (5,8%) eine TAVI-assoziierte IE. Patienten mit einer IE hatten ein durchschnittliches Alter von 80,1 Jahren (±8,0) und 31,5% waren Frauen. Diese Charakteristika unterschieden sich signifikant von denjenigen der Patienten ohne IE (n=7054), die ein durchschnittliches Alter von 82,0 Jahren (±6,4) aufwiesen und in 50,1% weiblich waren. Keine signifikanten Unterschiede fanden sich in den Prävalenzen der folgenden Komorbiditäten und Parameter: Diabetes mellitus 29,5%, Dyslipidämie 54,4%, arterielle Hypertonie 83,9%, koronare Herzkrankheit 55,0%, vorgängige Herzoperation 14,8%, COPD 13,4%, periphere arterielle Verschlusskrankheit 15,4% und zerebrovaskuläre Verschlusskrankheit 12,1%. Die durchschnittliche linksventrikuläre Auswurffraktion betrug 53,8% (±15,5) und das perioperative Risiko wurde mit einem durchschnittlichen STS PROM («Society of Thoracic Surgeons Predicted Risk of Mortality») von 5,0 (±3,9) angegeben.
Inzidenz der IE nach TAVI
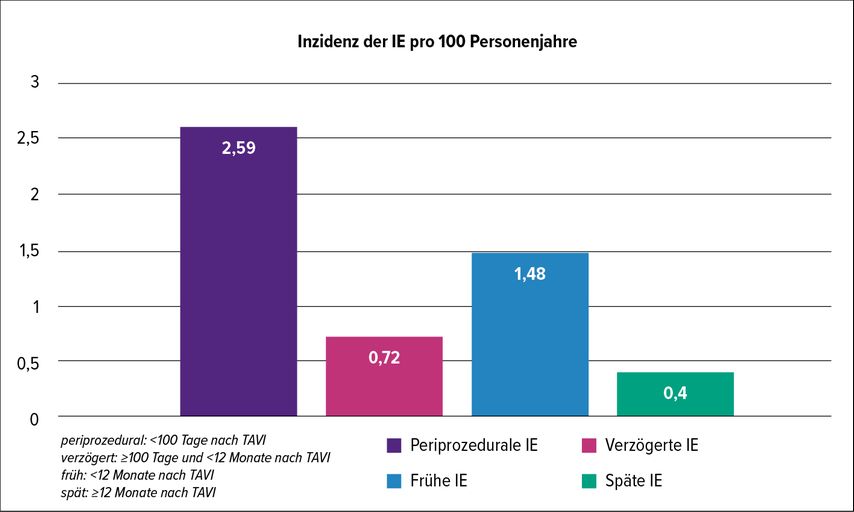
Die Inzidenz der IE betrug über den Beobachtungszeitraum von fünf Jahren 1,0/100Personenjahre (95% CI: 0,85–1,17). Interessant war die Beobachtung, dass bei der periprozeduralen IE die Inzidenz besonders hoch war mit 2,59/100Personenjahre (95% CI: 1,95–3,44). Die verzögerte IE wies eine Inzidenz von 0,72/100Personenjahre (95% CI: 0,54–0,97) auf und die späte IE eine von 0,40/100Personenjahre (95% CI: 0,31–0,53) (Abb. 1).
Abb. 1: Inzidenz der infektiösen Endokarditis (IE) pro 100 Personenjahre unterteilt nach dem Zeitpunkt des Auftretens nach TAVI
Endokarditis-spezifische Charakteristika
Insgesamt erfüllten 94 Patienten (63,1%) die Kriterien einer definitiven IE gemäss Duke. Bei praktisch allen Patienten (n=148, 99,3%) lagen positive Blutkulturen vor. Die echokardiografischen Befunde wurden in 47,7% als nicht konklusiv oder normal beurteilt, 36,2% wiesen Vegetationen auf, 9,4% eine lokale Abszessbildung und 8,7% eine neu aufgetretene Klappeninsuffizienz.
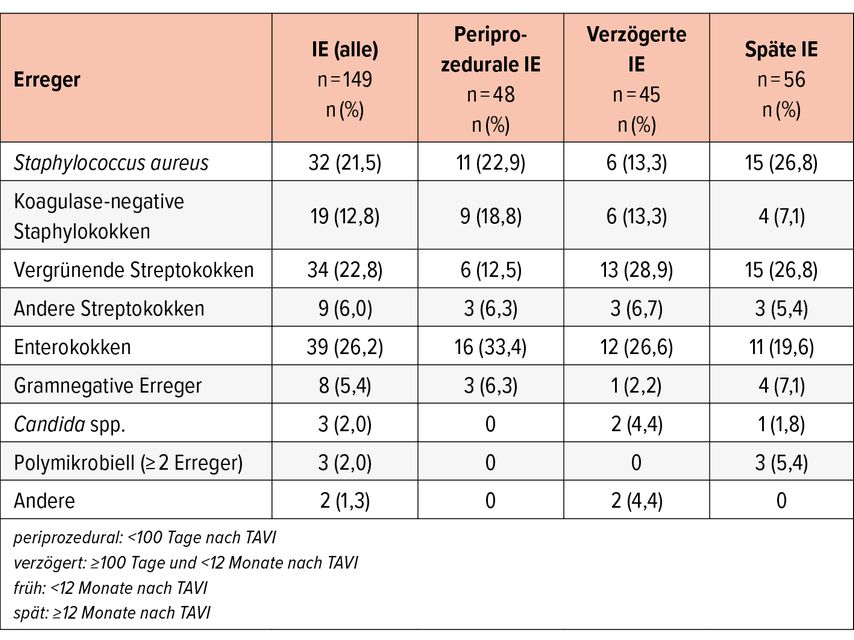
Die mikrobiologischen Befunde sind in Tabelle 2 zusammengefasst. Insgesamt waren Enterokokken (26,2%) dominant, gefolgt von vergrünenden Streptokokken (22,8%) und Staphylococcus aureus (21,5%). Interessant ist die Verteilung der Mikroorganismen je nach Zeitpunkt des Auftretens der IE nach TAVI, wonach Enterokokken vor allem bei der frühen IE dominierten (30,1%), vergrünende Streptokokken und S. aureus bei der späten IE (je 26,8%).
Tab. 2: Erregerspektrum der infektiösen Endokarditis (IE) unterteilt nach dem Zeitpunkt des Auftretens nach TAVI
Verglichen mit Patienten ohne IE wurde die TAVI bei Patienten mit einer IE häufiger im Katheterlabor als im Hybridoperationssaal eingelegt (55,7% vs. 42,8%; p=0,024). Ausserdem erhielten Patienten mit einer IE häufiger eine mechanisch expandierbare Klappe (13,3% vs. 4,2%; p<0,001) und wurden seltener mittels Ballon-Valvuloplastie prädilatiert (57% vs. 63,5%; p=0,003).
In der multivariablen Analyse konnten verschiedene Risikofaktoren für eine IE nach TAVI identifiziert werden. Bei den Patientencharakteristika waren dies das jüngere Alter (HR: 0,97; 95% CI: 0,94–0,99) und das männliche Geschlecht (HR: 1,99; 95% CI: 1,40–2,82), bei den periprozeduralen Faktoren das Durchführen der Intervention im Katheterlabor und nicht im Hybridoperationssaal (HR: 1,65; 95% CI: 1,19–2,29) und die fehlende Prädilatation mittels Ballon-Valvuloplastie (HR: 1,49; 95% CI: 1,07–2,07).
Bemerkenswert ist auch die Tatsache, dass 47,9% der Patienten mit einer periprozeduralen IE eine inadäquate Antibiotikaprophylaxe bei der TAVI Prozedur erhalten haben, welche in der Mehrheit aus einem Cephalosporin der ersten oder zweiten Generation bestand.
Outcome
Bei der Outcome-Analyse hinsichtlich Mortalität und Schlaganfall wurde ein «case-control matching» angewendet und 148 IE-Patienten wurden mit 579 gematchten Kontrollen ohne IE verglichen. Das 1:4-Matching berücksichtigte die Zeit bis zur IE-Diagnose nach TAVI und erfolgte nach Alter, Geschlecht, Jahr der TAVI Prozedur und dem STS PROM. Für alle IE-Patienten zusammengenommen betrug die HR für Mortalität 6,55 (95% CI: 4,44–9,67) und diejenige für Schlaganfall 4,03 (95% CI: 1,54–10,52). Getrennt nach dem Zeitpunkt des Auftretens der IE nach TAVI wiesen die IE-Patienten in allen Kategorien eine höhere Mortalität auf mit einer HR von 7,19 (periprozedurale IE), 5,05 (verzögerte IE) und 7,34 (späte IE), allerdings wiesen nur Patienten mit einer späten IE ein signifikant höheres Risiko für einen Schlaganfall auf (HR: 11,92; 95% CI: 2,76–51,53).
Diskussion
Insgesamt liegt die Inzidenz der TAVI-assoziierten IE in der Schweiz bei 1,0/100Personenjahre und damit im Bereich der in der Literatur beschriebenen Inzidenzen.6 Besonders hoch war die Inzidenz in der periprozeduralen Phase (<100 Tage nach TAVI), wobei bei diesen Patienten Enterokokken die häufigsten Erreger waren. Bemerkenswerterweise erhielt knapp die Hälfte der Patienten mit einer periprozeduralen IE eine inadäquate Antibiotikaprophylaxe bei der TAVI Prozedur. Dies sicherlich auch deshalb, weil zum Studienzeitpunkt die empfohlene Prophylaxe aus einem Cephalosporin der ersten oder zweiten Generation bestand, welche beide eine Lücke bei den Enterokokken aufweisen. Hier sollten nun die oben beschriebenen Empfehlungen zu infektionspräventiven Aspekten bei TAVI eine Optimierung bringen, vor allem die Empfehlung einer Enterokokken-aktiven periinterventionellen Antibiotikaprophylaxe mit Amoxicillin/Clavulansäure (Tab. 1).18 Auch die hohe Rate an vergrünenden Streptokokken (insgesamt 22,8%, bei der späten IE 26,8%) spricht für ein Verbesserungspotenzial in der Prophylaxe, insofern als Patienten mit einer TAVI, so wie auch Patienten mit einem chirurgischen AKE, vor und nach der Klappeneinlage regelmässig dentalhygienisch und bei Bedarf zahnärztlich behandelt werden sollten. Patienten mit einer TAVI müssen im Besitz eines Endokarditisausweises sein, damit der Bedarf einer Antibiotikaprophylaxe vor definierten Eingriffen klar ersichtlich ist.
Abb. 2: Bei der infektiösen Endokarditis nach TAVI finden sich am häufigsten Enterokokken, gefolgt von vergrünenden Streptokokken und Staphylococcus aureus
Risikofaktoren für die Entwickung einer IE nach TAVI sind die aus der Literatur bekannten Faktoren wie das jüngere Alter und das männliche Geschlecht.6 Dass das Durchführen der Intervention im Katheterlabor und nicht im Hybridoperationssaal mit einem erhöhten IE-Risiko assoziiert ist, ist allerdings neu. Auch hier können Hygieneaspekte erklärend herangezogen werden, die möglicherweise im Hybridoperationssaal besser definiert sind und strikter eingehalten werden – nicht zuletzt deshalb, weil das Personal regelmässig geschult wird. So könnte der Umgang mit chirurgischen Desinfektionsstandards besser sein, der Personenverkehr geringer und das Wissen um die Notwendigkeit einer absoluten Asepsis beim Umgang mit Implantaten vertrauter. Allerdings sind dies Spekulationen, die in einer prospektiven Studie sauber evaluiert werden müssten, bevor die TAVI Prozedur in einem Katheterlabor als definitiver Risikofaktor angesehen werden kann.
Nicht nur die Morbidität von Patienten mit einer IE nach TAVI ist beträchtlich, sondern auch die Mortalität. Letztere ist eine der höchsten überhaupt und liegt im Spital bei 30–40%, was sicherlich auch mit der in aller Regel polymorbiden Patientenpopulation hohen Alters erklärt werden kann.6 In der aktuellen Analyse bestand ein fast siebenfach erhöhtes Sterberisiko für Patienten mit einer IE, wobei das erhöhte Risiko über alle definierten Zeitintervalle nach TAVI (periprozedural, verzögert, spät) gegeben war. Das vierfach erhöhte Risiko für einen Schlaganfall war vor allem bei Patienten mit einer späten IE nach TAVI vorhanden, was mit der höheren Rate an S. aureus-Infektionen erklärt werden könnte.
Aufgrund des schlechten Outcomes im Falle einer TAVI-assoziierten IE kommt optimierten peri- und postinterventionellen Hygiene- und Präventionsmassnahmen eine enorme Bedeutung zu.
Literatur:
1 Leon MB et al.: Transcatheter or surgical aortic valve replacement in intermediate-risk patients. N Engl J Med 2016; 374: 1609-20 2 Mack MJ et al.: Transcatheter aortic valve replacement with a balloon-expandable valve in low-risk patients. N Engl J Med 2019; 380: 1695-705 3 Mack MJ et al.: 5-year outcomes of transcatheter aortic valve replacement or surgical aortic valve replacement for high surgical risk patients with aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet 2015; 385: 2477-84 4 Heredia-Rodriguez M et al.: Evolution of the incidence, mortality, and cost of infective endocarditis in Spain between 1997 and 2014. J Gen Intern Med 2018; 33: 1610-3 5 Carnero-Alcazar M et al.: Transapical aortic valve prosthetic endocarditis. Interact Cardiovasc Thorac Surg 2010; 11: 252-3 6 Regueiro A et al.: Association between transcatheter aortic valve replacement and subsequent infective endocarditis and in-hospital death. JAMA 2016; 316: 1083-92 7 Kolte D et al.: Comparison of incidence, predictors, and outcomes of early infective endocarditis after transcatheter aortic valve implantation versus surgical aortic valve replacement in the United States. Am J Cardiol 2018; 122: 2112-9 8 Moriyama N et al.: Prosthetic valve endocarditis after transcatheter or surgical aortic valve replacement with a bioprosthesis: results from the FinnValve Registry. EuroIntervention 2019; 15: e500-7 9 Butt JH et al.: Long-term risk of infective endocarditis after transcatheter aortic valve replacement. J Am Coll Cardiol 2019; 73: 1646-55 10 Regueiro A et al.: Infective endocarditis following transcatheter aortic valve replacement: comparison of balloon- versus self-expandable valves. Circ Cardiovasc Interv 2019; 12: e007938 11 Amat-Santos IJ et al.: Infective endocarditis after transcatheter aortic valve implantation: results from a large multicenter registry. Circulation 2015; 131: 1566-74 12 Slipczuk L et al.: Infective endocarditis epidemiology over five decades: a systematic review. PLoS One 2013; 8: 1-17 13 Mangner N et al.: Cardiac surgery compared with antibiotics only in patients developing infective endocarditis after transcatheter aortic valve replacement. J Am Heart Assoc 2018; 7: e010027 14 Oliver L et al.: Infective endocarditis in octogenarians. Heart 2017; 103: 1602-9 15 Allegranzi B et al.: New WHO recommendations on intraoperative and postoperative measures for surgical site infection prevention: an evidence-based global perspective. Lancet Infect Dis 2016; 16: e288-303 16 WHO: Global guidelines on the prevention of surgical site infection. Geneva: World Health Organisation, 2016. Accessed 15.5.2019 17 Habib G et al.: 2015 ESC Guidelines for the management of infective endocarditis: the Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by: European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). Eur Heart J 2015; 36: 3075-128 18 Conen A et al.: A review of recommendations for infective endocarditis prevention in patients undergoing transcatheter aortic valve implantation. EuroIntervention 2020; 16: 1135-40 19 Lalani T et al.: In-hospital and 1-year mortality in patients undergoing early surgery for prosthetic valve endocarditis. JAMA Intern Med 2013; 173: 1495-504 20 Stortecky S et al.: Infective endocarditis after transcatheter aortic valve replacement. J Am Coll Cardiol 2020; 75: 3020-30 21 Li JS et al.: Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000; 30: 633-8
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...