Aktuelle Entwicklungen in der Kardio-Onkologie nach neuen ESC-Leitlinien
Autorinnen:
Dr. Christina Kronberger
Ao. Univ.-Prof. Dr. Jutta Bergler-Klein, FESC, FHFA, FEACVI & Board Member des ESC Council of Cardio-Oncology
Universitätsklinik für Innere Medizin II, Abteilung für Kardiologie, Kardio-Onkologie-Ambulanz,Medizinische Universität Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Integration von Kardiologie in die Onkologie hat in den letzten Jahren an Bedeutung gewonnen. Krebs und Herz-Kreislauf-Erkrankungen gehören zu den führenden Todesursachen weltweit und Mediziner werden durch die Komorbiditäten beider Erkrankungen vor große Herausforderungen gestellt. Die Leitlinien zielen u.a. darauf ab, das kardiovaskuläre Basisrisiko zu definieren und krebstherapiebedingte kardiovaskuläre Toxizitäten (CTR-CVT) zu minimieren. Sie stellen Behandlungsrichtlinien für CTR-CVT bereit, um die Fortsetzung der Krebstherapie zu gewährleisten und langfristig das kardiovaskuläre Risiko nach der Krebstherapie zu überwachen.
Keypoints
-
Die Leitlinien sehen vor, dass initial immer eine individuelle Bewertung des kardiovaskulären Risikos von Patienten erfolgen sollte.
-
Regelmäßige kardiologische Screenings vor, während und nach der Krebstherapie tragen zu einer erhöhten Sicherheit bei und verringern Herzschäden.
-
Eine enge interdisziplinäre Kooperation ermöglicht individuell angepasste Therapien sowohl fürkardiovaskuläre als auch onkologische Bedürfnisse.
-
Auf die Nachsorge von Krebsüberlebenden sollte der Fokus gelegt werden, um Spätschäden frühzeitig zu behandeln.
Die Empfehlungen der kardio-onkologischen Leitlinien basieren auf einem fünfstufigen Ansatz, der mit einer Grundrisikobewertung beginnt, gefolgt von der Überwachung während der Krebstherapie und dem Management von kardiovaskulären Komplikationen während der Therapie.1 Ein zentraler Aspekt ist die Risikostratifizierung am Ende der Krebstherapie, auf die langfristige Strategien für Überlebende folgen. Jede Phase wird individuell auf die Bedürfnisse des Patienten abgestimmt, um eine optimale Versorgung und Überwachung zu gewährleisten. Dieser 5-stufige Ansatz setzt sich aus folgenden Keypoints zusammen:
Initial personalisierte Risikoeinschätzung
Eine klinische Untersuchung, EKG, Echokardiografie (bei hohem und sehr hohem Risiko) und Biomarker wie NT-proBNP und Troponin gehören zur initialen Einschätzung des kardiovaskulären Risikos. Spezifische Tools wie der HFA-ICOS-Score unterstützen die Risikoabschätzung. So können Patienten mit erhöhtem kardiovaskulärem Risiko präzise identifiziert und frühzeitig kardioprotektive Maßnahmen ergriffen werden.
Prävention und Früherkennung kardiovaskulärer Risiken
Die Einführung regelmäßiger kardiologischer Screenings vor, während und nach der Krebstherapie haben den Versorgungsstandard verbessert undhelfen, das Risiko von Herzschäden zu minimieren, sodass die Krebstherapie sicher fortgeführt werden kann.
Multidisziplinäre Zusammenarbeit
Ein zentraler Fortschritt durch die neuen ESC-Leitlinien ist die engere Zusammenarbeit zwischen Kardiologen, Onkologen und anderen Fachbereichen. Diese Kooperation ermöglicht individuell angepasste Therapieansätze, die sowohl kardiovaskuläre als auch onkologische Bedürfnisse berücksichtigen. Aus Wien war Ao. Univ.-Prof. Dr. Bergler-Klein Mitautorin der aktuellen ESC-Leitlinien.1
Prävention und Früherkennung Krebstherapie-bedingter kardiovaskulärer Toxizitäten (CTR-CVT)
Regelmäßige kardiologische Untersuchungen während der Krebstherapie sind entscheidend. ACE-Hemmer, Betablocker und Statine werden für Risikopatienten empfohlen, um Herzschäden vorzubeugen, insbesondere bei Therapien mit Anthrazyklinen und Anti-HER2-Antikörpern.
Langfristige Überwachung für Krebsüberlebende
Die Leitlinien legen großen Wert auf die Nachsorge bei Krebsüberlebenden. Regelmäßige Kontrollen helfen, Herzinsuffizienz oder andere Spätfolgen frühzeitig zu erkennen und zu behandeln.
Wichtige Veränderungen in neuen ESC-Leitlinien
Vor Therapiebeginn: grundlegende Bewertung des kardiovaskulären Risikos
Die Leitlinie betont die Wichtigkeit einer umfassenden Bewertung des kardiovaskulären Risikos vor Beginn der Krebstherapie (Klasse-1B-Empfehlung). Diese Risikobewertung umfasst eine gründliche kardiologische Untersuchung, ein Ruhe-Elektrokardiogramm (EKG) bei allen Patienten (einschließlich der Messung des QT-Intervalls mit Fridericia-Korrektur), eine transthorakale Echokardiografie bei Patienten mit hohem oder sehr hohem Risiko für CTR-CVT und die Bestimmung von kardialen Biomarkern, wie NT-proBNP und kardialem Troponin. Risikofaktoren wie Hypertonie, Diabetes mellitus, Dyslipidämie und bestehende Herzerkrankungen müssen ebenfalls erfasst werden. Zur Unterstützung dieser Risikobewertung werden verschiedene Risikobewertungstools empfohlen, darunter der von der Heart Failure Association (HFA) und der International Cardio-Oncology Society (ICOS) entwickelte HFA-ICOS-Score. Er ist ein Instrument, das speziell zur Abschätzung des Risikos einer krebstherapiebedingten kardiovaskulären Toxizität (CTR-CVT) entwickelt wurde. Eine Studie aus dem CARDIOTOX-Register hat die Fähigkeit des HFA-ICOS-Scores bestätigt, das Risiko einer durch Anthrazykline verursachten Kardiotoxizität erfolgreich vorherzusagen.2 Diese Validierung unterstreicht die praktische Anwendbarkeit des Scores zur Verbesserung der Risikostratifikation und Überwachung von Patienten, die sich einer potenziell kardiotoxischen Krebstherapie unterziehen werden. Je nach Krebstherapie werden die Variablen im HFA-ICOS-Score unterschiedlich gewichtet, wodurch das Risiko in Kategorien von gering bis sehr hoch eingeteilt wird. Diese Kategorien stellen die Grundlage für die weitere Betreuung dar.
Nach der Risikostratifikation empfiehlt die Leitlinie, Patienten mit hohem oder sehr hohem Risiko für kardiovaskuläre Toxizität oder bestehende kardiovaskuläre Erkrankungen an spezialisierte Kardiologen mit kardio-onkologischer Expertise zu überweisen. Diese enge Zusammenarbeit zwischen Onkologen und Kardiologen, die bisher eher selten ist, wird durch die neuen Leitlinien immer häufiger zur Norm und ist von entscheidender Bedeutung, um die kardiovaskuläre Sicherheit der fortlaufenden Krebstherapie zu gewährleisten. Die Leitlinien geben dafür folgende echokardiografische Empfehlungen:
Besonders empfohlen wird die Messung der linksventrikulären Ejektionsfraktion (LVEF) und des „global longitudinal strain“ (GLS) als sensitiver Parameter zur frühzeitigen Erkennung subklinischer kardialer Schäden bei Patienten mit hohem und sehr hohem Risiko. Die Messung der dreidimensionalen LVEF wäre die ideale Methode, ist jedoch aufgrund begrenzter Verfügbarkeit nicht immer realisierbar.
In Fällen, in denen die transthorakale Echokardiografie keine ausreichenden Informationen liefert, empfiehlt die Leitlinie den Einsatz der kardialen Magnetresonanztomografie, die eine Klasse-IIa-Empfehlung erhalten hat. Weitere empfohlene Basisuntersuchungen umfassen das Lipidprofil, die Nüchternglukose oder den HbA1c sowie die Beurteilung der Nierenfunktion.
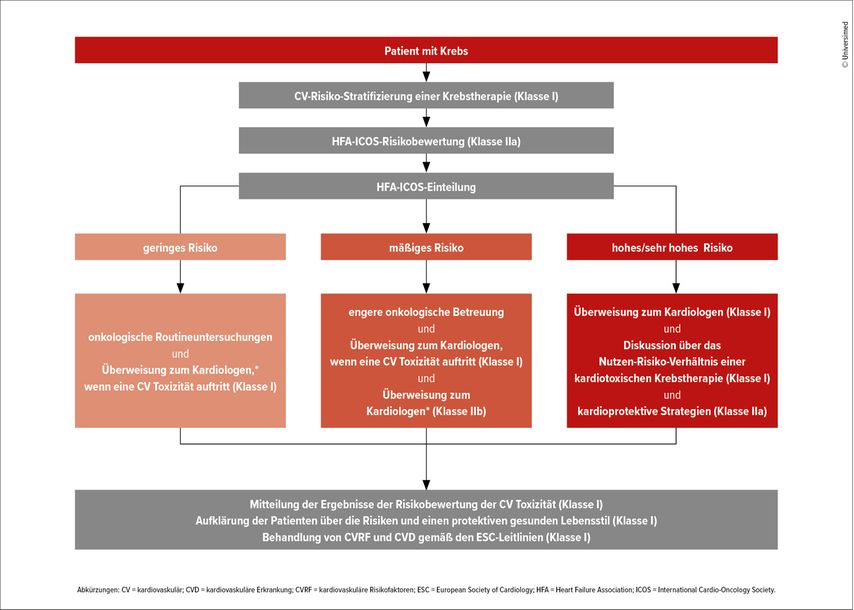
Die wichtigsten Empfehlungen der ESC-Leitlinien für die Bewertung des kardiovaskulären Risikos von Krebspatienten sowie die empfohlenen Maßnahmen werden in einem grafischen Algorithmus zusammengefasst (Abb. 1).3
Abb. 1: Übersicht über die ESC-Empfehlungen zur Bewertung des kardiovaskulären Risikos bei Krebspatienten (nach der Deutschen Gesellschaft für Kardiologie, Herz- und Kreislaufforschung e. V. 2023)3
Prävention von kardiovaskulärer Toxizität
Die ESC-Leitlinien betonen die Wichtigkeit einer regelmäßigen kardiologischen Überwachung vor, während und nach der Krebstherapie. Eine gründliche Risikostratifizierung sowie eine kurz- und langfristige Nachsorge sind essenziell, um Patienten zu identifizieren, die ein Risiko für CTR-CVT haben oder bereits darunter leiden. Der Begriff CTR-CVT umfasst unter anderem eine ventrikuläre Dysfunktion (krebstherapieinduzierte kardiale Dysfunktion; CTRCD), vaskuläre Toxizität, Myokarditis, Bluthochdruck und verlängerte QT-Intervalle.
Die Primärprävention von CTR-CVT zielt darauf ab, die Entwicklung von therapiebedingten kardiovaskulären Schäden bei Patienten ohne kardiovaskuläre Erkrankungen zu vermeiden oder zu minimieren.
Kardioprotektive Maßnahmen zur Prävention oder Behandlung von CTR-CVT hängen von der spezifischen Krebstherapie ab. Dazu kann die Reduzierung der Dosis oder der Exposition gegenüber potenziell kardiotoxischen Substanzen gehören. Idealerweise sollten solche Entscheidungen in einem multidisziplinären Team mit Onkologen, Hämatologen und Kardiologen getroffen werden. Eine Abwägung des Nutzen-Risiko-Verhältnisses der Krebstherapie mit der Schwere und den Auswirkungen der CTR-CVT ist erforderlich.
Für die primäre Prävention empfehlen die Leitlinien, potenziell kardiotoxische Medikamente, soweit dies möglich ist, zu minimieren. Da jedoch viele dieser Medikamente, wie Anthrazykline und Therapien gegen den humanen epidermalen Wachstumsfaktor-Rezeptor 2 (HER2), etwa Trastuzumab, für die Krebstherapie unerlässlich sind, werden zusätzliche Schutzmaßnahmen empfohlen, um das Risiko einer Herzinsuffizienz oder anderer kardiovaskulärer Schäden zu verringern. Folgende Maßnahmen werden empfohlen:
Angiotensin-Converting-Enzym-Hemmer (ACE-Hemmer) oder Angiotensinrezeptorblocker (ARB) sowie Betablocker (insbesondere Carvedilol, sofern keine Kontraindikation besteht, bzw. alternativ Bisoprolol, Metoprolol-Succinat oder Nebivolol werden bei Patienten mit hohem oder sehr hohem Risiko empfohlen (Empfehlung IIa B für Anthrazyklinbehandlungen oder Therapien gegen HER2; Empfehlung IIa C für andere kardiotoxische Therapien mit Herzinsuffizienzrisiko). Statine werden bei Patienten mit hohem oder sehr hohem kardiovaskulärem Risiko ebenfalls empfohlen (Klasse-IIa-Empfehlung).
Zusätzliche Strategien zur primären Prävention beinhalten den Einsatz von Dexrazoxan oder liposomalen Anthrazyklinen, sofern Patienten Anthrazykline erhalten haben und ein hohes oder sehr hohes Risiko einer CTR-CVT haben (beides Klasse-IIa-Empfehlungen).
Behandlung von kardiovaskulärer Toxizität
Die Sekundärprävention bezieht sich auf Interventionen bei Patienten mit vorbestehenden kardiovaskulären Erkrankungen, einschließlich früherer CTR-CVT, und neu auftretender CTR-CVT während einer Krebstherapie.
Die ESC-Leitlinien weisen darauf hin, dass insbesondere die regelmäßige Kontrolle kardialer Biomarker sowie die transthorakale Echokardiografie eine zentrale Rolle bei der Verlaufsbeurteilung spielen.
Die Leitlinien geben hier individuell ausgearbeitete Überwachungsprotokolle zur Frequenz von kardialen Biomarkern und transthorakaler Echokardiografie für wichtige kardioonkologische Therapien vor.
Unter Anthrazyklin-Chemotherapie bei Patienten mit hohem oder sehr hohem Risiko für CTR-CVT wird eine transthorakale Echokardiografie alle zwei Chemotherapiezyklen (alle 6 bis 8 Wochen) empfohlen. Zusätzlich sollten kardiale Biomarker bei jedem Chemotherapiezyklus (alle 3 bis 4 Wochen) bestimmt werden (beides Klasse- I-Empfehlungen).
Unter Anti-HER2-Therapie bei Patienten mit hohem oder sehr hohem Risiko für CTR-CVT sollte alle drei Monate eine transthorakale Echokardiografie erfolgen (Klasse-I-Empfehlung). Die regelmäßige Überwachung der kardialen Biomarker wird ebenfalls empfohlen (Klasse-IIa-Empfehlung).
Management kardiovaskulärer Toxizität
Die Therapie von CTR-CVT aufgrund von Anthrazyklinen und HER2-gerichteten Therapien richtet sich nach Schweregrad und Symptomatik der Patienten, wobei die individuelle klinische Situation berücksichtigt wird. Die Leitlinien geben spezifische Empfehlungen für verschiedene Symptome und Schweregrade der Toxizität vor.
Bei asymptomatischen Patienten mit moderater CTRCD unter HER2-gerichteter Therapie empfehlen die Leitlinien die Fortsetzung der HER2-gerichteten Therapie mit engmaschiger kardiologischer Überwachung. Dies kann vielen Patienten eine unnötige Unterbrechung ihrer wirksamen Krebstherapie ersparen.
Für asymptomatische Patienten mit milden CTRCD unter Anthrazyklin-Therapie wird die Gabe von ACE-Hemmern, ARBs und/oder Betablockern empfohlen (Klasse-IIa- oder -IIb-Empfehlung, abhängig vom Einzelfall).
Bei asymptomatischen Patienten mit mäßiger oder höhergradiger CTRCD soll eine multidisziplinäre Beratung erfolgen, die beispielsweise die Onkologie und Kardiologie zur gemeinsamen Einschätzung des Therapieerhalts oder -abbruchs einbezieht. Parallel ist eine Herzinsuffizienztherapie zu beginnen (Klasse-I-Empfehlung).
Je nach Schwere der CTRCD (ab mäßiger Form) sollte die Anthrazyklintherapie vorübergehend unterbrochen oder ganz gestoppt werden (Klasse-I-Empfehlung). Hierbei ist es wichtig, interdisziplinär die individuelle Situation und Prognose der Patienten zu berücksichtigen.
Die Leitlinien bieten zudem detaillierte Empfehlungen zur Behandlung von Toxizitäten durch Immuncheckpoint-Inhibitoren, Inhibitoren des vaskulären endothelialen Wachstumsfaktors (=VEGF-Inhibitoren), chimäre Antigenrezeptor-T-Zellen und hämatopoetische Stammzelltherapien. Ein ausführlicher Algorithmus zum Management und zur Therapie von Myokarditis unter Immuncheckpoint-Inhibitoren wird ebenfalls angeführt.
Andere therapieassoziierte kardio-vaskuläre Risiken erkennen und überwachen
Die Leitlinien enthalten auch detaillierte Empfehlungen zur Erkennung und Überwachung anderer kardiovaskulärer Risiken. Darunter befinden sich die koronare Herzkrankheit z.B. durch Fluoropyrimidine oder VEGF-Inhibitoren, Bluthochdruck z.B. durch VEGF-Inhibitoren oder Tyrosinkinasehemmer und die QTc-Verlängerung z.B. durch VEGF-Inhibitoren sowie Tyrosinkinasehemmer wie Nilotinib und Dasatinib. Das Risiko für Vorhofflimmern wird im Zusammenhang mit Ibrutinib, einem Bruton-Tyrosinkinasehemmer, angeführt.
Bewertung des kardiovaskulären Risikos am Ende der Krebstherapie
Am Ende der Krebstherapie ist eine Risikobewertung entscheidend, um Patienten mit einem erhöhten Risiko zu identifizieren, die langfristig kardiovaskulär überwacht werden sollten. Hierbei werden folgende Kriterien herangezogen:
-
Ein hohes oder sehr hohes Ausgangsrisiko basierend auf der HFA-ICOS-Risikobewertung.
-
Eine kardiotoxische Krebstherapie mit bekanntem hohem Risiko für langfristige kardiovaskuläre Schäden.
-
Mäßige bis hochgradige CTR-CVT während der Krebsbehandlung.
-
Neu aufgetretene kardiale Dysfunktion, festgestellt 3 bis 12 Monate nach Therapieabschluss (z.B. Veränderungen in der transthorakalen Echokardiografie, neu erhöhte kardiale Biomarker oder neue kardiovaskuläre Symptome).
Die initiale Risikobewertung sollte innerhalb des ersten Jahres nach der Behandlung erfolgen. Im Anschluss daran folgt eine kontinuierliche Überwachung der Risikofaktoren gemäß den ESC-Leitlinien zur Prävention kardiovaskulärer Erkrankungen in der klinischen Praxis aus 2021.
Langzeitüberwachung des kardiovaskulären Risikos nach erfolgter Krebstherapie
Die Langzeitüberwachung basiert auf einer Risikostratifizierung, die die kumulative Anthrazyklindosis und die mittlere Herzdosis der Strahlentherapie berücksichtigt. Wichtige Maßnahmen umfassen: eine jährliche kardiovaskuläre Risikobewertung, die sofortige Überweisung an einen Kardiologen bei neu auftretenden kardiovaskulären Symptomen, eine erneute umfassende Beurteilung des kardiovaskulären Risikos nach fünf Jahren, eine gezielte Patientenaufklärung sowie die konsequente Optimierung von kardiovaskulären Risikofaktoren.
Fazit
Praxistipp
Der HFA-ICOS-Score, der als interaktives Tool in der „ESC Pocket Guidelines App“ verfügbar ist, steht unter https://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Guidelines-derivative-products/ESC-Mobile- Pocket-Guidelines zur Verfügung.Die Fortschritte in der Kardioonkologie und die ESC-Leitlinien haben wesentliche Verbesserungen in der Betreuung von Krebspatienten mit kardiovaskulären Risiken gebracht. Durch die Förderung einer multidisziplinären Zusammenarbeit und einer proaktiven Überwachung kann die kardiovaskuläre Gesundheit von Krebspatienten besser geschützt und ihre Lebensqualität verbessert werden. Da viele Empfehlungen jedoch auf Expertenmeinungen und kleineren Studien basieren, ist zusätzliche Forschung notwendig, um evidenzbasierte Standards für diesen wachsenden Bereich zu schaffen. Von 20. bis 21. Juni 2025 findet hierzu der erste ESC-Kongress für Kardio-Onkologie statt.
Literatur:
1 Lyon AR, Bergler-Klein J et al.: 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS). Eur Heart J 2022; 43(41): 4229-361 2 Rivero-Santana B et al.: Anthracycline-induced cardiovascular toxicity: validation of the Heart Failure Association and International Cardio-Oncology Society risk score. Eur Heart J 2024; doi: 10.1093/eurheartj/ehae496 3 Deutsche Gesellschaft für Kardiologie – Herz- und Kreislaufforschung e. V.: ESC pocket guidelines. Kardio-Onkologie. Grünwald: Börm Bruckmeier Verlag 2022
weiterführende Literatur:
● Kronberger C, Bergler-Klein J et al.: Characteristics and outcomes of patients with a history of cancer enrolled in our prospective HFpEF registry. Eur Heart J 2024; 45(1): doi: 10.1093/eurheartj/ehae666.797 ● van der Meer P et al.: Guidelines in practice: chest pain and dyspnoea in a patient actively treated for cancer. präsentiert am ESC-Kongress am 31.8.2024 ● Banerjee S et al.: Cardiovascular disease management in patients with cancer. Präsentiert am ESC-Kongress am 31.8.2024
weiterführende Links:
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...