Ajustements posologiques pratiques pendant la grossesse et l’allaitement
Auteures:
Andrea Burch, MSc1,3
Verena Gotta, PhD2
1Schweizerische Akademie für Perinatale Pharmakologie (SAPP), Zürich
2Universitäts-Kinderspital beider Basel, UKBB
Pädiatrische Pharmakologie & Pharmakometrie
3Spitalapotheke Universitätsspital Zürich
E-mail: andrea.burch@usz.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Des changements pharmacocinétiques significatifs peuvent survenir pendant la grossesse ainsi que le post-partum. La procédure optimale en matière d’ajustement posologique n’a toutefois été étudiée cliniquement que pour quelques substances, ce qui est mis en lumière par des exemples. À l’avenir, les modèles informatiques pharmacométriques contribueront de plus en plus à formuler des recommandations posologiques sur la base d’études cliniques ou virtuelles peu invasives.
Keypoints
-
On observe souvent des concentrations plasmatiques de médicaments plus faibles chez les femmes enceintes que chez celles qui ne le sont pas, ce qui entraîne un risque de diminution de l’efficacité ou de la durée d’action.
-
Cela nécessite un suivi étroit et/ou, le cas échéant, un ajustement posologique, respectivement de l’intervalle entre les doses, pendant la grossesse (pour obtenir l’effet souhaité) ainsi que le post-partum (pour prévenir les effets indésirables liés à la dose).
-
L’enfant à naître ou allaité doit également être pris en compte dans l’évaluation du rapport bénéfice-risque lié à l’ajustement posologique.
-
Les modèles pharmacométriques permettent de faire des prédictions quantitatives sur les changements de cinétique ainsi que leur variabilité pendant la grossesse et l’allaitement, même si les données cliniques à ce sujet sont encore insuffisantes ou inexistantes.
Changements pharmacocinétiques pendant la grossesse et l’allaitement
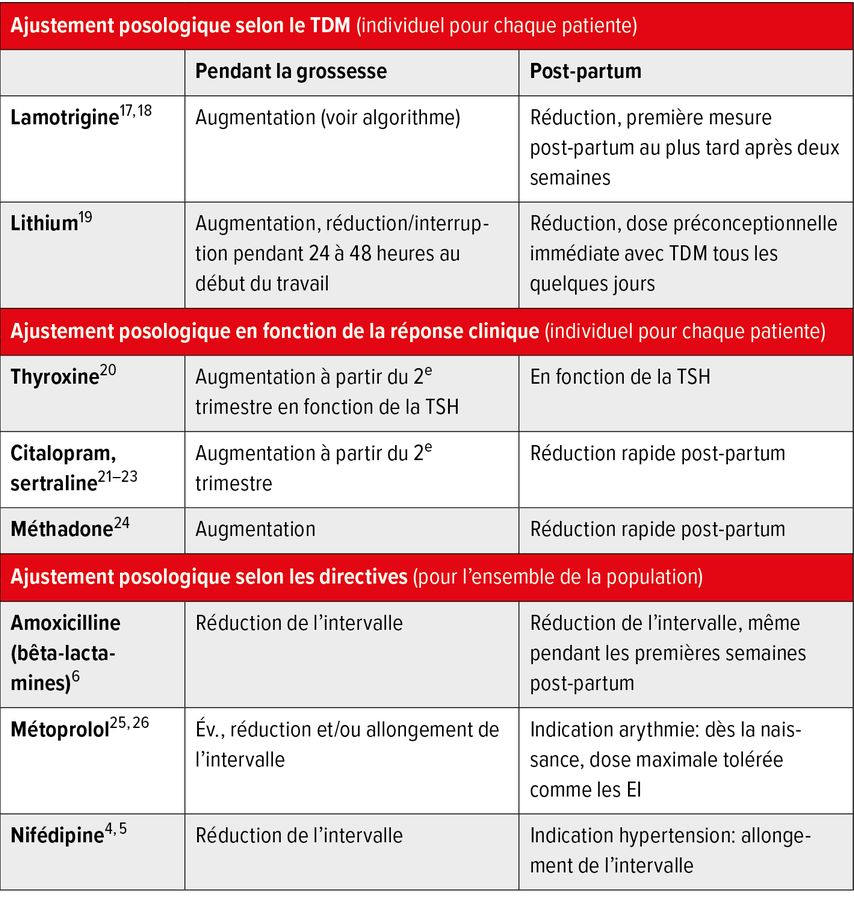
Des modifications physiologiques pendant la grossesse et le post-partum surviennent chez la mère, mais aussi chez l’enfant ou l’enfant à naître.1–3 Comme la question d’un ajustement posologique pendant et après la grossesse se pose, des exemples cliniques d’ajustement posologique chez la mère sont d’abord illustrés ci-dessous (Tab. 1), suivis d’une discussion sur l’évaluation du rapport bénéfice-risque et le développement de la recherche grâce à la pharmacométrie.
Tab. 1: Exemples d’ajustement posologique selon le «Therapeutic Drug Monitoring» (TDM), la réponse clinique ou les directives. TSH = thyréostimuline
Approches pour l’ajustement posologique chez la mère
Médicaments liés à la grossesse – exemple de la nifédipine
Si un traitement antihypertenseur par la nifédipine est indiqué pendant la grossesse, il faut savoir que la clairance augmente pendant la grossesse via le CYP3A4, ce qui s’accompagne d’un temps d’élimination plus court de la nifédipine.4,5 Cela peut entraîner une diminution de l’efficacité au cours de la journée. Il est possible d’y remédier en réduisant l’intervalle entre les doses. Les concentrations de médicaments plus constantes et les valeurs de tension artérielle plus stables ainsi obtenues sont également associées à une meilleure tolérance, en particulier lorsque les médicaments sont utilisés comme tocolytiques chez des femmes fondamentalement normotendues qui souffrent davantage de céphalées dues aux variations de tension artérielle associées à la nifédipine.
Médicaments non liés à la grossesse – exemple de la pénicilline G ou des bêta-lactamines
Les antibiotiques bêta-lactames atteignent leur efficacité maximale lorsque les concentrations plasmatiques sont aussi constantes que possible et supérieures à la concentration minimale inhibitrice (CMI) de l’agent pathogène à éradiquer. En raison de l’augmentation du volume de distribution et de la clairance rénale des pénicillines pendant la grossesse, la pénicilline G doit être administrée à un intervalle plus court pour le traitement des femmes enceintes porteuses du streptocoque B, afin d’obtenir des taux d’action efficaces.6,7
Traitement préexistant chez la mère – exemple de la lamotrigine
Il a été démontré que les concentrations plasmatiques de l’antiépileptique lamotrigine diminuent au cours des deuxième et troisième trimestres en cas de dose constante.8 Ceci est pertinent dans la mesure où une baisse des concentrations de plus de 35% est un facteur prédictif d’une fréquence accrue des crises.9 En revanche, les concentrations plasmatiques augmentent pendant le post-partum. Cela peut entraîner des symptômes de surdosage en l’absence d’un ajustement posologique. Il est donc recommandé d’ajuster la posologie en fonction de chaque patiente, conformément à la mesure de la concentration plasmatique («Therapeutic Drug Monitoring», TDM).
Traitement de la mère pertinent pour l’enfant à naître – exemple du traitement antirétroviral
Ces dernières années, plusieurs études ont décrit une réduction de l’exposition aux médicaments dans le plasma chez les femmes enceintes sous traitement antirétroviral par darunavir, elvitégravir et le booster cobicistat, en particulier au cours des deuxième et troisième trimestres.10,11 Cela s’explique par une augmentation du métabolisme hépatique via les cytochromes P450. L’exposition réduite augmente théoriquement le risque d’échec thérapeutique chez la mère, mais aussi le risque de transmission mère-enfant.12,13 Actuellement, il n’existe cependant aucun rapport de cas réel à ce sujet et l’approche adéquate pour l’ajustement posologique reste incertaine.
Évaluation du rapport bénéfice-risque pour l’enfant
La question de savoir si un traitement médicamenteux est préférable pendant et après la grossesse, et, le cas échéant, à quelle dose, relève d’une évaluation du rapport bénéfice-risque pour la mère et l’enfant, en tenant compte des risques connus et inconnus pendant la grossesse et l’allaitement. L’idéal est une gestion prospective dès le désir d’enfant ou le début du traitement pendant la grossesse. Par exemple, le risque de diminution de l’efficacité d’un traitement antidépresseur par le citalopram pendant la grossesse doit être évalué par rapport au risque de troubles d’adaptation du nouveau-né après la naissance. Des modifications physiologiques chez la mère et l’enfant surviennent pendant le post-partum, dont il faut tenir compte lors de l’évaluation de la compatibilité avec l’allaitement, en plus du passage des médicaments dans le lait maternel. Par exemple, les concentrations plasmatiques de citalopram mesurées chez le nourrisson allaité diminuent d’un facteur supérieur à 20 au cours des deux premiers mois de vie, alors que la concentration dans le lait reste stable,14 notamment en raison de l’augmentation constante de la capacité d’élimination du nourrisson.
Recommandations posologiques pharmacométriques en cas de données insuffisantes
Idéalement, les recommandations posologiques pendant la grossesse et l’allaitement devraient être basées sur des données cliniques concernant la relation dose-effet (pharmacocinétique), l’efficacité et la sécurité. Dans la pratique, il est cependant souvent impossible ou difficile de collecter de telles données pour la mère et l’enfant. Alors que les données sur la sécurité sont déjà collectées de manière aussi systématique que possible dans le cadre de la tératovigilance, celles sur la pharmacocinétique et sur l’efficacité qui en dépendent font souvent défaut.
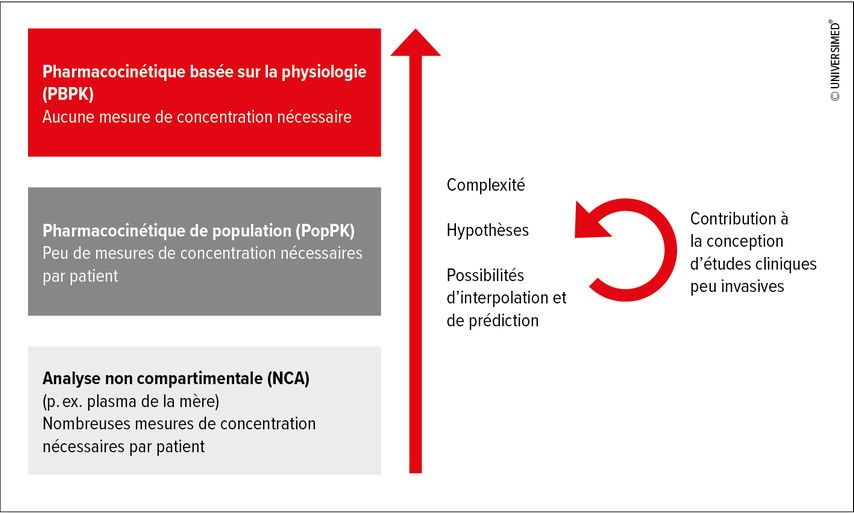
Les approches pharmacométriques soutiennent ici la prédiction quantitative des changements de cinétique pendant la grossesse et l’allaitement en utilisant le moins de mesures cliniquement invasives possibles de la concentration de médicaments chez la mère et l’enfant (Fig. 1): par rapport à l’analyse classique non compartimentale, qui nécessite de nombreuses mesures de concentration par patient, l’analyse par pharmacocinétique de population se contente de quelques-unes. De plus, elles permettent d’obtenir des informations pertinentes sur la variabilité inter- et intra-individuelle ainsi que sur les processus physiologiques.15 Des modèles pharmacocinétiques physiologiques complexes permettent aussi de faire des prédictions sur la seule base de paramètres physiologiques «spécifiques au système» connus pendant la grossesse ou chez le nourrisson (p.ex. débit cardiaque et perfusion des organes, débit de filtration glomérulaire, activité enzymatique hépatique) en interaction avec des propriétés «spécifiques au principe actif» connues (p.ex. propriétés physico-chimiques, affinité pour certaines enzymes).16 Le nombre de médicaments caractérisés par pharmacométrie ne cesse d’augmenter. Cela contribue à l’établissement d’approches pour l’ajustement posologique et à la conception d’autres études cliniques pour évaluer les prédictions basées sur la physiologie.
Fig. 1: Approches pharmacométriques pour la prédiction et la quantification des changements de cinétique pendant et après la grossesse et l’allaitement (adaptée et modifiée selon van Hasselt JG et al. 2012).27 L’intégration de paramètres physiologiques et spécifiques au médicament connus (hypothèses) dans des modèles de complexité croissante permet de réduire la nécessité de mesures cliniques invasives (p.ex. mesure de la concentration plasmatique) et de prédire l’exposition aux médicaments dans différents espaces de distribution (p.ex. plasma, fœtus, lait, nouveau-né), qui peut être évaluée par des études cliniques peu invasives
Littérature:
1 Ito S: Mother and Child: Medication use in pregnancy and lactation. Clin Pharmacol Ther 2016; 100: 8-11 2 Constantine MM: Physiologic and pharmacokinetic changes in pregnancy. Front Pharmacol 2014; 5:65 3 Palahniuk RJ et al. Pregnancy decreases the requirement for inhaled anesthetic agents. Anesthesiology 1974; 41: 82-34 ter Laak MA et al.: Pharmacokinetics of nifedipine slow-release during sustained tocolysis. Int J Clin Pharmacol Ther 2015; 53: 84-91 5 Silberschmidt AL et al.: Nifedipine concentration in maternal and umbilical cord blood after nifedipine gastrointestinal therapeutic system for tocolysis. BJOG 2008; 115: 480-5 6 Andrew MA et al.: Amoxicillin pharmacokinetics in pregnant women: modeling and simulations of dosage strategies. Clin Pharmacol Ther 2007; 81: 547-56 7 Johnson JR et al. Optimal dosing of penicillin G in the third trimester of pregnancy for prophylaxis against group B Streptococcus. Am J Obstet Gynecol 2001; 185: 850-3 8 Franco V et al.: Changes in lamotrigine pharmacokinetics during pregnancy and the puerperium. Ther Drug Monit 2008; 30: 544-7 9 Pennell PB et al.: Lamotrigine in pregnancy: clearance, therapeutic drug monitoring, and seizure frequency. Neurology 2008; 70(22Pt2): 2130-6 10 Momper JD et al.: Elvitegravir/cobicistat pharmacokinetics in pregnant and postpartum women with HIV. AIDS 2018; 32: 2507-16 11 Momper JD et al.: Pharmacokinetics of darunavir and cobicistat in pregnant and postpartum women with HIV. AIDS 2021; 35: 1191-9 12 Swissmedic: DHPC – Genvoya® (elvitégravir/cobicistat/emtricitabine/ténofovir alafénamide) / Stribild® (elvitégravir/cobicistat/emtricitabine/ténofovir disoproxil) / Tybost® (cobicistat). Disponible sur https://www.swissmedic.ch/swissmedic/fr/home/medicaments-a-usage-humain/surveillance-du-marche/health-professional-communication--hpc-/dhpc_evgcobi_pregnancy.html ; dernier access 29.8.2024 13 Swissmedic: DHPC – Prezista® (darunavir). Disponible sur https://www.swissmedic.ch/swissmedic/fr/home/medicaments-a-usage-humain/surveillance-du-marche/health-professional-communication--hpc-/dhpc-prezista_darunavir.html ; dernier access 29.8.2024 14 Heikkinen T et al.: Citalopram in pregnancy and lactation. Clin Pharmacol Ther 2002; 72: 184-91 15 Gotta V et al.: [Understanding and reducing the risk of adverse drug reactions in pediatric patients]. Ther Umsch 2015; 72: 679-86 16 Dallmann A et al.: Physiologically based pharmacokinetic modeling in pregnancy: a systematic review of published models. Clin Pharmacol Ther 2018; 104: 1110-24 17 EURAP Study Group: Seizure control and treatment in pregnancy: observations from the EURAP epilepsy pregnancy registry. Neurology 2006; 66: 354-60 18 Sabers A: Algorithm for lamotrigine dose adjustment before, during, and after pregnancy. Acta Neurol Scand 2012; 126: e1-4 19 Wesseloo R et al.: Lithium dosing strategies during pregnancy and the postpartum period. Br J Psychiatry 2017; 211: 31-6 20 Soldin OP et al.: Therapeutic drug monitoring during pregnancy and lactation: thyroid function assessment in pregnancy-challenges and solutions Ther Drug Monit 2010; 32: 265-8 21 O’Brien L et al.: Changes in antidepressant metabolism in pregnancy evidenced by metabolic ratios in hair: a novel approach. Forensic Sci Int 2010; 196: 93-6 22 Freeman MP at al.: Pharmacokinetics of sertraline across pregnancy and postpartum. J Clin Psychopharmacol 2008; 28: 646-53 23 Sit DK et al.: Changes in antidepressant metabolism and dosing across pregnancy and early postpartum J Clin Psychiatry 2008; 69: 652-8 24 Ke AB et al.: Expansion of a PBPK model to predict disposition in pregnant women of drugs cleared via multiple CYP enzymes, including CYP2B6, CYP2C9 and CYP2C19 Br J Clin Pharmacol 2014; 77: 554-70 25 Roston TM et al.: Caring for the pregnant woman with an inherited arrhythmia syndrome. Heart Rhythm 2020; 17: 341-8 26 Haas DM, D’Alton M: Pharmacogenetics and other reasons why drugs can fail in pregnancy: higher dose or different drug? Obstet Gynecol 2012; 120: 1176-9 27 van Hasselt JGC et al.: The status of pharmacometrics in pregnancy: highlights from the 3(rd) American conference on pharmacometrics. Br J Clin Pharmacol 2012; 74: 932-9
Das könnte Sie auch interessieren:
L’hyperglycémie pendant la grossesse
Le diabète sucré pendant la grossesse est associé à des risques pour la mère et l’enfant.1 Le Pr Dr méd. Roger Lehmann, de Zurich, a expliqué lors du cours Diabetes Update Refresher du ...
APL à haut risque: nouveau traitement de référence? – CML: asciminib par rapport au traitement de première ligne par ITK
La leucémie promyélocytaire aiguë (APL), une forme rare de leucémie myéloïde aiguë, pourrait bientôt bénéficier d’un nouveau traitement de référence moins toxique. Chez les patient·es ...
Communications et posters sélectionnés
Lors du congrès annuel des pneumologues suisses, qui s’est tenu du 29 au 31mai 2024 à Baden, les pneumologues suisses ont donné un aperçu de leurs multiples recherches. Nous vous ...