Helicobacter pylori: qu’est-ce qui reste tel quel, qu’est-ce qui change?
Auteur:
Prof. Dr méd. Joachim Labenz
Privatpraxis für Gastroenterologie
am Diakonie Klinikum Jung-Stilling
Siegen
E-mail: info@joachim-labenz.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La redécouverte d’Helicobacter pylori (HP) en 1983 a entraîné l’un des plus grands changements de paradigme en médecine: le véritable ulcère, jusqu’alors jugé comme une maladie liée à l’acidité et souvent traitée par des opérations mutilantes, est devenue une maladie infectieuse guérissable. C’est à juste titre que les deux chercheurs australiens Robin Warren (pathologiste) et Barry Marshall (interniste) ont reçu le prix Nobel de physiologie ou médecine en 2005. Récemment, la directive S2k correspondante de la Société allemande de gastroentérologie et des maladies digestives et métaboliques (DGVS) a été adaptée pour, entre autres, mettre en œuvre le changement de paradigme international dans le traitement.
Keypoints
-
Les infections à HP sans gastrite n’existent pas.
-
Indépendamment des symptômes et des lésions, la gastrite à HP est une maladie infectieuse et constitue donc toujours une indication de traitement.
-
Un dépistage de l’HP doit être effectué chez les patients présentant un risque de cancer de l’estomac.
-
Des méthodes diagnostiques endoscopiques et non invasives sont utilisées en fonction des questions cliniques.
-
Le traitement de première intention est la quadrithérapie bismuthée.
-
Les échecs thérapeutiques doivent être traités en tenant compte de la résistance individuelle.
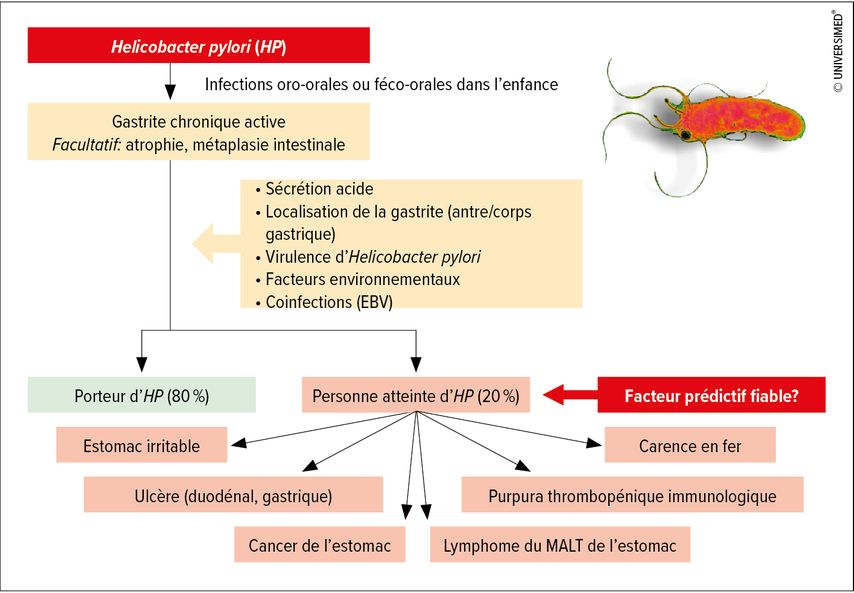
L’infection à Helicobacter pylori est probablement la maladie infectieuse la plus répandue dans le monde après les caries. Près de la moitié de la population mondiale est infectée.1 En Allemagne aussi, environ 30% des adultes sont probablement encore infectés. La transmission de l’infection se fait à l’âge préscolaire (Fig. 1). Dans les pays développés, le mode de transmission oro-orale est probablement dominant. Les principales sources d’infection sont les personnes infectées dans l’environnement familial.2
Conséquences cliniques dans le tractus gastro-intestinal
Gastrite
L’infection à Helicobacter pylori n’est pas invasive. L’interaction de la bactérie avec l’épithélium gastrique déclenche une réaction immunitaire complexe dont le phénotype conduit obligatoirement au tableau clinique de la gastrite chronique active (type B), une coexistence de signes de réponse immunitaire non spécifique avec des granulocytes neutrophiles et spécifique avec des lymphocytes ainsi que des plasmocytes. De plus, le germe intervient dans la physiologie de l’estomac par le biais de ses propres produits et de la réponse immunitaire induite. S’il s’agit par exemple d’une gastrite prononcée dans l’antre, on observe une augmentation de la sécrétion acide, alors qu’on observe une inhibition de la sécrétion acide, par exemple par l’interleukine 1β, si la réaction inflammatoire est plus prononcée dans le corps gastrique. L’atrophie et la métaplasie intestinale sont associées à un risque accru de cancer de l’estomac.3 Environ 80% des personnes souffrant d’une infection chronique restent asymptomatiques tout au long de leur vie, alors qu’une sur cinq tombe malade (Fig. 1).
Ulcère, carcinome et lymphome du MALT
L’Helicobacter pylori est une condition requise, mais insuffisante seule, dans la pathogenèse des ulcères duodénaux et gastriques vrais, en utilisant la terminologie de la logique conditionnelle. En d’autres termes: «sans Helicobacter pylori, aucun ulcère». L’ancien principe «sans acide, aucun ulcère», en vigueur depuis 1910, n’a pas été invalidé pour autant, mais élargi à «sans acide ni Helicobacter pylori, aucun ulcère». De plus, l’Helicobacter pylori augmente le risque d’ulcère sous AAS et AINS.3
Les patients infectés par Helicobacter pylori présentent globalement un risque deux à trois fois plus élevé de développer un cancer de l’estomac. Des analyses récentes ont démontré de manière impressionnante la pertinence synergique de l’infection et des anomalies génétiques dans le domaine des gènes de réparation de l’ADN.2,3 Outre la prédisposition familiale, les marqueurs de risque histologiques, tels qu’une gastrite plus prononcée dans le corps gastrique, une métaplasie intestinale et une atrophie, sont importants. Une étude contrôlée par placebo avec un suivi sur 26,5ans a montré une réduction de 43% de l’incidence du cancer de l’estomac.4 Chez les parents au premier degré de patients atteints de cancer de l’estomac, l’éradication de l’infection permet de réduire de moitié le risque associé.5
Le lymphome du MALT («mucosa-associated lymphoid tissue») de l’estomac est étroitement et causalement associé à l’infection à Helicobacter pylori. Sa croissance dépend d’Helicobacter pylori en tant que stimulus antigénique. Aujourd’hui, l’éradication d’Helicobacter pylori est le traitement de première intention aux stades précoces, lorsque le lymphome se limite encore à la paroi de l’estomac.3
Estomac irritable
Les patients souffrant d’infection à Helicobacter pyloriprésentent un risque de survenue accru d’un estomac irritable. En cas d’estomac irritable Helicobacter pylori positif, l’éradication de l’infection entraîne la disparition ou l’atténuation des symptômes chez une partie des patients.6 Il n’existe toutefois aucun facteur prédictif fiable du succès thérapeutique, de sorte qu’une différenciation entre la dyspepsie liée à l’Helicobacter pylori et l’estomac irritable au sens strict est uniquement possible après l’éradication de l’infection.
Manifestations extragastriques
Le purpura thrombopénique immunologique (PTI, maladie de Werlhof) est une indication confirmée pour le diagnostic et le traitement de l’infection à Helicobacter pylori. Chez environ la moitié des patients, on peut s’attendre à une augmentation des thrombocytes après l’éradication d’Helicobacter pylori.3 En cas d’anémie par carence en fer chronique, une éradication d’Helicobacter pylori est également possible après avoir soigneusement exclu une autre cause, car des essais randomisés contrôlés ont mis en évidence un effet thérapeutique.
Dépistage d’Helicobacter pylori – chez qui et comment?
Toutes les personnes présentant un risque accru de cancer de l’estomac (parents au premier degré de patients atteints d’un cancer de l’estomac, personnes originaires de régions à forte prévalence,comme les pays d’Asie, d’Europe de l’Est, d’Amérique du Sud) doivent se voir proposer un diagnostic approprié.3 Un dépistage endoscopique est recommandé à partir de 40ans. Une option pertinente consiste à combiner le dépistage d’Helicobacter pylori avec la coloscopie préventive.
Diagnostic d’une infection à Helicobacter pylori: quel test est indiqué et quand?
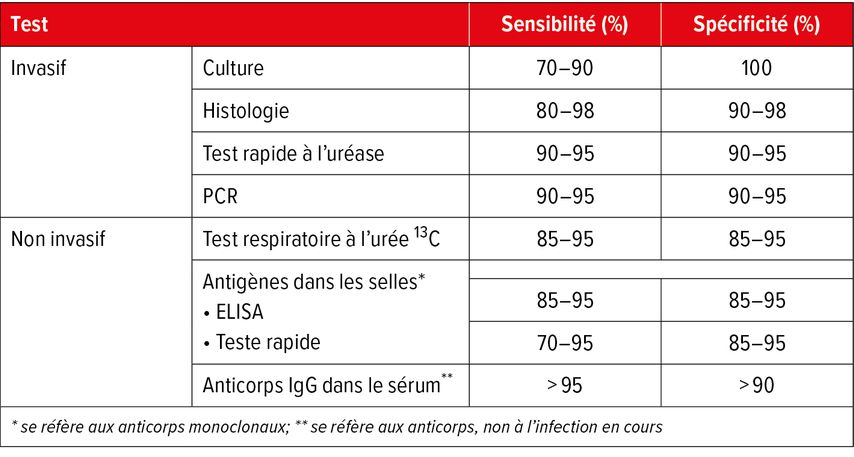
Pour diagnostiquer une infection à Helicobacter pylori, on dispose de méthodes invasives (endoscopie nécessaire) et non invasives, avec des sensibilités et des spécificités variables (Tab. 1).3 On peut en outre faire la distinction entre les méthodes directes, qui détectent le germe ou ses composants, et celles indirectes. Ces dernières sont basées sur la détection de l’activité uréase ou d’une réponse immunitaire. Il faut retenir qu’il n’existe aucun test diagnostique de référence. La culture est spécifique; il n’existe aucune méthode avec une sensibilité de 100%. La condition préalable à un traitement est la détection fiable d’une infection en cours, laquelle ne peut être garantie par la présence d’anticorps dans le sang. La sérologie ne joue donc pas un rôle essentiel en Allemagne, tout au plus comme diagnostic d’exclusion.
Tab. 1: Sensibilité et spécificité des tests invasifs et non invasifs pour la recherche d’une infection à Helicobacter pylori (modifiées selon Choi IJ et al. 2020)5
Les traitements préalables par des antibiotiques et des inhibiteurs de la pompe à protons (IPP) peuvent entraîner une suppression de la colonisation d’Helicobacter pylori dans l’estomac et donc occasionner des résultats de test faux négatifs. C’est pourquoi il est recommandé de respecter un intervalle de deux semaines entre la prise d’IPP, ou de quatre semaines après un traitement antibiotique, et un diagnostic d’infection à Helicobacter pylori.
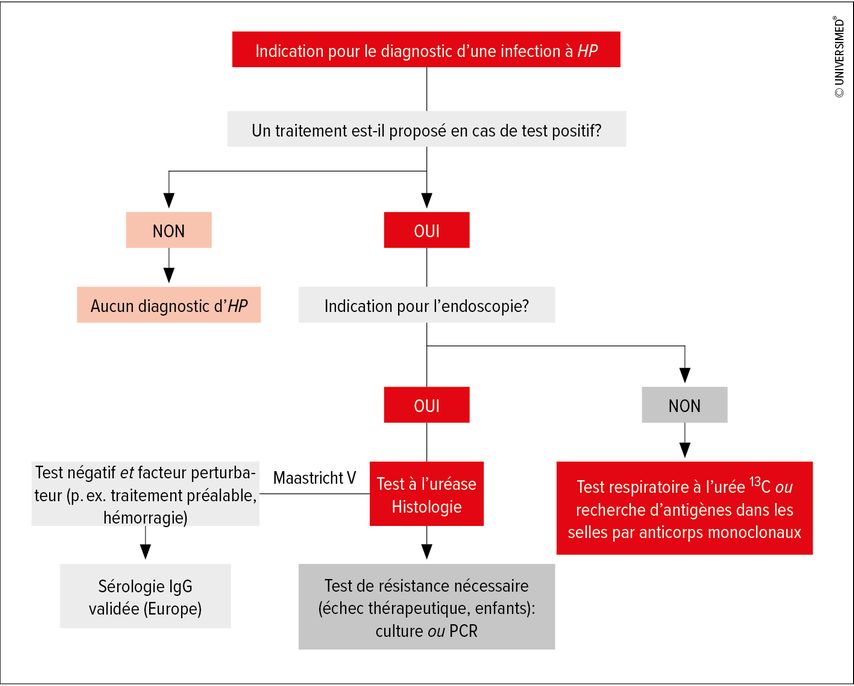
La figure 2 résume les recommandations allemandes actuelles en matière de diagnostic d’infection à Helicobacter pylori.3 La détection de l’infection impliquant toujours un traitement, il convient de se demander, avant d’initier le diagnostic, si l’on traiterait en cas de détection de germes. En outre, il est important de clarifier la question de savoir si le résultat endoscopique (et donc aussi histologique) est pertinent pour la décision thérapeutique. Si la réponse est négative, une détection non invasive des germes au moyen d’un test respiratoire à l’urée13C ou d’une recherche d’antigènes dans les selles par anticorps monoclonaux suffit.
Fig. 2: Algorithme pour le diagnostic d’une infection à Helicobacter pylori (modifié selon la directive S2k surHelicobacter pylori 2022)3
Dans le concept thérapeutique actuel, la détection de la résistance joue un rôle plus important qu’auparavant. En raison de l’augmentation de la résistance primaire de l’Helicobacter pylori à la clarithromycine et à la lévofloxacine, ces antibiotiques ne devraient plus être utilisés sans un contrôle préalable de la résistance. La culture est coûteuse et sujette aux contaminations. Une bonne alternative est la détection de la résistance par PCR à partir des biopsies.3
Un contrôle du traitement doit être effectué après chaque éradication d’Helicobacter pylori.3 La précision est suffisante au plus tôt quatre semaines après la fin du traitement (les IPP doivent également être interrompus pendant au moins deux semaines!). Le test respiratoire à l’urée13C et une recherche d’antigènes dans les selles par anticorps monoclonaux sont tous deux appropriés. En cas de statut après un ulcère compliqué, chez les patients souffrant d’ulcère gastrique ou d’un lymphome du MALT, un contrôle endoscopique est impératif et peut alors être combiné à un contrôle biopsique du succès thérapeutique.
Indication de traitement de l’infection à Helicobacter pylori: changement de paradigme
Au niveau international, et maintenant pour la première fois dans la nouvelle directive allemande, un changement de paradigme a eu lieu en ce qui concerne les indications de traitement. D’une part, il repose sur la constatation scientifique que l’évolution d’une gastrite à Helicobacter pylori ne peut pas être prédite de manière fiable. D’autre part, il se base sur des données scientifiques probantes selon lesquelles l’éradication d’Helicobacter pylori permet de réduire drastiquement le risque de cancer de l’estomac et d’ulcère peptique, également induit par les AINS. La gastrite à Helicobacter pylori est donc une maladie infectieuse, indépendamment des symptômes et des maladies secondaires.3 Cette constatation implique qu’il y a toujours une indication de traitement en cas de détection d’une infection à Helicobacter pylori.
Traitement de l’infection à Helicobacter pylori: un changement de mentalité s’impose
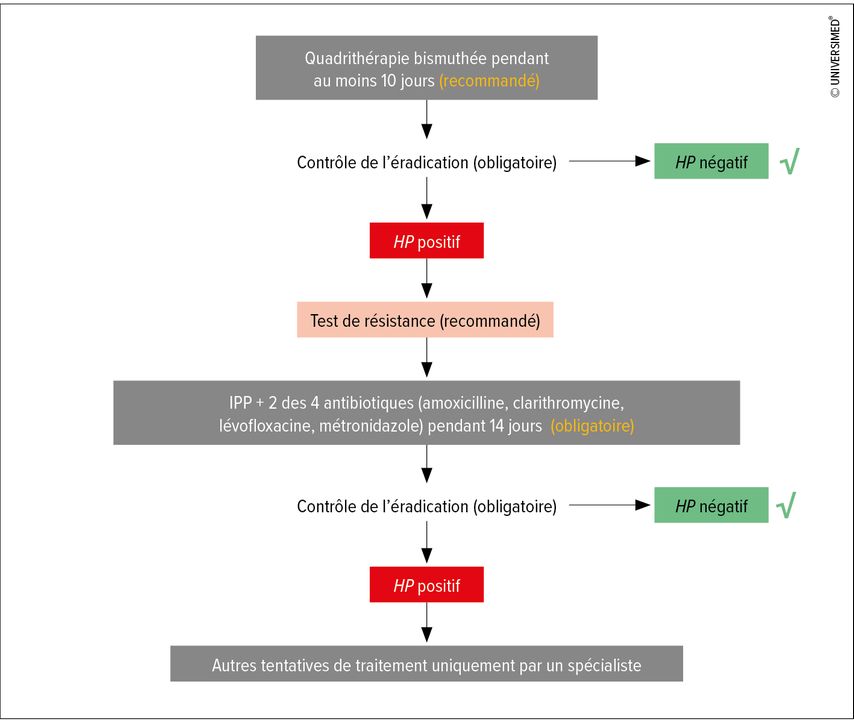
Le traitement de première intention actuel, une trithérapie incluant un IPP sur une semaine, ne peut plus être recommandé en raison de l’augmentation croissante de la résistance. Un changement de paradigme dans le traitement est ainsi observé dans la directive actuelle de la DGVS.3 Seule la quadrithérapie bismuthée (BQT; IPP + bismuth + tétracycline + métronidazole) est recommandée en tant que traitement de première intention pendant dix jours, à condition qu’aucune résistance n’ait été détectée (Fig. 3). Malgré sa complexité, ce schéma thérapeutique à 14 comprimés par jour répartis sur quatre prises s’est révélé efficace dans de nombreuses études, méta-analyses et également dans de grandes études de registre, avec un profil d’effets secondaires acceptable.
Fig. 3: Algorithme pour le traitement d’une infection à Helicobacter pylori (modifié selon la directive S2k sur Helicobacter pylori 2022)3
S’il ne permet pas d’éradiquer l’infection, il est recommandé de passer à l’étape suivante, à savoir une trithérapie incluant un IPP sur deux semaines (Fig. 3). Il convient de choisir deux des quatre antibiotiques suivants sur la base de l’antibiogramme: amoxicilline, clarithromycine, lévofloxacine, métronidazole. Si ce traitement échoue également, il est recommandé de suivre un traitement individualisé par un spécialiste particulièrement expérimenté dans le domaine.
Réinfections à Helicobacter-pylori
Le risque de réinfection est faible dans les pays occidentaux (<1%/an), à condition que le traitement recommandé ait été suivi de manière adéquate et que toute persistance de l’infection ait été recherchée au moyen de méthodes appropriées quatre semaines ou plus après la fin du traitement. En conséquence, aucun contrôle systématique du statut infectieux n’est recommandé.
Fig. 4: L’infection à Helicobacter pylori est fréquente et toujours cliniquement pertinente, que ce soit comme cause d’une maladie ou facteur de risque d’une maladie secondaire pertinente. Chez les patients présentant des symptômes ou des lésions du tractus gastro-intestinal supérieur, un purpura thrombopénique immunologique, une carence en fer après exclusion d’autres causes et des facteurs de risque de cancer de l’estomac, la recherche adéquate de l’infection est obligatoire. Le traitement est complexe, mais presque toujours efficace s’il est suivi correctement
Littérature:
1 Zamani M et al.: Systematic review with meta-analysis: the worldwide prevalence of Helicobacter pylori infection. Aliment Pharmacol Ther 2018; 47: 868-76 2 Labenz J et al.: Gastritis: Update 2020. Gastroenterologie up2date 2020; 16: 277-300 3 Fischbach W et al.: Aktualisierte S2k-Leitlinie Helicobacter pylori und gastroduodenale Ulkuskrankheit der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) 2022. Z Gastroenterol 2023; 61: 544-606 4 Yan L et al.: Effect of Helicobacter pylori eradication on gastric cancer prevention: updated report from a randomized controlled trial with 26.5 years of follow-up. Gastroenterology 2022; 163: 154-62 5 Choi IJ et al.: Family history of gastric cancer and Helicobacter pylori treatment. N Engl J Med 2020; 382: 427-36 6 Ford AC et al.: Efficacy of Helicobacter pylori eradication therapy for functional dyspepsia: updated systematic review and meta-analysis. Gut 2022; 71: 1967-75
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...