Nouvelle option thérapeutique pour l’œsophagite à éosinophiles
Compte-rendu:
Dre Corina Ringsell
Rédactrice
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Lors du congrès annuel de la Société Suisse de Gastroentérologie (SSG) à Interlaken, le Pr Dr méd. Luc Biedermann, médecin adjoint à la clinique de gastroentérologie et d’hépatologie de l’Hôpital universitaire de Zurich, a présenté une substance prometteuse dans le traitement de l’œsophagite à éosinophiles (EoE).
Keypoints
-
Le dupilumab inhibe l’IL-4 ainsi que l’IL-13 et constitue le premier traitement avancé de l’EoE.
-
Dans les études cliniques d’autorisation, la substance active a démontré une efficacité constante en ce qui concerne les critères d’évaluation histologiques, endoscopiques et cliniques.
-
Les expériences cliniques en dehors des études menées en Suisse sont très positives et encourageantes.
-
Les patient·es atteint·es d’EoE présentant une maladie réfractaire, une intolérance aux corticoïdes ou des maladies atopiques concomitantes sont les parfait·es candidat·es pour le traitement par le dupilumab.
-
Il existe une efficacité potentielle également dans les formes sévères d’EoE, y compris les sténoses – év. même en traitement de première ligne («top-down»).
Dans la physiopathologie de l’œsophagite à éosinophiles (EoE), un déséquilibre entre les lymphocytes T auxiliaires de type 1 (Th1) et de type 2 (Th2) joue un rôle important.1 Dans les maladies allergiques et atopiques, comme l’EoE, les Th2 prédominent, le phénomène étant déclenché par la présence d’interleukine 4 (IL-4). Les Th2 produisent à leur tour de l’IL-4, 5, 9 et 13, ce qui entraîne une infiltration de granulocytes éosinophiles et basophiles ainsi que de mastocytes.1 Ces cellules favorisent et entretiennent les processus inflammatoires dans l’œsophage. En l’absence de traitement, on observe une évolution vers une fibrose, un remodelage tissulaire et des sténoses.2 Les personnes concernées souffrent de troubles tels que la dysphagie et l’obstruction œsophagienne. Selon L. Biedermann, c’est pourquoi les principaux objectifs du traitement sont de prévenir le remodelage ou de le réduire en cas d’EoE sévère, de contrôler les symptômes et de prévenir les obstructions œsophagiennes. L’anticorps monoclonal dupilumab intervient dans ces processus en inhibant l’IL-4 et 13.2
Résultats encourageants des études cliniques
L. Biedermann a présenté une étude de phase III en trois parties comparant le dupilumab à un placebo chez des patient·es atteint·es d’EoE.2 Elle a porté sur des personnes âgées de 12 ans et plus dont l’EoE persistait pendant huit semaines malgré l’administration de fortes doses d’inhibiteurs de la pompe à protons (IPP). Tou·tes les participant·es avaient un score de 10 ou plus au «Dysphagia Symptom Questionnaire» (DSQ) au début de l’étude, avec un score médian de 33,6 dans la partie A et de 36,7 dans la partie B.
Dans la partie A, 81 patient·es ont été randomisé·es selon un rapport 1:1 et ont reçu soit 300mg de dupilumab toutes les semaines, soit un placebo. Dans la partie B, 240 patient·es ont été randomisé·es 1:1:1 et ont reçu 300mg de dupilumab toutes les semaines ou 300mg de dupilumab toutes les deux semaines (plus un placebo pendant les semaines sans dupilumab) ou un placebo. Les critères d’évaluation primaires des parties A et B étaient la rémission histologique (définie par <6 éosinophiles/HPF) et la variation absolue du score du DSQ à la semaine 24. La partie C incluait les patient·es qui avaient terminé les parties A ou B. Le groupe A–C a reçu 300mg de dupilumab toutes les semaines pendant 28 semaines supplémentaires (y compris le groupe précédemment sous placebo). Dans le groupe B–C, les patient·es du groupe sous dupilumab ont poursuivi le schéma thérapeutique pendant 28 semaines. Le groupe sous placebo a été randomisé et traité également pendant 28 semaines supplémentaires par 300mg de dupilumab soit toutes les semaines, soit toutes les deux semaines.2
Dans la partie A, 60% des personnes traitées par le dupilumab ont obtenu une rémission histologique (par rapport à 5% sous placebo). Dans la partie B, 59% des patient·es ayant reçu du dupilumab une fois par semaine et 60% de ceux·elles en ayant reçu une fois toutes les deux semaines ont obtenu une rémission histologique. L’effet s’est également maintenu dans la partie C pendant un total de 52 semaines. À la semaine 52, les patient·es ayant reçu un placebo dans les parties A et B et le dupilumab dans la partie C ont obtenu des résultats similaires à ceux·elles des groupes sous traitement actif à la semaine 24.2
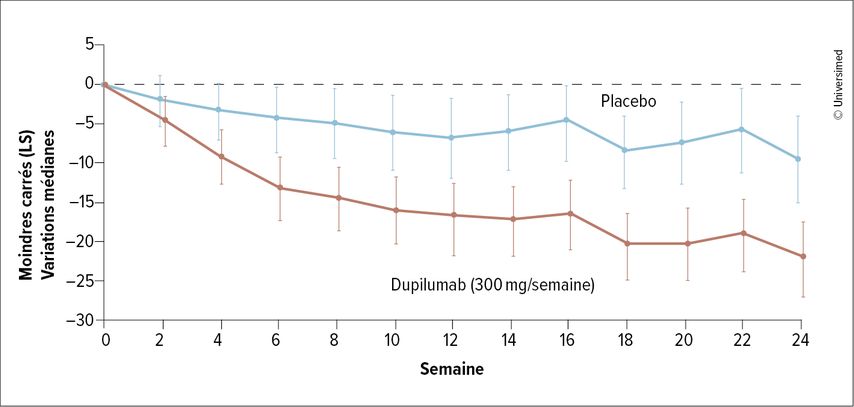
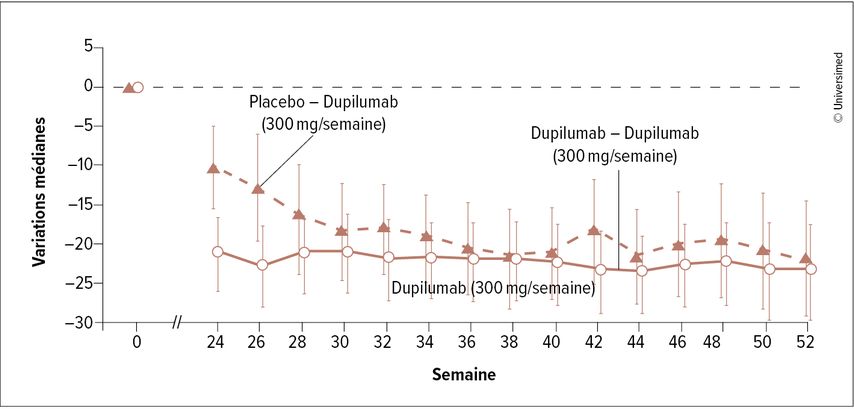
Il en a été de même pour le deuxième critère d’évaluation d’évolution du DSQ: sous dupilumab, le score du DSQ s’est amélioré de 21,9 points (par rapport à 9,6 points sous placebo) dans la partie A (Fig.1) et de 23,8 points (par rapport à 13,9 points) dans la partie B. Cet effet s’est également maintenu dans la partie C, et les patient·es qui sont passé·es du placebo au dupilumab ont à nouveau obtenu des scores similaires à ceux des patient·es du groupe sous traitement actif dans la partie A ou B (Fig.2).2
Fig.1: Variations médianes du score du «Dysphagia Symptom Questionnaire» (DSQ) entre le début de l’étude et la semaine 24 chez les patient·es de la partie A (modifiée selon Dellon ES et al. 2022)2
Fig.2: Variation médiane du score du «Dysphagia Symptom Questionnaire» (DSQ) chez les patient·es du groupe A–C dans la partie C (modifiée selon Dellon ES et al. 2022)2
Des effets secondaires ont été observés chez 60 à 86% des patient·es, tous groupes confondus, principalement des réactions au site d’injection dans les groupes sous dupilumab.2
Dupilumab chez les enfants
L. Biedermann a démontré que le dupilumab était efficace et sûr non seulement chez les adultes, mais aussi chez les enfants, à l’aide d’une étude de phase III en deux parties incluant des enfants âgés de un à onze ans.3 Dans la partie A, les enfants ont été traités pendant 16 semaines par le dupilumab soit à forte dose, soit à faible dose, soit par un placebo. À la fin des 16 semaines, les enfants des groupes sous dupilumab ont continué à recevoir le même schéma pendant 36 semaines, tandis que ceux du groupe sous placebo ont été randomisés pour recevoir soit une forte dose soit une faible dose de dupilumab (partie B).3 À la fin de la partie A, 68% des enfants recevant la forte dose et 58% de ceux recevant la faible dose avaient atteint le critère d’évaluation primaire de rémission histologique (par rapport à 3% sous placebo). L’effet s’est également maintenu dans la partie B.3
Combinaison avec des corticoïdes oraux ou des IPP?
L. Biedermann a également abordé la question de savoir si le dupilumab pouvait être combiné avec des corticoïdes oraux ou des IPP. Dans l’étude d’autorisation, les patient·es ont dû arrêter les corticoïdes oraux, c’est pourquoi il n’existe aucune donnée ni recommandation à ce sujet.2 Les IPP étaient en revanche autorisés et pouvaient être pris à une dose fixe. Cependant, la prise ou non d’IPP n’a pas fait de différence en ce qui concerne la réponse au dupilumab.
Qui peut bénéficier d’un traitement par le dupilumab?
L’expert a cité quatre groupes de patient·es atteint·es d’EoE chez qui un traitement par le dupilumab pourrait être pertinent:
-
Patient·es ne répondant pas aux autres médicaments; par exemple, 10% des patient·es atteint·es d’EoE ne répondent pas au budésonide.
-
Patient·es chez qui le budésonide a été maintenu pendant plus d’un an; dans ce cas, on observe une perte d’efficacité chez environ un quart des patient·es.
-
Patient·es intolérant·es aux corticoïdes.
-
Patient·es présentant des comorbidités atopiques modérées ou sévères.
L’activité de l’EoE peut également influencer le choix du traitement, car les corticoïdes oraux ont une efficacité moindre dans les cas sévères. Pour déterminer l’activité de la maladie, une conférence de consensus multidisciplinaire a développé en 2021 l’«Index of Severity for Eosinophilic Esophagitis» (I-SEE). Il comprend les domaines suivants: «Symptômes et complications», «Caractéristiques inflammatoires» et «Atteinte fibrosténosante».4 Dans chacun de ces domaines, 1 à 15 points sont attribués en fonction du degré de sévérité, puis additionnés. La somme indique l’activité de la maladie: <1: EoE inactive; 1–6: EoE faiblement active; 7–14: EoE modérément active; >15: EoE sévèrement active.4 Une application I-SEE correspondante de l’American Gastroenterological Association est même disponible depuis peu.
L. Biedermann a conclu que le dupilumab peut être un traitement efficace pour les patient·es souffrant d’allergies de longue date, une alternative à une corticothérapie de longue durée, et une bonne option pour les patient·es atteint·es d’EoE très sévère ou avancée afin d’éviter les complications à long terme.
Source:
Congrès 2024 de la SSG, 12 et 13 septembre 2024, Interlaken
Littérature:
1 Yoshimoto T: The hunt for the source of primary interleukin-4: how we discovered that natural killer T cells and basophils determine T helper type 2 cell differentiation in vivo. Front Immunol 2018: 9: 716 2 Dellon ES et al.: Dupilumab in adults and adolescents with eosinophilic esophagitis. N Engl J Med 2022; 387: 2317-30 3 Chehade M et al.: Dupilumab for eosinophilic esophagitis in patients 1 to 11 years of age. N Engl J Med 2024; 390: 2239-51 4 Dellon ES et al.: A clinical severity index for eosinophilic esophagitis: development, consensus, and future directions. Gastroenterology 2022; 163: 59-76
Das könnte Sie auch interessieren:
Séquelles cardiopulmonaires à long terme après une infection sévère par le SARS-CoV-2
Le SARS-CoV-2 a entraîné une crise sanitaire mondiale et a posé des défis considérables aux systèmes de santé.1 Si le Covid-19 était initialement considérée comme une maladie ...
Posters et communications sélectionnés
Lors du congrès annuel de la Société Suisse d’Endocrinologie et de Diabétologie, les endocrinologues et diabétologues suisses ont fourni une vue d’ensemble de leurs nombreuses recherches ...
Analogues de l’incrétine par rapport à la chirurgie bariatrique
La question du meilleur traitement pour la perte de poids a fait l’objet d’un débat pour et contre dans le cadre du congrès 2024 de l’EASD. Alors que la facilité d’accès et la bonne ...