Personne fébrile au retour d’un voyage
Compte-rendu:
Dr méd. Norbert Hasenöhrl
Journaliste médical
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La fièvre est généralement l’un des principaux symptômes chez les personnes au retour d’un voyage et est souvent accompagnée de symptômes gastro-intestinaux tout comme dermatologiques. Lors de l’Update Refresher du FOMF, le PD Dr méd. Andreas Neumayr a expliqué à quoi les médecins de premiers recours doivent également penser lorsqu’ils voient des personnes malades au retour d’un voyage. La règle est toujours la même: ce qui est fréquent survient fréquemment, ce qui est rare survient rarement.
En cas de fièvre, il est possible, en tenant compte d’autres paramètres cliniques et/ou de laboratoire, d’établir une classification dans laquelle se retrouvent la plupart des maladies tropicales et quelques autres maladies infectieuses (Fig. 1).
Fig. 1: Diagnostic différentiel syndromique chez les personnes fébriles au retour d’un voyage: examen clinique et de laboratoire (selon Neumayr/Swiss TPH)
«Après avoir observé le tableau clinique et les paramètres de laboratoire, nous nous posons généralement trois questions importantes chez un patient fébrile au retour d’un voyage», explique le PD Dr méd. Andreas Neumayr, Chief Medical Officer à l’Institut Tropical et de Santé Publique Suisse de Bâle. «Il s’agit tout d’abord de la période d’incubation, que nous pouvons généralement assez bien délimiter chez les personnes de retour de voyage. Nous savons par exemple que s’il s’est écoulé au moins 21 jours entre le retour du voyage et le début des symptômes, il ne peut pas s’agir d’une fièvre hémorragique virale comme Ebola ou Lassa», a-t-il ajouté. La question suivante qui se pose est celle de la plausibilité de l’épidémiologie, qui a bien sûr quelque chose à voir avec la fréquence d’une maladie dans la zone de voyage concernée. La troisième concerne les risques d’exposition spécifiques, p.ex. contact avec de l’eau douce (leptospirose, bilharziose), consommation de lait non pasteurisé (brucellose, salmonellose, FSME, tuberculose), consommation de viande de porc crue (trichinose) ou visite de grottes (histoplasmose, maladie à virus de Marburg), pour n’en citer que quelques-uns.
Diagnostic de laboratoire
«L’examen de laboratoire en médecine tropicale est relativement limité, ce qui est peut-être dû au fait que la médecine tropicale est justement souvent pratiquée dans des environnements disposant de peu de ressources», poursuit A. Neumayr. «Cela commence déjà par le fait que nous réalisons souvent la numération formule sanguine manuellement, c’est-à-dire par examen microscopique, ce qui a des raisons concrètes.» En outre, les taux de CRP, de transaminases et de créatinine sont déterminés, une analyse urinaire et, le cas échéant, des hémocultures sont effectués, et du «sérum initial» est prélevé, lequel est dans un premier temps seulement congelé, mais n’est pas encore analysé concrètement. «Le ‹sérum initial› a pour but de répondre, très rarement, à des questions auxquelles nous ne pouvons répondre que par sérologie, et pour lesquelles nous avons besoin d’un sérum de comparaison afin de pouvoir prouver, par exemple, des augmentations ultérieures du titre», a expliqué le spécialiste. «Il n’existe aucune règle trop rigide en ce qui concerne les hémocultures: le moment du prélèvement est beaucoup lié au jugement clinique», a-t-il déclaré.
En cas de séjour dans une région où sévit le paludisme au cours des douze derniers mois, un examen microscopique du paludisme (sang EDTA) et un test diagnostique rapide du paludisme (en général un immunodosage avec des anticorps contre P. falciparum) sont utilisés. En cas de séjour dans une zone à risque pour les arbovirus au cours des deux dernières semaines, un test de dengue (test rapide ou PCR) sera effectué et, le cas échéant, les virus du chikungunya ou du Zika seront également recherchés.
Cas 1 – Paludisme
Il s’agit d’un Suisse de 32 ans qui est rentré il y a trois semaines d’un voyage de quatre semaines en Afrique de l’Ouest. «Sur la base de ces informations, il est déjà possible d’exclure certains diagnostics différentiels, comme les arbovirus ou les agents pathogènes de la fièvre hémorragique», a constaté A. Neumayr.
Depuis deux jours, le patient a de la fièvre et des frissons, accompagnés de céphalées et de douleurs articulaires de type grippal. La tension artérielle est de 110/85mmHg, la fréquence cardiaque de 96battements/min et la température de 38,2°C. L’examen physique ne révèle aucune anomalie. À l’examen de laboratoire, on relève une thrombocytopénie de 87000/µl et une CRP de 43mg/l.
«Notre premier diagnostic différentiel en cas de combinaison de fièvre et de thrombocytopénie est le paludisme», ajoute-t-il. Si l’on se pose désormais les trois questions susmentionnées, on trouve une période d’incubation plausible qui peut varier d’une semaine à plusieurs mois. L’épidémiologie est très plausible, car le paludisme est fréquent en Afrique de l’Ouest. En ce qui concerne le risque d’exposition, le spécialiste a précisé: «la prise d’une prophylaxie antipaludique n’exclut pas une contamination et une anamnèse des piqûres de moustiques n’a aucun sens».
En cas de fièvre pendant ou après un séjour dans une zone de paludisme, il faut toujours exclure immédiatement un paludisme, même si une chimioprophylaxie a été prise par sécurité. «Cela ne veut pas dire que la prophylaxie est inutile. Bien au contraire, elle protège de manière fiable contre les évolutions sévères et le décès par paludisme», a souligné A. Neumayr. Il est toutefois impossible de distinguer cliniquement le paludisme d’autres infections fébriles (comme la grippe, la dengue, la fièvre typhoïde, etc.). La présence de toux sèche ou de diarrhée n’exclut pas non plus un paludisme.
«Quand je dis que le dépistage doit être ‹immédiat›, j’entends vraiment le jour même», a-t-il souligné. L’examen microscopique est et reste l’actuel examen de référence pour le diagnostic du paludisme. «Si l’expertise nécessaire pour l’examen microscopique fait toutefois défaut, un test rapide peut être préférable, car ces tests sont très fiables en soi. L’examen microscopique est en voie de disparition, car il faut en faire régulièrement pour être vraiment capable de le faire, et le paludisme n’est pas si fréquent en Europe», a ajouté A. Neumayr.
Un autre point est également important: chez les patients non immuns (généralement les voyageurs européens), des symptômes peuvent survenir avant que la parasitémie ne soit suffisamment prononcée pour être diagnostiquée par examen microscopique ou test rapide. Un seul test négatif, que ce soit un examen microscopique ou un test rapide, n’exclut donc pas un paludisme. Pour l’exclure avec une probabilité proche de la certitude, il faut trois séries négatives d’examen microscopique/de test rapide à 12–24 heures d’intervalle ou un examen microscopique ET une PCR négatifs.
«En ce qui concerne les tests rapides, il faut savoir qu’ils ne sont pas fiables à 100% pour les espèces non falciparum et qu’ils peuvent donner des faux négatifs en cas de parasitémie faible», a expliqué A. Neumayr. «C’est pourquoi on utilise de plus en plus la PCR, qui présente une excellente sensibilité et spécificité. Même si une PCR est utilisée, il faut tout de même procéder au moins une fois à un examen microscopique, parce que le diagnostic différentiel d’une personne fébrile au retour d’un voyage comprend également des agents pathogènes, potentiellement mortels, qui ne sont contenus dans aucune PCR multiplex et pour lesquels il n’existe pas non plus d’autres tests spécifiques», a averti l’intervenant. «Il s’agit par exemple des trypanosomes (voir ci-dessous), des borrélies, en tant qu’agents pathogènes de la fièvre récurrente, ou des babésies. On les observe toutefois tous très bien au microscope.»
Chez le patient décrit ci-dessus, un test rapide positif indique la présence de Plasmodium falciparum, ce qui est confirmé au microscope, dans la goutte épaisse et sur le frottis. La parasitémie est de 0,5% (pourcentage de cellules sanguines infectées), il s’agit donc d’un paludisme léger.
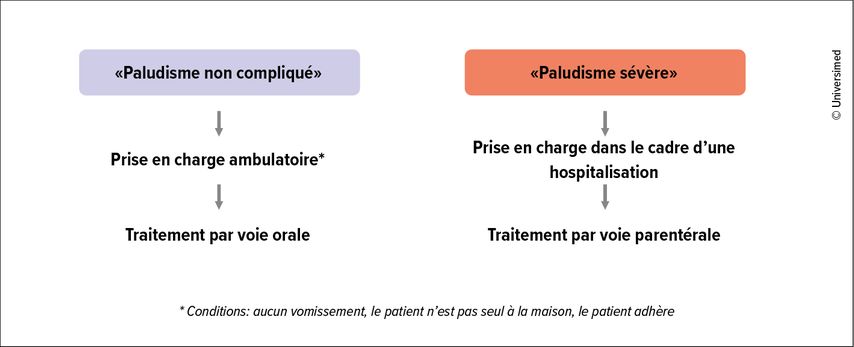
Pour la décision thérapeutique, on stratifie entre paludisme non compliqué et paludisme sévère (Fig.2). Il existe des critères de l’OMS pour la classification d’un paludisme sévère, qui englobent toute une série d’aspects, tels que l’atteinte neurologique, le SDRA, l’acidose, le choc circulatoire, l’anémie sévère ou l’hyperparasitémie.
Le paludisme est traité par l’association artéméther/luméfantrine (Raimet®) PO pendant cinq jours. Dans ce contexte, un suivi clinique et de laboratoire (numération formule sanguine et examen microscopique) doit être effectué quotidiennement jusqu’à ce que les parasites ne soient plus détectables au microscope dans le sang et que le nadir plaquettaire soit surmonté. «Les tests rapides et la PCR ne sont pas appropriés pour le suivi, car ils restent tous deux positifs pendant des semaines (test rapide) à des mois (PCR)», a souligné A.Neumayr.
Cas 2 – Fièvre de dengue
La Suissesse de 28 ans est rentrée il y a cinq jours d’un voyage de trois semaines en Thaïlande. Depuis deux jours, elle se plaint de fièvre, de fortes céphalées frontales et de myalgies. Depuis la veille, elle présente en outre un exanthème maculopapuleux généralisé. La tension artérielle est de 105/78mmHg, la fréquence cardiaque de 98battements/min et la température de 38,4°C. L’exanthème maculopapuleux couvre le tronc et les extrémités. L’examen de laboratoire révèle une thrombocytopénie (65000/µl) et une CRP élevée (28mg/l).
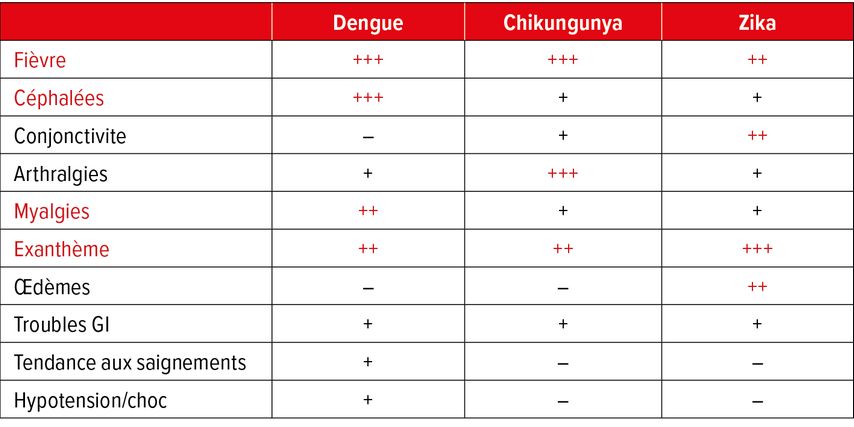
La constellation de fièvre, d’exanthème et de thrombocytopénie parle en faveur d’une infection virale, plus concrètement d’une arbovirose – là encore, la dengue est la plus probable. Les trois arbovirus les plus fréquents sont la dengue, ainsi que le chikungunya et le Zika, dont les symptômes typiques diffèrent légèrement (Tab. 1). La fièvre et les céphalées sont les symptômes cardinaux de la dengue. Des myalgies, des arthralgies et un exanthème peuvent survenir, mais la douleur n’est pas aussi intense ni autant focalisée sur les petites articulations que dans le cas du chikungunya. La période d’incubation (< 14 jours) est plausible pour la dengue chez cette femme, tout comme l’épidémiologie et le risque d’infection (piqûre de moustique).
Lors du diagnostic, même si l’exanthème plaide en sa défaveur, il convient d’exclure un paludisme (éventuellement comorbide) par un examen microscopique et un test rapide. En ce qui concerne la dengue elle-même, il existe un test double qui peut détecter à la fois l’antigène NS1 (positif chez cette patiente) ainsi que les anticorps IgM et IgG (encore négatifs chez cette patiente). Une PCR de la dengue à partir d’un prélèvement sanguin n’est utile que pendant les trois ou quatre premiers jours, car l’ARN du virus n’est pratiquement plus détectable dans le sang par la suite. En revanche, les antigènes NS1 sont détectables plus longtemps et, à partir du jour 4 ou 5, les anticorps IgM et, par la suite, IgG deviennent également positifs.
L’évolution de la fièvre de dengue est relativement homogène. Les trois premiers jours constituent la phase fébrile avec virémie, mais le patient n’est pas en danger pendant cette période. Les jours 4 et 5 constituent la phase critique, car c’est à ce moment que le choc circulatoire, les hémorragies et la défaillance viscérale peuvent survenir. «La prudence est de mise à ce stade, surtout lorsque la fièvre baisse et que les taux de thrombocytes et de leucocytes chutent», a averti le spécialiste. La phase de récupération commence à partir du jour 6.
Les critères d’une dengue sévère sont une fuite de plasma sévère, une hémorragie sévère et des troubles organiques sévères. «La plupart des patients n’ont toutefois pas besoin d’être hospitalisés, même dans la phase critique, il suffit généralement de les voir tous les jours», a nuancé A.Neumayr.
La dengue non compliquée est traitée en ambulatoire. Le traitement est symptomatique et comprend notamment du paracétamol (ou de l’ibuprofène) PO. L’acide acétylsalicylique est interdit en raison du risque d’hémorragie. La dengue sévère doit faire l’objet d’une hospitalisation, la priorité étant donnée au remplacement liquidien; une gestion des hémorragies et de la coagulation peut également être nécessaire, ainsi que, le cas échéant, des mesures de soins intensifs.
Cas 3 – Rickettsiose
Ce Suisse de 44 ans est rentré il y a deux jours d’Afrique du Sud, où il a effectué un safari de 7 jours dans le parc national Kruger. Depuis son retour, il se plaint de symptômes pseudo- grippaux, de céphalées et de douleurs articulaires. Sa température est de 37,8° C et il présente un exanthème maculopapuleux disséminé, une seule lésion cutanée avec nécrose centrale sur la jambe droite (escarre) et une lymphadénopathie palpable au niveau de l’aine droite. La CRP est de 45mg/l, les thrombocytes de 73000/µl, la créatinine et les transaminases sont normales.
En cas de fièvre, d’exanthème, de lésion cutanée focale et de thrombocytopénie, le diagnostic différentiel se porte sur une rickettsiose.
Dans ce cas également, il convient d’exclure en outre un paludisme. Une PCR à partir d’un échantillon prélevé au bord de l’escarre confirme une rickettsiose chez ce patient. Le traitement est le suivant: 2x 100mg de doxycycline/j pendant 7 jours.
Last, not least: la trypanosomiase
«Il existe une deuxième combinaison de fièvre et de lésion cutanée qu’il faut connaître: il s’agit du chancre de la maladie du sommeil (ou trypanosomiase africaine) à l’endroit de la morsure de la mouche tsé-tsé», a poursuivi A. Neumayr. Cette infection est typique de l’Afrique subsaharienne et se divise en forme à Trypanosoma brucei gambiense en Afrique de l’Ouest et en forme à Trypanosoma brucei rhodesiense en Afrique de l’Est. La forme de trypanosomiase d’Afrique de l’Ouest présente une évolution plutôt lente, tandis que celle d’Afrique de l’Est est beaucoup plus agressive. Le diagnostic est souvent posé par examen microscopique, lors de la recherche d’agents pathogènes du paludisme. Le traitement dépend de l’âge, du poids, du tableau clinique, du type d’agent pathogène et de la disponibilité des médicaments.
Source:
FOMF Allgemeine Innere Medizin Update Refresher, 16 novembre 2023, Zürich
Littérature:
auprès de l’intervenant
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...