Blick in die Zukunft der MS-Diagnose und -Therapie
Bericht:
Dr. Alexander Kretzschmar
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Auf der 40. ECTRIMS-Jahrestagung standen wichtige Themen wie die neuen McDonald-Kriterien zur MS-Diagnose sowie neue krankheitsmodifizierende Therapien der unterschiedlichen MS-Verlaufsformen auf der Agenda. Positive Nachrichten gibt es für Mütter mit hochaktiver MS in der Stillperiode. Intensiv diskutiert wurde auch der Einsatz der Blut-basierten Biomarker Serum-Neurofilament-Leichtketten (sNfL) und sGFAP (Serum Glial Fibrillary Acidic Protein). Hier gibt es wachsende Erfahrungen vor allem aus den großen MS-Zentren.
Revision der McDonald-Kriterien 2024 vorgestellt
Zu Beginn der ECTRIMS-Jahrestagung stellte Prof. Xavier Montalban, Barcelona, die inzwischen konsentierten Vorschläge für eine Revision der McDonald-Kriterien vor. Sie wurden von einem internationalen Advisory Committee on Clinical Trials in MS mit 55 MS-Expert:innen aus 16 Ländern auf einer Sitzung Ende 2023 erstellt. Mit der finalen Diskussion sowie der endgültigen Verabschiedung und Publikation der McDonald-Kriterien 2024 rechnet Montalban bis Anfang 2025.1
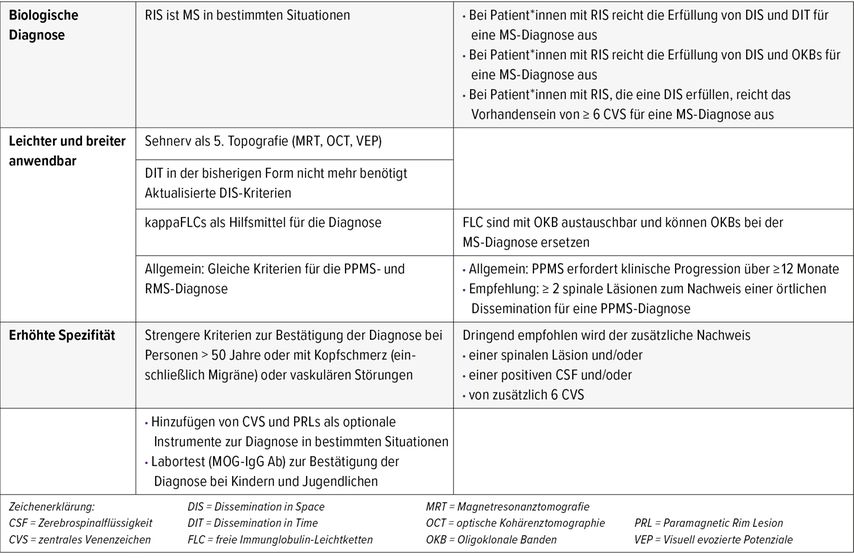
Tabelle 1 zeigt die wesentlichen Änderungen. In den neuen McDonald-Kriterien 2024 werden neue Biomarker berücksichtigt, beispielsweise zentrales Venenzeichen (CVS), paramagnetische Randläsion (PRL), kappa-freie Immunglobulin-Leichtketten (kappaFLC) oder visuell evozierte Potenziale und optische Kohärenztomografie (OCT). Gleichzeitig wurden die Kriterien für die räumliche Dissemination (DIS) erweitert, der Nachweis einer zeitlichen Dissemination (DIT) ist in der bisherigen Form nicht mehr erforderlich. Dadurch sollen die Möglichkeiten einer biologisch fundierten Diagnose der MS erweitert und breiter anwendbar werden. Außerdem kann die Diagnose in ausgewählten Fällen besser spezifiziert werden, so Montalban. Erleichtert werden soll auch die Diagnose einer MS bei Zufallsbefunden im MRT.1
Aktualisierte Kriterien zur räumlichen Dissemination
Der Sehnerv kann als 5. anatomischer Ort zum Nachweis einer DIS dienen, wenn es keine bessere Erklärung für die Pathologie des Sehnervs gibt. Eine DIS ist erfüllt, wenn zwei von fünf Regionen betroffen sind, unabhängig davon, ob diese Läsionen symptomatisch sind. Bei Patient:innen mit typischen Symptomen und typischen Läsionen in einer Region reicht das Vorhandensein von sechs CVS oder PRL und DIT oder positivem Liquorbefund aus, um eine DIS nachzuweisen. FLC sind mit OKB austauschbar und können OKB bei der MS-Diagnose ersetzen. Vorsicht sollte man bei älteren und vaskulär komorbiden Patient:innen walten lassen.1
Generell gelten die revidierten Kriterien auch für Kinder. Zusätzlich sollte von einer MS ausgegangen werden, wenn sich in der Hälfte der Läsionen CVS zeigen. Im Alter <12 Jahren sowie bei älteren Kindern mit atypischer Präsentation ist die Testung auf Antikörper gegen das Myelin-Oligodendrozyten-Glykoprotein (MOG-IgG Ab) für eine MOG-Enzephalomyelitis sinnvoll. Die McDonald-Kriterien 2024 sollten auch für die Diagnostik einer primär progredienten MS (PPMS) gelten. Erforderlich ist hier der Nachweis einer klinischen Progression über ≥12 Monate sowie zum Nachweis der DIS ≥2 spinale Läsionen.1
Neue Therapiestudien mit Licht und Schatten
In den „late-breaking oral presentations“ wurden mehrere Phase-III-Studien zu neuen Wirkstoffen vorgestellt. Für den Inhibitor der Bruton-Tyrosinkinase (BTKi) Tolebrutinib wurden Daten der placebokontrollierten Phase-III-Studie HERCULES zur Therapie der inaktiven schubfreien sekundär progressiven MS (SPMS) sowie in den Phase-III-Studien GEMINI I und II bei Patient:innen mit schubförmiger MS (RMS) vorgestellt. Die MS-STAT2-Studie untersuchte die Therapie mit Simvastatin bei Patient:innen mit nichtaktiver, schubfreier SPMS.
Tolebrutinib bei der inaktiven SPMS und RMS
Randomisiert wurden in HERCULES 1131 Patient:innen (Tolebrutinib: n=754 bzw. Placebo: n=377: im Mittel 48,9 Jahre; 60,2% bzw. 64,2% Frauen; EDSS im Mittel 5,49 bzw. 5,59). Primärer Endpunkt war die nach 6 Monaten bestätigte Behinderungsprogression (6mCDP). Hier reduzierte Tolebrutinib nach 45 Monaten das Risiko für eine 6mCDP gegenüber Placebo um 31% (Tolebrutinib: 26,9%; Placebo: 37,2%; p=0,0026), berichtete Prof. Robert J. Fox, Cleveland. Auch bei den sekundären Endpunkten der nach 3 Monaten bestätigten Behinderungsprogression (3mCDP) und der nach 6 Monaten bestätigten Verringerung der Behinderungsprogression (6mCDI) erwies sich Tolebrutinib als signifikant überlegen (3mCDP: –24%; Tolebrutinib: 32,6%; Placebo: 41,5%; p=0,013; 6mCDI: Tolebrutinib: 10,0%; Placebo: 5%; p=0,021). Auch bei neuen/sich vergrößernden T2-Läsionen ergab sich ein signifikanter Unterschied zugunsten des BTKi: (p=0,011). Kein Unterschied bestand beim Verlust des Hirnvolumens (BVL: p=0,16). „HERCULES zeigt als erste klinische Studie eine Verlangsamung der Behinderungsprogression bei der inaktiven, schubfreien SPMS“, fasste Fox die Wirksamkeitsdaten zusammen.2
Die Primäranalyse des Sicherheitsprofils zeigte für einige unerwünschte Ereignisse (UE) einen Anstieg gegenüber Placebo, beispielsweise Covid-19-Infektionen (25,5% vs. 22,7%), Nasopharyngitis (9,3% vs. 6,9%), Arthralgie (6,5% vs. 51,%), Influenza (5,6% vs. 3,5%) Hypertonie (5,1% vs. 2,9%). Ferner kam es zu einem leichten Anstieg der schweren unerwünschten Ereignisse (SUE: Tolebrutinib 15%; Placebo 10%). Leberenzymerhöhungen um mehr als das Dreifache der oberen Normschwelle (ULN) traten unter Tolebrutinib in 4,1% der Fälle vs. 1,6% (Placebo) auf. 0,5% der Teilnehmer:innen entwickelten unter dem BTKi ALT-Erhöhungen um mehr als das 20-Fache des ULN (Placebo: 0%) in den ersten 90 Tagen nach Therapiebeginn. Sie normalisierten sich in den meisten Fällen folgenlos, so Fox.2
In den beiden Ereignis-getriebenen, aktiv kontrollierten, parallelen Phase-III-Studien GEMINI I und II wurden die Teilnehmer:innen mit einer RMS (EDSS bei Baseline im Mittel 2,42 bzw. 2,37) entweder mit Tolebrutinib 60 mg oral (zusammen n=933) oder Teriflunomid 14mg (zusammen n=940) behandelt. Der primäre Endpunkt war die Reduktion der jährlichen Schubrate; sekundäre Endpunkte waren u.a. die Zunahme bzw. Abnahme der Behinderung (6mCDW, 3mCDW bzw. 6mCDI).3
Beim primären Endpunkt zeigte sich kein Unterschied zwischen dem Tolebrutinib-Arm und dem Teriflunomid-Arm (gepoolt jeweils 0,12; p=0,80). Die Schubraten waren in beiden GEMINI-Studien insgesamt auffällig niedrig. Bei den MRT-Endpunkten war Tolebrutinib entweder dem Teriflunomid signifikant unterlegen (neue Gd+ T1-Läsionen) oder vergleichbar (neue/sich vergrößernde T2-Läsionen). Bei den sekundären Endpunkten war Tolebrutinib jedoch gegenüber Teriflunomid signifikant überlegen. Bei der 6mCDW reduzierte Tolebrutinib das Risiko für Behinderungsprogression um 29% (Tolebrutinib: 9,9%; Placebo: 13,2%; p=0,023) und bei der 3mCDW um 27% (Tolebrutinib: 14,7%; Placebo: 18,5%; p=0,018). Zum Hirnvolumenverlust zeigte Tolebrutinib in GEMINI I signifikant weniger Hirnatrophie (p=0,0002), während in GEMINI II keine Unterschiede zu Teriflunomid bestanden.3
Das Sicherheitsprofil war konsistent mit demjenigen in HERCULES. Auch hier gab es in den ersten 90 Tagen der Therapie unter Tolebrutinib Leberenzymerhöhungen (ALT-Erhöhungen um mehr als das 20-Fache des ULN in 0,5% vs. 0,1% unter Placebo).3
Fazit: Tolebrutinib führte bei der RMS im Vergleich zu Teriflunomid zu einer signifikanten Reduktion der Behinderungsprogression, bestätigt nach 3 und 6 Monaten trotz fehlender Überlegenheit bei der Schubratenreduktion. Die Ergebnisse lassen laut Prof. Jiwon Oh, Toronto, viele Fragen offen. Sie unterstützen aber die Hypothese, dass die akuten fokalen Entzündungsvorgänge und die schleichende („smoldering“) Neuroinflammation zwei voneinander unterschiedliche biologische Prozesse sind.3
Simvastatin enttäuscht
Nach den positiven Ergebnissen der Phase-IIb-Studie MS-STAT sorgten die Daten der randomisierten, doppelblinden, placebokontrollierten Phase-III-Studie MS-STAT2 für Enttäuschung. In der Phase-IIb-Studie reduzierte die Therapie mit Simvastatin 80mg/qd bei 140 SPMS-Patient:innen nach zwei Jahren das Ganzhirnvolumen im Vergleich zu Placebo signifikant um im Mittel 43% (p=0,003). In MS-STAT2 mit 964 Patient:innen (im Mittel 54 Jahre) mit nichtaktiver, schubfreier SPMS war der primäre Studienendpunkt die Zeit bis zu einer bestätigten EDSS-Behinderungsprogression. Nach 48 Monaten bestand zwischen der Simvastatin-Gruppe (140 Progressionsereignisse) und Placebo (133 Ereignisse) kein signifikanter Unterschied (Hazard-Ratio [HR]: 1,13; 95% Konfidenzintervall [KI]: 0,91–1,39; p=0,26). Die Schubrate (sekundärer Endpunkt) war unter Placebo mit 68 Ereignissen signifikant geringer als unter Simvastatin (98 Ereignisse; p=0,04). In der Covid-19-Gruppe gab es kein Signal für eine Überlegenheit von Simvastatin, so Erstautor Prof. Jeremy Chataway, London. In der Studie gab es keine unerwarteten schweren unerwünschten Ereignisse (SAE); in einem Fall trat in der Simvastatin-Gruppe eine Rhabdomyolyse auf.4
AntiCD20-Therapie prä- und postpartum
Die meisten verfügbaren krankheitsmodifizierenden Therapien (DMT) sind nicht zum Einsatz während der Schwangerschaft oder der Stillzeit zugelassen. Vorgestellt wurden jetzt Analysen der beiden offenen Phase-IV-Studien MINORE und SOPRANINO zur B-Zell-Konzentration und dem plazentaren Transfer von Ocrelizumab während der Schwangerschaft sowie zur Exposition in der Muttermilch und in den Babys. Primärer Studienendpunkt von MINORE war der Anteil von Babys mit B-Zell-Spiegeln unterhalb der unteren Normschwelle (ULN) in der 6. Lebenswoche. Hier war kein Ocrelizumab im Nabelschnurblut zum Zeitpunkt der Geburt bei 32/34 Müttern (94,3%) sowie nach 6 Wochen im Blut der Babys bei 97,1% (32/33) nachweisbar. Nach 6 Wochen lagen die B-Zell-Siegel bei allen Babys im Normbereich.5
Die SOPRANINO-Studie untersuchte erstmals prospektiv die pharmakodynamischen Effekte von Ocrelizumab in der Muttermilch von 13 stillenden Frauen mit MS oder CIS. Die Mütter erhielten die erste Infusion frühestens nach 2 Wochen. 46% der Babys erhielten nur Muttermilch. Ko-primäre Endpunkte waren der Anteil der Kinder mit B-Zell-Zahlen unterhalb des ULN im Blut 30 Tage nach der ersten post-partum Ocrelizumab-Infusion der Mutter sowie die in der Muttermilch nachweisbare tägliche Ocrelizumab-Dosis. Die relative Ocrelizumab-Dosis für die Neugeborenen in der Muttermilch war mit 0,3–0,8% vernachlässigbar und Ocrelizumab im Serum der Babys nicht nachweisbar (unterhalb der Nachweisgrenze von 156ng/ml). Auch hier lagen die B-Zell-Siegel nach 6 Wochen bei allen Babys im Normbereich.6 Die Erstautorin Prof. Riley Bove, San Francisco, wertete die Ergebnisse der beiden Studien als positives Zeichen für stillende Mütter mit hochaktiver RMS.
Blutbasierte Biomarker – Tipps für die Praxis
Bei einem Symposium diskutierten MS-Expert:innen über ihre Erfahrungen mit Blut-basierten Biomarkern im Routineeinsatz.7 Insgesamt sind sNfL vor allem mit einer akuten Neuroinflammation assoziiert, sie korrelieren mit dem Ausmaß des neuroaxonalen Schadens und der künftigen Behinderungsprogression. Das sGFAP ist vor allem mit der nichtentzündlichen Progression assoziiert. Langzeit-Messungen der Swiss Multiple Sclerosis Cohort Study Group zeigen hierzu einen signifikant deutlicheren Rückgang der sNfL-Z-Scores über die Zeit unter HET-Antikörpern im Vergleich zu den Plattform-Immuntherapien.8 Damit wird eine individuelle Vorhersage des Krankheitsverlaufes und des Ansprechens auf eine DMT möglich, stellte Prof. Amit Bar-Or, Philadelphia, fest. Erhöhte Werte weisen auf ein höheres Risiko für eine kurz- und langfristige entzündungsbedingte Progression hin. Einig sind sich die Expert:innen, dass sich das sNfL-Monitoring in der Praxis etablieren wird, während das sGFAP erst einmal der Forschung vorbehalten bleibt. Die prognostische Aussagekraft könnte aber deutlich steigen, wenn sNfL und sGFAP kombiniert würden.
Die sNfL sind ein nützliches zusätzliches Werkzeug zur Therapieentscheidung. Ein sNfL-Anstieg besitzt jedoch eine andere Zeitkinetik, als das MRT aufzeigt, merkte Prof. Stefan Bittner, Mainz, an. „Das sNfL wird vor dem MRT auffällig.“ Für Bar-Or ist die sNfL-Bestimmung nützlich etwa bei Patient:innen mit unklarem Bild oder zur Unterscheidung zwischen echten und Pseudoschüben. Bei einem hohen sNfL sollte man zeitnah ein MRT durchführen, auch wenn dies aktuell nicht vorgesehen ist, riet Bittner. Persistierend hohe sNfL-Werte deuten laut Bar-Or auf eine starke schubunabhängige Progression hin (PIRA; Progression Independent of Relapse Activity).9 Das Routine-sNfL-Monitoring sollte alle 3–6 Monate erfolgen, empfahlen die Expert:innen.
Dr. Enric Monreal, Madrid, stellte eine 12-monatige Beobachtungsstudie an 13 Kliniken in Großbritannien vor. Ausgewertet wurden Blutproben (sNfL und sGFAP) von 725 Patient:innen. Für die Praxis ergibt sich daraus:
-
Patient:innen mit niedrigem sNfL (und niedrigem sGFAP) können mit Plattform-DMT oder hocheffektiven Therapien (HET) behandelt werden.
-
Patient:innen mit niedrigem sNfL und hohem sGFAP können mit allen verfügbaren DMT behandelt werden, sind aber auch Kandidaten für die in klinischen Studien untersuchten Inhibitoren der Bruton-Tyrosinekinase (BTKi) und
-
Patient:innen mit hohem sNfL sind optimale Kandidaten für den frühen Einsatz von HET.10
Quelle:
40. Jahrestagung des European Committee for Treatment and Research in Multiple Sclerosis (ECTRIMS), 18.–20. September 2024, Kopenhagen
Literatur:
1 Montalban X et al.: Revised McDonald criteria 2023. ECTRIMS 2024; Abstract O012 2 Fox RJ et al.: Efficacy and safety of tolebrutinib versus placebo in non-relapsing secondary progressive multiple sclerosis: results from the phase 3 HERCULES Trial. ECTRIMS 2024; Abstract O136 3 Oh J et al.: Efficacy and safety of tolebrutinib versus teriflunomide in relapsing multiple sclerosis: results from the phase 3 GEMINI 1 and 2 trials. ECTRIMS 2024; Abstract O135 4 Chataway J et al.: Evaluating the effectiveness of simvastatin in slowing the progression of disability in secondary progressive multiple sclerosis (MS-STAT2 trial): a multicentre, randomised placebo-controlled, double-blind, phase 3 clinical trial. ECTRIMS 2024; Abstract O134 5 Hellwig K et al.: B-cell levels and placental transfer in infants potentially exposed to ocrelizumab during pregnancy: Primary analysis of the prospective multicentre, open-label Phase IV MINORE study. ECTRIMS 2024; Abstract P087 6 Bove R et al.: B-cell levels and breastmilk transfer in infants of lactating women with multiple sclerosis treated with ocrelizumab: Primary results of the prospective multicenter, open-label Phase IV study SOPRANINOECTRIMS 2024; Abstract O039 7 Satellitensymposium “The now and future of MS care: Integrating high-efficacy therapies, biomarkers und novel treatment targets”. ECTRIMS 2024; Sponsor: Novartis Corporation, New York 8 Benkert P et al.: Serum neurofilament light chain for individual prognostication of disease activity in people with multiple sclerosis: a retrospective modelling and validation study. Lancet Neurol 2022; 21(3): 246-57 9 Bar-Or A et al.: Blood neurofilament light levels predict non-relapsing progression following anti-CD20 therapy in relapsing and primary progressive multiple sclerosis: findings from the ocrelizumab randomised, double-blind phase 3 clinical trials. eBioMedicine 2023; 93: 104662 10 Monreal E et al.: Serum neurofilament light chain and glial fibrillary acidic protein levels at disease onset unveil immunological pathways of disability acquisition in multiple sclerosis. ECTRIMS 2024; Abstract O061
Das könnte Sie auch interessieren:
Wie lässt sich die Zeit bis zur Diagnose der amyotrophen Lateralsklerose verkürzen?
Die amyotrophe Lateralsklerose (ALS) gilt als unaufhaltsam fortschreitende neurodegenerative Erkrankung, die im Durchscnitt drei bis vier Jahre nach Symptombeginn mit dem Tod durch ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...