Hohe Therapiepersistenz und Therapiezufriedenheit unter Praxisbedingungen
Bericht: Dr. Therese Schwender
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine aktuelle Zwischenanalyse der nach der Zulassung von Zeposia® (Ozanimod) gestarteten deutschen Postmarketing-Studie OzEAN liefert vielversprechende Ergebnisse: Nach 12 Monaten zeigten sich unter Praxisbedingungen eine hohe Behandlungspersistenz und Therapiezufriedenheit sowie eine mit Studien vergleichbare Wirksamkeit und Sicherheit.1–11
Im Anschluss an die Zulassung von Zeposia® (Ozanimod) zur Behandlung von Erwachsenen mit einer schubförmig remittierend verlaufenden Multiplen Sklerose (RRMS) wurde in Deutschland mit OzEAN eine Postmarketing-Studie ins Leben gerufen.1 In diese prospektive, nichtinterventionelle Studie werden seit März 2021 deutschlandweit erwachsene Patient:innen mit bestätigter RRMS aufgenommen, um unter Praxisbedingungen ihre Therapiepersistenz gegenüber der Zeposia®-Behandlung (primärer Endpunkt) sowie die Wirksamkeit, Sicherheit und verschiedene PROs («patient-reported outcomes») zu bewerten.1
Hohe Persistenz und Zufriedenheit unter Praxisbedingungen
Die erste Zwischenanalyse mit Datenschnittpunkt 15. Juni 2023 ergab, dass 69,1% der 317 bisher eingeschlossenen Menschen mit RRMS Frauen waren.1 Das mittlere Alter betrug 39,6 Jahre, bei 40,7% waren seit der Diagnose RRMS weniger als 2 Jahre vergangen und gut ein Drittel (36,3%) der Patient:innen war therapienaiv (niedriger Anteil bedingt durch in Deutschland zugelassene Indikation). In diesem Kollektiv wurden nun die Persistenz sowie die Behandlungszufriedenheit, erhoben mithilfe des TSQM v1.4 (Treatment Satisfaction Questionnaire for Medication), erfasst.1 Dabei zeigte sich, dass nach 12 Monaten 81% der Teilnehmenden weiterhin unter Therapie mit Zeposia® waren.1 Die Behandlung wurde von 60 Patientinnen und Patienten abgebrochen, darunter von 16 aufgrund von behandlungsbedingten Nebenwirkungen. Die Zufriedenheit der Patient:innen mit der Zeposia®-Therapie erwies sich als hoch, besonders hoch in den Kategorien Verträglichkeit und Komfort.1
Mit Studien vergleichbare Wirksamkeit und Sicherheit
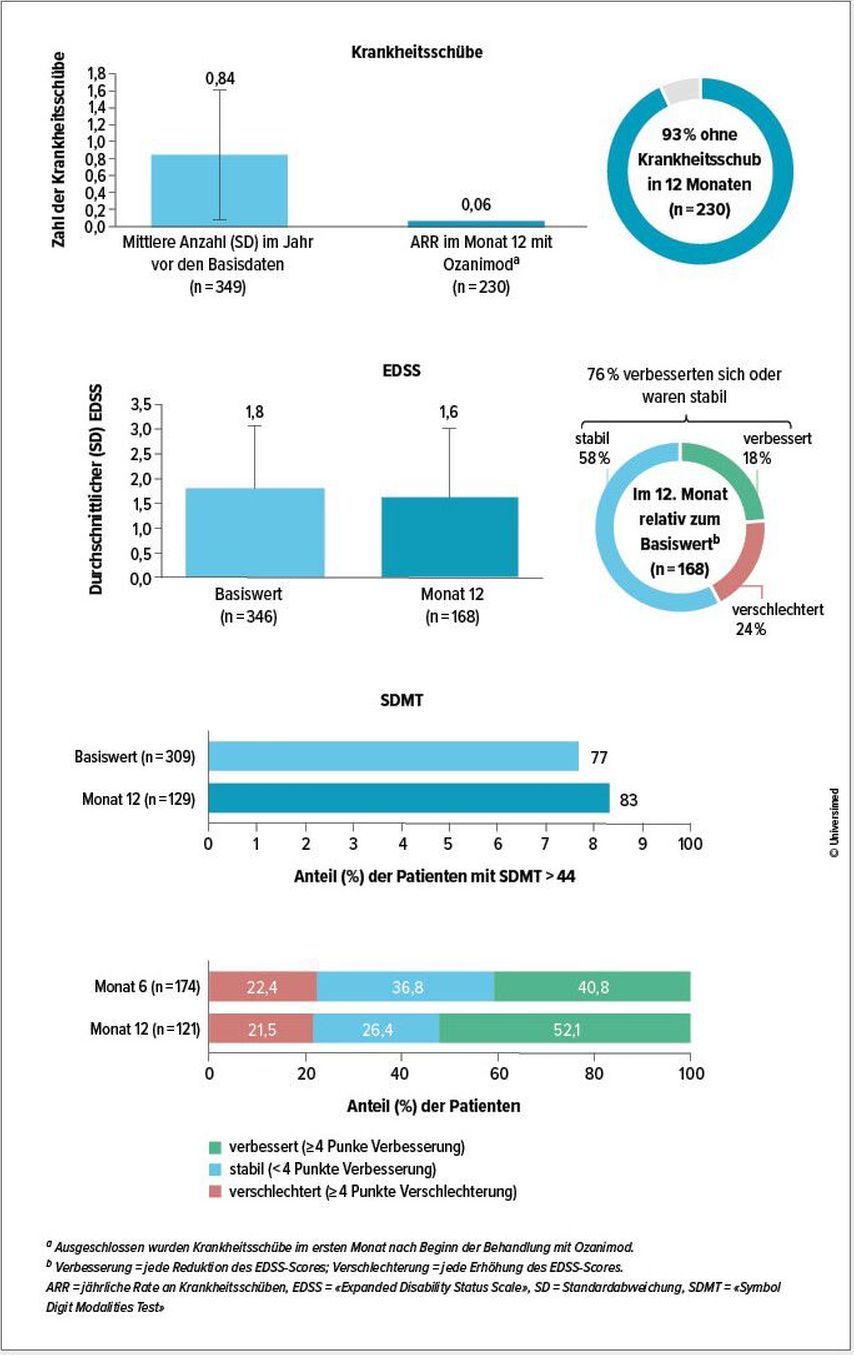
Die am ECTRIMS in Kopenhagen präsentierte aktuellste Analyse von OzEAN (Datenschnittpunkt: 15. März 2024, n=389) lieferte nun erstmals auch Daten in Bezug auf Wirksamkeit und Sicherheit von Zeposia® unter Alltagsbedingungen.2 Diese ergaben, dass nach einem Jahr die jährliche Schubrate bei 0,06 lag. Insgesamt 93% der Teilnehmenden (n = 230) waren während 12 Monaten schubfrei geblieben (Abb. 1).2 Der EDSS(«Expanded Disability Status Scale»)-Score erwies sich bei 76% der Teilnehmenden (n=168) als stabil oder verbessert gegenüber dem Ausgangswert (Abb. 1).2 Die kognitive Verarbeitungsgeschwindigkeit, gemessen mit dem SDMT («Symbol Digit Modalities Test»), hatte sich nach 12 Monaten (n=121) bei 52,1% der Patientinnen und Patienten um mindestens 4 Punkte verbessert und war bei 26,4% stabil geblieben (Abb. 1).2 Damit scheint die Wirksamkeit von Zeposia® im praktischen Alltag mit der in den klinischen Phase-III-Studien beobachteten Wirksamkeit übereinzustimmen.2–5
Abb. 1: Während der einjährigen Behandlung mit Zeposia® war die Schubrate niedrig und das Ausmass der Behinderung sowie die kognitive Verarbeitungsgeschwindigkeit blieben überwiegend stabil oder verbesserten sich2
Das allgemeine Sicherheitsprofil von Zeposia® in OzEAN stimmte ebenfalls mit den Resultaten der klinischen Studien überein.2–4,6 Lediglich die Rate an unerwünschten Ereignissen, die zum Abbruch der Behandlung führten, lag mit 6,9% der OzEAN-Teilnehmenden (27/389) höher als in den Studien. Solche Ereignisse werden jedoch generell in realen Kohorten tendenziell häufiger beobachtet als in klinischen Studien, wie dies auch die Daten zu anderen RRMS-Therapien zeigen.7–10
Fazit
Die Ergebnisse der Interimsanalyse der deutschen Postmarketing-Studie OzEAN unterstreichen das Potenzial von Zeposia® als eine im Alltag effektive und gut verträgliche Therapieoption für Menschen mit RRMS. So zeigten sich nach 12 Monaten eine hohe Behandlungspersistenz und -zufriedenheit, vor allem in den Kategorien Verträglichkeit und Komfort, sowie eine mit den klinischen Studien übereinstimmende Wirksamkeit und Sicherheit.1–11
Sponsored Content
Mit freundlicher Unterstützung durch Bristol Myers Squibb SA
2084-CH-2400123, 12/24
Literatur:
1 Ziemssen T et al.: Interim analysis of OzEAN: a prospective, noninterventional study to evaluate the utilization and effectiveness of ozanimod in clinical practice in patients with relapsing-remitting multiple sclerosis. ECTRIMS-ACTRIMS Oktober 2023, Mailand/I. P1458. 2 Buttmann M et al.: One-year real-world clinical effectiveness and safety of ozanimod for relapsing-remitting multiple sclerosis in Germany: an interim analysis of the prospective, non-interventional OzEAN study. ECTRIMS Oktober 2024, Kopenhagen/DK. P387. 3 Comi G et al.: Safety and efficacy of ozanimod versus interferon beta-1a in relapsing multiple sclerosis (SUNBEAM): a multicentre, randomised, minimum 12-month, phase 3 trial. Lancet Neurol 2019; 18: 1009-20 4 Cohen JA et al.: Safety and efficacy of ozanimod versus interferon beta-1a in relapsing multiple sclerosis (RADIANCE): a multicentre, randomised, 24-month, phase 3 trial. Lancet Neurol 2019; 18: 1021-33 5 DeLuca J et al. Effect of ozanimod on symbol digit modalities test performance in relapsing MS. Mult Scler Relat Disord. 2021; 48: 102673 6 Cree BA et al.: Long-term safety and efficacy of ozanimod in relapsing multiple sclerosis: Up to 5years of follow-up in the DAYBREAK open-label extension trial. Mult Scler. 2022; 28: 1944-62 7 Frisell T et al.: Comparative analysis of first-year fingolimod and natalizumab drug discontinuation among Swedish patients with multiple sclerosis. Mult Scler 2016; 22: 85-93 8 Cohen JA et al.: Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N Engl J Med 2010; 362: 402-15 9 Bucello S et al. Real world experience with teriflunomide in multiple sclerosis: the TER-Italy study. J Neurol 2021; 268: 2922-32 10 O’Connor P et al.: Randomized trial of oral teriflunomide for relapsing multiple sclerosis. N Engl J Med 2011; 365: 1293-303 11 Fachinformation Zeposia® (Ozanimod). www.swissmedicinfo.ch.
Gekürzte Fachinformation Zeposia® (Ozanimod)
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Für weitere Informationen siehe Fachinformation Zeposia® auf www.swissmedicinfo.ch .
I: Multiple Sklerose (MS): Indiziert zur Behandlung von erwachsenen Patienten mit schubförmig remittierend verlaufender MS. Colitis Ulcerosa (CU): Indiziert zur Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer aktiver CU, die entweder auf konventionelle Therapien oder die Behandlung mit einem Biologikum ungenügend angesprochen haben, nicht mehr ansprechen oder die Therapie nicht tolerierten. D: Hartkapseln 0.23/0.46/0.92 mg oral einmal täglich. Dosistitrationsschema: Tag 1–4: 0.23 mg; Tag 5–7: 0.46 mg; ab Tag 8: 0.92 mg. KI: Überempfindlichkeit gegen Wirk-/Hilfsstoffe; Behandlung nicht beginnen bei Patienten, die in den letzten 6 Monaten folgende Erkrankungen hatten: Myokardinfarkt, instabile Angina pectoris, Schlaganfall, transitorische ischämische Attacke, dekompensierte Herzinsuffizienz mit erforderlicher Hospitalisierung, Herzinsuffizienz Klasse III/IV, anamnestisch bekannter oder aktuell vorliegender atrioventrikulärer (AV) Block zweiten Grades (Typ II), AV-Block dritten Grades, sinuatrialer Block, Sinusknotensyndrom (ohne funktionstüchtigen Herzschrittmacher); schwere unbehandelte Schlafapnoe; immundefizienter Zustand; erhöhtes Risiko für opportunistische Infektionen; schwere aktive oder aktive chronische Infektionen (Hepatitis, Tuberkulose); aktive maligne Erkrankung; schwere Leberinsuffizienz; bestehendes Makulaödem; Schwangerschaft und bei Frauen im gebärfähigen Alter, die keine zuverlässige Methode zur Empfängnisverhütung anwenden. WH/VM: Vor Therapieeinleitung: kardiale Untersuchung (EKG), Leberfunktionstest, grosses Blutbild (BB), ophthalmologische und dermatologische Untersuchung, Untersuchung der Lungenfunktion bei Patienten mit schweren Lungenerkrankungen, Begleitmedikationen prüfen. Während der ersten Zeposia® Gabe kann es zu einer vorübergehenden Abnahme der Herzfrequenz kommen; bei Patienten mit vorbestehenden Herzerkrankungen ist eine Überwachung bei der ersten Gabe empfohlen. Erhöhungen von Aminotransferasen sind möglich und werden regelmässig überwacht. Zeposia® hat eine immunsuppressive Wirkung, die Patienten für ein Infektionsrisiko prädisponiert. Es sollte ein Sonnenschutz verwendet werden, keine gleichzeitige Phototherapie (UVB, PUVA-Photochemotherapie). Während der Behandlung sollten regelmässig ein BB, ein Leberfunktionstest, ein Blutdrucktest und eine augenärztliche Untersuchung bei Patienten mit Uveitis, Diabetes mellitus oder einer zugrundeliegenden/begleitenden Netzhauterkrankung durchgeführt werden. Bei bestätigter Gesamtlymphozytenzahl < 0.2 × 109/l oder bei bestätigtem Makulaödem Behandlung unterbrechen. Impfung gegen VZV ohne dokumentierte Immunität ≥ 1 Monat vor Beginn empfohlen. UW: Sehr häufig (≥ 10 %): Nasopharyngitis, Lymphopenie. Häufig (≥ 1 %, < 10 %): Pharyngitis, virale Atemwegsinfektion, Harnwegsinfektion, Herpes Zoster, Herpes simplex, Kopfschmerzen, Lungenfunktionstest abnormal, Bradykardie, Hypertonie, orthostatische Hypotension, ALT, GGT und Bilirubin erhöht, periphere Ödeme. P: Zeposia® Starterpackung: 7 Hartkapseln (4 × 0.23 mg, 3 × 0.46 mg); Zeposia® 0.92 mg: 28 Hartkapseln. Abgabekategorie B. Vollständige Fachinformation unter www.swissmedicinfo.ch . Bristol Myers Squibb SA, Hinterbergstrasse 16, 6312 Steinhausen. Stand der Information: März 2025.
Literatur auf Anfrage