Zeposia® senkt Hirnvolumenverlust auf Niveau der Allgemeinbevölkerung
Bericht: Dr. Therese Schwender
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Menschen mit Multipler Sklerose weisen gegenüber der Allgemeinbevölkerung einen höheren Verlust an Hirnvolumen auf.1 Cohen et al. haben nun anhand der Daten der Phase-III-Studien RADIANCE und SUNBEAM sowie ihrer offenen Verlängerungsphase DAYBREAK gezeigt, dass sich der Verlust an Hirnvolumen durch die bis zu 5 Jahre dauernde Behandlung mit Zeposia® (Ozanimod) deutlich und anhaltend reduzieren lässt.2
Während bei gesunden Personen das Hirnvolumen im Rahmen des normalen Alterungsprozesses um weniger als 0,4% pro Jahr abnimmt, können Menschen mit Multipler Sklerose (MS) einen höheren Hirnvolumenverlust aufweisen.1 Dieser beschleunigte Verlust geht mit einem höheren Risiko für eine Beeinträchtigung der kognitiven Funktionen, für ein Fortschreiten der körperlichen Behinderung und für eine geringere Lebensqualität einher.3–5
Zeposia® erhält das Hirnvolumen
Frühere Analysen der Daten der beiden Phase-III-Studien SUNBEAM (Studiendauer >12 Monate) und RADIANCE (Studiendauer 24 Monate) machten bereits deutlich, dass eine Behandlung mit Zeposia® (Ozanimod 0,92mg/Tag) im Vergleich zu intramuskulärem Interferon beta-1a (IFN beta-1a) bei Menschen mit schubförmig-remittierend verlaufender MS (RRMS) den Verlust an Gesamthirnvolumen (WBV), an Volumen der kortikalen grauen Substanz (CGMV) und an Thalamusvolumen (TV) signifikant zu reduzieren vermochte.6,7
Nachdem die Teilnehmenden von SUNBEAM und RADIANCE anschliessend in die offene Verlängerungsphase (OLE) DAYBREAK eingeschlossen und kontinuierlich mit Zeposia® weiterbehandelt bzw. von IFN beta-1a auf den S1P-Rezeptormodulator umgestellt werden konnten (n=2256), waren Cohen et al. nun in der Lage, den Verlauf des Hirnvolumenverlusts über einen Zeitraum von bis zu 5 Jahren weiter zu untersuchen (Daten-Cut-off: 7. April 2023).2
Hirnvolumenverlust auf normalem Niveau
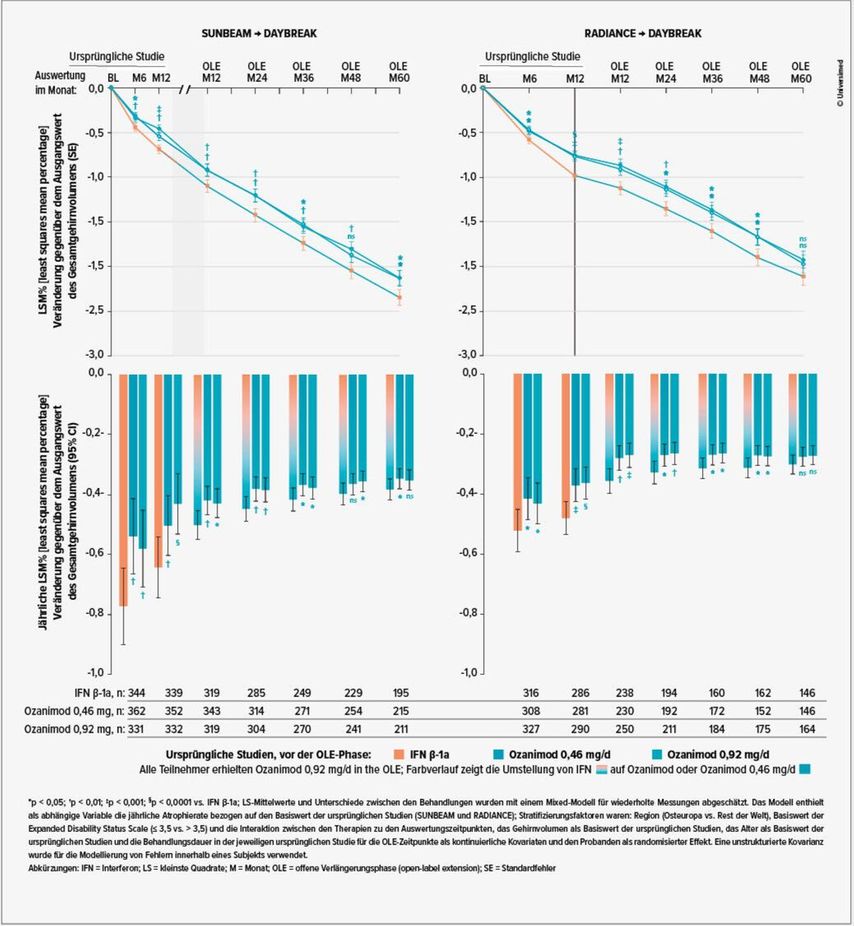
Wie die aktuelle Auswertung zeigte, wiesen diejenigen Studienteilnehmenden, die während SUNBEAM bzw. RADIANCE und bis zum Monat 60 der OLE kontinuierlich mit Zeposia® behandelt worden waren, eine stabile und niedrige Rate eines Verlusts an WBV auf (jährliche LSM%[least squares mean percentage]-Veränderung gegenüber dem Ausgangswert in RADIANCE bzw. SUNBEAM von –0,27 bzw. –0,35)(Abb. 1).2 Die mittlere jährliche Rate des Verlusts an WBV war mit 0,27 bei denjenigen Teilnehmenden mit der längsten kontinuierlichen Zeposia®-Therapie (2 Jahre in RADIANCE und 5 Jahre in der DAYBREAK OLE) niedriger als der Verlust bei gesunden Personen. Der Verlust an CGMV (–0,30) und TV (–0,57) fiel in der Studienpopulation ähnlich aus wie bei gesunden Kontrollpersonen (CGMV –0,28; TV –0,48).2
Abb. 1: Prozentuale (jährliche) Veränderungen im Gesamthirnvolumen während der Phase-III-Studien SUNBEAM und RADIANCE bis zum Monat 60 der offenen Verlängerungsphase DAYBREAK2
Deutliche Verbesserung nach Therapiewechsel
Im Weiteren analysierten Cohen et al. den Verlauf des Hirnvolumens bei denjenigen Studienteilnehmenden, die in SUNBEAM bzw. RADIANCE mit IFN beta-1a behandelt und zu Beginn der DAYBREAK OLE auf Zeposia® umgestellt wurden.2 Teilnehmende mit kontinuierlicher Zeposia®-Behandlung wiesen im Vergleich zu mit IFN beta-1a vorbehandelten Patientinnen und Patienten eine signifikant geringere jährliche LSM%-Reduktion im WBV auf (vom Ausgangwert der ursprünglichen Studie bis zum Monat 48 der DAYBREAK OLE [RADIANCE] bzw. bis zu Monat 60 der DAYBREAK OLE [SUNBEAM]).2
Bei den Teilnehmenden aus RADIANCE führte die Umstellung von IFN beta-1a auf Zeposia® zu einer Reduktion des Verlusts an WBV (jährliche LSM%-Veränderung zwischen RADIANCE-Ausgangwert und RADIANCE Monat 24 bzw. DAYBREAK- OLE-Ausgangswert und DAYBREAK OLE Monat 24: –0,48 bzw. –0,19).2 Ein ähnliches Muster liess sich bei den Teilnehmenden von SUNBEAM sowie für die jährliche LSM%-Veränderung im TV aufzeigen.
Beim CGMV ergab sich bei den mit IFN beta-1a behandelten Studienteilnehmenden eine hohe jährliche LSM%-Veränderung zwischen SUNBEAM-Baseline und Monat 12 bzw. zwischen RADIANCE-Baseline und Monat 24 (–1,02 bzw. –0,59).2 Zwölf Monate nach Umstellung auf Zeposia® im Rahmen der DAYBREAK OLE liess sich jedoch eine Umkehr dieses Trends beobachten (jährliche LSM%-Zunahme gegenüber DAYBREAK OLE von 0,10 bei Teilnehmenden aus SUNBEAM und 0,20 bei Teilnehmenden aus RADIANCE). Die weiteren Verluste an CGMV blieben auf niedrigem Niveau.2
Fazit
Die Behandlung von Menschen mit RRMS mit Zeposia® in den randomisierten Studien RADIANCE und SUNBEAM reduzierte die Raten eines Hirnvolumenverlusts im Vergleich zum Ausgangswert.2 Die mittlere jährliche Rate des Verlusts an WBV war mit 0,27 bei denjenigen Teilnehmenden mit der längsten kontinuierlichen Zeposia®-Therapie (2 Jahre in RADIANCE und 5 Jahre in der DAYBREAK OLE) niedriger als der Verlust bei gesunden Personen. Zudem wiesen Studienteilnehmende, die kontinuierlich mit Zeposia® behandelt wurden, einen geringeren WBV-Verlust im Vergleich zu denjenigen Personen auf, die von IFN beta-1a auf Zeposia® umgestellt wurden.1,2
Sponsored Content
Mit freundlicher Unterstützung durch Bristol Myers Squibb SA
2084-CH-2400122, 12/24
Quelle:
40. Jahrestagung des European Committee for Treatment
and Research in Multiple Sclerosis (ECTRIMS), 18.–20.
September 2024, Kopenhagen
Literatur:
1 Kappos L et al.: Inclusion of brain volume loss in a revised measure of ‚no evidence of disease activity‘ (NEDA-4) in relapsing-remitting multiple sclerosis. Mult Scler 2016; 22: 1297-305 2 Cohen JA et al.: Whole brain, cortical grey matter, and thalamic volume changes during 5–7 years of ozanimod in relapsing MS: final results from the DAYBREAK open-label extension study. ECTRIMS Oktober 2024, Kopenhagen/DK. P1623 3 Miyazaki Y et al.: Stages of brain volume loss and performance in the Brief International Cognitive Assessment for Multiple Sclerosis. Mult Scler Relat Disord 2022; 67: 104183 4 Uher T et al.: Evolution of brain volume loss rates in early stages of multiple sclerosis. Neurol Neuroimmunol Neuroinflamm 2021; 8: e979 5 Mowry EM et al.: Quality of life in multiple sclerosis is associated with lesion burden and brain volume measures. Neurology 2009; 72: 1760-5 6 Comi G et al.: Safety and efficacy of ozanimod versus interferon beta-1a in relapsing multiple sclerosis (SUNBEAM): a multicentre, randomised, minimum 12-month, phase 3 trial. Lancet Neurol 2019; 18: 1009-20 7 Cohen JA et al.: Safety and efficacy of ozanimod versus interferon beta-1a in relapsing multiple sclerosis (RADIANCE): a multicentre, randomised, 24-month, phase 3 trial. Lancet Neurol 2019; 18: 1021-33
Gekürzte Fachinformation Zeposia® (Ozanimod)
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Für weitere Informationen siehe Fachinformation Zeposia® auf www.swissmedicinfo.ch .
I: Multiple Sklerose (MS): Indiziert zur Behandlung von erwachsenen Patienten mit schubförmig remittierend verlaufender MS. Colitis Ulcerosa (CU): Indiziert zur Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer aktiver CU, die entweder auf konventionelle Therapien oder die Behandlung mit einem Biologikum ungenügend angesprochen haben, nicht mehr ansprechen oder die Therapie nicht tolerierten. D: Hartkapseln 0.23/0.46/0.92 mg oral einmal täglich. Dosistitrationsschema: Tag 1–4: 0.23 mg; Tag 5–7: 0.46 mg; ab Tag 8: 0.92 mg. KI: Überempfindlichkeit gegen Wirk-/Hilfsstoffe; Behandlung nicht beginnen bei Patienten, die in den letzten 6 Monaten folgende Erkrankungen hatten: Myokardinfarkt, instabile Angina pectoris, Schlaganfall, transitorische ischämische Attacke, dekompensierte Herzinsuffizienz mit erforderlicher Hospitalisierung, Herzinsuffizienz Klasse III/IV, anamnestisch bekannter oder aktuell vorliegender atrioventrikulärer (AV) Block zweiten Grades (Typ II), AV-Block dritten Grades, sinuatrialer Block, Sinusknotensyndrom (ohne funktionstüchtigen Herzschrittmacher); schwere unbehandelte Schlafapnoe; immundefizienter Zustand; erhöhtes Risiko für opportunistische Infektionen; schwere aktive oder aktive chronische Infektionen (Hepatitis, Tuberkulose); aktive maligne Erkrankung; schwere Leberinsuffizienz; bestehendes Makulaödem; Schwangerschaft und bei Frauen im gebärfähigen Alter, die keine zuverlässige Methode zur Empfängnisverhütung anwenden. WH/VM: Vor Therapieeinleitung: kardiale Untersuchung (EKG), Leberfunktionstest, grosses Blutbild (BB), ophthalmologische und dermatologische Untersuchung, Untersuchung der Lungenfunktion bei Patienten mit schweren Lungenerkrankungen, Begleitmedikationen prüfen. Während der ersten Zeposia® Gabe kann es zu einer vorübergehenden Abnahme der Herzfrequenz kommen; bei Patienten mit vorbestehenden Herzerkrankungen ist eine Überwachung bei der ersten Gabe empfohlen. Erhöhungen von Aminotransferasen sind möglich und werden regelmässig überwacht. Zeposia® hat eine immunsuppressive Wirkung, die Patienten für ein Infektionsrisiko prädisponiert. Es sollte ein Sonnenschutz verwendet werden, keine gleichzeitige Phototherapie (UVB, PUVA-Photochemotherapie). Während der Behandlung sollten regelmässig ein BB, ein Leberfunktionstest, ein Blutdrucktest und eine augenärztliche Untersuchung bei Patienten mit Uveitis, Diabetes mellitus oder einer zugrundeliegenden/begleitenden Netzhauterkrankung durchgeführt werden. Bei bestätigter Gesamtlymphozytenzahl < 0.2 × 109/l oder bei bestätigtem Makulaödem Behandlung unterbrechen. Impfung gegen VZV ohne dokumentierte Immunität ≥ 1 Monat vor Beginn empfohlen. UW: Sehr häufig (≥ 10 %): Nasopharyngitis, Lymphopenie. Häufig (≥ 1 %, < 10 %): Pharyngitis, virale Atemwegsinfektion, Harnwegsinfektion, Herpes Zoster, Herpes simplex, Kopfschmerzen, Lungenfunktionstest abnormal, Bradykardie, Hypertonie, orthostatische Hypotension, ALT, GGT und Bilirubin erhöht, periphere Ödeme. P: Zeposia® Starterpackung: 7 Hartkapseln (4 × 0.23 mg, 3 × 0.46 mg); Zeposia® 0.92 mg: 28 Hartkapseln. Abgabekategorie B. Vollständige Fachinformation unter www.swissmedicinfo.ch . Bristol Myers Squibb SA, Hinterbergstrasse 16, 6312 Steinhausen. Stand der Information: März 2025.
Literatur auf Anfrage