CAR-Ts & bispezifische AK: welche Daten bei älteren Patient:innen wichtig sind
Bericht:
Katarzyna Mühlbachler-Pietrzykowska, MRes
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Behandlung älterer Patient:innen mit CAR-T-Zell-Therapien und bispezifischen Antikörpern kann eine besondere Herausforderung darstellen. Prof. Dr. Marion Subklewe von der Ludwig-Maximilians-Universität München präsentierte auf der diesjährigen Jahrestagung der Deutschen, Österreichischen und Schweizerischen Gesellschaften für Hämatologie und Medizinische Onkologie zu dieser Thematik u.a. Real-World-Evidence-Daten und eine Metaanalyse zur „non-relapse mortality“.
Personalisierte Krebsbehandlung bei älteren Betroffenen
Hämatologische Malignome können zwar in jedem Alter auftreten, sind aber bei älteren Erwachsenen mit einem Durchschnittsalter von 70 Jahren zum Zeitpunkt der Diagnose häufiger anzutreffen.1 Die Krebsbehandlung bei diesen Patient:innen kann aufgrund von Komorbiditäten und Gesundheitsproblemen wie Herz-Kreislauf-Erkrankungen, eingeschränkter Nieren- und Leberfunktion, Polypharmazie und veränderter Körperzusammensetzung, zu denen häufig auch noch kognitive und psychologische Faktoren hinzukommen, eine Herausforderung darstellen. Ein individuell auf die/den jeweilige/n Patientin/Patienten zugeschnittener Ansatz ist daher unerlässlich.
Um die Fitness älterer Patient:innen mit Lymphomen besser beurteilen zu können, wurde das vereinfachte geriatrische Assessment (GA) entwickelt, das Alter, Aktivitäten des täglichen Lebens (ADL), instrumentelle ADL (IADL) und die Cumulative Illness Rating Scale-Geriatric (CIRS-G) umfasst. Darauf aufbauend kombiniert der Elderly Prognostic Index (EPI) das GA mit dem International Prognostic Index (IPI) und den Hämoglobinwerten, um die Patient:innen in drei Risikogruppen einzuteilen, wobei bei Patient:innen mit niedrigem Risiko ein Drei-Jahres-Gesamtüberleben (OS) von 87% erreicht wird, mehr als doppelt so viel wie bei Betroffenen mit hohem Risiko (42%).2 Trotz seiner Nützlichkeit wird das vereinfachte GA jedoch nur selten in klinischen Studien für CAR(„Chimeric Antigen Receptor“)-T- oder bispezifische Therapien bei Patient:innen mit rezidiviertem/refraktärem (r/r) B-Zell-Non-Hodgkin-Lymphom (B-NHL) eingesetzt.
Relevante Studiendaten
Axi-cel setzt neue Maßstäbe
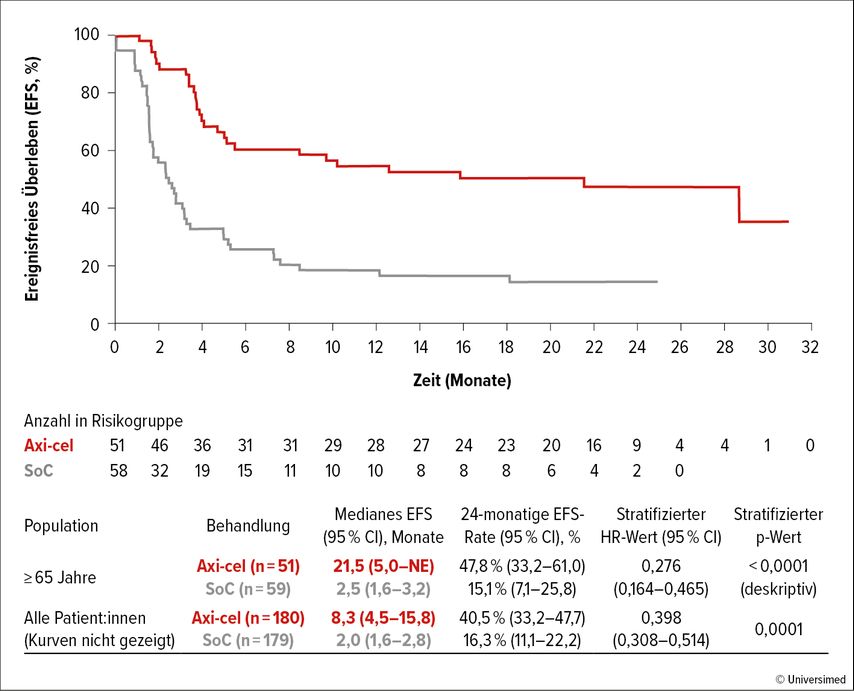
ZUMA-7 (NCT03391466) ist eine randomisierte Phase-III-Studie, in der Axicabtagen-Ciloleucel (Axi-cel) im Vergleich zur Standardtherapie (SoC) bei Patient:innen mit diffusem großzelligem B-Zell-Lymphom (DLBCL), die für eine autologe Stammzelltransplantation (ASCT) infrage kommen, untersucht wurde. Axi-cel verlängerte das ereignisfreie Überleben (EFS) signifikant und erreichte ein medianes EFS von 8,3 Monaten im Vergleich zu 2 Monaten in der SoC-Gruppe (HR: 0,398). Bei Betroffenen über 65 Jahren war der Vorteil für das EFS sogar noch ausgeprägter, mit einem Median von 21,5 Monaten für Axi-cel gegenüber 2,5 Monaten für SoC (HR: 0,276; Abb. 1). Die objektive Ansprechrate (ORR) war bei Axi-cel ebenfalls höher (83% gegenüber 50% bei SoC), einschließlich kompletter Ansprechraten (CR) bei 65% gegenüber 32%. Bei den Patient:innen über 65 Jahren betrug die ORR mit Axi-cel 88% gegenüber 52% mit SoC.3,4
Abb. 1: Axi-cel bei Patient:innen ≥65 Jahre mit r/r LBCL in der ZUMA-7-Studie (modifiziert nach Westin JR et al.)4
Die Phase-II-Studie Alycante(NCT04531046) untersuchte Axi-cel als Zweitlinientherapie bei Patient:innen mit aggressivem B-NHL, die für eine ASCT nicht infrage kommen. Sowohl das EFS als auch das progressionsfreie Überleben (PFS) waren in den verschiedenen Altersgruppen ähnlich, mit einem Median von 12,3 Monaten für das EFS und 11,8 Monaten für das PFS. Die ORR lag bei 90,3%, die Rate des kompletten metabolischen Ansprechens (CMR) bei 79%.5
Die Wirksamkeit von Liso-cel
TRANSFORM (NCT03575351), eine randomisierte Phase-III-Studie, verglich Lisocabtagen-Maraleucel (Liso-cel) mit SoC bei transplantationsfähigen Hochrisikopatient:innen mit r/r aggressivem B-NHL. Liso-cel verlängerte das mediane EFS signifikant auf 10,1 Monate gegenüber 2,3 Monaten in der SoC-Gruppe (HR: 0,35) und zeigte einen klinischen Nutzen in verschiedenen Untergruppen. Die CR-Rate war unter Liso-cel höher (66% gegenüber 39%), und auch die ORR war höher (86% gegenüber 48%). Das PFS war in der Liso-cel-Gruppe deutlich länger (HR: 0,41), mit weniger Progressionsereignissen und einer verlängerten Gesamtüberlebenszeit.6
Die Phase-II-Studie PILOT (NCT03483103) untersuchte die Wirksamkeit und Sicherheit von Liso-cel bei erwachsenen Patient:innen mit r/r aggressivem B-NHL, die für eine hämatopoetische Stammzelltransplantation nicht infrage kommen. In dieser Studie erreichten 80% der Betroffenen ein objektives Ansprechen, wobei 54% eine CR erreichten. Das mediane PFS aller Patient:innen betrug 9 Monate, während das mediane EFS 7,2 Monate betrug.7
Das Potenzial von bispezifischen Antikörpern bei r/r B-NHL
In einer offenen Phase-I/II-Studie (NCT03075696) wurde die Wirksamkeit von Glofitamab, sowohl allein als auch in Kombination mit Obinutuzumab, nach einer Vorbehandlung mit Obinutuzumab bei Patient:innen mit aggressivem r/r B-NHL evaluiert. Die Studie ergab eine ORR von 52% und eine CR-Rate von 39%, die über alle Altersgruppen hinweg gleich war. Das PFS lag nach sechs Monaten bei 46% und nach zwölf Monaten bei 37%, während das OS nach zwölf Monaten 50% erreichte.8
Die offene Phase-I/II-Studie EPCORE™-NHL-1-Studie (NCT03625037) mit Epcoritamab ergab bei Patient:innen mit r/r großzelligem B-Zell-Lymphom (LBCL) eine ORR von 63,1%, wobei 38,9% der Patient:innen eine CR erreichten. Das mediane PFS betrug 4,4 Monate. Die Ansprechraten variierten je nach Alter: Patient:innen unter 65 Jahren hatten eine ORR von 56,3%, die 65- bis 74-Jährigen eine ORR von 68,8% und die Betroffenen ab 75 Jahren eine ORR von 72,4%.9
Überschaubares Sicherheitsprofil
Die Raten des schweren Zytokinfreisetzungssyndroms (CRS) und des Immuneffektorzell-assoziierten Neurotoxizitätssyndroms (ICANS) variierten in den verschiedenen Studien. ZUMA-7 berichtete über CRS des Grades 3 oder höher bei 6% der Patient:innen und ICANS bei 21%, während Alycante 8% CRS und 14,5% ICANS aufwies. TRANSFORM berichtete über 1% CRS und 4% ICANS, während PILOT 1,6% CRS und 5% ICANS meldete. Unter den bispezifischen Therapien zeigte Glofitamab 4% für schweres CRS und 3% für ICANS und Epcoritamab 3% für CRS und 2,5% für ICANS.3–9
Die Daten aus der Praxis
Real-World Evidence (RWE) der GETH-TC/GELTAMO-Studiengruppe zeigt, dass die CAR-T-Zell-Therapie bei älteren Betroffenen sowohl sicher als auch wirksam ist und bei den unter 70-Jährigen (n=341) und den über 70-Jährigen (n=71) zu ähnlichen Ergebnissen führt. Einen Monat nach der Infusion lag die ORR bei 70% bei jüngeren und bei 69% bei älteren Patient:innen. Auch die CR-Raten waren ähnlich, mit 38% in der Gruppe der Jüngeren gegenüber 45% in der Gruppe der Älteren. Das OS und das EFS zeigten keine signifikanten Unterschiede zwischen den Altersgruppen. Darüber hinaus zeigte sich nach 12 Monaten bei 4% der jüngeren gegenüber 6% der älteren Betroffenen eine rezidivfreie Sterblichkeit („non-relapse mortality“, NRM), d.h. Tod aus beliebiger Ursache ohne vorheriges Rezidiv oder Fortschreiten der Erkrankung.10
Ein weiterer Beleg für die Wirksamkeit der CAR-T-Zell-Therapie bei älteren Patient:innen mit r/r LBCL sind die Erkenntnisse aus der GLA/DRST-Studie. Betroffene über 65 Jahren erreichten eine ORR von 69% und eine CR-Rate von 43%, verglichen mit 58% ORR und 31% CR in der Kohorte der Jüngeren. Die kumulative 12-Monats-Inzidenz der NRMwar jedoch bei Patient:innen über 65 Jahren höher (9% gegenüber 3% bei Patient:innen unter 65 Jahren; HR: 2,25).11
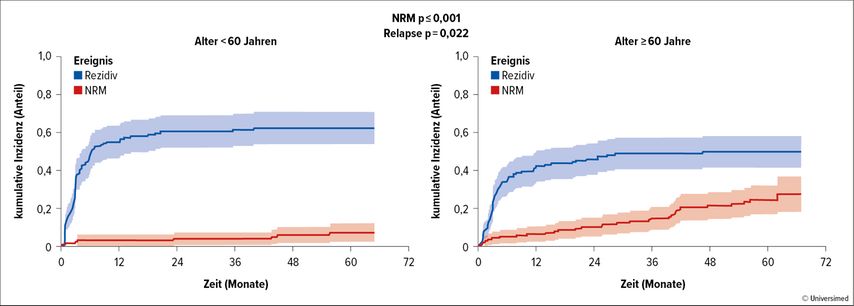
In einer Analyse von 275 LBCL-Betroffenen, die mit Axi-cel behandelt wurden, lag die ORR bei 82% und die CR-Rate bei 64%. Das mediane PFS betrug 8,7 Monate, während das mediane OS 34,9 Monate betrug. Von den 158 Todesfällen, die während der Nachbeobachtungszeit auftraten, waren drei Viertel auf einen Lymphomrückfall und ein Viertel auf NRM-Ereignisse zurückzuführen. Zu den häufigsten NRM-Ursachen gehörten Infektionen (52,5%) und sekundäre Malignome (22,5%). Bei Patient:innen im Alter von 60 Jahren und älter war die Wahrscheinlichkeit eines Lymphomrückfalls geringer, aber das Risiko einer NRM war höher (Abb. 2).12
Abb. 2: 5-Jahres-Follow-up von Axi-cel (SoC) bei LBCL-Patient:innen (modifiziert nach Jain MD et al.)12
„Non-relapse mortality“: Metaanalyse bei CAR-T-Zell-Patient:innen
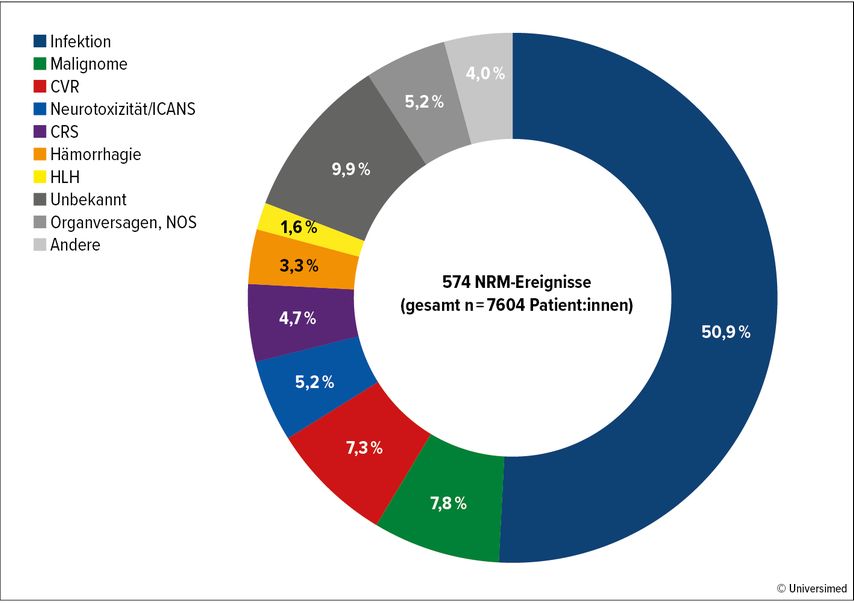
Um einen besseren Einblick in die NRM bei Lymphom- und Myelompatient:innen zu erhalten, die mit CAR-T-Zell-Therapien behandelt werden, führten die Wissenschaftler:innen eine umfassende Analyse durch, die 18 klinische Studien und 28 Real-World-Studien mit Daten von insgesamt 7604 Betroffenen umfasste (Abb. 3). Die Mehrheit dieser Patient:innen hatte ein LBCL (76,4%), gefolgt von Myelomen (15,7%), Mantelzell-Lymphomen (MCL) (4,5%) und indolenten Lymphomen (IL) (3,5%). Die Gesamt-NRM-Rate für alle Krankheiten betrug 6,8%, wobei MCL (10,6%) und Myelom (8%) höhere Raten aufwiesen als IL (5,7%) und LBCL (6,1%).
Abb. 3: In Nature Medicine publizierte Metaanalyse der „non-relapse mortality“ (NRM) bei Lymphom- und Myelompatient:innen, die mit CAR-T-Zell-Therapien behandelt worden waren (modifiziert nach Cordas dos Santos DM et al.)13
Etwa die Hälfte der Todesfälle ohne Rückfall war auf Infektionen zurückzuführen, wobei der Erreger in 35% dieser Fälle identifiziert wurde. Bei den Patient:innen mit bekanntem Erreger war Covid-19 die Hauptursache für 53,4% der Infektionen, gefolgt von Pilzinfektionen (19,4%), bakteriellen Infektionen (21,4%) und viralen Infektionen, die nicht auf Covid zurückzuführen waren (4,8%).
Sekundäre Malignome waren die zweithäufigste Ursache von NRM und trugen zu 7,8% der Todesfälle bei, wobei das myelodysplastische Syndrom (MDS) oder die akute myeloische Leukämie (AML) ein Drittel dieser Fälle ausmachten. An dritter Stelle rangierten kardiovaskuläre oder respiratorische Ereignisse (CVR), die 7,3% der Todesfälle ohne Rezidiv verursachten, vor allem aufgrund von Atemversagen (23,3%), thromboembolischen Ereignissen im ZNS (20,9%) und Herzstillstand (18,6%). Darüber hinaus waren 5,2% bzw. 4,7% der Todesfälle ohne Rezidiv auf CAR-T-Zell-bedingte Nebenwirkungen wie das ICANS und das CRS zurückzuführen.
Die Analyse ergab, dass Infektionen unter realen Bedingungen häufiger vorkamen und für 64,6% der Todesfälle verantwortlich waren, verglichen mit 59,1% in klinischen Studien. Immunbedingte Nebenwirkungen wie CRS, ICANS und hämophagozytische Lymphohistiozytose (HLH) traten in der Praxis doppelt so häufig auf und waren für 16,6% der Todesfälle verantwortlich im Vergleich zu 7,9% in klinischen Studien. Umgekehrt traten in klinischen Studien häufiger CVR-Ereignisse auf (16,5%) als unter realen Bedingungen (6,2%).13
In ähnlicher Weise berichtete das DESCAR-T-Register (Lysa-Studie) über eine NRM-Rate von 5% bei LBCL, wobei die meisten Fälle (81%) als späte NRM klassifiziert wurden, die nach dem 28. Tag auftraten. Tödliche akute Toxizitäten waren selten, und Infektionen waren mit 56,2% die häufigste Ursache für NRM.14
Hämatotoxizität bei CAR-T-Zell-Patient:innen
Eine multizentrische Analyse von 258 DLBCL-Betroffenen, die mit einer CAR-T-Zell-Therapie behandelt wurden, ergab, dass 72% eine ausgeprägte Neutropenie aufwiesen, die als absolute Neutrophilenzahl von weniger als 100 Zellen/ml definiert war. Außerdem hatten 64% dieser Patient:innen eine anhaltende Neutropenie, die 21 Tage oder länger andauerte.
Diese Zytopenien, einschließlich der anhaltenden Neutropenie, blieben häufig auch nach der Lymphdepletion und dem Abklingen des akuten CRS bestehen, wodurch sich das Risiko schwerer Infektionen erheblich erhöhte. Die Analyse zeigte auch ein biphasisches Muster der Neutropenie, das durch eine anfängliche vorübergehende Erholung des Blutbildes, gefolgt von einem „zweiten Dip“, gekennzeichnet ist. Die Thrombozytopenie hingegen erreichte ihren Tiefpunkt in der Regel im zweiten Monat.15
ICAHT-Einstufungkönnte Management der CAR-T-Zell-Therapie verbessern
Während die prophylaktischen Leitlinien auf der Tiefe und der Dauer der Neutropenie basieren, da das Infektionsrisiko mit beiden Faktoren zusammenhängt, erfasst die CTCAE-Einstufung die unterschiedlichen Muster der Neutrophilenerholung bei den Patient:innen nicht vollständig, da sie die Tiefe, nicht aber die Dauer der Neutropenie berücksichtigt.
Um diese Herausforderung zu bewältigen, haben die Europäische Gesellschaft für Blut- und Knochenmarktransplantation (EBMT) und die European Hematology Association (EHA) 36 CAR-T-Zell-Expert:innen einberufen, um Leitlinien für die beste Praxis zu entwickeln. Gemeinsam führten sie ein Klassifizierungssystem zur Einstufung der Immuneffektorzell-assoziierten Hämatotoxizität (ICAHT) mit den Stufen 1–4 ein. Bei frühen Zytopenien (Tage 0–30 nach der Behandlung) berücksichtigt das System sowohl die Tiefe als auch die Dauer der Neutropenie, während die späte ICAHT (nach Tag 30) ausschließlich nach dem Schweregrad der Neutropenie eingestuft wird.16
Die Anwendung dieses neuen ICAHT-Einstufungssystems auf eine Kohorte von 549 Patient:innen, die mit einer CAR-T-Zell-Therapie wegen r/r B-Zell-Malignomen behandelt wurden, ergab klare Muster bei der hämatologischen Erholung und den damit verbundenen Risiken. Der Schweregrad der ICAHT korrelierte mit der kumulativen Dauer der schweren Neutropenie, dem Vorhandensein von multilinearen Zytopenien und dem erhöhten Bedarf an Thrombozyten- und Erythrozytentransfusionen. Bei Patient:innen mit Mantelzell-Lymphom (MCL) war die Inzidenz von ICAHT Grad 3 oder 4 am höchsten (28%), verglichen mit Betroffenen mit LBCL (23%) und multiplem Myelom (MM, 15%). Schwere ICAHT war mit einer höheren Rate schwerer Infektionen (49% gegenüber 13%), einer erhöhten Sterblichkeit ohne Rezidiv (14% gegenüber 4%) und schlechteren Überlebensergebnissen (1-Jahres-PFS-Rate von 35% gegenüber 51% und Gesamtüberlebensrate von 52% gegenüber 73%) verbunden, was ihre kritischen Auswirkungen auf die Patient:innenergebnisse unterstreicht.17
Quelle:
„CART-Zellen und bispezifische Antikörper – Erfahrungen bei älteren Patienten“, Jahrestagung der Deutschen, Österreichischen und Schweizerischen Gesellschaften für Hämatologie und Medizinische Onkologie, 11. Oktober 2024, Basel
Literatur:
1 Smith A et al.: Br J Haematol 2010; 148(5): 739-53 2 Wallace DS et al.: Blood 2024; online ahead of print 3 Locke FL et al.: N Engl J Med 2022; 386(7): 640-54 4 Westin JR et al.: Clin Cancer Res 2023; 29(10): 1894-905 5 Houot R et al.: Nat Med 2023; 29(10): 2593-601 6 Kamdar M et al.: Lancet 2022; 399(10343): 2294-308 7 Sehgal A et al.: Lancet Oncol 2022; 23(8): 1066-77 8 Dickinson MJ et al.: N Engl J Med 2022; 387(24): 2220-31 9 Thieblemont C et al.: J Clin Oncol 2023; 41(12): 2238-47 10 Bailén R et al.:Transplant Cell Ther 2024; 30(10): 988.e1-11 11 Dreger P et al.: Bone Marrow Transplant 2023; 58(2): 229-32 12 Jain MD et al.: JClin Oncol 2024; 42(30): 3581-92 13 Cordas dos Santos DM et al.: Nat Med 2024; 30(9): 2667-78 14 Lemoine J et al.: Blood Adv 2023; 7(21): 6589-98 15 Rejeski K et al.: Blood 2021; 138(24): 2499-513 16 Rejeski K et al.: Blood 2023; 142(10): 865-77 17 Rejeski K et al.:Blood Adv 2024; 8(8): 1857-68
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...