Neue Therapieoption: O-Zanubrutinib
Autorin:
PD Dr. med. Karin Hohloch
Fachärztin für Medizinische Onkologie, Hämatologie und Allgemeine Innere Medizin
Klinik für Hämatologie und Onkologie Hirslanden Zürich
E-Mail: karin.hohloch@kho.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Kombinationstherapie Zanubrutinib plus Obinutuzumab verspricht gute Ergebnisse bei der Therapie des follikulären Lymphoms. In der Studie ROSEWOOD wurde sie untersucht – einen Überblick zur Studie bietet der folgende Artikel.
Das follikuläre Lymphom (FL) ist das zweithäufigste Non-Hodgkin-Lymphom (NHL) und macht etwa 5% aller hämatologischen Neoplasien aus.1 In den westlichen Ländern liegt die altersstandardisierte Inzidenzrate bei zwei bis vier FL-Fällen pro 100000 Menschen pro Jahr.
Die Entwicklungen in der Behandlung von FL, vor allem die Einführung der CD20-Antikörper (CD20-AK) und zuletzt die CAR-T-Zell-Therapie sowie die bispezifischen Antikörper haben zu einer signifikanten Verbesserung der Überlebensrate geführt.2–4 Trotz grosser Fortschritte in der Therapie ist das follikuläre Lymphom aber nach wie vor eine unheilbare Erkrankung mit kontinuierlichen Rezidiven und im Verlauf kürzeren krankheitsfreien Intervallen.
Ca. 80% aller Patient:innen haben einen indolenten Verlauf mit einer fast normalen Lebenserwartung, 20% der Patient:innen haben einen aggressiven Verlauf und erleiden frühe und häufige Rezidive und sterben meist am Lymphom.3 Die klinische Heterogenität der Erkrankung stellt eine Herausforderung dar, unter Berücksichtigung des Alters, der Komorbiditäten und der Wahrscheinlichkeit eines Rezidivs die richtige Therapie für den jeweiligen Zeitpunkt zu finden.4
Die ROSEWOOD-Studie
Die ROSEWOOD-Studie5 untersuchte die Wirksamkeit und Sicherheit der Kombinationstherapie Zanubrutinib plus Obinutuzumab (ZO) im Vergleich zur Monotherapie mit Obinutuzumab (O) bei Patient:innen mit rezidiviertem oder refraktärem follikulärem Lymphom (r/r FL), die zuvor mindestens zwei Therapielinien durchlaufen hatten.
Die Studie zielte darauf ab, neue therapeutische Möglichkeiten für Patient:innen zu entwickeln, bei denen Standardtherapien aufgrund von Rückfällen oder Resistenzen nicht mehr wirksam sind.
Studiendesign und Methodik
217 Patient:innen mit rezidiviertem oder refraktärem follikulärem Lymphom und mit einem ECOG-Performance-Status von 0–2 (Grad 1–3a), die ≥2 Therapien und einen CD20-AK erhalten haben, wurden in einer Phase-II-Studie 2:1 randomisiert.
Dabei erhielten 145 Patient:innen ZO und 72 O. In beiden Armen wurde das Obinutuzumab in einer Dosis von 1000mg an den Tagen 1, 8 und 15 in Zyklus 1 und an Tag 1 in Zyklus 2–6 gegeben, danach als Erhaltungstherapie 1x alle acht Wochen (20 Infusionen, zwei Jahre Erhaltungstherapie). Im Kombinationsarm wurde Zanubrutinib 2xtgl. in einer Dosis von 160mg gegeben.
Der primäre Endpunkt war die Gesamtansprechrate (ORR), die mittels PET-CT ermittelt wurde. Sekundäre Endpunkte waren die Dauer des Ansprechens (DOR), das progressionsfreie Überleben (PFS) und das Gesamtüberleben (OS).
Ergebnisse
Der primäre Endpunkt der Studie (ORR) wurde erreicht. Nach einer mittleren Nachbeobachtungszeit von 20,2 Monaten zeigte die Kombinationstherapie ZO eine signifikant höhere ORR (69%) im Vergleich zur Monotherapie mit O (46%). Die komplette Remissionsrate (CR) lag bei 39% in der ZO-Gruppe und bei 19% in der Monotherapie-Gruppe.
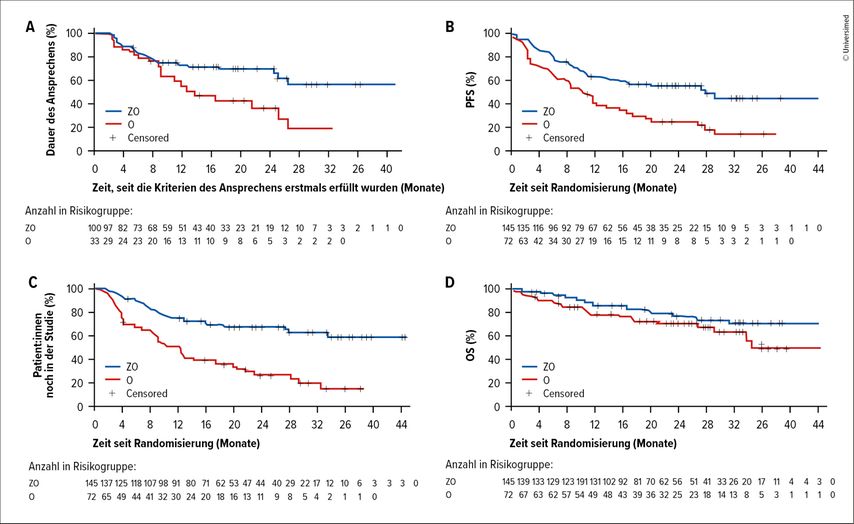
Auch die sekundären Endpunkte (DOR, PFS, OS) wurden erreicht (Abb. 1). Die Dauer des Ansprechens (DOR) war im Median im ZO-Arm noch nicht erreicht, im O-Arm lag sie im Median bei 14 Monaten. Das mediane PFS betrug 28,0 Monate für ZO im Vergleich zu 10,4 Monaten für O, was auf eine deutlich verbesserte Wirksamkeit der Kombinationstherapie hindeutet. Die Zeit bis zur nächsten Behandlung (TTNT) war für ZO noch nicht abschätzbar und lag bei 14 Monaten für den O-Arm. Das Gesamtüberleben (OS) nach zwei Jahren betrug 77% für ZO gegenüber 71% für O.
Abb.1: Dauer des Ansprechens (DOR), progressionsfreies Überleben (PFS), Zeit bis zur nächsten Behandlung (TTNT) und Gesamtüberleben (OS) in der ROSEWOOD-Studie, unter Zanubrutinib plus Obinutuzumab (ZO) vs. Obinutuzumab (modifiziert nach Zinzani PL et al.)5. A: mDOR bei ZO noch nicht erreicht, mDOR für O 14 Monate. B: Das mediane PFS war signifikant länger mit ZO (blaue Kurve; 28,0 Monate; 95% CI: 16,1–NE) im Vergleich zu O (rote Kurve; 10,4 Monate; 95% CI: 6,5–13,8); HR: 0,50 (95% CI: 0,33–0,75; p<0,001). C: TTNT für ZO noch nicht abschätzbar, für O 12,2 Monate. D: OS nach 24 Monaten war für ZO 77% vs. O 71%
Allerdings konnten Patient:innen bei Progress unter O in den ZO-Arm wechseln (Cross-over: 34 Patient:innen).
Sicherheit und Verträglichkeit
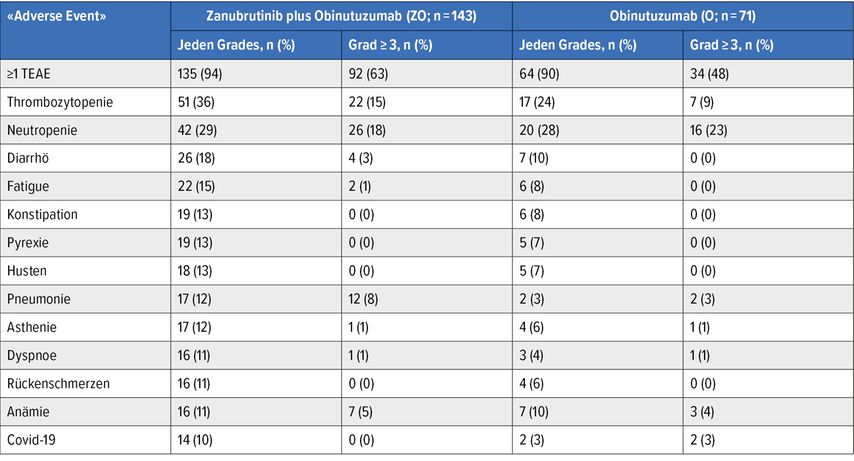
Die Nebenwirkungen der ZO-Kombinationstherapie waren beherrschbar und entsprachen dem zu erwartenden Sicherheitsprofil der einzelnen Medikamente. Zu den häufigsten Nebenwirkungen bei ZO gehörten Thrombozytopenie, Neutropenie, Durchfall und Müdigkeit. Schwere Nebenwirkungen (Grad ≥3) traten bei 63% der Patient:innen in der ZO-Gruppe und bei 48% in der O-Gruppe auf (Tab. 1). Infektionen waren im Kombinationsarm numerisch höher als im O-Monotherapie-Arm.
Tab.1: Toxizitäten. Die Rate schwerer Nebenwirkungen ≥3 war unter ZO höher als unter O (63% vs. 48%). Schwere Thrombozytopenien und Pneumonien, Diarrhöen und Dyspnoe waren unter ZO häufiger, Pyrexie (13% vs. 20%) und infusionsbedingte Reaktionen (3% vs. 10%) traten bei der Obinutuzumab-Monotherapie häufiger auf. Grad ≥3 Neutropenie (24% vs. 23%) und Anämie (5% vs. 6%) waren in beiden Gruppen ähnlich. Insgesamt wurden unter ZO 20% und O 21% G-CSF eingesetzt, 3% und 4% haben ≥1 Erythrozytenkonzentrat erhalten, 6% und 3% ≥1 Thromboyztenkonzentrat erhalten
Die Behandlungsdauer im ZO-Arm war allerdings fast doppelt so lang wie in der O-Monotherapie-Gruppe (12,2 Monate vs. 6,5 Monate), sodass sich, bezogen auf die Behandlungsdauer, ein vergleichbares Infektionsrisiko in beiden Armen zeigte.
Nebenwirkungen von besonderem Interesse sind unter BTK-Inhibitoren Blutungen und Herzrhythmusstörungen. Unter ZO kam es bei 28%, unter O bei 13% der Patient:innen zu Blutungen; schwere Blutungen traten in beiden Gruppen bei je zwei Patient:innen auf. Zu Vorhofflimmern (VHF) kam es bei 3% im ZO- und 1% im O-Monotherapie-Arm, bei einem Patienten im ZO-Arm trat ein VHF ≥3 Grad auf.
Schlussfolgerung
Die ROSEWOOD-Studie zeigt, dass die Kombination von Zanubrutinib und Obinutuzumab bei Patient:innen mit rezidiviertem oder refraktärem follikulärem Lymphom eine vielversprechende Behandlungsoption darstellt, die signifikant bessere Ansprechraten und ein verlängertes progressionsfreies Überleben bietet als die bisher zur Verfügung stehenden Therapien ab der dritten Linie (abgesehen von CAR-T-Zell-Therapie und Therapie mit bispezifischen AK). Das Sicherheitsprofil der Kombinationstherapie war akzeptabel und die Therapie wurde gut toleriert.
Die Wahl von Obinutuzumab-Monotherapie als Vergleichsarm, der in dieser Indikation nicht zugelassen bzw. etabliert ist, ist ungewöhnlich und wurde zur besseren Vergleichbarkeit der beiden Arme so gewählt. Eine weitere Begründung war, dass viele Patient:innen in den Vortherapien bereits Rituximab bekommen hatten oder Rituximab-refraktär (53%) waren.
Zur Positionierung von ZO im Therapiealgorithmus bei follikulären Lymphomen ist ein Vergleich mit anderen hochwirksamen Kombinationen notwendig. Dazu wird aktuell die Phase-III-Studie MAHOGANY (ZO vs. R2) durchgeführt (ClinicalTrials.gov identifier: NCT05100862).
Ab der dritten Therapielinie stehen allerdings bereits jetzt zusätzliche zugelassene und hocheffektive therapeutische Optionen bei Patient:innen mit r/r FL zur Verfügung, so zum Beispiel R2, der bispezifische AK Mosunetuzumab, die CAR-T-Zell-Therapie Tisa-cel sowie eine wahrscheinlich in der Zukunft immer weniger eingesetzte allogene Stammzelltransplantation.
Literatur:
1 Carbone A et al.: Follicular lymphoma. Nat Rev Dis Primers 2019; 5(1): 83 2 Salles G, Ghesquières H: Current and future management of follicular lymphoma. Int J Hematol 2012; 96(5): 544-51 3 Sarkozy C et al.: Cause of death in follicular lymphoma in the first decade of the rituximab era: a pooled analysis of French and US cohorts. J Clin Oncol 2019; 37(2): 144 4 Zinzani PL et al.: Current and future therapies for follicular lymphoma. Exp Hematol Oncol 2024; 13(1): 87 5 Zinzani PL et al.: ROSEWOOD: a phase II randomized study of zanubrutinib plus obinutuzumab versus obinutuzumab monotherapy in patients with relapsed or refractory follicular lymphoma. J Clin Oncol 2023; 41(33): 5107-17
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...