Staging Lungenkarzinom – die radiologische Perspektive
Autorin:
Dr. Anna Katharina Luger
Stv. Leiterin für Thoraxradiologie und onkologische Radiologie
Universitätsklinik für Radiologie Innsbruck
E-Mail: anna.luger@i-med.ac.at
Das Staging des Lungenkarzinoms nach der achten Version des TNM(Tumor-Nodus-Metastasen)-Stagings stellt den aktuellen Goldstandard dar. Dieser Artikel bietet eine Übersicht über die T-, N- und M-Deskriptoren mit Hinweisen für die radiologische Befundung.
Das Staging einer Tumorerkrankung gehört zu den wichtigsten, aber auch zeitaufwendigsten Aufgaben in der Radiologie. Dabei ist die exakte Beurteilung der zahlreichen Bildakquisitionen von Schädel bis Becken von eminenter Bedeutung. Aktuell, seit dem Jahr 2017, ist die achte Version des TNM-Stagings der IASLC („International Association for the Study of Lung Cancer“) in Verwendung.1
Das TNM-Staging setzt sich aus drei Komponenten entsprechend den Buchstaben zusammen: der T-Deskriptor (= Tumor) umfasst die Ausdehnung des Primärtumors, N (=Nodus) bezeichnet die Beteiligung der regionalen Lymphknoten und M (= Metastasen) steht für das Vorliegen von Fernmetastasen. Zunächst wird ein cTNM-, also klinisches Stadium anhand von klinischer Untersuchung, Bildgebung und Biopsie erfasst. Nach chirurgischer Resektion und histopathologischer Aufarbeitung wird das pTNM-, also das pathologische Stadium generiert.
Im Folgenden sollen alle drei Komponenten und ihre diagnostischen Möglichkeiten diskutiert werden.
T-Kategorie: Kernpunkt Tumorgröße
Die T-Kategorie basiert hauptsächlich auf der Tumorgröße, in Kenntnis dessen, dass die Tumorgröße zu den wichtigsten Prädiktoren für das Outcome bei Lungenkarzinomen gehört.2 Die verschiedenen Ebenen des T-Stadiums sind Tx, T0, Tis, und T1 bis T4, wobei T1 und T2 noch einmal in die Untergruppen a-c bzw. a-b unterteilt werden können.
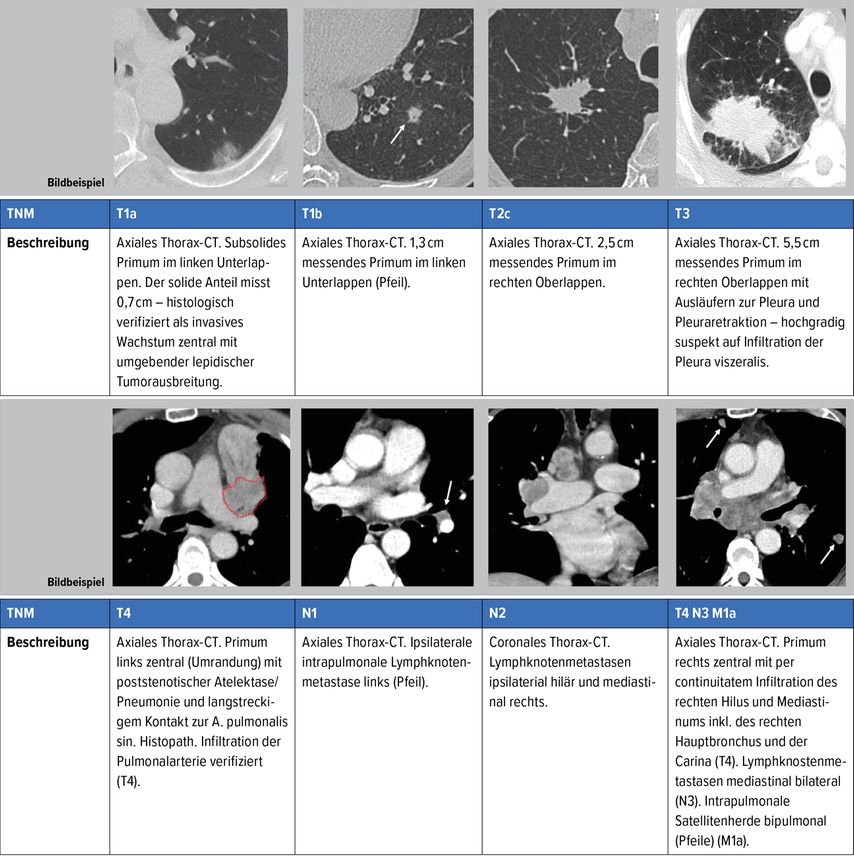
Zur Bestimmung der T-Kategorie wird der längste Durchmesser des Primärtumors gemessen. Der längste Durchmesser liegt dabei nicht zwangsläufig in der axialen Bildschichtung, die primär zur Bildbeurteilung herangezogen wird. Es ist daher essenziell, zur korrekten Bestimmung auch koronale und sagittale Rekonstruktionen anzufertigen. Dabei kann eine semiautomatische Volumetrie im PACS („Picture Archiving and Communication System“) hilfreich sein. In Abbildung 1 sind beispielhafte Computertomografie(CT)-Befunde des TNM-Stagings gezeigt.
Die Stufen Tx und T0 sind radiologisch von geringer Bedeutung. Tis (Carcinoma in situ) kann nur anhand der histopathologischen Aufarbeitung des Resektionsspezimens festgelegt werden. T1 ist definiert als eine Tumorgröße von unter 3 cm und eine zirkumferentielle Einbettung des Primums in das Lungenparenchym. Es hat sich gezeigt, dass die genaue Ausdehnung (jeder einzelne Zentimeter zählt) einen statistisch signifikanten Einfluss auf das Überleben hat, sodass die T1-Kategorie in weitere drei Untergruppen entsprechend der Größe gegliedert ist.
Als Neuerung wurde in der achten Version des Stagings eine T1a(mi)-Untergruppe für minimal invasive Adenokarzinome (MIA) eingeführt. Korrespondierend, wie bei der oben genannten Carcinoma-in situ(AIS)-Kategorie, lässt sich dies nur histopathologisch festlegen.
Eine Besonderheit ist bei der Ausmessung der Größe von subsoliden Rundherden zubeachten.3 Bei prädominant oder gemischt lepidisch wachsenden Adenokarzinomen wird in der histopathologischen Aufarbeitung nicht nur der Gesamtdurchmesser, sondern insbesondere auch der invasive Anteil gemessen, der wiederum für die Benennung der T-Kategorie herangezogen wird.
Radiologisch korreliert der invasive Tumoranteil gut mit in der CT sichtbaren, soliden Tumoranteilen und der lepidisch wachsende Anteil mit dem CT-Korrelat der Milchglasverdichtung. Ein lepidisch prädominant wachsendes Adenokarzinom der Gesamtgröße von 2,9 cm mit einem soliden Anteil von 0,7 cm und einem Milchglasanteil von 2,5 cm entspräche somit einer T1a-Kategorie. Nun liegt bei der initialen CT-Befundung zumeist kein pathologisches Ergebnis vor. In der Praxis hat es sich bewährt, in Kenntnis der Korrelation aus Milchglasverdichtung mit nicht invasivem Wachstum im radiologischen Befund sowohl den Gesamtdurchmesser als auch den Durchmesser des soliden Anteils anzugeben.
Auch reine Milchglasnoduli können sich histopathologisch als AIS erweisen. Hier wird der Gesamtdurchmesser angegeben. Die T-Kategorie entspricht jedoch in jedem Fall einem Tis, zumindest bis zu einer Größe von 3 cm. Ab einem Cut-off-Wert von 3cm wird der Tumor als T2 klassifiziert. Analog der T1-Kategorien wird auch hier in T2-Untergruppen entsprechend 1cm- Schritten gegliedert.
Allerdings gibt es noch weitere Kriterien, abgesehen von der Größe, die einen T2-Tumor definieren: Infiltration der viszeralen Pleura, postobstruktive Pneumonie/Atelektase und Infiltration des Hauptbronchus. Die postobstruktive Pneumonie/Atelektase ist hierbei nicht selbst als Prädiktor zu sehen, sondern sie repräsentiert vielmehr eine Infiltration des Bronchus und eine endobronchiale Ausbreitung mit entsprechend verschlechterter Prognose.
Es kann teilweise sehr schwer sein, die Grenzen eines Tumors von der unmittelbar anschließenden postobstruktiven Pneumonie/Atelektase in der CT zu differenzieren. Die Lokalisation ist zwar aus logischen Gründen an der Spitze der triangulären Konsolidierung zu erwarten, jedoch selbst mit Kontrastmittelunterstützung lässt sich oft atelektatische/pneumonische Konsolidierung nicht suffizient von Tumorgewebe differenzieren. Hier kann eine Positronen-Emissionstomografie (PET) sehr hilfreich sein, da sich die Glukosestoffwechselaktivität des Primums zumeist sehr deutlich von einer Atelektase/Pneumonie abhebt.
Die Infiltration der Pleura viszeralis ist ein Kriterium, das letztlich der histologischen Aufarbeitung vorbehalten ist. Bildmorphologisch imponieren eine Lagebeziehung zur Pleura und/oder eine Pleuraretraktion als hochgradig verdächtig. Die weiteren Cut-off-Werte zur T3- bzw. T4-Kategorie sind 5 und 7cm, wobei ab diesen Tumorgrößen tatsächlich die zumeist vorliegende Infiltration der umliegenden Strukturen für die Definition in T3 und T4 eine größere Rolle spielt.
Zu T3 gehören die Infiltration der Thoraxwand, des Perikards und des N. phrenicus (CT-morphologisch kaum identifizierbar). Zu T4 gehören die Infiltration der Karina, der Trachea, des Zwerchfells, des Mediastinums, des Ösophagus, der Wirbelkörper, des Herzens, der großen Gefäße und des N. laryngeus recurrens (CT-morphologisch kaum identifizierbar).
Es ist zu beachten, dass intrapulmonale ipsilaterale Metastasen nicht als Fernmetastasen zählen, sondern in die T-Kategorie fallen. Absiedlungen im selben Lappen wie das Primum fallen in die T3-Kategorie, Absiedlungen ipsilateral, jedoch im anderen Lungenlappen, zählen zu T4.
N-Kategorie: Lymphknotenbefall
Fehlende Lymphknotenmetastasen definieren die N0-Kategorie. N1 beschreibt ipsilateral peribronchiale, interlobäre oder hiläre Lymphknotenmetastasen. Bei ipsilateral paratrachealen und infrakarinalen Lymphknotenmetastasen erfolgt die Einordnung als N2 und ein kontralateraler und/oder supraklavikulärer Lymphknotenbefall ist als N3 zu werten.4
Die Lymphknotenmetastasen werden mittels einer Lymphknotenkarte definierten Stationen zugeordnet („IASLC lymph node map“ von 2009). Eine ausführliche Beschreibung findet sich zum Beispiel in der Publikation von El-Sherief AH et al.5
Diese Karte unterscheidet dabei 14 Stationen, die wiederum in sieben Zonen zusammengefasst werden. Die Verwendung von Zonen ist insbesondere hilfreich bei ausgedehnter, also die Regionen überschreitender Lymphadenopathie. Anhand der betroffenen Regionen kann die Zuordnung in N1 bis N3 des TNM-Stagings erfolgen.
Insbesondere die Differenzierung in ipsilateral und kontralateral ist für das N-Stadium bzw. für die Prognose von Bedeutung. Somit ist die Kenntnis der Grenzen der einzelnen Stationen in der CT elementar. Die Grenze zwischen den unteren paratrachealen Lymphknoten (Station 4R und 4L) wird beispielsweise an der linkslateralen Trachealwand gezogen, und nicht etwa wie häufig angenommen entlang der Mittellinie der Trachea. Dahingegen wird beispielsweise die Trennung in rechts/links für die prävaskulären Lymphknoten (Station 3A) entlang der Mitte der Trachea gezogen und die Grenze für paraösophageale Lymphknoten (Station 8) entlang der Mitte des Ösophagus.
In zukünftigen Versionen des TNM-Stagings könnten weitere Unterkategorien von N1 bis N3 folgen, die neben der Lokalisation auch die Anzahl der betroffenen Regionen berücksichtigen.
M-Kategorie: Prognose durch Metastasen
Die Fernmetastasierung eines Lungenkarzinoms erfolgt häufig in Leber, Knochen, Pleura, Peritoneum, Nebennieren, Gehirn und Nieren.6 Die M-Kategorie beschreibt die Lokalisation und Anzahl der Fernmetastasen.7
M1a bezieht sich dabei auf intrathorakale Metastasen: intrapulmonale Absiedlungen auf der Gegenseite, Pleura- oder Perikardkarzinosen bzw. maligne Pleuraergüsse. Als Neuerung wurde in der achten Version des TNM-Stagings die M1b- und M1c-Kategorie neu definiert. M1b inkludiert eine solitäre extrathorakale Metastase in einem Organ. Hierunter fallen auch extraregionale Lymphknotenmetastasen. Diese neue Kategorie beschreibt eine oligometastatische Situation, die sich mit einer signifikant besseren Prognose gegenüber der nächsthöheren Kategorie M1c abgehoben hat. M1c bedeutet das Vorliegen mehrerer Fernmetastasen und ist mit der schlechtesten Prognose assoziiert.
Gleiches Stadium, ähnliche Prognose
Anhand der Zusammensetzung aus T-, N-, und M-Stadium wird die Stadieneinteilung vorgenommen, die sowohl für die Wahl der Therapie als auch für die Prognose der Patienten entscheidend ist. Patienten gleicher Stadien zeigen eine ähnliche Prognose.
Literatur:
1 Goldstraw P et al.: International Association for the Study of Lung Cancer Staging and prognostic factors committee, advisory boards, and participating institutions; International Association for the Study of Lung Cancer Staging and prognostic factors committee advisory boards and participating institutions. The IASLC lung cancer staging project: proposals for revision of the TNM stage groupings in the forthcoming (eighth) edition of the TNM classification for lung cancer. J Thorac Oncol 2016; 11(1): 39-51 2 Rami-Porta R et al.: IASLC staging and prognostic factors committee, advisory boards and participating institutions. The IASLC lung cancer staging project: proposals for the revisions of the T descriptors in the forthcoming eighth edition of the TNM classification for lung cancer. J Thorac Oncol 2015; 10(7): 990-1003 3 Travis WD et al.: International Association for the Study of Lung Cancer Staging and prognostic factors committee and advisory board members. The IASLC lung cancer staging project: proposals for coding T categories for subsolid nodules and assessment of tumor size in part-solid tumors in the forthcoming eighth edition of the TNM classification of lung cancer. J Thorac Oncol 2016; 11(8): 1204-23 4 Asamura H et al.: International Association for the Study of Lung Cancer Staging and prognostic factors committee, advisory board members, and participating institutions. The International Association for the Study of Lung Cancer lung cancer staging project: proposals for the revision of the N descriptors in the forthcoming 8th edition of the TNM classification for lung cancer. J Thorac Oncol 2015; 10(12): 1675-84 5 El-Sherief AH et al.: International Association for the Study of Lung Cancer (IASLC) lymph node map: radiologic review with CT illustration. Radiographics 2014; 34(6): 1680-91 6 Budczies J et al.: The landscape of metastatic progression patterns across major human cancers. Oncotarget 2015; 6(1): 570-83 7 Eberhardt WE et al.: International Association for Study of Lung Cancer Staging and prognostic factors committee, advisory board members, and participating institutions. The IASLC lung cancer staging project: proposals for the revision of the M descriptors in the forthcoming eighth edition of the TNM classification of lung cancer. J Thorac Oncol 2015; 10(11): 1515-22
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...