Von neuen Standards und Paradigmenwechsel
Bericht:
Mag. pharm. Irene Senn, PhD
Die gemeinsame Frühjahrstagung der Österreichischen Gesellschaft für Hämatologie und Medizinische Onkologie (OeGHO) und der Arbeitsgemeinschaft hämatologischer und onkologischer Pflegepersonen in Österreich (AHOP) fand in diesem Jahr in Innsbruck statt. Ein traditionelles Highlight war das „Best of Oncology“-Symposium, welches den Kongressabschluss am Samstag bildete. Aus der Fülle an Studien präsentierte Assoc. Prof. Priv.-Doz. Dr. Martin Pichler (Graz, Augsburg) eine Auswahl anbedeutsamen Ergebnissen bei verschiedenen Tumorentitäten.
Gastrointestinale Tumoren
Pembrolizumab beim fortgeschrittenen Magenkarzinom
Die KEYNOTE-859-Studie untersucht die Kombination von Pembrolizumab plus Chemotherapie (CT) bei Patient*innen mit lokal fortgeschrittenem oder metastasiertem Magenkarzinom (GC). Die Ergebnisse der Interimsanalyse wurden beim Virtual Plenary der Europäischen Gesellschaft für Medizinische Onkologie (ESMO) im Februar vorgestellt.1
Sie bestätigten einen statistisch signifikanten Vorteil im Gesamtüberleben (OS) von etwa 1,5 Monaten in der Gesamtpopulation. Ähnliche Ergebnisse wurden in allen Subgruppen gesehen, unabhängig vom PD-L1-Status. „Wie die Zulassung aussehen wird, wissen wir noch nicht, vermutlich wird sie aber mit einem Biomarker-Score assoziiert sein“, so die Einschätzung Pichlers. „Die Daten geben einen eindeutigen Hinweis, dass Betroffene mit hoher Mikrosatelliteninstabilität (MSI-h) von der Checkpoint-Blockade in der Erstlinie profitieren. Dementsprechend könnte künftig eine MSI-Testung schon vor der Erstlinie zielführend sein.“
Claudin 18.2 als neues Target beimMagenkarzinom
Eine weitere Biomarker-getriebene Therapieoption ist Zolbetuximab – die erste Substanz, welche Claudin 18.2. (CLDN18.2) als Target nutzt. CLDN18.2 ist ein Bestandteil der Tight Junctions im Magen und eine besonders vielversprechende Zielstruktur, da sie weitgehend tumorspezifisch ist. Die Bindung des CLDN18.2-Antikörpers Zolbetuximab löst den Zelltod an den Tumorzellen aus.
Eine CLDN18.2-Positivität in ≥75% der Tumorzellen, wie sie im Rahmen der SPOTLIGHT-Studie gefordert war, liegt bei etwa 30–40% der Magenkarzinome vor. Die Phase-III-Studie prüft Zolbetuximab + mFOLFOX6 vs. Placebo + mFOLFOX6 in der Erstlinie beim lokal fortgeschrittenen inoperablen oder metastasieren CLDN18.2+/HER2-Adenokarzinoms des Magens oder des gastroösophagealen Übergangs.2 Durch die Zugabe von Zolbetuximab konnte eine signifikante Verlängerung des medianen progressionsfreien Überlebens (mPFS) um 2 Monate (10,6 vs. 8,7 Monate; Zolbetuximab vs. Placebo) und des OS um 3 Monate (18,2 vs. 15,5 Monate) erreicht werden. Die Kombination bietet somit einen neuen potenziellen Standard für die Subgruppe der CLDN18.2-positiven GC-Patient*innen.
Bevacizumab beim mCRC in der Drittlinie: Ein neuer Standard?
Beim Kolorektalkarzinom (CRC) gibt es spannende Entwicklungen in der Drittlinie. Die Phase-III-Studie SUNLIGHT untersucht die Wirksamkeit und Sicherheit von Bevacizumab in Kombination mit Trifluridin/Tipiracil (TAS-102) in der Behandlung von Patient*innen mit refraktärem, metastasiertem CRC. Durch die zusätzliche Gabe des VEGF(„Vascular endothelial growth factor“)-Hemmers wurde sowohl das mediane OS (von 7,5 auf 10,8 Monate) als auch das PFS (von 2,4 auf 5,6 Monate) signifikant verlängert.3 „Das ist durchaus beachtlich, ein Ansprechen in dieser Form kennen wir für TAS102 nicht“, so Pichler. TAS102 unter Zugabe von Bevacizumab kann somit als neuer Standard in der Drittlinie gewertet werden.
Neoadjuvantes Dostarlimab beimdMMR-Rektumkarzinom
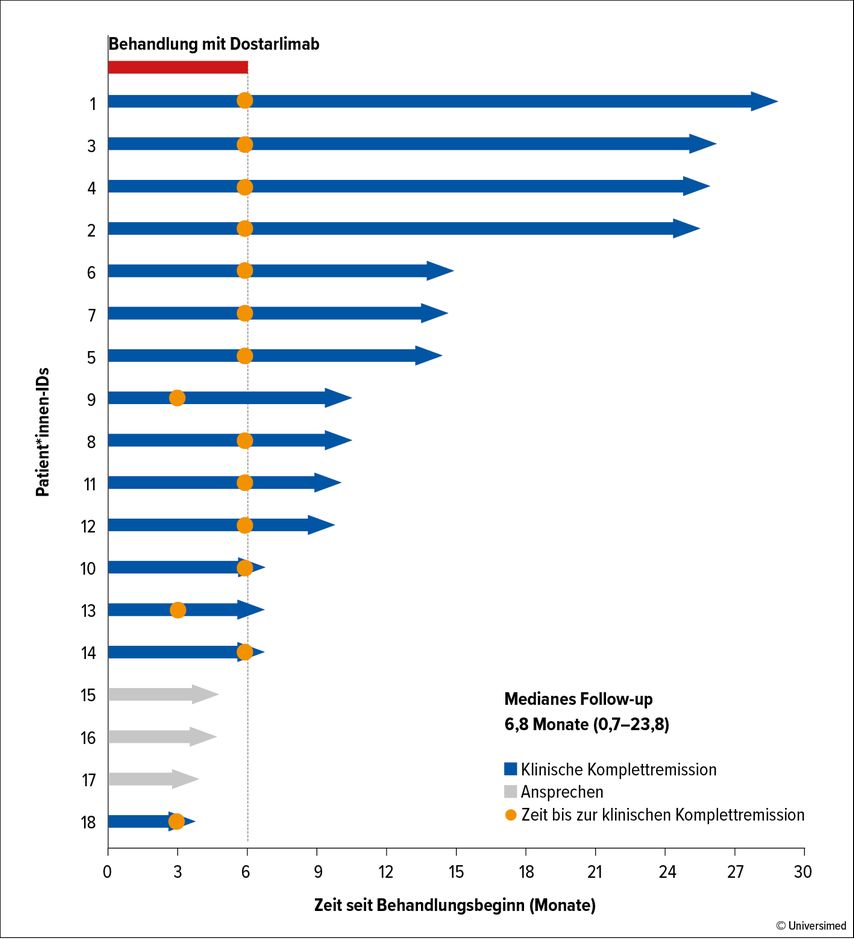
Medial für großes Aufsehen sorgte die einarmige Phase-II-Studie NCT04165772, welche den neoadjuvanten Einsatz des PD-1-Inhibitors Dostarlimab bei Patient*innen mit lokal fortgeschrittenem Rektumkarzinom und MSI-h oder Mismatch-Repair-Defizienz (dMMR) untersuchte. Obwohl bislang nur Daten von 14 Patient*innen berichtet wurden, sind die Ergebnisse äußerst bemerkenswert. Nach einer 6-monatigen Nachbeobachtungszeit war bei keiner/keinem der Proband*innen ein Resttumor nachweisbar. Alle Patient*innen zeigten ein klinisch vollständiges Ansprechen (Abb. 1).4
Abb. 1: Die neoadjuvante Therapie mit dem PD-1-Inhibitor Dostarlimab führte bei allen bisher berichteten Patient*innen zu einer Komplettremission. Sollte dieses Ergebnis bestätigt werden, könnten dMMR-Rektumkarzinome zukünftig unter Organerhalt therapierbar werden. Modifiziert nach Cercek A et al.4
Die Ergebnisse müssen nun in größeren, prospektiven Kohorten und über einen längeren Beobachtungszeitraum validiert werden. Sollten sie bestätigt werden, würde dies einen Paradigmenwechsel in der Behandlung von dMMR-Rektumkarzinomen einleiten und diese unter Organerhalt therapiebar machen.
Mammakarzinom
Trastuzumab-Deruxtecan bei HER2-low-Tumoren
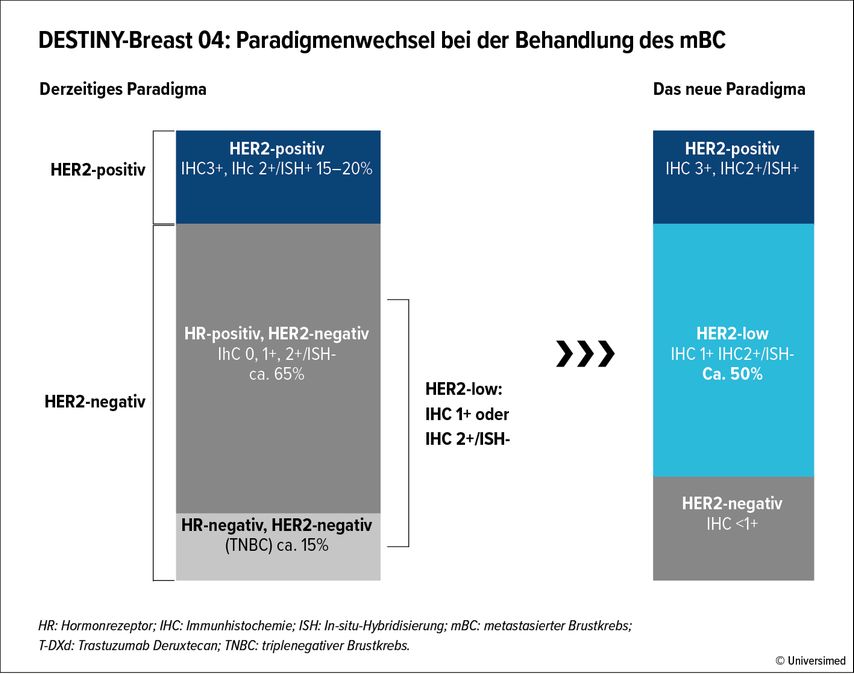
„Eine der wichtigsten Veränderungen des letzten Jahres war die neue Definition HER2-low“, so die Ansicht Pichlers. Immerhin 50% der HR+/HER2– und 30% der triplenegativen Mammakarzinome können als „HER2-low“ klassifiziert werden (Abb. 2). Diese Population wurden im Rahmen der DESTINY-Breast04-Studie untersucht und erhielt randomisiert Trastuzumab-Deruxtecan (T-DXd) oder eine CT nach Wahl des Arztes/der Ärztin. Primärer Endpunkt war das PFS der HR+-Population. Als sekundäre Endpunkte wurden das PFS bei der gesamten Studienpopulation und das OS der HR+ sowie der gesamten Studienpopulation ausgewertet.
Abb. 2: In der Behandlung des mBC zeichnet sich ein Paradigmenwechsel ab. Etwa 50% der früher als HER2-negativ definierten Patient*innen werden im neuen Paradigma als HER2 low klassifiziert – und diese Population profitiert von einer Therapie mit T-DXd. Modifiziert nach Modi S et al.5, Miglietta F et al. 7 und Tarantino P et al. s et al.8
Bei HR+ Patientinnen lag das mediane PFS im T-DXd Behandlungsarm bei 10,1 Monaten gegenüber 5,4 Monaten in der Kontrollgruppe. Ein vergleichbares Ergebnis mit 9,9 gegenüber 5,1 Monaten wurde in der Gesamtpopulation gesehen. Auch das OS wurde relevant verlängert.5,6 „Bei vorbehandelten Patientinnen mit HER2-low Tumoren ist T-DXd damit neuer Therapiestandard und hat sich mittlerweile in der Praxis etabliert“, berichtete Pichler.
Orales Elacestrant bei fortgeschrittenemBrustkrebs
Viele Neuerungen gab es auch beim HR+-/HER2– metastasierten Brustkrebs (mBC). Elacestrant ist ein oraler SERD (selektiver Östrogen-Rezeptor-Degrader) und wird in der Phase-III-Studie EMERALD an 478 Patient*innen mit HR+ mBC geprüft, die zuvor bereits ein bis zwei endokrine Therapien (ET) in Kombination mit einem CDK4/6-Inhibitor erhalten haben. Die Studie erreichte beide primären Endpunkte.
Sowohl das PFS in der Gesamtpopulation als auch das PFS in der Subgruppe mit ESR1(Estrogen Rezeptor 1)-Mutation konnte signifikant verlängert werden.9 Besonders ausgeprägt profitierten jene Patient*innen von Elacestrant, die zuvor ≥18 Monate einen CDK4/6-Inhibitor erhalten hatten oder deren Tumor ESR1-mutiert war. „Zukünftig wird sich wohl auch hier eine Testung in der Routine etablieren“, so die Einschätzung Pichlers. Von der FDA wurde Elacestrant kürzlich beim HR+, HER2–, ESR1-mutierten mBC zugelassen.
AKT-Hemmer Capivasertib bei HR+ mBC
Ein Highlight auf dem SABCS 2022 waren die Daten der CAPItello-291-Studie zum selektiven AKT-Hemmer Capivasertib.10 Die Ergebnisse bestätigten die Überlegenheit der Kombination Capivasertib + Fulvestrant vs. Placebo + Fulvestrant beim HR+ mBC in der Zweitlinie. Der duale Studienendpunkt wurde erreicht.
Das mediane PFS konnte durch die zusätzliche Capivasertib-Gabe sowohl in der Gesamtpopulation als auch in der Population mit AKT-Signalweg-Alterationen um fast 4 Monate verlängert werden (7,2 vs. 3,6 bzw. 7,3 vs. 3,1 Monate). Zudem wurde die Substanz relativ gut vertragen, sodass noch dieses Jahr mit einer Zulassung gerechnet werden kann.
Nichtkleinzelliges Bronchialkarzinom (NSCLC)
„Der Einzug der Immuntherapie in die kurative Situation war das Highlight in der Studienlandschaft im vergangen Jahr“, zeigte sich Priv. Doz. Dr. Gudrun Absenger (Graz) in der Podiumsdiskussion im Anschluss an den Vortrag überzeugt: „Die Behandlung des NSCLC wird sich in den kommenden Jahren durch die perioperative Chemoimmuntherapie grundlegend verändern.“
Nivolumab plus CT in der Neoadjuvanz
Die Ergebnisse der CheckMate-816-Studie belegen eindrücklich den Nutzen des Checkpoint-Inhibitors Nivolumab im neoadjuvanten Setting. In die Studie wurden 179 Patient*innen mit operablem NSCLC eingeschlossen und entweder mit Nivolumab + CT oder Placebo + CT behandelt, gefolgt von einer operativen Resektion in beiden Studienarmen.
Das ereignisfreie Überleben (EFS) konnte im Vergleich zur alleinigen CT hochsignifikant verlängert werden (31,6 vs. 20,8 Monate). Auch in Hinblick auf den zweiten primären Endpunkt – die pathologische Komplettremission (pCR) – war Nivolumab signifikant überlegen (24% vs. 2%).11 Auf Basis dieser Resultate wurde Nivolumab von der FDA beim NSCLC im neoadjuvanten Setting bereits zugelassen.
Atezolizumab als erste Immuntherapie in der Adjuvanz
Atezolizumab wurde als erster Checkpoint-Inhibitor Anfang 2022 von der EMA zur adjuvanten Behandlung des NSCLC bei Nachweis einer PD-L1-Expression auf ≥50% der Tumorzellen zugelassen. Grundlage hierfür waren die Daten der IMpower010-Studie.12,13 Durch die zusätzliche adjuvante Gabe von Atezolizumab nach vollständiger Resektion und adjuvanter Chemotherapie konnte ein signifikant verlängertes krankheitsfreies Überleben (DFS) erreicht werden. In der PD-L1-positiven Population waren nach 24 Monaten 74,6% vs. 61,0% (Atezolizumab vs. Best Supportive Care) und nach 36 Monaten 60% vs. 48,2% der Patient*innen tumorfrei.
Pembrolizumab adjuvant unabhängig vom PD-L1-Status
Auch Pembrolizumab wird in der adjuvanten Therapiesituation untersucht. In der Studie PEARLS/KEYNOTE-091 zeigte sich in der Gesamtpopulation eine signifikante Verlängerung des medianen DFS unter Pembrolizumab (53,3 vs. 42,0 Monaten unter Placebo). Entgegen den Erwartungen wurde für Patient*innen mit einer PD-L1-Expression ≥50% kein erhöhter Benefit gefunden.14 Die FDA hat Pembrolizumab adjuvant bei NSCLC unabhängig von PD-L1-Status zugelassen; auf die EU-Zulassung wird mit Spannung gewartet.
Sotorasib beim KRAS-G12C NSCLC inder Zweitlinie
„Eine der spannendsten Studien aus dem letzten Jahr war CodeBreak 200“, so Pichler. Die Phase-III-Studie verglich Sotorasib mit Docetaxel, dem jahrelangen Therapiestandard in der Zweitlinie beim NSCLC mit KRASG12C-Mutation. Etwa 15% der NSCLC-Patient*innen weisen diesen Biomarker auf. CodeBreak 200 erreichte beide primären Endpunkte: Das PFS wurde signifikant von 4,5 Monaten unter Docetaxel auf 5,6 Monate unter Sotorasib verlängert. Auch hinsichtlich der ORR war Sotorasib der CT signifikant überlegen (28,1% vs. 13,2%). Kein Unterschied zwischen den beiden Behandlungsarmen konnte im OS gefunden werden.15,16 Auf Basis dieser Daten wurde die Substanz als erster KRAS-Hemmer als Monotherapie für Patient*innen mit fortgeschrittenem NSCLC mit KRASG12C-Mutation von der EMA zugelassen.
Prostatakarzinom
Niraparib plus Abirateron bei HRR-Alterationen
Etwa ein Drittel der Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) weist Mutationen in Genen der homologen Rekombinationsreparatur (HRR) auf. Der PARP-Inhibitor (PARPi) Niraparib wird in der MAGNITUDE-Studie bei mCRPC-Patienten mit und ohne HRR-Alterationen geprüft; die zweite Interimsanalyse wurde kürzlich beim Genitourinary Cancers Symposium der American Society of Clinical Oncology (ASCO GU) präsentiert.17,18 Nach einem medianen Follow-up von 18,6 Monaten zeigte sich ein signifikanter Vorteil im radiografischen PFS (rPFS) in der Subgruppe der BRCA1/2-positiven Patienten mit 16,6 Monaten (unter Niraparib) vs. 10,9 Monate (unter Placebo). Gleiches galt für Patienten mit anderen HRR-positiven Markern (16,5 Monate vs. 13,7 Monate). Bei Patienten ohne Alteration von HRR-Genen konnte keine Verlängerung des rPFS durch die zusätzliche Niraparib-Gabe erreicht werden. Die Kombination aus Niraparib plus Abirateron wurde zur Behandlung des mCRPC mit BRCA1/BRCA2-Mutationen vom CHMP zur Zulassung empfohlen.
Olaparib/Abirateron unabhängig vomMutationsstatus
Auch die PROpel-Studie untersucht den Einsatz eines PARPi beim mCRPC. In dieser Phase-III-Studie erhielten 796 Patienten in der ersten Therapielinie randomisiert Olaparib/Abirateron oder Abirateron. „Hervorzuheben ist, dass in dieser Studie die All-Comer-Population untersucht wurde“, betonte Pichler. Bei knapp 70% der Studienteilnehmer waren keine HRR-Mutationen nachweisbar. Durch die zusätzliche Olaparib-Gabe wurde das mediane rPFS um ca. 8 Monate von 16,6 auf 24,8 Monate verlängert.19 Bemerkenswert ist, dass der Benefit in allen Subgruppen beobachtet wurde – unabhängig von Alter, Performance-Status, initialem PSA-Wert und HRR-Status. Basierend auf diesen Daten gibt es mittlerweile bereits eine EMA-Zulassung.
Quelle:
„Best of Oncology“-Symposium, Frühjahrstagung der OeGHO & AHOP, 30. März bis 1. April 2023, Innsbruck
Literatur:
1 Rha SY et al.: Ann Oncol 2023; 34(3): 319-20 2 Shitara K et al.: J Clin Oncol 2023; 41: LBA292 3 Tabernero J et al.: JClin Oncol 2023; 41: 4 4 Cercek A et al.: N Engl J Med 2022; 386(25): 2363-76 5 Modi S et al.: J Clin Oncol 2022; 40: LBA3 6 Modi S et al.: N Engl J Med 2022; 387(1): 9-20 7 Miglietta F et al.: NPJ Breast Cancer 2021; 7(1): 137 8 Tarantino P et al.: J Clin Oncol 2020; 38(17): 1951-62 9 Bidard FC et al.: J Clin Oncol 2022; 40(28): 3246-56 10 Turner N et al.: SABCS 2022; Abstr. #GS3-04 11 Forde PM et al.: N Engl J Med 2022; 386(21): 1973-85 12 Felip E et al.: Lancet 2021; 398(10308): 1344-57 13 Wakelee HA et al.: JClin Oncol 2021; 39: 8500 14 Paz-Ares L et al.: Ann Oncol 2022; 33(4): 451-3 15 de Langen AJ et al.: Lancet 2023; 401(10378): 733-46 16 Johnson M: ESMO 2022; Abstr. #LBA10 17 Efstathiou E et al.: J Clin Oncol 2023; 41: 170 18 Chi KN et al.: J Clin Oncol 2022; 40: 12 19 Saad F et al.: J Clin Oncol 2022; 40: 11
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...