Das akute Kompartmentsyndrom der Extremitäten
Autoren:
Dr. Bernhard Maier
Dr. Thomas Haider
Universitätsklinik für Orthopädie und Unfallchirurgie,
Medizinische Universität Wien
Korrspondierender Autor:
Dr. Bernhard Maier
E-Mail: bernhard.maier@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das akute Kompartmentsyndrom ist ein altbekannter chirurgischer Notfall. Dennoch gestaltet sich die Diagnosestellung durch die Heterogenität in Ätiologie, die Vielzahl an möglichen Risikofaktoren und die oft eingeschränkte klinische Beurteilbarkeit in vielen Fällen herausfordernd. Die frühe Diagnosefindung ist von entscheidender Bedeutung, denn der frühe klinische Verdacht und die rechtzeitige chirurgische Intervention sind entscheidend für die Prognose!
Keypoints
Das ACS ist ein chirurgischer Notfall bei mitunter schwieriger Diagnostik.
Als begleitende Weichteilschädigung entsteht es überwiegend nach Frakturen und stumpfen Verletzungen, aber auch infolge inadäquat erscheinender Unfälle durch Druckanstieg in den myofaszialen Logen.
Unterschenkel und Unterarm zählen zu den häufigsten Lokalisationen.
Die Diagnosestellung erfolgt klinisch, wobei das zentrale Symptom ein unverhältnismäßiger Schmerz ist.
Die apparative ICP-Messung dient der Befundobjektivierung sowie Dokumentation und ist auch aus forensischen Gründen als Standard anzusehen.
Die Therapie der Wahl ist die Dermatofasziotomie mit vollständiger Spaltung der Muskelfaszie und Entlastung aller Muskellogen.
Die klinische Prognose sowie die Vermeidung schwerwiegender Komplikationen sind direkt von einem raschen und korrekten Diagnose- und Behandlungsalgorithmus abhängig.
Das akute Kompartmentsyndrom der Extremitäten (ACS) ist ein chirurgischer Notfall mit sofortigem Handlungsbedarf. Es entsteht überwiegend durch Trauma als begleitende Weichteilschädigung bei Frakturen oder bei stumpfen Verletzungen durch Druckanstieg in den anatomisch umschlossenen, myofaszialen Logen (Kompartimente).
Die klinische Prognose und der Erhalt der Funktionalität werden durch Diagnosezeitpunkt, Ausmaß, Verlaufsdauer sowie entscheidend durch eine rasche und suffiziente Therapie und ihre korrekte Indikationsstellung bestimmt. Eine verzögerte Detektion oder verspätete Therapieeinleitung kann zu schwerwiegenden Komplikationen, einschließlich des Verlustes der betroffenen Extremität, und zu lebensbedrohlichen Zuständen führen. Kontrakturen mit erheblichem sensomotorischem Defizit bis hin zum vollständigen Funktionsverlust sind mögliche Langzeitfolgen verspäteter Therapie.
Erkenntnisse und Aufzeichnungen über Langzeitschäden durch zu straffe, zirkuläre Verbände gehen bis in die Antike zurück. Die erste Publikation erfolgte 1881 durch Richard von Volkmann über die Entstehung von Kontrakturen und Paralysen an der oberen Extremität durch zu eng anliegende Bandagen. Frederick A. Matsen definierte 1975 das ACS „as a condition in which the circulation and function of tissues within a closed space are compromised by increased pressure within that space“.
Die Diagnosestellung stellt jedoch weiterhin eine Herausforderung dar. Im deutschsprachigen Raum existieren bis dato keine klaren Leitlinien zur Diagnostik und Therapie. Die deutliche Heterogenität der zugrunde liegenden Ursachen und Verletzungen sowie das Fehlen von klaren prädiktiven Kriterien und Risikofaktoren kommen erschwerend hinzu. Weitere Gründe für eine indifferente Klinik sind neurologische Beeinträchtigung, regionale oder allgemeine Anästhesieverfahren und patientengesteuerte Schmerztherapie. Die genaue Inzidenz ist nicht bekannt und variiert zwischen 3% und 17%. Die Ergebnisse aus der Literatur zeigen jedoch, dass das ACS eine prinzipiell häufige Komplikation nach Trauma darstellt, wobei insbesondere Frakturen und Gefäßverletzungen häufig assoziierte Pathologien sind. Auch offene Frakturen können zu einem ACS führen. In 30% der Fälle liegt dem ACS eine reine Weichteilverletzung ohne Nachweis einer Knochenbeteiligung zugrunde. Häufig liegt nur ein minimales, inadäquat erscheinendes Trauma vor. McQueen et al. beschrieben ein erhöhtes Risiko und Vorkommen mit 7,3/100000 Einwohner pro Jahr bei jungen Männern unter 30 Jahren. Die Inzidenz bei Frauen war mit 0,7/100000 Einwohner pro Jahr signifikant geringer. Eine Fraktur des Tibiaschaftes wurde mit 11,6% als häufigste zugrunde liegende Pathologie im Erwachsenenalter identifiziert. An zweiter Stelle liegen Fußverletzungen, die circa 6% aller ACS ausmachen und häufig nach Motorradunfällen auftreten. Im Bereich der oberen Extremität tritt ein ACS mit einer Häufigkeit von 3,1% bei Unterarmschaftfrakturen und von 0,25% bei distalen Radiusfrakturen auf.
Zahlreiche weitere Ursachen wurden beschrieben und reichen von inadäquat angebrachten zirkulären Gipsverbänden, postoperativen Schwellungszuständen, langer Steinschnittlagerung und Paravasaten bis zu thermischen Verletzungen, Schlangenbissen, septischen Krankheitsbildern, Myositiden und nephrotischem Syndrom. Zu beachten ist, dass auch ein minimales, oft inadäquat erscheinendes Ereignis ein immanentes Risiko für ein Logensyndrom darstellt.
Pathophysiologie
Das ACS ist ein progressiver, dynamischer Prozess. Pathophysiologisch handelt es sich bei der Entstehung um ein multifaktorielles Geschehen. Ätiologisch liegen eine Veränderung des Kompartmentvolumens von außen bzw. eine Vermehrung des Kompartmentinhalts von innen zugrunde. Diese Mechanismen treten isoliert oder parallel auf.
Die Theorie des arteriovenösen Gradienten sowie der Zusammenhang zwischen dem Logendruck („intra-compartmental pressure“, ICP) und dem diastolischen und mittleren arteriellen Blutdruck kennzeichnen die theoretische Grundlage der lokalen Hämodynamik. Durch Anstieg des Gewebedrucks in den faszialen Logen kommt es zur Beeinträchtigung der Mikrozirkulation. Wenn der interstitielle Druck den kapillaren Perfusionsdruck übertrifft, kommt es zur raschen Entstehung eines Circulus vitiosus (Abb.1). Eine Reduktion des venösen Abflusses und der Perfusion resultiert in zellulärer Hypoxie und bewirkt die Auslösung einer inflammatorischen Kaskade, die durch chemotaktische Mediatoren, wie Zytokine, Histamine und Prostaglandine, gesteuert wird. Die darauf folgende Bildung von freien Radikalen und die zunehmende Azidose lösen eine gesteigerte Reperfusion aus und dies führt zur reflektorischen Erhöhung der Kapillarpermeabilität („capillary leak syndrome“) mit Zunahme des Ödems und weiterem Druckanstieg. Der direkte Zusammenhang zwischen dem progredienten Zelltod und der Hypoxie begründet das enge diagnostische Zeitfenster und die Notwendigkeit einer frühzeitigen Therapieeinleitung. Eine prolongierte Ischämie bei verzögertem oder inadäquatem Management kann daher zu irreversiblen, ausgedehnten Nekrosen mit schweren Funktionseinschränkungen, Verlust der Extremität, Rhabdomyolyse und akutem Nierenversagen führen.
Ein wichtiges Merkmal des ACS ist die lange erhaltene makrovaskuläre arterielle Perfusion mit tastbaren Pulsen, bis der interstitielle Druck den systolischen Druck übersteigt und bereits Ischämien vorliegen.
Klinik, Diagnostik, Biomarker, Differenzialdiagnosen
Die Diagnosestellung erfolgt klinisch anhand der Anamnese, der Beschwerdecharakteristik und der erhobenen Untersuchungsbefunde. Im Gegensatz zu bewusstseinsklaren und kooperativen Patienten gestaltet sich dies bei bewusstseinsgetrübten oder intubierten Patienten sowie Säuglingen und Kleinkindern in der Praxis oft herausfordernd. Durch die ausgeprägte Heterogenität der Ursachen, Erscheinungsformen, Lokalisationen und Verläufe steht der erste Verdacht im Mittelpunkt.
Das klinische Kardinalsymptom ist ein ausgeprägter analgetikaresistenter Schmerz mit passivem Dehnungsschmerz und einer verminderten Elastizität der Muskelgruppe und des Kompartiments. Par- und Hypästhesien durch ödem- und druckbedingte Störung der Leitfunktion des Nervens können ein weiteres Frühzeichen darstellen. Das Verteilungsmuster lässt Rückschlüsse auf das betroffene Kompartiment zu. Das Vollbild der klassischen „6 P“ (pain [out of proportion], pressure, paresthesia, paralysis, pallor, pulslessness) präsentiert sich erst im Spätstadium und kann irreführend sein, da es eher die Beschwerden eines arteriellen Gefäßverschlusses beschreibt. In der rezenten Literatur wurden für die klinische Einschätzung eine niedrige diagnostische Sensitivität und hohe Spezifität mit resultierendem schwachem prädiktivem Wert demonstriert. Der Schmerz ist beim wachen Patienten nichtsdestotrotz das wichtigste Symptom eines ACS. Im Säuglings- und Kleinkindesalter ist die Diagnosestellung durch eine eingeschränkte Verbalisierung zusätzlich erschwert. Als Anhaltspunkt können bei diesen Patienten Symptome wie vermehrte Angst, Agitiertheit und erhöhter Analgetikabedarf („3 A“) den Verdacht eines vorliegenden ACS erhärten.
Laborchemische Parameter steigen unspezifisch im Rahmen eines Traumas an. Muskelschaden und -nekrose spiegeln sich in Werten wie z.B. Kreatinkinase und Myoglobin wider und können somit für die Diagnosefindung eines ACS nicht herangezogen werden. Jedoch kann die Dynamik dieser Parameter unterstützend in der Diagnosefindung herangezogen werden. Aufgrund der insgesamt geringen prädiktiven Aussagekraft vorhandener Biomarker spielen diese in der Diagnostik des ACS sonst keine Rolle.
Die Entstehung ist ein dynamischer Prozess, wodurch eine engmaschige klinische Verlaufsbeobachtung vor allem bei drohendem ACS essenziell ist, da sich das Vollbild auch erst nach Stunden präsentieren kann. Eine zusätzliche apparative Diagnostik mittels invasiver Logendruckmessung ist bei unklaren klinischen Untersuchungsbefunden oder eingeschränkter Kommunikation bei Bewusstseinstrübung bzw. im Kindes- und Jugendalter indiziert. Die ICP- Messung dient der Befundobjektivierung sowie Dokumentation und ist auch aus forensischen Gründen als Standard anzusehen. In der Literatur werden dieser Methode eine hohe Sensitivität (94%), ein positiver prädiktiver Wert von 93% und eine Spezifität von 98% bei gleichzeitig hohem negativem prädiktivem Wert von 99% zugeschrieben. Verschiedene Techniken stehen für die Logendruckmessung und somit zur Objektivierung des ACS zur Verfügung.
Im Allgemeinen werden zwei Theorien der Druckermittlung unterschieden. Einerseits kann der gemessene Logendruck als eigenständiger Wert herangezogen werden. Der physiologische ICP wird bei Erwachsenen mit 8mmHg und im Kindesalter mit 10–15mmHg angegeben. Als Schwellenwert für die Entscheidung zur Fasziotomie wird in der Literatur häufig ein Wert über 30mmHg angeführt.
Die zweite Methode verwendet das sogenannte Druckdifferenzial (ΔP, auch Perfusionsdruck). Der gemessene Logendruck wird hierbei vom aktuellen diastolischen Blutdruck subtrahiert. Ein Wert von unter(!) 30mmHg gilt hier als Indikation zur Fasziotomie. In der Literatur lässt sich kein Vorteil einer der beiden Methoden der Grenzwertbestimmung finden.
Aufgrund der Druckunterschiede in den Kompartimenten wird eine Messung mit ca. 5cm Abstand zur Fraktur empfohlen. Zugleich ist es entscheidend, den ICP aller Logen der betroffenen Extremität zu ermitteln. Sollte ein Kompartiment die festgelegten Grenzwerte überschreiten, ist das Vorliegen eines ACS bewiesen und eine Fasziotomie umgehend durchzuführen. Normalwerte schließen jedoch ein ACS nicht aus. Im Zweifelsfall sind die klinische Einschätzung und Erfahrung hinsichtlich des weiteren Vorgehens vorrangig.
Nicht-invasive Methoden der Logendruckmessung stehen noch vor der Einführung in die klinische Routine. Der erfolgreiche Einsatz der Nahinfrarot-Spektroskopie und die ultraschallgestützte Messung der Faszienexkursion im präklinischen Setting zeigten beispielsweise vielversprechende Ergebnisse.
Abb. 2: Zustand nach Dermatofasziotomie aller anatomischen Logen und temporärer Deckung mit Epigard® bei manifestem Kompartmentsyndrom der Hand nach „crush injury“
Lokalisation
Das ACS tritt überwiegend an den Extremitäten auf und war vormals ausschließlich als Komplikation in diesen Bereichen bekannt. In den letzten Jahren wurde sein Auftreten jedoch auch in anderen Organsystemen, z.B. im Abdomen, beschrieben. Es kann überall dort entstehen, wo sich Organe in einem anatomisch abgegrenzten Raum befinden und eine Volumenzunahme im betroffenen Kompartiment zu einer Funktionseinschränkung und Schädigung führt.
Das ACS der oberen Extremität
Das ACS der oberen Extremität ist selten. Es überwiegt die Lokalisation am Unterarm, in 18% der Fälle als Folge von Frakturen und in 23% bei reinen Weichteilverletzungen („crush injuries“). Im Kindesalter ist die suprakondyläre Humerusfraktur als häufigste Ätiologie beschrieben.
Am Oberarm finden sich 3 Kompartimente: die deltoidale Loge und das, durch die Fascia brachii und ihren Septen geteilte ventrale (Flexoren) bzw. dorsale (Extensoren) Kompartiment. Die Unterarmfaszie, Fascia antebrachii, umhüllt 3 Muskelgruppen. Ausgehend von der Fascia antebrachii ziehen 3 Septen, die im Zusammenschluss mit Radius und Ulna sowie der Membrana interossea 3 Muskellogen bilden: das ventrale Kompartiment (Flexoren), das dorsale Kompartiment (Extensoren) und das Compartimentum antebrachii extensorum pars radialis sive lateralis. Das Ligamentum carpi volare fixiert den nicht im Canalis carpi ziehenden M. palmaris longus und die ulnaren Nerven.
In der Hand werden, abhängig von der Literaturquelle, zwischen 6 und 12 Logen beschrieben. Hierbei handelt es sich vereinfacht um Thenar, Hypothenar, Adduktoren, Mm. interossei, den Karpalkanal und die einzelnen Finger, die weiter unterteilt werden. Sensomotorische Defizite im Innervationsgebiet des jeweiligen Nerven lassen Rückschlüsse auf das betroffene Kompartiment zu.
Zahlreiche Zugänge sind für die Fasziotomie im Bereich der oberen Extremität beschrieben, die profunde anatomische Kenntnisse für eine suffiziente Entlastung aller Kompartimente unter Schonung der neurovaskulären Strukturen voraussetzen. Am Unterarm ist vor allem die Wichtigkeit der Entlastung des Karpalkanals zu betonen. An den Fingern erfolgt die Fasziotomie, unter Beachtung der Greif- und Auflagefläche, durch einen mittaxialen Schnitt.
Das ACS der unteren Extremität
Der Unterschenkel stellt den am häufigsten von einem ACS betroffenen Extremitätenabschnitt dar, wobei in mehr als der Hälfte aller Fälle eine Unterschenkelfraktur ursächlich vorliegt. Der Oberschenkel ist weitaus seltener betroffen. Junge Männer unter 35 Jahren werden in der Literatur als Risikogruppe angeführt. In einer Studie von McQueen et al. aus dem Jahr 2015 wurde bei jedem 10. Patienten mit diaphysärer Tibiafraktur ein ACS diagnostiziert und junges Alter als wichtigster prädiktiver Faktor angeführt. Dies wird auf die besser ausgebildete Muskultur und die damit verbundene geringere Reservekapazität innerhalb der Faszienräume zurückgeführt. Frakturcharakteristika und Begleitfaktoren, die ein erhöhtes Risiko für die Entwicklung eines ACS bewirken, sind ein direktes Trauma (speziell, wenn die Brüche von Tibia und Fibula auf gleicher Höhe lokalisiert sind), Frakturen im Bereich der Tibia-Diaphyse, hohe kinetische einwirkende Energie, ausgeprägter Weichteilschaden, Gefäßverletzungen und bestehende Komorbiditäten.
Abb. 3: Vollständige laterale Kompartmentspaltung am Unterschenkel (a), temporäre Deckung der Fasziotomiestellen mit Epigard® (b) sowie Reposition und Retention mit gelenksüberbrückendem Fixateur externe bei multifragmentärer proximaler Unterschenkelfraktur
Im Unterschenkel werden 4 Kompartimente, die durch eine straffe Bindegewebsschicht voneinander getrennt sind, unterschieden: die Tibialis-anterior-Loge, die Peroneusloge sowie die tiefe und oberflächliche Beugeloge. Die Tibialis-anterior-Loge ist zumeist die primär betroffene Loge, da sie das kleinste Kompartiment ist und somit ein Funktionsausfall klinisch zuerst bemerkt wird. Die Begrenzung dieses Kompartiments ist, bedingt durch den ausgedehnten direkten Kontakt zur Tibia, unnachgiebig und weist somit die geringste Reservekapazität auf. Klinisch präsentiert sich dies zusätzlich durch spezifische motorische und sensible Ausfälle. Ein Ausfall des Nervus peroneus führt zu einer Fußheberschwäche und einer Sensibilitätsstörung im Interdigitalraum zwischen der I. und II. Zehe, dem sensiblen Versorgungsgebiet des Nervus peroneus profundus. Die Beteiligung der tiefen Flexorengruppe kann eine Ausdehnung auf das Fußkompartiment nach sich ziehen.
Therapie des ACS: „in dubio pro incisionem“
Die Ruhigstellung der Extremität, die Entfernung aller einengenden Verbände und die Lagerung auf Herzhöhe sind Sofortmaßnahmen bei Verdacht auf ein (drohendes) ACS. Aufgrund der Verminderung der Mikrozirkulation und der daraus resultierenden raschen Progredienz sind eine Hochlagerung und Kryotherapie streng kontraindiziert.
Die Therapie der Wahl dieses chirurgischen Notfalls ist die Dermatofasziotomie mit vollständiger längsgerichteter Spaltung der Muskelfaszie und Entlastung aller Muskellogen. Eine minimal invasive, subkutane Spaltung der Faszien ist kontraindiziert. Das Ausmaß des Debridements richtet sich nach der Vitalität der Muskulatur, die anhand von Farbe, Kontraktilität, Konsistenz und kapillarer Blutung beurteilt wird. Nach Spaltung wird die Haut nicht sofort verschlossen, da dies als Rebound-Phänomen zu einem erneuten Druckanstieg führen würde. In der Literatur finden sich für die chirurgische Behandlung am Unterschenkel 2 Lehrmeinungen: Die Entlastung aller 4 Kompartimente kann durch einen unilateralen Zugang mit lateralseitigem Hautschnitt erfolgen. Hierbei ist insbesondere auf den Verlauf des Nervus peroneus superficialis zu achten. Die andere Möglichkeit besteht in einer zusätzlichen medialen Längsinzision, welche von Mubarak 1977 wieder eingeführt und empfohlen wurde. Dabei werden die tiefe und oberflächliche Flexorenloge über den medialen Zugang dekomprimiert. Unabhängig von der gewählten Methode ist eine vollständige Entlastung aller 4 Kompartimente obligat. In der Literatur zeigen sich vergleichbare Ergebnisse der beiden Zugangswege in Bezug auf die Rate an postoperativen Infektionen und Pseudarthrosenbildung. Die Entscheidung obliegt letzten Endes der Erfahrung und der Vorliebe des Operateurs.
Der temporäre Wundverschluss erfolgt mit Hydrokolloidverbänden bzw. Hautersatzstoffen (z.B. Epigard®) oder Vakuumversiegelung. Die erste Weichteilrevision findet meist nach 48 Stunden statt, wobei eine Dermotraktion zur Verkleinerung nach Maßgabe der Schwellung durchgeführt werden kann. Der definitive spannungsfreie Wundverschluss nach ausreichender Konsolidierung erfolgt durch Direktnaht, Spalthautdeckung oder plastisch-chirurgische Lappendeckung.
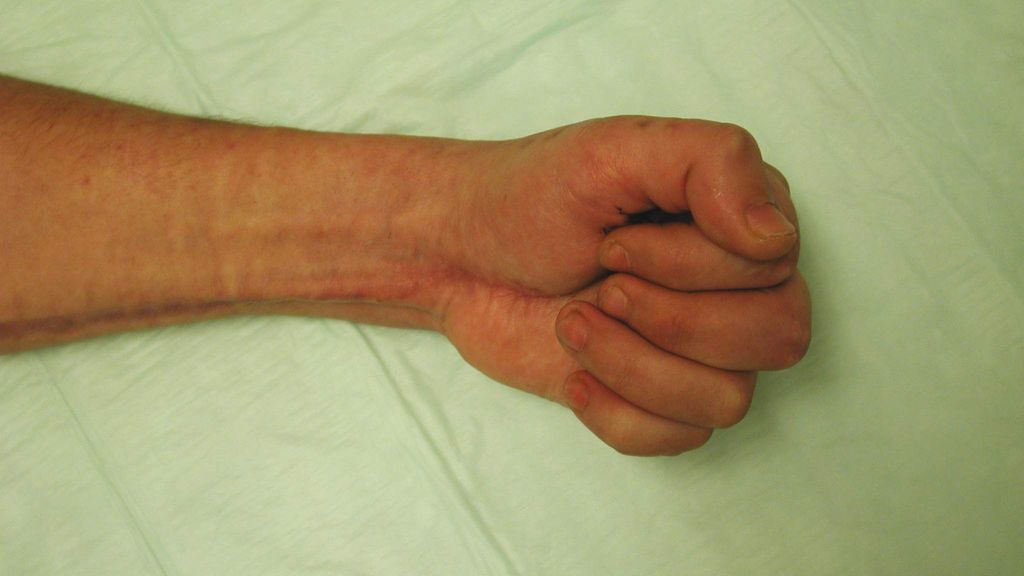
Abb. 4: Einklemmung des Unterarms in einer Pressmaschine mit multiplen Frakturen der Mittelhand und instabilem Handgelenk. Sofortige Revision und Dermatofasziotomie, Stabilisierung mit Fixateur externe und temporärer Deckung. Postoperatives Ergebnis
Akutes vs. chronisches Kompartmentsyndrom
Das chronische Kompartmentsyndrom („chronic exertional compartment syndrome“) wird im Sinne der Vollständigkeit abschließend angeführt. Es handelt sich um ein Missverhältnis aus Logen- und Perfusionsdruck, das durch Sport, vor allem bei Ausdauersportarten, ausgelöst wird. Pathognomonisch sind Beschwerden über der betroffenen Muskelloge, die ausschließlich während sportlicher Aktivität auftreten und nach Beendigung spontan sistieren. Bei ausbleibender Besserung durch konservative Maßnahmen und Modifikation der Trainingsgewohnheiten besteht die Möglichkeit einer operativen Intervention. Eine Logendruckmessung nach Sport kann zur Diagnose führen. Aufgrund des heterogenen klinischen Bildes mit ausschließlich temporär auftretenden Symptomen wird diese Form des Kompartmentsyndroms in vielen Fällen erst spät diagnostiziert.
Danksagung:
Wir bedanken uns bei Prof. Dr. T. Heinz für seine Tätigkeit als Lektor, bei OA Dr. G. Pajenda und Dr. L. Zak für die Bereitstellung des Bildmaterials.
Literatur:
bei den Verfassern
Das könnte Sie auch interessieren:
Frühe Unterwassertherapie nach totaler Hüft- und Knieendoprothese
Eine frühzeitige Durchführung der Unterwassertherapie mit wasserdichtem Folienverband ab dem vierten postoperativen Tag ist im Allgemeinen sicher, wirksam und ohne Nebenwirkungen.
Aktuelles zur anteromedialen Knieinstabilität
Kombinierte Verletzungen des medialen Kollateral- (MCL) und des vorderen Kreuzbandes (VKB) zählen zu den häufigsten multiligamentären Knieverletzungen. Bei vermeintlich isolierten VKB- ...
Arthroskopische Behandlung von Glenoidrandfrakturen
In der Literatur werden die Begriffe knöcherne Bankart-Läsion und Glenoidrandfraktur häufig synonym verwendet, obwohl sie sich hinsichtlich Pathomechanismus und Therapie deutlich ...






