Funktionsdiagnostik und künstliche Intelligenz in der Pneumologie
Autor:
Ass. Dr. Paul von Boetticher
Abteilung für Pneumologie
Ordensklinikum Linz
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Digitalisierung und künstliche Intelligenz (KI) revolutionieren gerade viele medizinische Bereiche, auch in der Pneumologie kommen sie zunehmend in der täglichen Praxis zum Einsatz. Interessante Entwicklungen sind zum Beispiel bei der Atemfunktionsdiagnostik, in der Therapie mit digitalisierten Inhalatoren und in der Bildgebung zu vermelden, wo die KI bei Lungenkrebs-Screenings und der Früherkennung von interstitiellen Lungenerkrankungen neue Möglichkeiten eröffnen könnte.
Keypoints
-
KI in der Medizin ist auf dem Vormarsch, das supportive Potenzial in der Pneumologie ist enorm – mit Nutzen und Risiko sollten wir uns jetzt vermehrt auseinandersetzen.
-
Wir brauchen eine Optimierung von Schnittstellen und Datenschutz.
-
KI-Unterstützung kann der Schlüssel im Hinblick auf den zukünftigen Personalengpass sein – besonders ILD-, COPD- und Lungenkarzinom-Patienten könnten von KI-gestützten Screenings profitieren.
-
Bitten Sie Ihren Software-Provider für Atemfunktionsuntersuchung um ein Update der Referenzwerte und Befunddarstellung gemäß aktueller ÖGP-Vorgabe – so erhalten Sie LLN, Z-Scores, FEF etc.
Atemfunktionsdiagnostik inklusive der Spirometrie (wörtlich: „Vermessung der Atmung“), findet breite Anwendung bei Screening, Diagnostik und Follow-up von Lungenerkrankungen im Bereich der Pneumologie sowie der inneren Medizin bis hin zur Allgemein- und Arbeitsmedizin.
Ein Großteil der Spirometrien wird im ambulanten Setting durchgeführt, dabei werden österreichweit und auch international unterschiedliche Standards in der Durchführung sowie der Befunddarstellung und der Interpretation verwendet. Letzteres führt in der Praxis zu relevanten Qualitätsunterschieden der Untersuchungen, infolgedessen zu einer limitierten Vergleichbarkeit der Befunde und im schlimmsten Fall zu fehlenden oder falschen therapeutischen Konsequenzen für Patienten. Wie zukünftig Standardisierungen aussehen und welche Möglichkeiten sich durch den Einsatz von künstlicher Intelligenz in der Pneumologie ergeben könnten, wird im Folgenden diskutiert.
Spirometrie
Die Spirometrie ist die am häufigsten verwendete pulmonale Funktionsdiagnostik. Zur Diagnosestellung und zum Follow-up von obstruktiven Lungenerkrankungen, welche einen Großteil von Morbidität und Mortalität im Bereich der Pneumologie ausmachen, bleibt sie als zentraler Wegweiser unerlässlich. Insbesondere die Nichtinvasivität sowie die schnelle Verfügbarkeit und die relativ kostengünstige Durchführbarkeit machen die Spirometrie so relevant.
Bekannte und häufig beschriebene Schwächen der Spirometrie sind zum einen die relativ hohe Compliance-Anforderung an den Patienten, die Streuung von Messwerten je nach verwendeten Referenzwerten sowie zum anderen die teilweise eingeschränkte Reproduzierbarkeit von Messungen, bei der es auf Zusammenspiel von Patient, Untersucher und „Anordner/Interpretierer“ (Arzt) ankommt.
Standardisierung von Referenzwerten
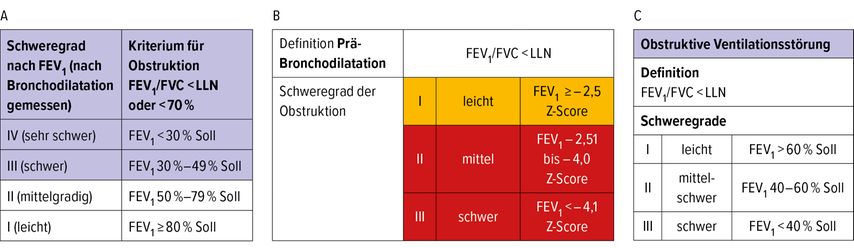
Des Weiteren lässt sich eine Limitation der Vergleichbarkeit von Untersuchungen schon am Beispiel der Referenzwerte bzw. Schweregradeinteilung beschreiben, während die Österreichische Gesellschaft für Pneumologie (ÖGP) und die Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP) sich aktuell für eine Verwendung von Werten der Global Lung Initiative (GLI) inkl. LLN(„lower limit of normal“; unterer Grenzwert)- und Z-Score mit einer dreistufigen Graduierung aussprechen,1 in welche zukünftig ggf. auch Werte aus der LEAD-Studie2 einfließen (Abb. 1).
Abb. 1: Graduierung des Schweregrads einer Atemwegsobstruktion im Vergleich, modifiziert nach A: S2k-Leitlinie zur Diagnostik und Therapie von Patienten mit chronisch obstruktiver Bronchitis und Lungenemphysem (COPD) 201811, B: ÖGP-Skriptum Spirometrie 20231, C: Nationale Versorgungsleitlinie COPD 202112(FEV1= Einsekundenkpazität; FVC= forcierte Vitalkapazität; FEV1/FVC= relative Einsekundenkapazität; LLN= unterer Grenzwert)
Der GOLD-Report empfiehlt auch im Jahr 2024 primär die Verwendung der altbewährten FEV1/FVC-Ratio <70% mit anschließender vierstufiger Graduierung anhand des FEV1,wenn es um die Diagnose einer COPD geht.3 Die Österreichische Gesellschaft für Arbeitsmedizin muss sich hingegen laut Gesetzgeber mit den Sollwerten nach Forche und Neuberger zurechtfinden.4 Hintergrund hierzu ist unter anderem, dass die meisten Therapiestudien aus dem angloamerikanischen Raum kommen und deshalb analog zum GOLD-Report durchgeführt werden. Dass die Verwendung von LLN- und Z-Score zu weniger unterdiagnostizierten jungen und zu weniger überdiagnostizierten älteren Patienten führt, ist dagegen im deutschsprachigen Raum seit vielen Jahre akzeptiert.
Ihr Patient – zugewiesen vom niedergelassenen Lungenfacharzt, zuvor erstdiagnostiziert vom betrieblichen Arbeitsmediziner – könnte also theoretisch in Ihrer Lungenambulanz die dritte möglicherweise unterschiedliche COPD-Grad-II-Diagnose erhalten.
Während die nationale und internationale Standardisierung von Referenzwerten und Untersuchungen in der Pneumologie sowie in der Medizin generell ein Jahrzehnte altes Streitthema bleibt, ergibt sich aktuell eine Vielzahl neuer Möglichkeiten und Fragestellungen durch dasVoranschreiten der Digitalisierung und den Einsatz von künstlicher Intelligenz.
Künstliche Intelligenz
Insbesondere spannende Entwicklungen gibt es bei der durch künstliche Intelligenz (KI) unterstützten Interpretation von Atemfunktionsdiagnostik. Zum Beispiel konnte die ArtiQ-Software mit anschaulichen Befunden nachweislich Pneumologen bei der Diagnosestellung von interstitiellen Lungenerkrankungen helfen. Daten hierzu wurden bereits im European Respiratory Journal sowie während der ÖGP-Jahrestagung veröffentlicht; weitere Veröffentlichungen werden erwartet.5
Die KI stellt derzeit immer dann ein spannendes Tool dar, wenn es um „pattern recognition“ geht – also vor allem Bilderkennung. Aber auch das Erkennen von Zahlenfolgen wird durch die Big-Data-Algorithmen sehr effizient bearbeitet. Hier ist die KI – aufgrund der gigantischen Datenmengen und deren rascher Verarbeitung – der menschlichen bereits weit überlegen. Zum Pionierfach in der Medizin entwickelt sich in diesem Bereich bereits die Radiologie,6 wovon folglich auch die Pneumologie, insbesondere im Hinblick auf Lungenkrebs-Screenings und ILD-Früherkennung, erheblich profitieren könnte.
Diese Entwicklungen sind vor allem vor dem Hintergrund der sich zukünftig weiter zuspitzenden Personalengpässe im Zusammenspiel mit einem höheren Patientenaufkommen spannend. Während bei vielen Kollegen noch Ängste und Unsicherheiten bestehen, wie sich die KI in der Medizin etablieren wird, zum Beispiel in Anbetracht der ungeklärten rechtlichen Rahmenbedingungen und offenen ethischen Fragestellungen, zeigt sich bei anderen bereits die Hoffnung, die bevorstehenden Personalmängel durch Hilfe von KI abpuffern zu können. Um es in den Worten von Dr. Narges Ahmidi vom Fraunhofer-Institut für Kognitive Systeme, München, auszudrücken: „Kein guter Arzt muss befürchten, durch die KI ersetzt zu werden. Im Gegenteil: Ein guter Arzt weiß die neuen Potenziale für sich und vor allem zum Wohle seiner Patienten zu nutzen.“7 Auch die Einschätzung von Dr. Danai Khemasuwan, Richmond, USA, welcher sich in viel zitierten Arbeiten mit den Möglichkeiten der KI in der Pneumologie auseinandergesetzt hat, ist hier erwähnenswert: KI wird zwangsläufig Teil der klinischen Praxis. In Anbetracht dessen, wie die KI andere Branchen schon heute positiv beeinflusst, ist die Zukunft bereits da.8
Abgesehen von den Möglichkeiten durch die KI sollten wir in Österreich auch eine Verbesserung der Schnittstellen forcieren. Angefangen bei zahlreichen digitalen Medizinprodukten in Kliniken, zwischen denen derzeit kein Austausch stattfindet, bis hin zur teilweise unvollständig etablierten elektronischen Gesundheitsakte bleiben hier viele Bereiche im Alltag unzufriedenstellend.
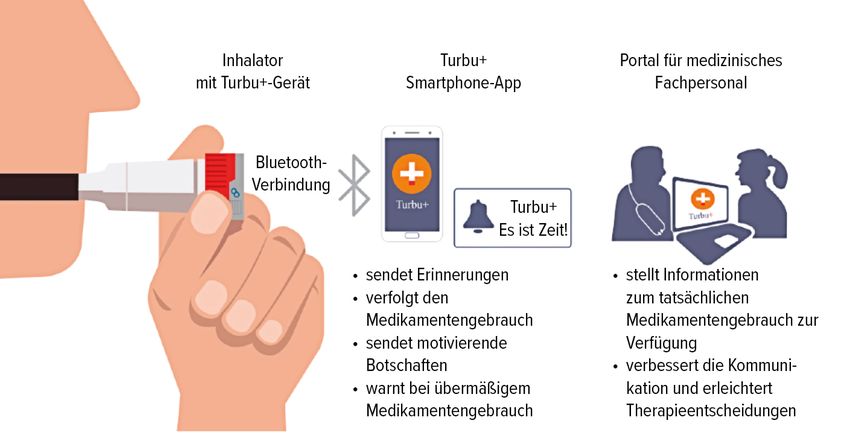
Für Aufsehen sorgte jüngst die italienische Veröffentlichung zum Turbu+-Programm.9 Ziel war es, einem immerwährenden Problem der Pneumologie mit einem digitalen Inhalator zu begegnen: der niedrigen Adhärenz bei inhalativen Therapien von Asthmapatienten – je nach Quelle <50% bis zu >70%. Der digitale Inhalator gibt nicht nur sofortiges Feedback an das Patienten-Smartphone zum Zeitpunkt der Routineanwendung, damit diese nicht verpasst wird, sondern konnte auch die Inhalationstechnik selber qualitativ bewerten (Abb. 2). In der Studie konnte zwar eine hohe Medikationsadhärenz dokumentiert werden, ob diese eindeutig auf den elektronisch überwachten digitalen Inhalator zurückzuführen war, blieb aber offen.9
Abb. 2: Digitaler Inhalator (modifiziert nach Rumi G et al. 2022)9
Schließen möchte ich mit einer offenen Frage und folgendem Denkanstoß: „Wenn wir es (hoffentlich) schaffen sollten, in Österreich ein Lungenkrebs-Screening zu etablieren, zum Beispiel, wie es Prof. Dr. Vogel-Claussen im Rahmen der HANSE-Studie10 vorgemacht hat, wer soll dann zukünftig die Tausenden zusätzlich anfallenden CT befunden?“
Literatur:
1ÖGP: Spirometrie, 3. Auflage. https://www.ogp.at/wp-content/uploads/Spirometrie-Skriptum-OeGP-2023.pdf ;zuletzt aufgerufen am 22.5.2024 2 The Austrian LEAD Study: https://leadstudy.at/ ; zuletzt aufgerufen am 22.5.2024 3 2024 GOLD Report: https://goldcopd.org/2024-gold-report/ ; zuletzt aufgerfufen am 22.5.2024 4 https://www.arbeitsinspektion.gv.at/Gesundheit_im_Betrieb/Gesundheitsueberwachung/Untersuchungsintervalle_und_Untersuchungsumfang.html ; zuletzt aufgerufen am 22.5.2024 5 Topalovic M et al.: Artificial intelligence outperforms pulmonologists in the interpretation of pulmonary function tests. Eur Respir J 2019; 53: 1801660 6 Bonekamp D, Schlemmer HP: Künstliche Intelligenz (KI) in der Radiologie? Urologe 2022; 61(4): 392-9 7 kvt impuls – Magazin der Kassenärztlichen Vereinigung Thüringen (KVT). Ausgabe 2/2023; https://www.kv-thueringen.de/fileadmin/media2/Kommunikation/kvtimpuls/2023/230630_Mitgliedermagazin_impuls_2_2023.pdf ; zuletzt aufgerufen am 22.5.2024 8 Khemasuwan D et al.: Artificial intelligence in pulmonary medicine: computer vision, predictive model and COVID-19. Eur Respir Rev 2020; 29(157): 200181 9 Rumi G, Canonica GW, Foster JM, Chavannes NH, Valenti G, Contiguglia R, Rapsomaniki E, Kocks JWH, De Brasi D, Braido F: Digital coaching using smart inhaler technology to improve asthma management in patients with asthma in Italy: community-based study. JMIR Mhealth Uhealth 2022; 10(11): e25879. Erratum in: JMIR Mhealth Uhealth 2022; 10(11): e44532 10 HANSE Studie SOLACE: https://www.hanse-lungencheck.de/ ; zuletzt aufgerufen am 22.5.2024 11 S2k-Leitlinie zur Diagnostik und Therapie von Patienten mit chronisch obstruktiver Bronchitis und Lungenemphysem (COPD) 2018; https://register.awmf.org/assets/guidelines/020-006l_S2k_COPD_chronisch-obstruktive-Lungenerkrankung_2018-01.pdf ; zuletzt aufgerufen am 22.5.2024 12 Nationale Versorgungsleitlinie COPD 2021. https://register.awmf.org/assets/guidelines/nvl-003k_S3_COPD_2021-09.pdf ; zuletzt aufgerufen am 22.5.2024
Das könnte Sie auch interessieren:
Neue Wege bei Bronchiektasen mit DPP-1-Inhibitoren
Bei Bronchiektasen werden vermehrt neutrophile Granulozyten in den Atemwegen nachgewiesen, die Serinproteasen freisetzen und so das Gewebe schädigen. Innovative Therapien wie der erste ...
COPD: neue Leitlinie für eine bessere Patientenversorgung
Die aktualisierte S2k-Leitlinie „Fachärztliche Diagnostik und Therapie der chronisch obstruktiven Lungenerkrankung (COPD) 2026“ wurde im Februar publiziert und beim DGP-Kongress im März ...