Mammakarzinom: Update Prognosefaktoren und Biomarker
Autoren:
Dr. med. Michael Schmid
PD Dr. med. Aurelia Noske
Institut für klinische Pathologie medica, Zürich
E-Mail: m.schmid@medica.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Prognostische und prädiktive Biomarker sind für die personalisierte Therapie des Mammakarzinoms unerlässlich. Der folgende Artikel gibt – unter Berücksichtigung der aktualisierten WHO-Klassifikation – einen Überblick.
Keypoints
-
Hormonrezeptoren und HER2 gehören zu den Standard-Biomarkern. Eine Östrogenrezeptorexpression von 1–10% entspricht neu einer geringen Positivität.
-
Der PD-L1-Status ist erforderlich zur Prädiktion von Therapien mit Immuncheckpoint-Inhibitoren beim metastasierten tripelnegativen Karzinom.
-
BRCA1/2-Keimbahnmutationen sind prädiktiv für Therapien mit PARP-Inhibitoren.
-
Der Nachweis von PIK3CA- und ESR1-Mutationen ist therapeutisch relevant und kann am Tumorgewebe oder mit einer Blutprobe (sog. «liquid biopsy») erbracht werden.
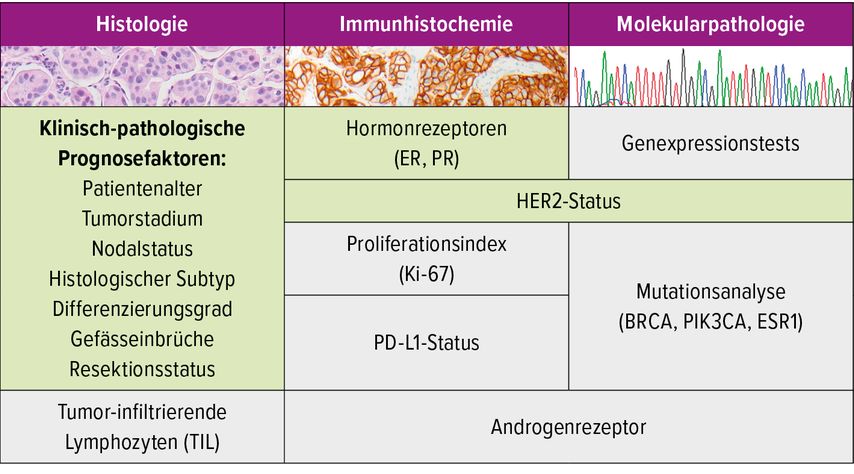
Die prognostischen und prädiktiven Biomarker für das Mammakarzinom (Abb. 1) wurden in der WHO-Klassifikation 2019 aktualisiert.1 Während Prognosefaktoren Aussagen über den zu erwartenden individuellen Krankheitsverlauf erlauben, liefern prädiktive Biomarker Hinweise auf das mögliche Ansprechen auf eine bestimmte Therapie.
Abb. 1: Prognostische und prädiktive Faktoren beim Mammakarzinom. Standard-Biomarker sind in Grün, ergänzende Biomarker in Grau dargestellt
Klinisch-pathologische Prognosefaktoren
Die traditionellen klinisch-pathologischen Prognosefaktoren, aufgelistet in Abbildung 1, gehören zu den Standardmarkern beim Mammakarzinom.
Tumor-infiltrierende Lymphozyten
Tumor-infiltrierende Lymphozyten (TIL) werden erstmalig in der WHO-Klassifikation angeführt. Tripelnegative und HER2-positive Karzinome mit vermehrten TIL sind mit einer besseren Prognose assoziiert und sprechen besser auf neoadjuvante Chemotherapien sowie Immuntherapien, z.B. mit Immuncheckpoint-Inhibitoren, an. TIL können am H&E-gefärbten histologischen Schnitt bestimmt werden. Die Angabe erfolgt in Prozent. Einen spezifischen Cut-off gibt es nicht, da sich die prognostische und prädiktive Bedeutung der TIL linear verhält.2
Hormonrezeptoren
Die immunhistochemische Bestimmung der Östrogen- (ER) und Progesteronrezeptoren (PR) erfolgt gemäss der ASCO/CAP-Leitlinie 2020. Eine Expression von ≥1% wird für beide Rezeptoren als positiv gewertet,3 wobei für den ER eine neue Kategorie eingeführt wurde. Bei einer ER-Expression von 1–10% ist nun von einer geringen Positivität auszugehen. Die Patienten können von einer endokrinen Therapie profitieren, allerdings verhalten sich diese Tumoren heterogen und können gemäss Genexpressionsstudien eher ER-negativen Tumoren ähneln. Für den PR gibt es bislang keine solche Kategorie, wobei sich eine geringe Expression prognostisch eher ungünstig auswirkt.
HER2-Status
Die immunhistochemische Analyse von HER2 beruht auf der Intensität und Ausprägung der membranären Expression auf einer vierstufigen Skala (Score 0 bis 3+) gemäss der ASCO/CAP-Leitlinie 2018.4 Tumoren ohne oder mit nur geringer Expression (Score 0, 1+) gelten als negativ, solche mit starker Expression (Score 3+) als positiv. Bei einem Score 2+ ist der HER2-Status unklar und eine In-situ-Hybridisierung zur Abklärung einer möglichen HER2-Amplifikation ist angezeigt.
Proliferationsindex (Ki-67)
Bei hormonrezeptorpositiven Karzinomen kann der Proliferationsmarker Ki-67 als Entscheidungshilfe für oder gegen eine Chemotherapie hilfreich sein. Die aktuelle WHO-Klassifikation diskutiert den Cut-off von 14 bzw. 15% zur Abgrenzung der luminalen molekularen intrinsischen Subtypen («A» versus «B»), gibt aber keine generelle Empfehlung.1 Ein kürzlich publiziertes Update der internationalen Ki-67-Arbeitsgruppe empfiehlt dagegen für ER-positive Tumoren mit einem Proliferationsindex ≥30% eine Chemotherapie und ≤5% einen Verzicht.5
Genexpressionstests
Beim frühen ER-positiven, HER2-negativen Mammakarzinom können Genexpressionstests die Risikoabschätzung und entsprechende Therapiewahl erleichtern. Zeigt die Gensignatur ein geringes Risikoprofil an, dann kann vor allem bei einem negativen Nodalstatus auf eine Chemotherapie verzichtet werden. Verschiedene Tests stehen zur Verfügung, wobei prospektive Daten nur für den 21-Gen-Recurrence-Score und die 70-Gen-Signatur vorliegen, die einen prognostischen Wert (Evidenzgrad 1a) bescheinigen.
Androgenrezeptor
Die Bestimmung der Expression des Androgenrezeptors (AR) erfolgt nur in bestimmten Konstellationen, z.B. beim metastasierten tripelnegativen Mammakarzinom (TNBC).6 Eine Subgruppe der TNBC ist durch eine Expression des AR gekennzeichnet, wo eine antiandrogene Therapie von Nutzen sein kann.
PD-L1-Status
Die Immuncheckpoint-Inhibitoren (Atezolizumab, Pembrolizumab) ermöglichen eine neue Therapie des fortgeschrittenen und metastasierten TNBC. Die Bestimmung von PD-L1 ist zur Prädiktion erforderlich und kann am Primärtumor- oder Metastasengewebe erfolgen. In den Zulassungsstudien (IMpassion130, Keynote- 355) wurden unterschiedliche immunhistochemische Assays und Scoring-Methoden verwendet.7,8 Demnach wird für Atezolizumab der sog. Immunzell(IC)-Score (Klon SP142, IC ≥1% positiv) und für Pembrolizumab hingegen der sog. Combined Positive Score (CPS) empfohlen, der die PD-L1-Expression nicht nur in Immunzellen, sondern auch in Tumorzellen berücksichtigt (Klon 22C3, CPS ≥10 positiv). Im Pathologiebericht sollten beide Scoring-Methoden angegeben sein.
BRCA-Mutationen
Bei 5–10% der Mammakarzinome sind Keimbahnmutationen in den BRCA1/2-Genen nachweisbar, die die DNA-Reparatur durch einen Verlust der sog. homologen Rekombination (HR) beeinträchtigen. Die Keimbahnmutationen gehen mit einem besseren Ansprechen auf Platin-haltige Chemotherapie einher und sind prädiktiv für PARP-Inhibitoren.9 Nicht nur bei fortgeschrittenen HER2-negativen Karzinomen, sondern auch im frühen Stadium, wie die aktuelle OlympiA-Studie zeigt, verlängert eine adjuvante Therapie mit Olaparib das invasive krankheitsfreie Überleben.10 Der Nachweis somatischer Mutationen hat bislang keinen prädiktiven Wert. Es ist davon auszugehen, dass PARP-Inhibitoren zukünftig auch bei Mammakarzinomen mit sog. «BRCAness» (Mutationen in HR-assoziierten Genen, wie u.a. PALB2, RAD51, BRIP1, ATM) und HR-Defizienz (HRD) therapeutisch relevant sind.11
PIK3CA-Mutationen
Mutationen der katalytischen α-Untereinheit von PI3K (PIK3CA) finden sich bei bis zu 30% der Mammakarzinome.12 Mehrheitlich sind hormonrezeptorpositive, HER2-negative Karzinome betroffen, welche aufgrund eines geringeren Ansprechens auf die endokrine und Chemotherapie eine schlechtere Prognose haben. Für diese Subgruppe wurde im fortgeschrittenen Stadium der PI3K-Inhibitor Alpelisib zugelassen, der zu einem längeren progressionsfreien Überleben führt.13 Voraussetzung für diese Therapie ist der Nachweis einer PIK3CA-Mutation am Tumorgewebe oder in einer Blutprobe (sog. «liquid biopsy»).14
ESR1-Mutationen
Mutationen im für den Östrogenrezeptor-α codierenden ESR1-Gen sind häufiger beim metastasierten Mammakarzinom (30–40%) als im Primärtumor (<5%) nachweisbar. Sie führen über eine Östrogen-unabhängige Aktivierung des Östrogenrezeptors zu einer endokrinen Resistenz,15 was sich prognostisch ungünstig auswirkt. Auch hier erfolgt der Mutationsnachweis wahlweise am Tumorgewebe oder anhand einer Blutprobe.
Weitere molekulare Aberrationen
Die Testung auf Mikrosatelliteninstabilität (MSI) ist aufgrund der geringen Rate an mikrosatelliteninstabilen Mammakarzinomen (sog. MSI-H) von <1,5% zum jetzigen Zeitpunkt keine Routineuntersuchung.16 Die Bestimmung der Gesamtmutationslast (sog. «tumor mutation burden», TMB) hingegen könnte in naher Zukunft an Bedeutung gewinnen. So weisen etwa 5% der Mammakarzinome eine hohe Gesamtmutationslast auf (≥10 Mutationen pro Megabase; sog. «high TMB») und vorläufige Daten zeigen in diesen Fällen ein besseres Ansprechen auf Immuncheckpoint-Inhibitoren.17 Genfusionen der neurotrophen Tyrosin-Rezeptor-Kinase (NTRK) finden sich beim metastasierten Mammakarzinom bei <1%.18 Ausgesprochen häufig (>90%) sind sie beim sekretorischen Subtyp, der jedoch sehr selten (<1% aller Mammakarzinome) ist. Alle soliden Tumoren mit molekularpathologisch nachgewiesener NTRK-Genfusion, Mammakarzinome jeglicher Art eingeschlossen, können tumoragnostisch mit NTRK-Inhibitoren behandelt werden.
Literatur:
1 WHO classification of tumours editorial board: Breast tumours. WHO classification of tumours. 5. Aufl. IARC Press, 2019 2 Salgado R et al.: The evaluation of tumor-infiltrating lymphocytes (TILs) in breast cancer: recommendations by an international TILs working group 2014. Ann Oncol 2015; 26(2): 259-71 3 Allison K et al.: Estrogen and progesterone receptor testing in breast cancer: ASCO/CAP guideline update. J Clin Oncol 2020; 38(12): 1346-66 4 Wolff A et al.: Human epidermal growth factor receptor 2 testing in breast cancer: American society of clinical oncology/college of American pathologists clinical practice guideline focused update. J Clin Oncol 2018; 36(20): 2105-22 5 Nielsen T et al.: Assessment of Ki67 in breast cancer: updated recommendations from the international Ki67 in breast cancer working group. J Natl Cancer Inst 2021; 113(7): 808-19 6 Gerratana L et al.: Androgen receptor in triple negative breast cancer: a potential target for the targetless subtype. Cancer Treat Rev 2018; 68: 102-10 7 Schmid P et al.: Atezolizumab and Nab-Paclitaxel in advanced triple-negative breast cancer. N Engl J Med 2018; 379(22): 2108-21 8 Cortes J et al.: Pembrolizumab plus chemotherapy versus placebo plus chemotherapy for previously untreated locally recurrent inoperable or metastatic triple-negative breast cancer (KEYNOTE-355): a randomised, placebo-controlled, double-blind, phase 3 clinical trial. Lancet 2020; 396(10265): 1817-28 9 Robson M et al.: Olaparib for metastatic breast cancer in patients with a germline BRCA mutation. N Engl J Med 2017; 377(6): 523-33 10 Tutt ANJ et al.: Adjuvant Olaparib for patients with BRCA1- or BRCA2-mutated breast cancer. N Engl J Med 2021; 384(25): 2394-405 11 Lord CJ et al.: BRCAness revisited. Nat Rev Cancer 2016; 16(2): 110-20 12 Shimoi T et al.: PIK3CA mutation profiling in patients with breast cancer, using a highly sensitive detection system. Cancer Sci 2018; 109(8): 2558-66 13 André F et al.: Alpelisib for PIK3CA-mutated, hormone receptor-positive advanced breast cancer. N Engl J Med 2019; 380(20): 1929-40 14 Banys-Paluchowski M et al.: Liquid biopsy in breast cancer. Geburtshilfe Frauenheilkd 2020; 80(11): 1093-104 15 Angus L et al.: ESR1 mutations: moving towards guiding treatment decision-making in metastatic breast cancer patients. Cancer Treat Rev 2017; 52: 33-40 16 Horimoto Y et al.: Microsatellite instability and mismatch repair protein expressions in lymphocyte-predominant breast cancer. Cancer Sci 2020; 111(7): 2647-54 17 Barroso-Sousa R et al.: Prevalence and mutational determinants of high tumor mutation burden in breast cancer. Ann Oncol 2020; 31(3): 387-94 18 Ross JS et al.: Abstract P2-09-15: NTRK fusions in breast cancer: clinical, pathologic and genomic findings. Cancer Res 2018; 78(4 Suppl): P2-09-15
Das könnte Sie auch interessieren:
Organische Quervernetzer als Schlüssel zur Osteoporoseprophylaxe
Osteoporose gehört zu den häufigsten altersbedingten Erkrankungen und betrifft vor allem postmenopausale Frauen. Während die Leitlinie zur Prävention vorrangig Kalzium und Vitamin D zur ...
Ernährung und Supplemente in der Menopause
Die Menopause ist eine Phase tiefgreifender hormoneller Veränderungen, die mit verschiedenen Beschwerden einhergehen kann. Parallel dazu wächst das Angebot an Ernährungskonzepten und ...
Hormonelle Veränderungen erkennen und begleiten
In Österreich sind rund 56% aller Frauen über 40 Jahre alt, die Menopause tritt im Mittel mit 51,7 Jahren ein. Damit verbringen Frauen etwa ein Drittel ihres Lebens in der Postmenopause ...