Infektiöse Endokarditis: eine ernst zu nehmende Erkrankung mit schwieriger Diagnostik
Autor:
PD Dr. med. Hajo Müller
Médecin adjoint agrégé, chargé de cours
Service de cardiologie
Unité d’échocardiographie
Hôpitaux universitaires de Genève
E-Mail: hajo.muller@hcuge.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die infektiöse Endokarditis ist eine ernst zu nehmende Erkrankung, die nach wie vor mit einer sehr hohen Mortalität und Morbidität verbunden ist. Die Diagnostik ist schwierig und stützt sich auf Blutkulturen und den Nachweis einer Herzläsion als Hauptkriterien. Die Einbindung von Kardiologen in den diagnostischen Prozess und die Therapie erfolgen im Rahmen eines multidisziplinären Ansatzes («Endokarditis-Team»). Die bildgebenden Verfahren der Wahl sind nach wie vor die transthorakale und die transösophageale Echokardiografie, die sich gegenseitig ergänzen.
Keypoints
-
Die infektiöse Endokarditis ist eine ernst zu nehmende Erkrankung, die nach wie vor mit einer sehr hohen Mortalität und Morbidität verbunden ist.
-
Bei Fieber in Kombination mit einer Klappenprothese, einem ischämischen Schlaganfall oder einer neu aufgetretenen Klappen- oder Herzinsuffizienz muss grundsätzlich an eine Endokarditis gedacht werden.
-
Die Diagnostik kann sich schwierig gestalten und stützt sich auf das klinische Bild, die Blutkulturen und den Nachweis einer Herzläsion durch bildgebende Verfahren.
-
Angesichts der schwierigen Diagnostik und des komplexen klinischen Bildes wird dringend empfohlen, die Patienten im Rahmen einer multidisziplinären Gruppe (Endokarditis-Team) zu beurteilen.
Klassifikationen und Definitionen
Die infektiöse Endokarditis (IE) kann nach verschiedenen Gesichtspunkten klassifiziert werden, etwa nach der Lokalisation der Infektion, dem Vorhandensein oder Fehlen von intrakardialem prothetischem Material oder der Art, wie sie erworben wurde.
Unterschieden wird zum einen zwischen der linksseitigen und der rechtsseitigen Klappenendokarditis. Zum anderen wird die Nativklappen-Endokarditis von der Klappenprothesen-Endokarditis abgegrenzt. Dies ist relevant, da Morbidität und Mortalität im Spital bei einer Klappenprothesen-Endokarditis höher sind als bei einer Nativklappen-Endokarditis und bei Ersterer zur nachhaltigen Ausräumung des Infektionsherds oder aufgrund von Komplikationen häufig eine operative Therapie notwendig ist. Die Protheseninfektion kann früh (<1 Jahr nach dem Eingriff, wahrscheinlich perioperativ erworben) oder spät (>1 Jahr, wahrscheinlich ausserhalb des Spitals erworben) auftreten, was die unterschiedliche Verteilung der auslösenden Erreger erklärt. Eine besondere Kategorie stellen IE im Zusammenhang mit prothetischem Material vom Typ Herzschrittmacher oder implantierbarer Defibrillator dar. Dabei handelt es sich um eine schwierig zu diagnostizierende Kategorie, die häufig den Einsatz zusätzlicher bildgebender Verfahren wie Kardio-CT oder PET/CT erfordert.1
Des Weiteren wird zwischen der ausserhalb des Spitals erworbenen («community-acquired») und der im Rahmen einer ambulanten oder stationären Versorgung erworbenen IE unterschieden. Innerhalb letzterer Kategorie kann je nach Hospitalisierungsdauer vor der Diagnose (>48h vs. <48h) zwischen der nosokomialen und der nicht nosokomialen IE unterschieden werden.2 Eine weitere Kategorie basierend auf der Art des Erwerbs stellt die IE infolge eines i.v. Drogenabusus dar, bei der häufig die rechtsseitigen Herzklappen betroffen sind; es darf jedoch nicht vergessen werden, dass auch linksseitige Klappeninfektionen in diesem Zusammenhang häufig auftreten.
Epidemiologie und Pathogenese
Die Inzidenz der IE nimmt zu. Derzeit sind epidemiologische Veränderungen in Form einer Dominanz von Infektionen mit Staphylokokken anstelle von Streptokokken sowie einer Zunahme der im Rahmen der medizinischen Versorgung erworbenen IE-Fälle zu beobachten, wobei im Vergleich zu früher Staphylokokken-IE häufiger und die Patienten älter sind.3−5 Die IE im Zusammenhang mit mechanischen oder biologischen Klappenprothesen machen etwa 10–30% der Fälle aus und sind häufig auf Staphylokokken oder Pilze als Erreger zurückzuführen.2,3 Auch perkutan implantierte Klappenprothesen sind betroffen, wobei es sich bei den auslösenden Erregern vorrangig um Staphylokokken und Enterokokken handelt.3,6,7 Im Allgemeinen steht am Beginn des pathogenetischen Prozesses, der durch eine Läsion des Endokards mit Thrombozyten- und Fibrinablagerungen («Pseudo-Vegetationen») begünstigt wird, eine Schleimhaut- oder Hautverletzung, die zu einer Bakteriämie und in der Folge zur Adhärenz und Besiedlung der Klappen und schliesslich zu infektiösen Vegetationen führt. Zu beachten ist dabei, dass Staphylococcus aureus in der Lage ist, auch ohne vorherige Läsion des Endokards Infektionen hervorzurufen, was wahrscheinlich seinen aggressiven Charakter2,8 und die hohe Inzidenz kardialer Infektionen im Fall einer Bakteriämie mit diesem Erreger erklärt.9 Linksseitige Infektionen sind deutlich häufiger zu beobachten und wahrscheinlich auf die linksseitig höheren Druckgradienten zurückzuführen.
Klinische Manifestationen, Hauptkomplikationen und Prognose
Die IE ist eine schwere Erkrankung und stellt aufgrund ihrer hohen Letalität einen Notfall dar. Die Spitalletalität liegt für alle Arten von Endokarditiden zusammengenommen bei 15–30%5,10,11 und scheint im Fall einer Klappenprothesen-IE noch höher zu sein (20–40%).2,3 Besondere Bedeutung kommt dabei der Staph.-aureus-bedingten IE zu, die häufiger zu schweren lokalen Komplikationen führt (Abszess oder Pseudo-Aneurysma sowie schwere Klappendysfunktion mit resultierender schwerer Herzinsuffizienz oder Schock) und mit einer Letalität von bis zu 80% einhergeht.2,12 Der zweite Grund, weshalb die IE als Notfall betrachtet werden muss, ist die hohe Rate an embolischen Komplikationen, die für eine hohe Morbidität verantwortlich ist. Am häufigsten treten Embolien in Hirn und Milz auf. Klinisch manifeste Embolien sind in etwa 30% der Fälle beschrieben,13 stumme Läsionen sind jedoch ein häufiges Phänomen. In einigen Fallserien waren bei 50–80% der Patienten Hirnläsionen nachweisbar.14−16 Das klinische Bild ist somit von den lokalen und embolischen Komplikationen geprägt. Die Prognose hängt von den Merkmalen des Patienten, der Erregerart, der Art allfälliger Komplikationen und den echokardiografischen Befunden ab. Echokardiografische Marker für eine schlechte Prognose sind zum Beispiel eine stark verminderte linksventrikuläre Ejektionsfraktion und Zeichen deutlich erhöhter linksventrikulärer oder pulmonaler Füllungsdrücke. Die drei Hauptkomplikationen, die eine Indikation zu einer frühen oder dringlichen operativen Therapie darstellen, sind eine Herzinsuffizienz im Kontext einer schweren Klappendysfunktion, eine unkontrollierte Infektion (lokal, abhängig von der Art des Erregers oder bei Nichtansprechen auf die Antibiose) sowie die Prävention einer arteriellen Embolie im Rahmen der Sekundär- oder Primärprävention.2,3 Zu beachten ist dabei, dass Lokalisation, Mobilität und Grösse (>10mm)13 der Vegetationen für die Stratifikation des Embolierisikos von Bedeutung sind. Die Grösse der Vegetationen scheint auch ein Prädiktor für die Letalität zu sein, wobei ein Wert >15mm als Schwellenwert gilt.13 Die Mehrheit der Schlaganfälle ist ischämischen Ursprungs. Im Fall einer Embolie ist die Letalität der IE höher. Es besteht eine Assoziation mit der Erregerart, insbesondere mit Staph. aureus.15−17 Die Embolien nehmen nach Beginn der Antibiotikatherapie, insbesondere nach der zweiten Woche, ab.18 Etwa 50% der Patienten mit einer IE werden operiert.19 Der einzigen bisher zur Verfügung stehenden randomisierten Studie zufolge scheinen bei hämodynamisch stabilen Patienten mit niedrigem Operationsrisiko, aber einer schweren Klappendysfunktion und Vegetationen >10mm durch eine frühe Operation Embolien verhindert werden zu können.20 Ein weiterer Vorteil einer frühen Operation besteht in der Möglichkeit, die Klappenfunktion durch Reparatur erhalten zu können, statt die Klappe bei fortgeschrittenen Schädigungen durch eine Prothese ersetzen zu müssen.21
Diagnostik
Die IE ist schwierig zu diagnostizieren. Die klinische Präsentation ist variabel und die Diagnose naheliegender, wenn ein akutes klinisches Bild mit Staph.-aureus-Bakteriämie besteht. Doch manchmal ist die Situation weniger klar, etwa bei Patienten, die aufgrund einer Bronchopneumonie ins Spital aufgenommen werden,22 oder bei einem durch eine vorangegangene Antibiotikagabe verfälschtes klinisches Bild. Schwieriger ist die Diagnostik auch im Fall eines subakuten/chronischen Bildes bei afebrilen Patienten mit reduziertem Allgemeinzustand und Gewichtsverlust als Hauptsymptomen. Ältere und/oder immunsupprimierte Patienten zeigen häufig ein atypisches klinisches Bild.23 Zu beachten ist, dass es IE gibt, die nicht mit einem Anstieg des C-reaktiven Proteins als Entzündungsmarker einhergehen.
Alarmzeichen für den Kliniker sind in der Regel Fieber (90%), ein Herzgeräusch bei der Auskultation (85%) sowie klinische Manifestationen einer Embolie (25–30%). Da häufig stumme Embolien in Hirn und Milz auftreten, wird bei klinischem Verdacht auf eine IE systematisch eine bildgebende Diagnostik empfohlen. Bei Fieber in Kombination mit einer Klappenprothese, einem ischämischen Schlaganfall oder einer neu aufgetretenen Klappen- oder Herzinsuffizienz muss grundsätzlich an eine IE gedacht werden. Auch ein klinisches Bild mit Fieber unklarer Genese oder multiplen septischen Arthritiden ist möglich. Nicht zuletzt können neu aufgetretene Erregungsleitungsstörungen in Form eines atrioventrikulären Blocks (AVB) auf einen Abszess mit Beteiligung der Leitungsbahnen hindeuten. Es ist nach peripheren IE-bedingten Läsionen in Form von vaskulären und immunologischen Phänomenen zu suchen. Darüber hinaus gibt die in den Blutkulturen nachgewiesene Erregerart (z.B. HACEK-Gruppe) die Richtung für die Diagnostik vor und erlaubt Rückschlüsse auf die Wahrscheinlichkeit einer IE.
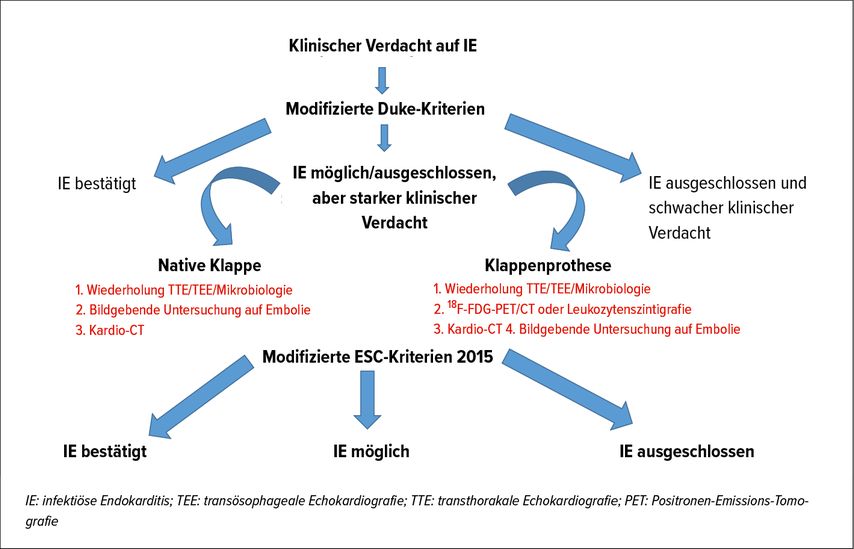
Klassischerweise stützt sich die Diagnostik auf die Duke-Kriterien, die zwei Hauptkriterien (Blutkulturen und kardiale Bildgebung) und mehrere Nebenkriterien umfassen,2,24 wobei diese bei bestimmten Subgruppen von Patienten jedoch deutlich unzuverlässiger sind, etwa bei Patienten mit Klappenprothese und intrakardialem prothetischem Material. Um die diagnostische Genauigkeit dieser Kriterien zu verbessern, hat die ESC 2015 modifizierte Kriterien veröffentlicht, die als zusätzliche Hauptkriterien bildgebende Untersuchungen mit Kardio-CT und/oder PET/CT und als neues Nebenkriterium den Nachweis embolischer Phänomene (auch wenn diese keine Symptome hervorrufen) mittels Bildgebung vorsehen (Abb. 1).3 Dadurch kann insbesondere bei Patienten mit intrakardialem prothetischem Material die Zahl der als mögliche IE eingestuften Fälle reduziert werden.25
Bildgebung
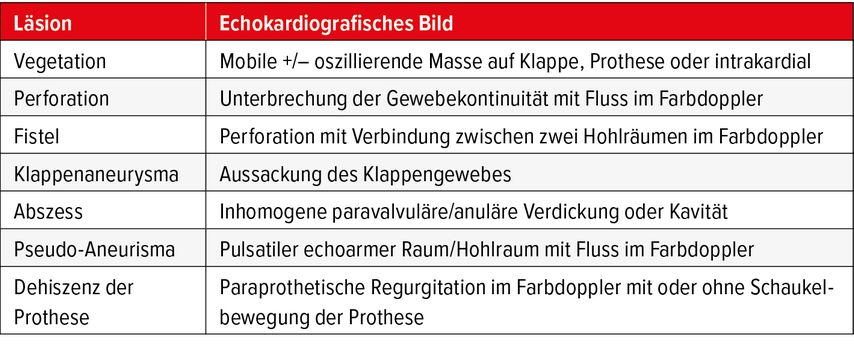
Die bildgebenden Verfahren der Wahl sind initial nach wie vor die transthorakale (TTE) und die transösophageale Echokardiografie (TEE), die sich gegenseitig ergänzen.2,3,26 Die wichtigsten echokardiografischen Hauptkriterien für eine IE sind valvuläre Läsionen in Form von Vegetationen, Perforation oder Aneurysma, paravalvuläre Läsionen in Form von Abszess, Fistel oder Pseudo-Aneurysma sowie eine Dehiszenz der Prothese mit neu aufgetretener paraprothetischer Regurgitation2,21,26,27 (Tab. 1, Abb. 2). Insgesamt wird die Sensibilität für den Nachweis einer Nativklappen-IE für die TTE auf 70% und für die TEE auf 96% beziffert.3 Die diagnostische Genauigkeit ist jedoch vor allem bei der TTE von Patienten mit Prothesen oder intrakardialem Material niedriger (Sensibilität von 50% bzw. 92%).3 Falsch positive Ergebnisse sind möglich, da es für eine infektiöse Vegetation in der Echokardiografie eine Reihe möglicher Differenzialdiagnosen wie Thrombus, nicht bakterielle Vegetation, Sehnenfadenruptur und Klappentumor gibt. Bei der Interpretation der Bilder ist deshalb stets der klinische Kontext zu berücksichtigen und nach Möglichkeit ein Vergleich mit früheren Untersuchungen vorzunehmen.
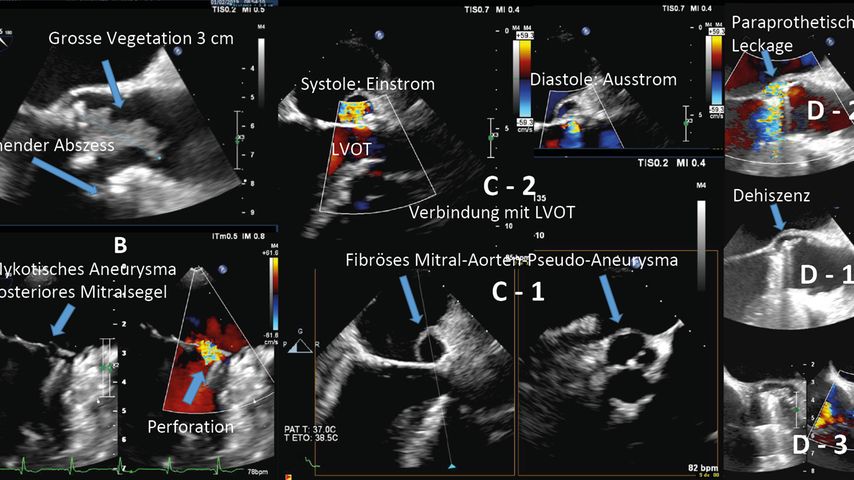
Abb. 2: Echokardiografie-Aufnahmen von Endokarditiden. A: 3cm grosse Vegetation an biologischer Aortenklappenprothese mit beginnendem periprothetischem Abszess im Bereich der anterioren Wand der Aortenwurzel. B: Mykotisches Aneurysma in Segment P1 des posterioren Segels der Mitralklappe mit Perforation (Farbdoppler-Fluss). C: Pseudo-Aneurysma der fibrösen Mitral-Aorten-Region (C-1), das mit dem linksventrikulären Ausflusstrakt (LVOT) in Verbindung steht, mit Füllung in der Systole und Austreibung in der Diastole (C-2) im Farbdoppler. D: Dehiszenz einer mechanischen Aortenklappenprothese (D-1) mit paraprothetischer Regurgitation (D-2) im posterioren Bereich. Kurzachsenblick (D-3)
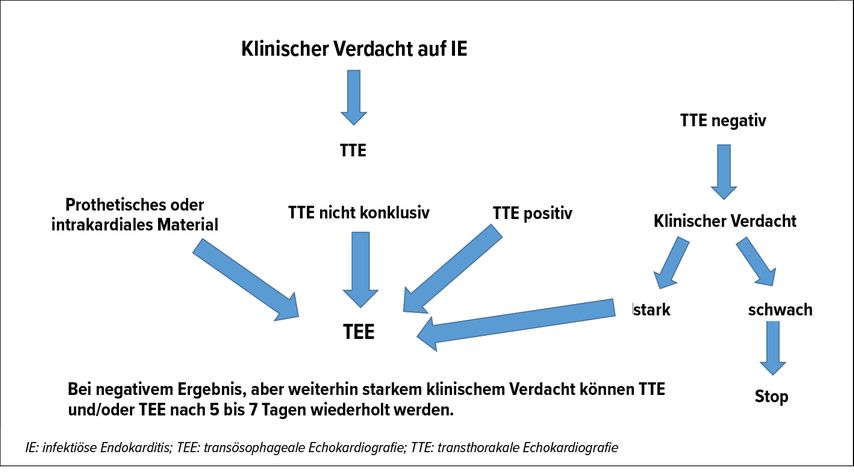
Je nach klinischem Verdacht und Ergebnis der initialen TTE wird im Anschluss eine TEE durchgeführt oder die IE als Diagnose ausgeschlossen. Falls die TTE zu einem positiven Befund führt oder nicht schlüssig ist oder falls prothetisches oder intrakardiales Material vorhanden ist, wird eine TEE vorgenommen. Fällt diese negativ aus, obwohl der klinische Verdacht nach wie vor stark ist, sollte eine der Untersuchungen nach 5 bis 7 Tagen wiederholt werden (Abb. 3). Im Sonderfall einer IE der rechtsseitigen Klappen, die anterior liegen, ist eine alleinige TTE mitunter ausreichend, da sich die rechtsseitigen Klappen mit diesem Verfahren gut darstellen lassen. Dennoch muss im Hinterkopf behalten werden, dass gleichzeitig auch die linksseitigen Klappen betroffen sein können, was bei geringstem Verdacht abgeklärt werden muss.
Abb. 3: Endokarditis-Verdacht – Indikationen zur Echokardiografie (modifiziert nach Habib et al., 2009, und Habib et al., 2015)2,3
Die Diagnostik von paravalvulären Komplikationen, insbesondere eines beginnenden Abszesses in der Umgebung von Klappenprothesen, kann sich schwierig gestalten, weshalb in dieser Situation eine ergänzende bildgebende Untersuchung mittels Kardio-CT empfohlen wird,3,28,29 auch wenn ihre Überlegenheit gegenüber der TEE nicht erwiesen ist.30 Zu berücksichtigen sind dabei auch die Toxizität des Kontrastmittels und die Strahlenbelastung. Dafür liefert die Untersuchung den Spezialisten der Herz- und Gefässchirurgie jedoch ergänzende Informationen für den Fall, dass ein Eingriff notwendig wird. Weitere diagnostische Verfahren zur Untersuchung auf einen periprothetischen oder extrakardialen Entzündungsherd sind die PET/CT oder die Szintigrafie mit radioaktiv markierten Leukozyten.1,3 Die Untersuchung ist nicht überall verfügbar, aber sehr nützlich bei der Suche nach einem beginnenden periprothetischen Abszess, wenn die TEE negativ ausgefallen ist, oder bei Verdacht auf eine Infektion des Aggregats bei Patienten mit Herzschrittmacher. Zu beachten ist, dass die PET/CT insbesondere in der Entzündungsphase nach der Operation zu falsch positiven Ergebnissen führen kann.1,3
Endokarditis-Team
Angesichts der schwierigen Diagnostik und des komplexen klinischen Bildes wird dringend empfohlen, die Patienten im Rahmen einer multidisziplinären Gruppe (Endokarditis-Team) zu beurteilen. Ein solches Team sollte sich aus Spezialisten für Infektiologie, Kardiologie und Herz- und Gefässchirurgie mit entsprechender Erfahrung zusammensetzen und bei Bedarf durch einen Neurologen ergänzt werden. Die Literatur deutet darauf hin, dass sich eine solche systematische Versorgung dieser komplexen Patienten positiv auf die Mortalität auswirkt.31,32
Literatur:
1 Bruun NE et al.: Cardiac imaging in infectious endocarditis. Eur Heart J 2014; 35: 624-32 2 Habib G et al.: Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009): the Task Force on the Prevention, Diagnosis, and Treatment of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by the European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and the International Society of Chemotherapy (ISC) for Infection and Cancer. Eur Heart J 2009; 30: 2369-413 3 Habib G et al.: 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by: European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). Eur Heart J 2015; 36: 3075-128 4 Fernández-Hidalgo N et al.: Contemporary epidemiology and prognosis of health care-associated infective endocarditis. Clin Infect Dis 2008; 47: 1287-97 5 Slipczuk L et al.: Infective endocarditis epidemiology over five decades: a systematic review. PLoS One 2013; 8: e82665 6 Khan A et al.: Infective endocarditis post-transcatheter aortic valve implantation (TAVI), microbiological profile and clinical outcomes: A systematic review. PLoS One 2020; 15: e0225077 7Amat-Santos IJ et al.: Infective endocarditis after transcatheter aortic valve implantation: results from a large multicenter registry. Circulation 2015; 131: 1566-74 8 Que YA et al.: Fibrinogen and fibronectin binding cooperate for valve infection and invasion in Staphylococcus aureus experimental endocarditis. J Exp Med 2005; 201: 1627-35 9 Rasmussen RV et al.: Prevalence of infective endocarditis in patients with Staphylococcus aureus bacteraemia: the value of screening with echocardiography. Eur J Echocardiogr 2011; 12: 414-20 10 Cahill TJ, Prendergast BD: Infective endocarditis. Lancet 2016; 387: 882-93 11 Murdoch DR et al.: Clinical presentation, etiology, and outcome of infective endocarditis in the 21st century: the International Collaboration on Endocarditis-Prospective Cohort Study. Arch Intern Med 2009; 169: 463-73 12 San Román JA et al.: Prognostic stratification of patients with left-sided endocarditis determined at admission. Am J Med 2007; 120: 369.e1-7 13 Thuny F et al.: Risk of embolism and death in infective endocarditis: prognostic value of echocardiography: a prospective multicenter study. Circulation 2005; 112: 69-75 14 Snygg-Martin U et al.: Cerebrovascular complications in patients with left-sided infective endocarditis are common: a prospective study using magnetic resonance imaging and neurochemical brain damage markers. Clin Infect Dis 2008; 47: 23-30 15 Cooper HA et al.: Subclinical brain embolization in left-sided infective endocarditis: results from the evaluation by MRI of the brains of patients with left-sided intracardiac solid masses (EMBOLISM) pilot study. Circulation 2009; 120: 585-91 16 Iung B et al.: Determinants of cerebral lesions in endocarditis on systematic cerebral magnetic resonance imaging: a prospective study. Stroke 2013; 44: 3056-62 17 Lebowitz D et al.: Disseminated emboli caused by a large Vegetation in Staphylococcus aureus Endocarditis. Am J Clin Microbiol Antimicrob 2018; 1: 1021 18 Dickerman SA et al.: The relationship between the initiation of antimicrobial therapy and the incidence of stroke in infective endocarditis: an analysis from the ICE Prospective Cohort Study (ICE-PCS). Am Heart J 2007; 154: 1086-94 19 Tornos P et al.: Infective endocarditis in Europe: lessons from the Euro heart survey. Heart 2005; 91: 571-5 20 Kang DH et al.: Early surgery versus conventional treatment for infective endocarditis. N Engl J Med 2012; 366: 2466-73 21 Müller H et al.: Mitral valve repair in acute extensive infectious endocarditis. Arch Cardiovasc Dis 2009; 102: 667-8 22 Mossaz L et al.: What seemed to be a typical pneumonia. Cardiovascular Medicine 2014; 16: 171 23 Pérez de Isla L et al.: Negative blood culture infective endocarditis in the elderly: long-term follow-up. Gerontology 2007; 53: 245-9 24 Li JS et al.: Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000; 30: 633-8 25 Saby L et al.: Positron emission tomography/computed tomography for diagnosis of prosthetic valve endocarditis: increased valvular 18F-fluorodeoxyglucose uptake as a novel major criterion. J Am Coll Cardiol 2013; 61: 2374-82 26 Habib G et al.: Recommendations for the practice of echocardiography in infective endocarditis. Eur J Echocardiogr 2010; 11: 202-19 27 Müller H et al.: Subaortic aneurysm caused by Paecilomyces lilacinus endocarditis. Arch Cardiovasc Dis 2008; 101: 803-4 28 Feuchtner GM et al.: Multislice computed tomography in infective endocarditis: comparison with transesophageal echocardiography and intraoperative findings. J Am Coll Cardiol 2009; 53: 436-44 29 Fagman E et al.: ECG-gated computed tomography: a new role for patients with suspected aortic prosthetic valve endocarditis. Eur Radiol 2012; 22: 2407-14 30 Sifaoui I et al.: Diagnostic performance of transesophageal echocardiography and cardiac computed tomography in infective endocarditis. J Am Soc Echocardiogr 2020; 33: 1442-53 31Chirillo F et al.: Impact of a multidisciplinary management strategy on the outcome of patients with native valve infective endocarditis. Am J Cardiol 2013; 112: 1171-6 32 Botelho-Nevers E et al.: Dramatic reduction in infective endocarditis-related mortality with a management-based approach. Arch Intern Med 2009; 169: 1290-8
Das könnte Sie auch interessieren:
Abklärung der Linksventrikelhypertrophie
Die Abklärung der Linksventrikelhypertrophie (LVH) rückt in den Fokus. Es stehen diverse neue Therapiemöglichkeiten sowohl bei hypertropher Kardiomyopathie (HCM) bzw. hypertropher ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...