Die erste internationale multidisziplinäre MASLD-Leitlinie 2024
Autoren:
Dr. Paul Horn, PhD
Prof. Dr. Frank Tacke
Medizinische Klinik m.S. Hepatologie und Gastroenterologie
Charité – Universitätsmedizin Berlin
Campus Virchow-Klinikum und Campus Charité Mitte
Berlin
E-Mail: paul.horn@charite.de
E-Mail: frank.tacke@charite.de
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die neue europäische Leitlinie zum Management der mit metabolischer Dysfunktion assoziierten steatotischen Lebererkrankung (MASLD) gibt detaillierte Empfehlungen zu Diagnose, Behandlung und Überwachung. Lebensstilinterventionen und die Behandlung kardiometabolischer Risikofaktoren sind weiterhin Grundpfeiler der Therapie und Prävention. Neuerungen beinhalten angepasste Strategien zu Screening und nichtinvasiver Überwachung der MASLD sowie die Empfehlung der Anwendung von Resmetirom bei nichtzirrhotischer MASH-Fibrose.
Keypoints
-
Die MASLD (mit metabolischer Dysfunktionassoziierte steatotische Lebererkrankung) ist weltweit die häufigste chronische Lebererkrankung.
-
Menschen mit einem erhöhten Risiko für MASLD und fortgeschrittener Fibrose sollten mittels einer mehrstufigen, nichtinvasiven Testung abgeklärt werden.
-
Der Grundpfeiler der Therapie der MASLD ist die Lebensstilintervention mit Gewichtsreduktion, Ernährungsumstellung und vermehrter körperlicher Aktivität.
-
Die pharmakologische Therapie umfasst neben neuen MASH-spezifischen Medikamenten die optimale Behandlung kardiometabolischer Risikofaktoren.
Die mit metabolischer Dysfunktionassoziierte steatotische Lebererkrankung (MASLD), früher „nichtalkoholische Fettleber“ genannt, ist heute weltweit die häufigste Ursache chronischer Lebererkrankungen und geht mit einer hohen kardiometabolischen und hepatischen Morbidität und Mortalität einher. Die aktualisierte europäische EASL-EASD-EASO-Leitlinie zum Management der MASLD berücksichtigt die umfangreichen Entwicklungen der letzten Jahre und gibt umfassende Empfehlungen zur Diagnose, Therapie und Überwachung der MASLD.1
Neue Definition und Risikofaktoren
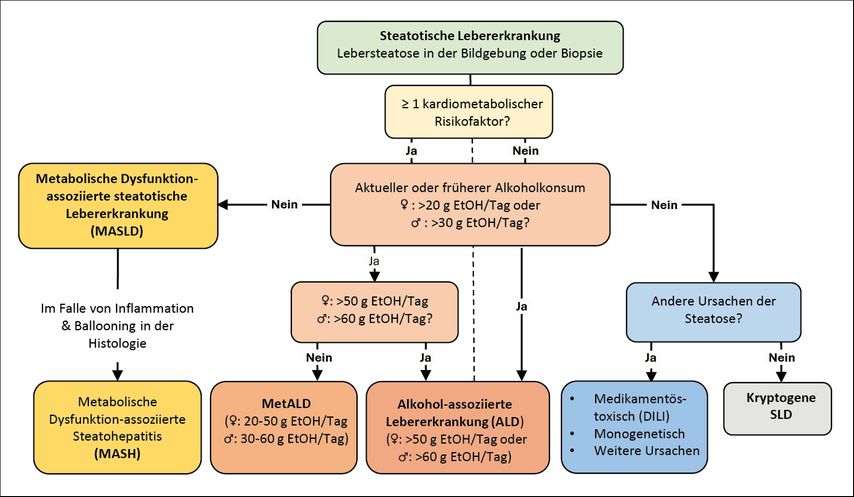
In der 2023 eingeführten neuen Krankheitsdefinition ersetzen die Begriffe MASLD und MASH (mit metabolischer Dysfunktionassoziierte Steatohepatitis) die Begriffe NAFLD und NASH (nichtalkoholische Fettleber bzw. Steatohepatitis).2 Die MASLD und MASH werden neben alkoholassoziierten Lebererkrankungen, anderen Ursachen der Leberzellverfettung und kryptogenen Ursachen unter dem Begriff der „steatotic liver disease“ (SLD oder steatotische Lebererkrankung) zusammengefasst (Abb. 1). In retrospektiven Analysen weist die MASLD-Population eine sehr große Überschneidung mit der NAFLD-Population auf.3
Abb. 1: Definition und Klassifikation der steatotischen Lebererkrankungen (modifiziert nach EASL-EASD-EASO Clinical Practice Guidelines 2024)1
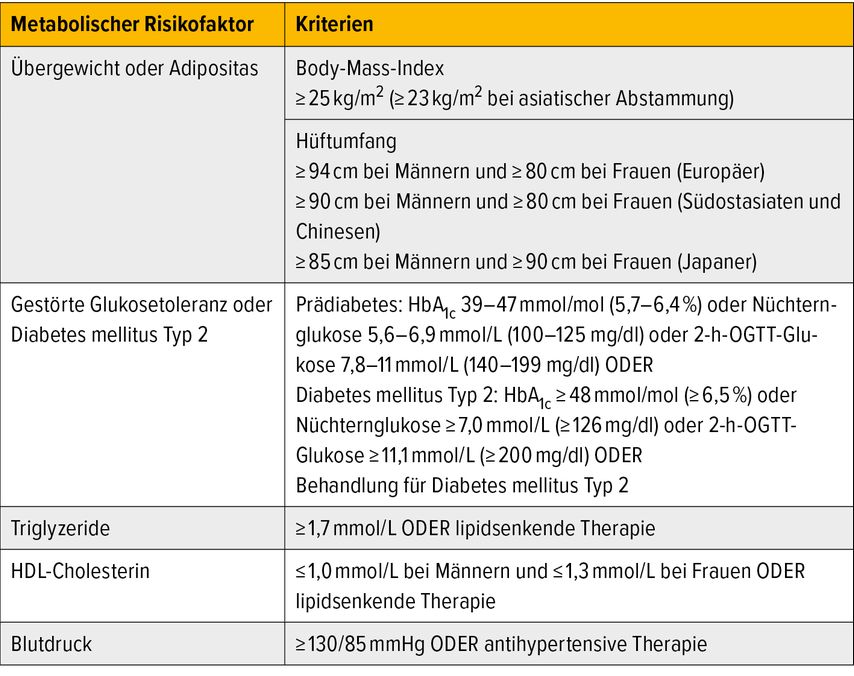
Die MASLD ist nun positiv definiert über den Nachweis einer Leberverfettung und das Vorliegen mindestens eines kardiometabolischen Risikofaktors (Tab. 1). Mit dem Begriff der MASLD mit moderatem Alkoholkonsum (MetALD; d.h. Frauen: 20–50g/Tag, Männer: 30–60g/Tag) wird dem in der klinischen Praxis häufig anzutreffenden Mischbild sowie der Erhöhung des Risikos für schwere Verläufe durch moderaten Alkoholkonsum Rechnung getragen.4
Tab. 1: Kardiometabolische Risikofaktoren für MASLD/MASH (modifiziert nach EASL-EASD-EASO Clinical Practice Guidelines 2024)1
Die Risikofaktoren Diabetes mellitus Typ2 (T2D) und Adipositas sind mit der größten Erhöhung des Risikos für das Auftreten einer MASLD sowie für schwerere Krankheitsverläufe assoziiert.5 Auch für Männer über 50 Jahre, postmenopausale Frauen und Personen mit mehreren kardiometabolischen Risikofaktoren besteht ein hohes Risiko für schwere Krankheitsverläufe.5,6
Screening und Monitoring
Ein allgemeines Screening auf steatotische Lebererkrankungen in der Allgemeinbevölkerung wird nicht empfohlen. In den folgenden Konstellationen mit hohem Risiko für MASLD und eine fortgeschrittene oder progrediente Erkrankung sollte auf das Vorliegen einer MASLD mit signifikanter Fibrose untersucht werden:
-
A: bei Vorliegen vonT2D,
-
B: bei Vorliegen einerabdominellen Adipositas und ≥1 zusätzlichen kardiometabolischen Risikofaktor oder
-
C: im Falle auffälliger Leberwerte
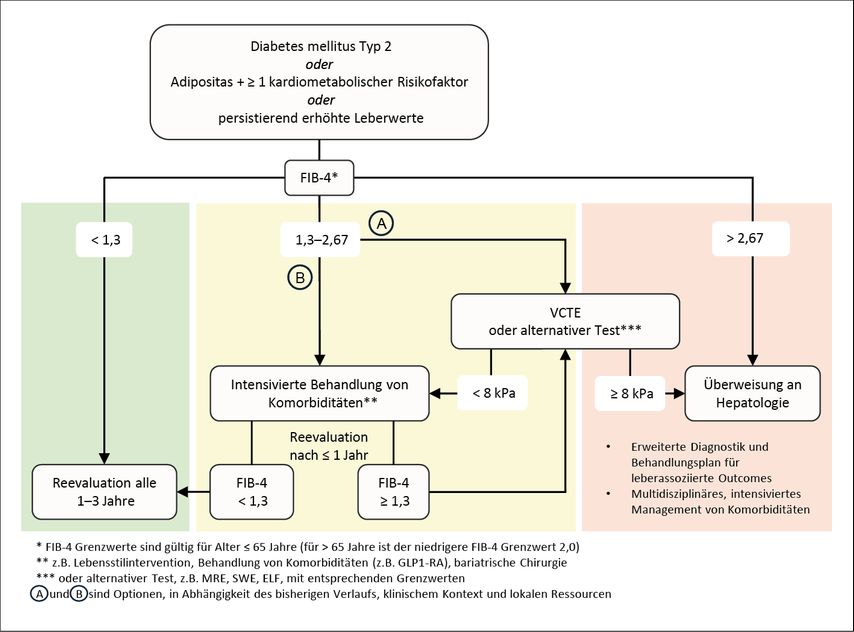
Die Leitlinie empfiehlt hier ein mehrstufiges Verfahren unter Zuhilfenahme nicht-invasiver Tests zur Abschätzung des Risikos einer MASLD mit fortgeschrittener Fibrose (Abb. 2). Im Falle eines mittleren Risikos (d.h. z.B. FIB-4 1,3 bis 2,67) besteht die Option eines intensivierten Therapieversuchs mit anschließender erneuter FIB-4-Testung zur Erfolgskontrolle nach einem Jahr.
Abb. 2: Nichtinvasives Assessment des Risikos für Leberfibrose und leberbezogene klinische Ereignisse (modifiziert nach EASL-EASD-EASO Clinical Practice Guidelines 2024)1
Nichtinvasive Verfahren zur Beurteilung der Leberfibrose rücken zunehmend in den Fokus der Risikostratifizierung und des Monitorings der MASLD und ersetzen in den meisten Fällen die Leberbiopsie.7 Unterschieden werden können serumbasierte Biomarker und Scores (sehr gut geeignet zum Ausschluss einer fortgeschrittenen Leberfibrose) sowie Messungen der Lebersteifigkeit (besser geeignet für die Vorhersage).7 Darüber hinaus gewinnen diese Tests zunehmende Bedeutung für die Beurteilung der Fibroseprogression sowie für die prognostische Abschätzung des Gesamtüberlebens und des Risikos für das Auftreten leberbezogener Ereignisse.8,9
Die Entwicklung eines hepatozellulären Karzinoms (HCC) ist eine wichtige und häufige Komplikation bei MASH, und für Personen mit MASLD-assoziierter Leberzirrhose wird in Übereinstimmung mit den aktuellen HCC-Leitlinien ein Screening mittels halbjährlicher Ultraschalluntersuchungen, ggf. in Kombination mit Bestimmung des Tumormarkers Alpha-Fetoprotein (AFP), empfohlen.10 Bei Vorliegen einer MASLD mit fortgeschrittener Fibrose (Stadium F3) sollte bei erhöhtem HCC-Risiko, z.B. bei Vorliegen eines T2D und Adipositas, höherem Lebensalter, Alkohol- oder Nikotinkonsum, die Aufnahme in ein HCC-Screeningprogramm erwogen werden.
Aufgrund des erhöhten Risikos für das Auftreten von kardiometabolischen Risikofaktoren und entsprechenden Komorbiditäten11–13 sollten Menschen mit MASLD bei Diagnosestellung und darauf folgend in regelmäßigen Abständen hinsichtlich des Vorliegens von etwa T2D, Dyslipidämie, Bluthochdruck und Niereninsuffizienz untersucht und entsprechend therapiert werden. Ebenso sind Patient:innen mit MASLD aufgrund des erhöhten Risikos für extrahepatische Krebserkrankungen14 angehalten, an entsprechenden Vorsorge- und Früherkennungsprogrammen teilzunehmen.
Prävention
Eine mediterrane Diät, die Vermeidung von hochprozessierten und gesüßten Nahrungsmitteln und Getränken sowie ein aktiver Lebensstil sind mit einer geringeren Häufigkeit von MASLD und HCC assoziiert.15,16 Politische Maßnahmen, wie die Einschränkung von Werbung für ungesunde Lebensmittel, die Subventionierung gesunder Lebensmittel, die Förderung von Nahrungsmittel-Reformulierungen durch die Industrie sowie die Verbesserung der Lebensmittel- und Gesundheitskompetenz in der Bevölkerung durch Nährwertkennzeichnungen könnten ein Weg sein, um die Prävalenz von Übergewicht, T2D und MASLD in der Bevölkerung zu senken.17
Nichtpharmakologisches Management
Die Gewichtsreduktion mittels diätetischer Maßnahmen und erhöhter körperlicher Aktivität stellt nach wie vor den Grundpfeiler jeder Therapie der MASLD dar. Eine Gewichtsreduktion kann zur Verringerung der Transaminasen, der Leberverfettung, der entzündlichen Aktivität sowie der Fibrose führen.18–20
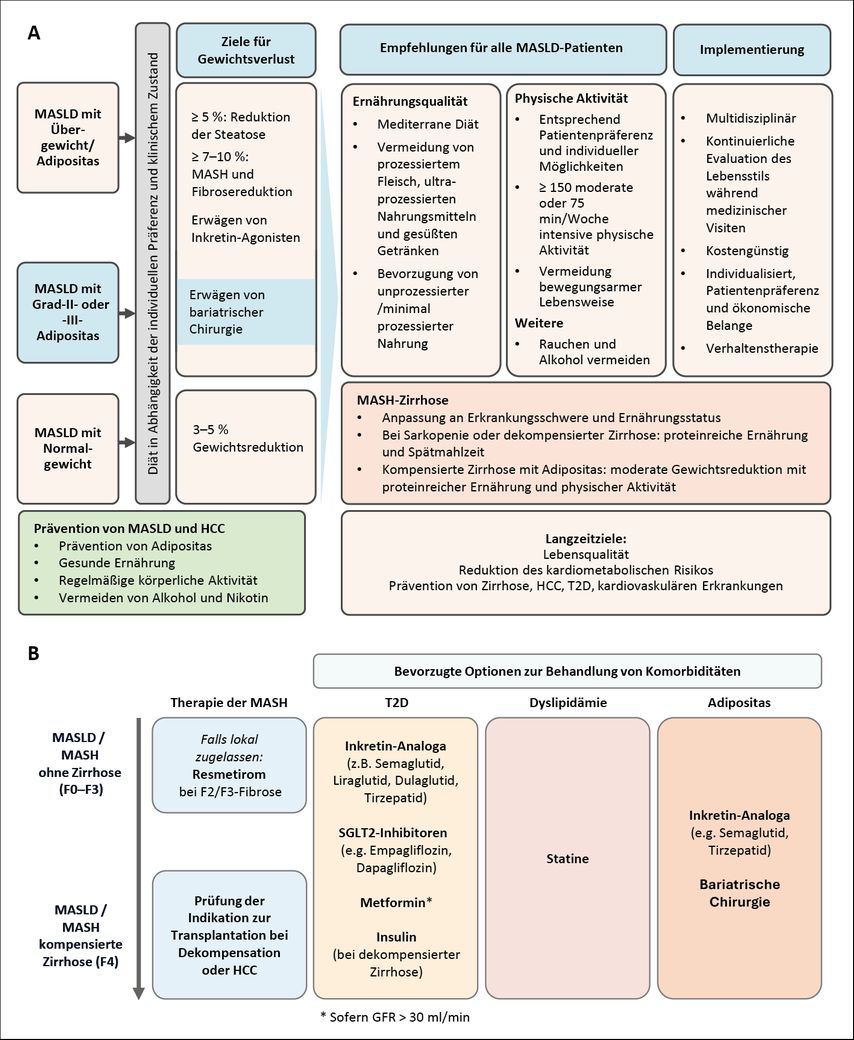
Es wird empfohlen, bei Übergewicht eine Gewichtsreduktion von mindestens 5% des Ausgangsgewichts zur Reduktion von Leberfett, 5 bis 10% zur Reduktion der entzündlichen Aktivität und über 10% zur Reduktion der Leberfibrose anzustreben.21 Die Maßnahmen zum Erreichen einer Körpergewichtsreduktion sind in der Abbildung 3A im Einzelnen aufgeführt und auch auf normalgewichtige Individuen mit MASLD anwendbar.
Abb. 3: Therapeutische Maßnahmen bei MASLD/MASH (modifiziert nach EASL-EASD-EASO Clinical Practice Guidelines 20241. A: nichtpharmakologische Therapie; B: pharmakologische Therapie
Pharmakologische Therapie
Auf Basis der positiven Ergebnisse der Phase-III-MAESTRO-NASH-Studie22 hat in den USA die FDA eine beschleunigte Zulassung für den Thyroidhormonrezeptor-β-Agonisten Resmetirom zur Behandlung der nichtzirrhotischen MASH mit signifikanter Fibrose (≥F2) erteilt. Unter der Voraussetzung der Verfügbarkeit und vorbehaltlich etwaiger Zulassungsbeschränkungen im europäischen Raum sollte Resmetirom daher für die Behandlung von Menschen mit nichtzirrhotischer MASH und signifikanter Fibrose in Erwägung gezogen werden. Für die Auswahl geeigneter Patient:innen kommen sowohl die Leberbiopsie als auch nichtinvasive Tests infrage. Auch zu weiteren Substanzklassen, etwa zu den Inkretin-Koagonisten Tirzepatid und Survodutid, liegen vielversprechende Daten vor,23,24 sodass in der näheren Zukunft mit einer zunehmend dynamischen Therapielandschaft gerechnet werden kann.
Die angepasste pharmakologische Therapie der kardiometabolischen Risikofaktoren stellt bereits heute einen wesentlichen Bestandteil im Management der MASLD dar. Für ihre jeweilige Indikation sollten, abhängig vom Krankheitsstadium, Glucagon-like-Peptide-1-Rezeptoragonisten (GLP1RA) und Koagonisten, Sodium-Glukose-Transporter-2(SGLT2)-Inhibitoren, Metformin und Statine bevorzugt eingesetzt werden, da diese die kardiovaskuläre Morbidität und Mortalität senken und die Krankheitsaktivität der MASH sowie potenziell das Risiko für die Entstehung eines HCC positiv beeinflussen können (Abb. 3B).
Chirurgische und endoskopische Therapie
Bei Betroffenen mit Adipositas und MASH, bei denen Lebensstilinterventionen oder medikamentöse Maßnahmen nicht zu einer ausreichenden Gewichtsreduktion führen, sind bariatrische Verfahren zu erwägen. Die bariatrische Chirurgie hat nicht nur positive Effekte auf das Körpergewicht, kardiometabolische Risikofaktoren oder das Krebsrisiko, sondern führt in bis zu 55% der Fälle innerhalb eines Jahres zur MASH-Resolution ohne Verschlechterung der Fibrose.25 Bei Vorliegen einer bereits fortgeschrittenen Lebererkrankung, d.h. einer kompensierten Leberzirrhose, sollten eine gründliche Nutzen-Risiko-Abwägung und die Durchführung durch ein erfahrenes multidisziplinäres Team erfolgen. Aufgrund der limitierten Evidenzlage können endoskopisch-bariatrische Verfahren derzeit nicht zur gezielten Therapie der MASH empfohlen werden.
Management von „end-stage“ MASLD und MASH
Die spezifischen Belange der MASH und ihrer Komorbiditäten sollten auch im Management der Zirrhose und ihrer Komplikationen Berücksichtigung finden. Bei dekompensierter Leberzirrhose und/oder HCC ist immer die Indikation zur Lebertransplantation zu prüfen!
Besondere Beachtung finden sollten Maßnahmen zur Reduktion des Risikos für eine Sarkopenie (d.h. proteinreiche Ernährung mit Spätmahlzeit, physiotherapeutische Begleitung einer Gewichtsreduktion), die optimale Kontrolle kardiometabolischer Risikofaktoren vor und nach Lebertransplantation sowie die Limitationen im nichtinvasiven Nachweis einer klinisch signifikanten portalen Hypertension bei Vorliegen eines BMI>30kg/m2. Zur Abschätzung des Risikos für eine klinisch signifikante portale Hypertension kann das ANTICIPATE-NASH-Modell eine Orientierung bieten.26
Fazit und Ausblick
Die umfangreichen wissenschaftlichen Bemühungen um ein besseres Verständnis der MASLD in den letzten Jahrzehnten haben zu einer solideren Evidenzbasis und detaillierteren klinischen Empfehlungen geführt, die uns mehr Sicherheit im Umgang mit MASLD geben. Dies gilt sowohl für die Früherkennung und Risikoabschätzung der Erkrankung (ohne Leberbiopsie) als auch für die Therapie und Überwachung. Die optimale Versorgung dieser komplexen Erkrankung erfordert eine interdisziplinäre und interprofessionelle Zusammenarbeit. Insbesondere die erste spezifische Medikamentenzulassung lässt hoffen, dass wir in den nächsten Jahren ein breites Spektrum spezifischer therapeutischer Maßnahmen zur Verfügung haben werden. Dennoch sollten weitere Anstrengungen unternommen werden, um effektive Präventionsprogramme zu etablieren und eine strukturelle Verbesserung der Versorgung dieser komplex erkrankten Patientengruppe zu erreichen.
Literatur:
1 European Association for the Study of the Liver et al.: EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024: S0168-8278(24)00329-5 2 Rinella ME et al.: A multi-society Delphi consensus statement on new fatty liver disease nomenclature. J Hepatol 2023; 79(6): 1542-56 3 Younossi ZM et al.: Clinical profiles and mortality rates are similar for metabolic dysfunction-associated steatotic liver disease and non-alcoholic fatty liver disease. J Hepatol 2024; 80(5): 694-701 4 Israelsen M et al.: Validation of the new nomenclature of steatotic liver disease in patients with a history of excessive alcohol intake: an analysis of data from a prospective cohort study. Lancet Gastroenterol Hepatol 2024; 9(3): 218-28 5 Golabi P et al.: Nonalcoholic fatty liver disease (NAFLD) and associated mortality in individuals with type 2 diabetes, pre-diabetes, metabolically unhealthy, and metabolically healthy individuals in the United States. Metabol 2023; 146: 155642 6 Yang JD et al.: Gender and menopause impact severity of fibrosis among patients with nonalcoholic steatohepatitis. Hepatol 2014; 59(4): 1406-14 7 European Association for the Study of the Liver: EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis – 2021 update. J Hepatol 2021; 75(3): 659-89 8 Siddiqui MS et al.: Diagnostic accuracy of noninvasive fibrosis models to detect change in fibrosis stage. Clin Gastroenterol Hepatol 2019; 17(9): 1877-85 9 Mozes FE et al.: Performance of non-invasive tests and histology for the prediction of clinical outcomes in patients with non-alcoholic fatty liver disease: an individual participant data meta-analysis. Lancet Gastroenterol Hepatol 2023; 8(8): 704-13 10 European Association for the Study of the Liver: EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol 2018; 69(1): 182-236 11 Mantovani A et al.: Non-alcoholic fatty liver disease and risk of incident diabetes mellitus: an updated meta-analysis of 501 022 adult individuals. Gut 2021; 70(5): 962-9 12 Mantovani A et al.: Non-alcoholic fatty liver disease and risk of fatal and non-fatal cardiovascular events: an updated systematic review and meta-analysis. Lancet Gastroenterol Hepatol 2021; 6(11): 903-13 13 Mantovani A et al.: Non-alcoholic fatty liver disease and risk of incident chronic kidney disease: an updated meta-analysis. Gut 2022; 71(1): 156-62 14 Mantovani A et al.: Non-alcoholic fatty liver disease and increased risk of incident extrahepatic cancers: a meta-analysis of observational cohort studies. Gut 2022; 71(4): 778-88 15 Zhang S et al.: Ultra-processed food consumption and the risk of non-alcoholic fatty liver disease in the Tianjin Chronic Low-grade Systemic Inflammation and Health Cohort Study. Int J Epidemiol 2022; 51(1): 237-49 16 Ma J et al.: Improved diet quality associates with reduction in liver fat, particularly in individuals with high genetic risk scores for nonalcoholic fatty liver disease. Gastroenterol 2018; 155(1): 107-17 17 Karlsen TH et al.: The EASL-Lancet Liver Commission: protecting the next generation of Europeans against liver disease complications and premature mortality. Lancet 2022; 399(10319): 61-116 18 Fernandez T et al.: Lifestyle changes in patients with non-alcoholic fatty liver disease: A systematic review and meta-analysis. PLoS One 2022; 17(2): e0263931 19 Koutoukidis DA et al.: The effect of the magnitude of weight loss on non-alcoholic fatty liver disease: A systematic review and meta-analysis. Metabolism 2021; 115: 154455 20 Haigh L et al.: The effectiveness and acceptability of Mediterranean diet and calorie restriction in non-alcoholic fatty liver disease (NAFLD): A systematic review and meta-analysis. Clin Nutr 2022; 41(9): 1913-31 21 Vilar-Gomez E et al.: Weight loss through lifestyle modification significantly reduces features of nonalcoholic steatohepatitis. Gastroenterol 2015; 149(2): 367-78 22 Harrison SA et al.: A phase 3, randomized, controlled trial of resmetirom in NASH with liver fibrosis. N Engl J Med 2024; 390(6): 497-509 23 Sanyal AJ et al.: A phase 2 randomized trial of survodutide in MASH and fibrosis. N Engl J Med 2024; doi: 10.1056/NEJMoa2401755 24 Loomba R et al.: Tirzepatide for metabolic dysfunction-associated steatohepatitis with liver fibrosis. N Engl J Med 2024; doi: 10.1056/NEJMoa2401943 25 Verrastro O et al.: Bariatric-metabolic surgery versus lifestyle intervention plus best medical care in non-alcoholic steatohepatitis (BRAVES): a multicentre, open-label, randomised trial. Lancet 2023; 401(10390): 1786-97 26 Pons M et al.: Noninvasive diagnosis of portal hypertension in patients with compensated advanced chronic liver disease. Am J Gastroenterol 2021; 116(4): 723-32
Das könnte Sie auch interessieren:
HBV-Reaktivierung unter Immunsuppression
Durch rezente Migrationsdynamiken befindet sich auch in Österreich die Prävalenz der Infektion mit dem Hepatitis-B-Virus (HBV) im Steigen. Besonders bei Patient:innen unter ...
OP-Freigabe bei Leberzirrhose
Patient:innen mit Leberzirrhose haben ein erhöhtes Risiko für Komplikationen und eine erhöhte Mortalität – daher muss eine detaillierte präoperative Evaluierung erfolgen. Es stehen ...
Top-Papers Hepatologie
Ganz im Sinne des Titels der Veranstaltung wurden auch beim diesjährigen Update Gastroenterologie-Stoffwechsel vom 14. bis 16. November 2024 in Innsbruck aktuelle Themen der ...