Therapie mit Calcineurin-Inhibitoren: Guidelines und klinische Perspektive
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei der schwerwiegenden Erkrankung Lupusnephritis mit erhöhter Morbidität und Mortalität sollte gemäss aktualisierten Therapieempfehlungen frühzeitig eine «Early combination»-Therapie, z.B. mit Voclosporin, in Erwägung gezogen werden.1 An einem Satellitensymposium im Rahmen der SGN-Jahrestagung wurden die neuen Therapieempfehlungen, die zugrunde liegende Evidenz und die Frage der geeigneten Therapie für den richtigen Patienten diskutiert.
Ein systemischer Lupus erythematodes (SLE) führt häufig zu einer renalen Beteiligung. Bereits bei der SLE-Diagnose findet sich bei 7–31% der Betroffenen eine Lupusnephritis (LN). Etwa die Hälfte der Patienten mit SLE entwickelt im Verlauf eine LN.2
Bei der LN lagern sich als Reaktion auf die SLE-bedingte Produktion von Autoantikörpern Immunkomplexe in den Nierenglomeruli ab und führen zur Entzündung und Schädigung.2 «Schon die erste Entzündungsepisode führt zu einem markanten Nephronenverlust und zu einer rapiden Abnahme der Nierenfunktion», sagte Prof. Dr. med. Jörg Latus vom Robert Bosch Krankenhaus in Stuttgart. Bei anhaltender Krankheitsaktivität kommt es zu einem fortschreitenden Verlust an Nephronen und zu einer frühzeitigen ESRD («end stage renal disease»).3Innerhalb von 15 Jahren nach der Diagnose werden bis zu einem Viertel aller LN-Patienten dialysepflichtig.1 Mit der LN nimmt auch das Mortalitätsrisiko zu: Dieses ist im Vergleich zur Normalbevölkerung um das 6- bis 26-Fache erhöht.4
Die Reduktion der Proteinurie ist ein wichtiger prognostischer Faktor für den Krankheitsverlauf der LN.5–7 Die Einteilung der LN erfolgt basierend auf der Histopathologie in die Klassen I–V. Für die Therapiewahl und -steuerung ist zusätzlich die Bestimmung des Aktivitäts- und Chronizitätsindex von Bedeutung.8,9 Um die Krankheitsaktivität zu bestimmen, ist auch heute noch eine Nierenbiopsie notwendig. Aktuell verfügbare Biomarker weisen zwar auf eine Nierenbeteiligung bei SLE hin, sie korrelieren aber schlecht mit dem Grad der Nierenschädigung.10 «Grundsätzlich gilt, dass wir mit der Diagnose schnell und mit der Therapie aggressiv sein müssen, um den Verlust der Nierenfunktion von Anfang an gering zu halten», so der Spezialist.
Für das Management der LN existieren die EULAR/ERA-EDTA-Empfehlungen von 2019.11 In den jüngst publizierten aktualisierten Empfehlungen der EULAR zum Management der SLE wird die LN ebenfalls adressiert (Abb. 1).1 Unverändert bleibt dabei die Empfehlung – sofern keine Kontraindikation besteht –, alle Patienten mit LN mit Hydroxychloroquin (HCQ) zu behandeln. Der Einsatz von Glukokortikoiden (GCS) als Teil der Induktions- und Erhaltungstherapie hat in der LN seinen Stellenwert. Aufgrund der nachteiligen Auswirkungen der langfristigen GCS-Anwendung empfiehlt die EULAR ein rasches «Tapering» der Erhaltungsdosis auf ≤5mg/Tag (Prednison-Äquivalenz).1,11 «Bei Einsatz einer Add-on-Therapie sollte die GCS-Dosis auf 2,5mg/Tag reduziert werden können», sagte Prof. Latus. Bei aktiver LN empfiehlt die EULAR generell eine immunsuppressive Therapie mit tief dosiertem Cyclophosphamid (CYC) oder Mycophenolat-Mofetil (MMF) kombiniert mit GCS. Die Therapieziele in der LN stützen sich unverändert auf definierte Zielwerte der Proteinurie-Reduktion, wie beispielsweise innerhalb von 12 bis 24 Monaten auf Werte von <0,5–0,7g/Tag. Wie zwei Kohortenstudien zeigten, ist dieser Cut-off-Wert prädiktiv für ein gutes renales Langzeit-Outcome.6,7 «Um dieses Therapieziel zu erreichen, braucht es oft mehr als eine Therapie mit Hydroxychloroquin, Kortikosteroiden und einem einzelnen Immunsuppressivum», so der Spezialist. Die Leitlinien empfehlen deshalb eine «Earlycombination»-Therapie respektive Add-on-Therapie mit einem Calcineurin-Inhibitor (CNI), insbesondere mit Voclosporin (VOC) oder Tacrolimus respektive dem Anti-BLyS-Antikörper Belimumab (BEL), in Erwägung zu ziehen.1
Kombination mit Voclosporin erlaubt schnelles GCS-Tapering
Die Basis für die Empfehlungen einer «Earlycombination»-Therapie bei aktiver LN lieferten die internationalen randomisierten doppelblinden und placebokontrollierten Phase-III-Studien BLISS-LN und AURORA 1.12,13 Die Ergebnisse der BLISS-LN zeigten, dass BEL als Add-on zur Standardtherapie bei signifikant mehr LN-Patienten zu einer Verbesserung der primären renalen Endpunkte führte (Urin-Protein-Kreatinin-Ratio [UPCR] ≤0,7mg/mg, max. Abfall der eGFR ≤20% verglichen mit der eGFR vor Auftreten des renalen Flares oder ≥60ml/min/1,73m2, keine Notfallmedikamente) als die Kontrollbehandlung mit Placebo (43% vs. 32%, p=0,03).12 Die AURORA-1-Studie verglich die «Earlycombination»-Therapie mit VOC versus Placebo bei Patienten mit aktiver proliferativer LN, die mit MMF und oralen GCS behandelt wurden. Dabei zeigte sich, dass nach einer 52-wöchigen Behandlungsdauer mit VOC signifikant mehr Patienten eine CRR («complete renal response») erreichten (41% vs. 23%, p<0,0001).13Eine CRR war definiert als UPCR ≤0,5mg/mg, stabile Nierenfunktion (eGFR ≥60ml/min/1,73m2 oder keine Abnahme der eGFR >20% im Vgl. zur Baseline), kein Gebrauch von Notfallmedikamenten und nicht mehr als 10mg Prednison-Äquivalent/Tag während 3 aufeinanderfolgenden Tagen oder mehr als 7 Tage von Woche 44 bis 52. Prof. Latus wies die Zuhörer zudem auf eine Besonderheit der AURORA-Studie hin: das schnelle GCS-Tapering auf eine Dosis von 2,5mg/Tag in den ersten 16 Wochen Therapie mit VOC. Das Sicherheitsprofil des CNI war in der AURORA-1-Studie auf einem vergleichbaren Niveau wie Placebo.13 «Trotzdem stellt sich beim Vergleich einer dreifachen mit einer zweifachen Immunsuppression immer die Frage nach der Wirkung und Sicherheit», sagte Prof. Latus. Eine Antwort auf die Unterschiede liefert eine 2023 an der Kidney Week in Philadelphia vorgestellte Propensity-Analyse der ALMS- vs. AURORA-1-Studien.14Diese konnte zeigen, dass die dreifache Immunsuppression mit VOC kombiniert mit niedrig dosierten GCS und MMF in der AURORA-1-Studie nach 3 und 6 Monaten hinsichtlich der Wirksamkeit ähnlich abschnitt wie die verglichene zweifache Immunsuppression mit hochdosierten GCS plus hochdosiertem MMF in der ALMS-Studie. Patienten, die mit einem VOC-basierten Therapieschema behandelt wurden, profitierten jedoch von einem besseren Sicherheitsprofil mit weniger MMF/GCS-assoziierten unerwünschten Wirkungen, wie Hyperglykämie, Cushing-Syndrom, (schweren) Infektionen, gastrointestinalen Erkrankungen.14 Zusammen mit den Ergebnissen der Verlängerungsstudie AURORA 2 liegen nun Erfahrungen über eine insgesamt 3-jährige Behandlungsdauer mit VOC als Add-on-Therapie vor.15
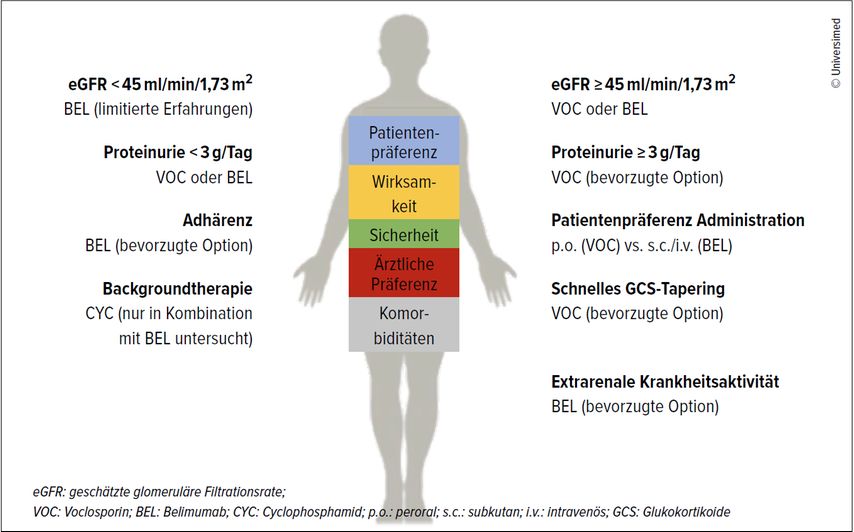
Abb. 1: Spezifische Erwägungen bei der Bewertung der optimalen, derzeit zugelassenen «Add-on»-Therapien für Patienten mit aktiver LN Klasse III–V (adaptiert nach Frangou E et al.)16
Welche Kombination für welchen Patienten?
Die ERA-Arbeitsgruppe für Immunnephrologie empfiehlt, bei der Wahl der zugelassenen Add-on-Therapien Kriterien wie die Wirksamkeit und Sicherheit, die Präferenzen des Patienten und Arztes sowie die Komorbiditäten zu berücksichtigen.16 Basierend auf den Daten der BLISS-LN- und AURORA-Studien ist sowohl VOC als auch BEL als «Earlycombination»-Therapie bei Patienten mit einer eGFR ≥45ml/min/1,73 geeignet. Bei einer eGFR <45ml/min ist eine Therapie mit BEL möglich, die Behandlung mit VOC wurde bei einer moderaten bis schweren Nierenfunktionseinschränkung nicht untersucht. Eine Proteinurie von ≥3g/Tag spricht für eine Behandlung mit VOC, bei Werten <3g/Tag ist eine Behandlung mit beiden Substanzen möglich. Bevorzugt der Patient oder die Patientin eine orale Applikationsform, wäre dies ein Kriterium für VOC. Eine schlechte Compliance ist dagegen ein Argument für eine parenterale Therapie und somit für BEL. Von Bedeutung ist auch die Backgroundtherapie mit Immunsuppressiva: BEL wurde in Kombination mit CYC und MMF untersucht, VOC in Kombination mit MMF. Ein schnelles GCS-Tapering ist ein Argument für eine Therapie mit VOC, das Vorhandensein von extrarenalen Erkrankungen für eine Behandlung mit BEL.
«Mit den verfügbaren Add-on-Therapien verfügen wir über gute Optionen, um unsere Patienten mit aktiver Lupus-Nephritis zu behandeln», sagte Prof. Latus.
Sponsored Content:
Mit freundlicher Unterstützung durch Otsuka Pharmaceutical GmbH
CH-LUP-2400025_02/2024
Kurzfachinformation:
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Für weitere Informationen, siehe Fachinformation/Patienteninformation Lupkynis auf
www.swissmedicinfo.ch.
Lupkynis (Voclosporinum) Kurzfachinformation. Indikation: Lupkynis ist in Kombination mit einer immunsuppressiven Basistherapie zur Behandlung von erwachsenen Patienten mit aktiver Lupusnephritis der Klassen III, IV oder V (einschl. Mischformen III/V und IV/V) indiziert. Dosierung: Empfohlene Dosis beträgt 23,7 mg (3 Weichkapseln à 7,9 mg) 2x täglich. Basis-Therapie in den klinischen Studien waren Mycophenolat Mofetil (MMF) und Kortikosteroide. Die Behandlung sollte von einer Ärztin/Arzt eingeleitet / überwacht werden, der Erfahrung mit der immunsuppressiven Therapie zur Behandlung von Systemischen Lupus Erythematodes bzw. Lupusnephritis hat. Kontraindikation: Überempfindlichkeit gegen den Wirkstoff / sonstige Bestandteile. Starke CYP3A4 Inhibitoren. Warnhinweise / Vorsichtsmassnahmen: Erhöhtes Risiko für das Auftreten von Lymphomen und anderen malignen Erkrankungen insbesondere der Haut unter Immunsuppressiva: ungeschützte Exposition gegenüber Sonnenlicht / UV-Strahlung vermeiden. Das Risiko für das Auftreten von bakteriellen, viralen, Pilz- und Protozoeninfektionen kann unter Immunsuppressiva, einschliesslich Voclosporin erhöht sein, ebenso das Risiko einer Neurotoxizität. Im Zusammenhang mit Calcineurin-Inhibitoren wurde über eine akute Verschlechterung der Nierenfunktion oder Abnahme der eGFR berichtet – regelmässige Überwachung der eGFR empfohlen. Ebenso wurde über Fälle von Aplasie der roten Blutkörperchen (pure red cell aplasia, PRCA) oder Hyperkaliämie berichtet. Voclosporin kann Hypertonie verursachen oder verschlimmern, der Blutdruck ist zu kontrollieren. In Kombination mit anderen Arzneimitteln, die bekanntermassen das QTc-Intervall verlängern, kann es zu einer klinisch signifikanten QTc-Verlängerung kommen. Bei Patienten mit erhöhtem Risiko einer QT-Verlängerung, ist ein EKG in Betracht zu ziehen und die Elektrolyte sind zu überwachen. Bei Leberfunktionsstörung (Child-Pugh-Klasse C) soll Voclosporin nicht angewendet werden. Impfungen beachten. Eine Lupkynis Weichkapsel enthält 21,6 mg Ethanol -die geringe Alkoholmenge hat keine wahrnehmbaren Auswirkungen-, und 28,7 mg Sorbitol. Ebenso kann es Spuren von Sojalecithin enthalten (mögliche Rückstände aus der Herstellung) Interaktionen: Siehe Kontraindikationen. Dosisreduktion bei mittelstarken CYP3A4-Inhibitoren. Gleichzeitige Anwendung mit starken und mittelstarken CYP3A4-Induktoren nicht empfohlen, Einfluss von Voclosporin auf die Pharmakokinetik von P-gp-, BCRP & OATP1B1/OATP1B3-Substrate. Anwendung von Voclosporin mit Mycophenolat Mofetil (MMF) ohne klinisch bedeutsame Auswirkungen auf die Konzentration von Mycophenolsäure (MPA). Schwangerschaft/Stillzeit; Lupkynis soll während der Schwangerschaft nicht angewendet werden, es sei denn, der erwartete Nutzen überwiegt das potenzielle Risiko, ebenso beim Stillen. Unerwünschte Wirkungen: sehr häufig: Infektion der oberen Atemwege, Anämie, Kopfschmerz, Hypertonie, Husten, Diarrhö, Bauchschmerzen, verminderte Glomeruläre Filtrationsrate häufig: Grippe, Herpes Zoster, Gastroenteritis, Harnwegsinfektion, Hyperkaliämie, verminderter Appetit, Kampfanfälle, Tremor, Übelkeit, Zahnfleischhyperplasie, Dyspepsie, Alopezie, Hypertrichose, akute Nierenerkrankung, akute Nierenschädigung. Packungen: 180 Weichkapseln. Konsultieren Sie bitte vor einer Verschreibung die vollständige Fachinformation, die auf der Homepage von Swissmedic unter www.swissmedicinfo.ch publiziert ist. Abgabekategorie: B, Zulassungsinhaberin: Otsuka Pharmaceutical (Switzerland) GmbH, Sägereistrasse 20, 8152 Opfikon. Stand: v003.
Quelle:
Satellitensymposium Otsuka Pharmaceutical GmbH, Jahreskongress der Schweizerischen Gesellschaft für Nephrologie, 7. bis 8. Dezember 2023, Lausanne
Literatur:
1 Fanouriakis A et al.: EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Ann Rheum Dis 2024; 83: 15-29 2 Mahajan A et al.: Systemic lupus erythematosus, lupus nephritis and end-stage renal disease: a pragmatic review mapping disease severity and progression. Lupus 2020; 29: 1011-20 3 Anders HJ et al.: Lupus nephritis. Nat Rev Dis Primers 2020; 6: 7 4 Kostopoulou M et al.:. An update on the diagnosis and management of lupus nephritis. Curr Rheumatol Rep 2020; 22: 30 5 Korbet SM et al.: Severe lupus nephritis: the predictive value of a ≥ 50% reduction in proteinuria at 6 months. Nephrol Dial Transplant 2013; 28: 2313-8 6Dall’Era M et al.: Predictors of long-term renal outcome in lupus nephritis trials: lessons learned from the Euro-Lupus Nephritis cohort. Arthritis Rheumatol 2015; 67: 1305-13 7 Tamirou F et al.: A proteinuria cut-off level of 0.7 g/day after 12 months of treatment best predicts long-term renal outcome in lupus nephritis: data from the MAINTAIN nephritis trial. Lupus Sci Med 2015; 2: e000123 8 Weening JJ et al.: The classification of glomerulonephritis in systemic lupus erythematosus revisited. Kidney Int 2004; 65: 521-30 9 Bajema IM et al.: Revision of the International Society of Nephrology/Renal Pathology Society classification for lupus nephritis: clarification of definitions, and modified National Institutes of Health activity and chronicity indices. Kidney Int 2018; 93: 789-96 10 Soliman S, Mohan C: Lupus nephritis biomarkers. Clin Immunol 2017; 185: 10-20 11 Fanouriakis A et al.: 2019 Update of the Joint European League Against Rheumatism and European Renal Association-European Dialysis and Transplant Association (EULAR/ERA-EDTA) recommendations for the management of lupus nephritis. Ann Rheum Dis 2020; 79: 713-23 12 Furie R et al.: Two-year, randomized, controlled trial of belimumab in lupus nephritis. N Engl J Med 2020; 383: 1117-28 13 Rovin BH et al.: Efficacy and safety of voclosporin versus placebo for lupus nephritis (AURORA 1): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet 2021; 397: 2070-80 14 Yap E et al.: Comparison of dual-immunosuppressive therapy and a voclosporin-based triple immunosuppressive regimen for lupus nephritis: a propensity analysis of the ALMS und AURORA 1 studies. Presented at ASN Kidney Week 2023, Philadelphia, PA, SA-PO877 15 Saxena A et al.: Safety and efficacy of long-term voclosporin treatment for lupus nephritis in the phase 3 AURORA 2 clinical trial. Arthritis Rheumatol 2024; 76: 59-67 16 Frangou E et al.: EULAR 2023 recommendations for SLE treatment: synopsis for the management of lupus nephritis – the European Renal Association (ERA) – Immune Nephrology Working Group (ERA-IWG) perspective. Nephrol Dial Transplant 2023: gfad230
Literatur auf Anfrage bei Otsuka Pharmaceutical (Switzerland) GmbH erhältlich