Regenerative Knorpeltherapien bei Kindern und Jugendlichen
Autoren:
Dr. Markus M. Schreiner
Priv.-Doz. Dr. Alexander Kolb
Univ.-Prof. Dr. Catharina Chiari
Universitätsklinik für Orthopädie und Unfallchirurgie, Abteilung für Orthopädie, Medizinische Universität Wien
Korrespondierende Autorin:
Univ.-Prof. Dr. Catharina Chiari
Knorpelschäden im Kindes- und Jugendalter treten vor allem im Rahmen einer Osteochondritis dissecans auf oder sind akut-traumatischer Genese. Eine sorgfältige klinisch-radiologische Abklärung ist Voraussetzung für eine erfolgreiche Therapie. Therapiealternativen reichen je nach Läsion und patienten-spezifischen Faktoren von konservativer Therapie über Anbohrung oder Refixierung des Fragmentes bis hin zu matrixassoziierter Chondrozytentransplantation, osteochondraler autologer Transplantation oder Rekonstruktion mittels Allografts.
Keypoints
-
Bei jungen Patient*innen mit offenen Wachstumsfugen und stabilen Läsionen sind hohe Heilungsraten durch eine konservative Behandlung zu erwarten.
-
Jede osteochondrale Läsion, die refixierbar ist, sollte refixiert werden.
-
MACT ± autologe Spongiosaplastik/OAT/Allografts sind Therapiealternativen bei nicht refixierbaren osteochondralen Läsionen.
-
Bei relevanten Achsfehlstellungen sollten gegebenenfalls additive Eingriffe im Sinne einer Wachstumslenkung oder Umstellungsosteotomie erfolgen.
Knorpelschäden im Kindes- und Jugendalter treten im Gegensatz zu Knorpelschäden bei Erwachsenen vor allem im Rahmen einer Osteochondritis dissecans auf. Die zweithäufigste Ursache von Knorpelschäden im Kindes- und Jugendalter ist akutes Trauma, z.B. im Sinne eines Distorsionstraumas, eines Sturzes oder einer Patellaluxation, was zu einer direkten Impressionsfraktur oder Abscherung von Knorpel mit entsprechenden freien Gelenkskörpern führen kann.
Osteochondritis dissecans
Osteochondritis dissecans (OD) ist die häufigste Ursache von Knorpelschäden bei Kindern und Jugendlichen. Es handelt sich dabei um eine erworbene und potenziell reversible idiopathische Läsion des subchondralen Knochens mit oder ohne Beteiligung des Knorpels, die im weiteren Verlauf zu einer Delamination und Sequestrierung führen kann. Obwohl die Erstbeschreibung durch König1 bereits im Jahre 1887 erfolgte, ist die genaue Ursache weiterhin unbekannt. Vermutlich handelt es sich um eine multifaktorielle Pathogenese unter der Beteiligung von lokalen vaskulären sowie mechanischen Faktoren. Für die Beteiligung von mechanischen Faktoren wie repetitiven Mikrotraumata sprechen die erhöhte Inzidenz bei sportlich aktiven Patient*innen sowie auch die klassische Lokalisation am posterolateralen Teil des medialen Femurkondyls, die durch repetitives Impingement an einer prominenten Eminentia intercondylaris verursacht sein könnte.2 OD betrifft am häufigsten das Kniegelenk, kann aber auch das Capitulum humeri oder den Talus betreffen. Am häufigsten ist der posterolaterale Teil des medialen Femurkondyls betroffen.
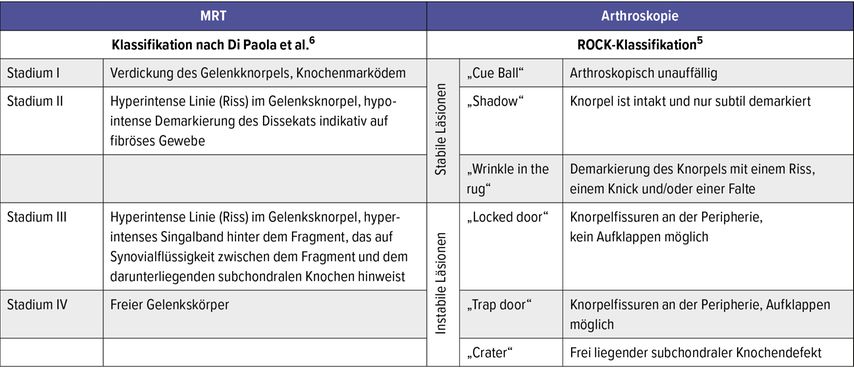
Im Laufe der Zeit wurde eine Vielzahl von verschiedenen nativradiologischen, MRT-basierten und arthroskopischen Klassifikationssystem vorgeschlagen, von denen sich bisher aber keines unangefochten durchsetzen konnte.3 Die meisten MR-basierten Klassifikationssysteme, wie auch die gebräuchliche Hefti-Klassifikation,4 beurteilen insbesondere das Ausmaß der Separierung zwischen dem OD-Fragment und dem darunterliegenden Knochenbett und versuchen hierbei in stabile und instabile Läsionen zu unterteilen. Damit bilden sie in weiterer Folge auch die Grundlage für die Entscheidung zwischen konservativer Therapie bzw. chirurgischen Therapiealternativen. Der Goldstandard hinsichtlich der Unterscheidung in stabile und instabile Läsionen sind jedoch weiterhin die arthroskopische Evaluierung und somit auch arthroskopische Klassifikationen wie die Klassifikation der ROCK Study Group (Tab. 1).5
Tab. 1: Gegenüberstellung eines MRT-basierten (Di Paola et al.6) und eines arthroskopischen Klassifikationssystem (Carey et al.5) für Osteochondritis-dissecans-Läsionen
Während OD-Läsionen bei Erwachsenen nur selten konservativ ausheilen, haben sie bei Kindern und Jugendlichen ein gutes Heilungspotenzial. Das klinische Outcome wird durch einige patientenspezifische sowie läsionsspezifische Faktoren beeinflusst. Positive prädiktive Faktoren sind junges Alter bzw. eine noch geöffnete Wachstumsfuge des distalen Femurs7 und das Fehlen einer subchondralen Sklerosezone im Nativröntgen.8 Negativ prädiktive Faktoren sind eine Flüssigkeitslamelle zwischen OD-Läsion und dem darunter liegenden Knochenbett,9 sehr aktive Patient*innen sowie eine atypische Lokalisation wie an der Patella oder dem lateralen Femurkondyl.
Klinische Untersuchung
Die klinische Präsentation von Knorpelschäden ist sehr heterogen und teilweise unspezifisch. Durch die fehlende Innervation des Knorpelgewebes können Knorpelschäden komplett asymptomatisch sein. Ein nicht unbeträchtlicher Teil an Diagnosen von OD-Läsionen erfolgt somit als Zufallsbefund, z.B. im Rahmen einer nativradiologischen Abklärung eines stattgehabten Traumas. Weitere Symptome reichen von belastungsabhängigen, diffusen und schlecht lokalisierbaren Schmerzen, rezidivierenden intraartikulären Ergüssen bis hin zu Ruheschmerzen und bei Vorhandensein von freien Gelenkskörpern auch rezidivierenden Bewegungseinschränkungen.
Bildgebung
Eine exakte und umfassende radiologische Abklärung ist Voraussetzung für eine fundierte Therapieentscheidung. Dies beinhaltet jedenfalls eine nativradiologische Bildgebung in 2 Ebenen. Abhängig vom betroffenen Gelenk sind hier gegebenenfalls zusätzliche Untersuchungen zu fordern. Bei OD-Läsionen des Kniegelenkes sollte zusätzlich eine Rosenberg-Aufnahme oder eine Tunnelaufnahme angefertigt werden, in der sich OD-Läsionen an der Prädilektionsstelle am posterolateralen medialen Femurkondyl überlagerungsfreier projizieren (Abb.1). Weiters sollte eine radiologische Abklärung der Gegenseite erfolgen, da in bis zu 29% der Fälle beide Kniegelenke betroffen sind, wovon wiederum bis zu 40% der Fälle asymptomatisch sein können.10 Die ergänzende Anfertigung von Ganzbeinröntgenaufnahmen im Stehen zur Vermessung der Beinachse ist essenziell. Bei entsprechender behandlungswürdiger Achsdeviation sowie noch geöffneten Wachstumsfugen sollten zusätzlich a/p-Röntgenaufnahmen der linken Hand zur Erstellung einer Wachstumsprognose erfolgen. In Abhängigkeit vom zu erwartenden Korrekturpotenzial kann zusätzlich zur operativen Therapie des Knorpelschadens auch ein Eingriff zur Wachstumslenkung indiziert sein.
Abb. 1: 12-jähriger männlicher Patient mit einer Osteochondritis dissecans am medialen Femurkondyl a/p (A), seitlich (B), Tunnelaufnahme (C)
Die MRT stellt den Goldstandard für die Diagnose, aber auch die Verlaufskontrolle von Knorpelschäden dar. Zu evaluieren sind hierbei neben der Größe und Lokalisation des Knorpelschadens auch eine etwaige Beteiligung des subchondralen Knochens im Sinne einer osteochondralen Läsion, aber auch etwaige subchondrale Zysten oder ein bestehendes Knochenmarksödem. Bei OD-Läsionen sollten fettunterdrückte T2-gewichtete Sequenzen in Bezug auf eine hyperintense Flüssigkeitslamelle zwischen dem OD-Fragment und dem darunterliegenden Knochen beurteilt werden. Der Nachweis einer solchen hyperintensen Flüssigkeitslamelle kann ein Hinweis auf eine Instabilität des Fragments sein und reduziert die Wahrscheinlichkeit einer konservativen Ausheilung.9 Hierbei ist jedoch zu berücksichtigen, dass sich die Stabilität eines OD-Fragmentes auf Grundlage einer MRT-Untersuchung nur unzureichend vorhersagen lässt.11
Die Verwendung des MOCART 2.0 Knee-Scores12 erlaubt nach erfolgter chirurgischer Knorpelreparatur die semiquantitative Bewertung des Knorpelreparaturgewebes und ermöglicht so eine standardisierte und objektive Bewertung des postoperativen Ergebnisses mit morphologischer MRT.
Bei Knorpelschäden mit subchondraler Beteiligung sowie insbesondere bei OD-Läsionen sollte zur genaueren Beurteilung der Affektion des subchondralen Knochens eine ergänzende Computertomografie erfolgen. Das CT erlaubt hier eine bessere Darstellung von etwaigen subchondralen Zysten sowie der Integrität und Größe des knöchernen Fragmentes und hilft somit bei der Entscheidungsfindung, ob eine Refixation des Fragmentes möglich und zielführend ist.
Therapie
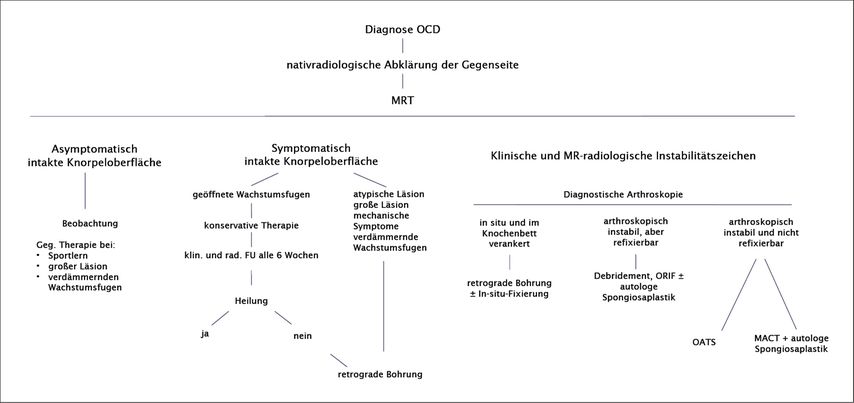
Die Behandlung von OD im Kindes- und Jugendalter ist kontroversiell und es fehlt an Evidenz im Sinne von prospektiv randomisierten Studien. Die Behandlungsentscheidungen orientieren sich an der Klinik, dem biologischen Alter der Patient*innen sowie läsionsspezifischen Faktoren wie Größe, Lokalisation und Stabilität (Abb. 2).
Konservative Therapie
OD-Läsionen im Kindes- und Jugendhalter haben ein signifikant besseres Heilungspotenzial als solche im Erwachsenenalter, wobei eine noch geöffnete Wachstumsfuge des distalen Femurs ein zusätzlicher positiver prognostischer Faktor ist. Die konservative Therapie ist dabei die primäre Wahl für stabile OD im Jugend- und Kindesalter. Die Säulen der konservativen Therapie bestehen aus Schonung und entlastender Mobilisierung.13 Obwohl es keine Evidenz dafür gibt, dass eine spezifische konservative Therapie, wie Physiotherapie oder eine teilbelastende Mobilisierung, den Heilungsverlauf positiv beeinflussen würde,14 werden meist zunächst konservative Therapieoptionen für 3–6 Monate empfohlen, bevor chirurgische Alternativen erwogen werden sollten.
Chirurgische Therapien
Retrograde Bohrung
Abb. 3: Arthroskopisch assistierte retrograde Bohrung bei einem 12-jährigen männlichen Patienten mit einer symptomatischen stabilen Osteochondritis-dissecans-Läsion am posterolateralen medialen Femurkondyl
Bei stabilen Läsionen mit intaktem Gelenkknorpel stellt die Anbohrung mittels mehrerer Kirschner-Drähte die chirurgische Behandlungsmethode der Wahl dar. Durch diesen Eingriff soll der sklerotische Rand der Läsion durchbrochen werden, was eine Freisetzung von Wachstumsfaktoren aus der gesunden Spongiosa darunter erlauben und zu einer Verbesserung der Durchblutung führen soll. Dafür kommt sowohl eine antegrade als auch eine retrograde Technik infrage, wobei die retrograde Bohrung den wesentlichen Vorteil bietet, ohne Schädigung der Gelenkoberfläche auszukommen (Abb. 3). Die retrograde Bohrung sollte unter sorgfältiger Bildwandlerkontrolle und unter Schonung der Wachstumsfuge erfolgen.15 Als Unterstützung bietet sich hierfür die Verwendung eines tibialen Kreuzband-Zielgerätes an. Insgesamt ist durch die Anbohrung bei der richtigen Indikationsstellung eine hohe Heilungsrate zu erwarten, wobei eine rezente Studie keinen Unterschied zwischen der antegraden und retrograden Technik feststellen konnte.16
Refixation
Generell gilt, dass jede instabile Läsion, die refixierbar ist, auch refixiert werden sollte. Sollten im Rahmen einer Anbohrung Zweifel an der Stabilität der Läsion bestehen, sollte ebenfalls eine zusätzliche Fixierung erfolgen. Wenn das Knochenbett zugänglich ist, sollte zusätzlich ein Débridement des fibrösen Gewebes erfolgen. Im Falle eines knöchernen Defektes zwischen Fragment und Knochenbett empfiehlt sich eine zusätzliche autologe Spongiosaplastik mit Knochenentnahme von der proximalen Tibia oder dem Beckenkamm.
Die Refixation kann mit verschiedenen metallischen oder resorbierbaren Implantaten erfolgen. Metallische Implantate haben mehrere Nachteile, wie die Gefahr der Migration und Tangierung des gegenüberliegenden Knorpelbelages, MRT-Artefakte, Bruch oder Lockerung und eine hohe Rate an Zweiteingriffen zur Materialentfernung. Dies hat zur Entwicklung von resorbierbaren Implantaten aus Polyglykolsäure (PGA) oder Polylactidsäure (PLA) geführt. Zur Refixation werden zwei bis vier dieser Implantate empfohlen, um das Fragment ausreichend unter Kompression zu setzen und rotationsstabil zu verankern. Dabei ist darauf zu achten, die Wachstumsfuge mit den Implantaten nicht zu tangieren. Durch Refixation mit resorbierbaren Implantaten lassen sich gute Ergebnisse erzielen. So konnte in einer rezenten Studie eine radiografische Heilungsrate von 97% nach einer Nachuntersuchungszeit von durchschnittlich 3,3 Jahren demonstriert werden.17 Resorbierbare Pins scheinen resorbierbaren Nägeln hinsichtlich des klinischen Outcomes überlegen zu sein.18 Ein wesentlicher Nachteil der resorbierbaren Implantate ist das Auftreten von Fremdkörperreaktionen im Rahmen der Resorption. Eine rezent entwickelte Alternative ohne Gefahr von Fremdkörperreaktionen stellt die Verwendung der SharkScrew®, eines allogenen Knochenschrauben-Transplantats, zur Refixation dar (Abb. 4, 5). Wesentliche Vorteile sind die die gute mechanische Stabilität bei gleichzeitig biologischer Verankerung mit guter Integration in den Knochen. Die Technik wird derzeit im Rahmen einer Multicenter-Studie evaluiert.
Sollte das Fragment nicht mehr refixierbar sein, muss auf alternative Reparaturtechniken wie die matrixassoziierte Chondrozytentransplantation oder den osteochondralen Autografttransfer zurückgegriffen werden. Dies ist in der pädiatrischen Population äußerst selten, entsprechend gering ist die wissenschaftliche Evidenz hinsichtlich des zu erwartenden Outcomes dieser Techniken.
Abb. 4: 13-jähriger männlicher Patient mit einer instabilen Osteochondritis-dissecans-Läsion am posterolateralen medialen Femurkondyl präoperativ (A, D), 3 Monate (B, E) sowie 12 Monate (C, F) nach Refixation mittels Shark-Screw
Abb. 5:13-jähriger männlicher Patient mit einer instabilen Osteochondritis-dissecans-Läsion am posterolateralen medialen Femurkondyl präoperativ (A, C) sowie 12 Monate (B, D) nach Refixation mittels Shark-Screw
Osteochondraler Autografttransfer
Der osteochondrale Autografttransfer (OAT) ist eine wirksame Behandlung für Knorpeldefekte kleiner als 2,5cm2. Hierbei wird ein osteochondraler Zylinder aus einem nicht gewichtsbelasteten Bereich des Knies an die Defektstelle übertragen. Wesentlicher Vorteil ist die gleichzeitige Adressierung des knöchernen Defektes und des Knorpeldefektes mit vitalem Knochen und Knorpel. Wesentliche Nachteile der Technik sind die Entnahmemorbidität und daraus folgend eine Limitation der behandelbaren Defektgröße. In einer prospektiv randomisierten Studie zeigte sich hierbei ein signifikant besseres Langzeitergebnis der OAT-Gruppe im Vergleich zur Mikrofrakturierungsgruppe nach 4,2 Jahren Follow-up. In den seltenen Fällen, in denen der Defekt die mittels OAT rekonstruierbare Größe übersteigt, kann auch ein osteochondraler Allograft eine Therapiealternative sein.19
Matrixassoziierte Chondrozytentransplantation
Größere Defekte (>4cm2) sind aufgrund der Entnahmemorbidität mit OAT nicht mehr sinnvoll behandelbar. Stattdessen kann eine matrixassoziierte Chondrozytentransplantation (MACT) mit oder ohne autologe Spongiosaplastik erfolgen. MACT ist eine zweizeitige Knorpelreparaturtechnik, bei der im Ersteingriff Knorpelgewebe aus einer nicht gewichttragenden Region entnommen wird. Diese Zellen werden anschließend in vitro expandiert, bevor sie je nach Technik arthroskopisch oder mittels Mini-Arthrotomie in einem Zweiteingriff replantiert werden. Nach einem sorgfältigen Débridement und der Herstellung von stabilen vertikalen Knorpelschultern werden die Knorpelzellen in eine Trägermatrix appliziert und diese wird in den Defekt aufgebracht. Im Falle eines knöchernen Defektes muss zusätzlich eine autologe Spongiosaplastik erfolgen. Als Donorstelle kommen hierbei die proximale Tibia oder der Beckenkamm infrage. Mithöfer et al. konnten hier in 96% der Fälle ein gutes oder ein exzellentes klinisches Ergebnis nach einem Follow-up von im Durchschnitt 47 Monaten berichten.20 Diese guten klinischen Ergebnisse wurden durch einen systematischen Review bekräftigt. Die häufigste beobachtete Komplikation war hierbei die Grafthypertrophie in 7% der Fälle, wobei 83% der Patient*innen mit einer MACT der ersten Generation mit einem Periostlappen versorgt wurden,21 die nachgewiesenerweise vermehrt zur Grafthypertrophie neigen.
Begleiteingriffe
Wie schon zuvor diskutiert, ist eine umfassende klinische und radiologische Abklärung vor der Therapieentscheidung und -einleitung unerlässlich. Dies beinhaltet bei Knorpelschäden im Bereich des Kniegelenks insbesondere Ganzbeinröntgen im Stehen zur Vermessung der Beinachse. Einerseits konnte bei OD-Läsionen ein Zusammenhang zwischen Achsabweichungen und instabilen Läsionen demonstriert werden.22 Andererseits müssen Instabilitäten oder Achsabweichungen chirurgisch adressiert werden, um optimale biomechanische Voraussetzungen für die Knorpelreparatur zu gewährleisten. Bei ausreichendem Restwachstum kann hier ein wachstumslenkender Eingriff im Sinne einer Hemiepiphysiodese erfolgen. Bei unzureichendem Korrekturpotenzial muss auf eine Korrekturosteotomie zurückgegriffen werden, wobei die Korrektur an dem für die Fehlstellung ursächlichen Ort zu erfolgen hat.
Literatur:
1 König F: The classic: on loose bodies in the joint. Clin Orthop Relat Res 2013; 471(4): 1107-15 2 Nambu T et al.: Deformation of the distal femur: a contribution towards the pathogenesis of osteochondrosis dissecans in the knee joint. J Biomech 1991; 24(6): 421-33 3 Andriolo L et al.: Classification systems for knee osteochondritis dissecans: a systematic review. Cartilage 2022; 13(3): 19476035221121789 4 Hefti F et al.: Osteochondritis dissecans: a multicenter study of the European Pediatric Orthopedic Society. J Pediatr Orthop B 1999; 8(4): 231-45 5 Carey JL et al.: Novel arthroscopic classification of osteochondritis dissecans of the knee: a multicenter reliability study. Am J Sports Med 2016; 44(7): 1694-8 6 Dipaola JD et al.: Characterizing osteochondral lesions by magnetic resonance imaging. Arthroscopy 1991; 7(1): 101-4 7 Paletta GA et al.: The prognostic value of quantitative bone scan in knee osteochondritis dissecans. Apreliminary experience. Am J Sports Med 1998; 26(1): 7-14 8 Ramirez A et al.: Juvenile osteochondritis dissecans of the knee: perifocal sclerotic rim as a prognostic factor of healing. J Pediatr Orthop 2010; 30(2): 180-5 9 De Smet AA et al.: Untreated osteochondritis dissecans of the femoral condyles: prediction of patient outcome using radiographic and MR findings. Skeletal Radiol 1997; 26(8): 463-7 10 Masquijo J, Kothari A: Juvenile osteochondritis dissecans (JOCD) of the knee: current concepts review. EFORT Open Rev 2019; 4(5): 201-12 11 Heywood CS et al.: Correlation of magnetic resonance imaging to arthroscopic findings of stability in juvenile osteochondritis dissecans. Arthroscopy 2011; 27(2): 194-9 12 Schreiner MM et al.: The MOCART (Magnetic Resonance Observation of Cartilage Repair Tissue) 2.0 Knee Score and Atlas. Cartilage 2021; 13(1 suppl): 571S-87S 13 Kocher MS et al.: Management of osteochondritis dissecans of the knee: current concepts review. Am J Sports Med 2006; 34(7): 1181-91 14 Andriolo L et al.: Osteochondritis dissecans of the knee - conservative treatment strategies: s systematic review. Cartilage 2019; 10(3): 267-77 15 Pennock AT et al.: Extra-articular, intraepiphyseal drilling for osteochondritis dissecans of the knee. Arthrosc Tech 2013; 2(3): e231-5 16 Gunton MJ et al.: Drilling juvenile osteochondritis dissecans: retro- or transarticular? Clin Orthop Relat Res 2013; 471(4): 1144-51 17 Adachi N et al.: Functional and radiographic outcomes of unstable juvenile osteochondritis dissecans of the knee treated with lesion fixation using bioabsorbable pins. JPediatr Orthop 2015; 35(1): 82-8 18 Weckstrom M et al.: Comparison of bioabsorbable pins and nails in the fixation of adult osteochondritis dissecans fragments of the knee: an outcome of 30 knees. Am J Sports Med 2007; 35(9): 1467-76 19 Tisano B et al.: Osteochondral allograft for unsalvageable osteochondritis dissecans in the skeletally immature knee. Orthop J Sports Med 2022; 10(2): 23259671211072515 20 Mithöfer K et al.: Functional outcome of knee articular cartilage repair in adolescent athletes. Am J Sports Med 2005; 33(8): 1147-53 21 DiBartola AC et al.: Clinical outcomes after autologous chondrocyte implantation in adolescents‘ knees: a systematic review. Arthroscopy 2016; 32(9): 1905-16 22 Gonzalez-Herranz P et al.: Femoral osteochondritis of the knee: prognostic value of the mechanical axis. J Child Orthop 2017; 11(1): 1-5
Das könnte Sie auch interessieren:
Aktuelle Versorgungskonzepte: Tibiakopffrakturen
Der folgende Beitrag fasst die aktuelle Evidenz zu Epidemiologie, Klassifikationssystemen und Behandlungsstrategien zusammen und beleuchtet dabei insbesondere Aspekte der anatomischen ...
Relevanz der Beinachse bei der Therapie von degenerativen Meniskusläsionen
Die Beinachse spielt eine zentrale Rolle in der Biomechanik des Kniegelenks und beeinflusst maßgeblich die Entstehung, den Verlauf sowie die Therapieoptionen degenerativer ...
Frühe Unterwassertherapie nach totaler Hüft- und Knieendoprothese
Eine frühzeitige Durchführung der Unterwassertherapie mit wasserdichtem Folienverband ab dem vierten postoperativen Tag ist im Allgemeinen sicher, wirksam und ohne Nebenwirkungen.