Sauerstoff ist ein Medikament: Die Langzeit-Sauerstofftherapie
Autor:
Dr. med. Stephan Wieser
FMH Pneumologie und Allg. Innere Medizin
Lungen-Klinik Bethanien
Zürich
E-Mail: s.wieser@lungen-klinik.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Nicht selten wird Sauerstoff unserer Intuition folgend nach dem Motto «Mehr hilft mehr» verabreicht. Doch sollte wie bei jeder Medikamententherapie – und um eine solche handelt es sich auch hier – der Einsatz auf der Basis von Evidenz und Pathophysiologie erfolgen. Im Folgenden soll die Langzeit-Sauerstofftherapie («long-term oxygen treatment», LTOT) diskutiert werden. Diese wird (im Gegensatz zur akuten Sauerstofftherapie) vom Patienten langfristig und selbstständig im Alltag angewendet.
Keypoints
-
Die Indikation zur LTOT ist gegeben, wenn nach optimaler Therapie auch in einer stabilen Krankheitsphase eine schwere chronische Hypoxämie besteht.
-
Eine Messung der Blutgase ist zur sorgfältigen Verschreibung unerlässlich.
-
Ziel der LTOT ist der Anstieg des PaO2 auf mindestens 60mmHg bzw. um 10mmHg.
-
Die Anwendungsdauer muss 15h/d oder mehr betragen, um einen Überlebensvorteil zu erreichen.
-
Eine mobile Therapie kann zum Erreichen der notwendigen Anwendungsdauer beitragen und allenfalls auch die Leistungsfähigkeit verbessern.
-
Eine mögliche Nebenwirkung der LTOT ist eine Hyperkapnie.
Sauerstoff ist Leben – und kann schaden
Sauerstoff ist die Lebensgrundlage eines Grossteils der Lebewesen, so auch des Menschen. Unsere Atmosphäre beinhaltet zu 21% Sauerstoff. Dieser erlaubt den effizienten aeroben Stoffwechsel, bei Mangel wird auf einen ineffizienten anaeroben Metabolismus umgestellt, der nur für kurze Zeit aufrechterhalten werden kann.
Hypoxie ist die Unterversorgung des Körpergewebes mit Sauerstoff und äussert sich klinisch mit Tachypnoe, Tachykardie, Arrhythmie, Hyper- und später Hypotension. Patienten empfinden Dyspnoe, sie werden initial unruhig, desorientiert, später lethargisch und komatös. Von den verschiedenen Formen der Hypoxie ist die hypoxäme Hypoxie, bedingt durch eine erniedrigte Sauerstoffspannung im Blut, einer Sauerstoffsubstitution am besten zugänglich.
Die unkontrollierte Gabe einer hohen inspiratorischen Fraktion von Sauerstoff resultiert in einer Hyperoxie. Sie ist ebenfalls nicht unproblematisch und kann über längere Zeit zu einer ZNS-Toxizität (Unruhe, Schwindel, Nausea, Tunnelblick, Tinnitus), aber auch durch die Freisetzung freier Radikale über längere Zeit zu einem diffusen Alveolarschaden führen.
Hypoxäme versus hyperkapnische respiratorische Insuffizienz
Um die Mechanismen einer Hypoxämie und damit deren optimale Behandlung zu verstehen, lohnt sich die Einteilung eines Atemversagens (respiratorische Insuffizienz) in seine beiden Komponenten: die Lunge als gasaustauschendes und die Atempumpe als ventilierendes System (Abb.1).
Bei Abnahme der gasaustauschenden Fläche, Störung der Diffusion oder der Lungenperfusion wird nur die O2-Aufnahme, aufgrund des ungleich höheren Diffusionskoeffizienten jedoch nicht die CO2-Abgabe klinisch relevant gestört. Die hypoxäme respiratorische Insuffizienz (Typ 1) zeigt sich in der Blutgasanalyse mit einem erniedrigten arteriellen Sauerstoffpartialdruck (PaO2), der Kohlendioxidpartialdruck (PaCO2) ist normal oder im Falle einer Hyperventilation erniedrigt. Die Therapie besteht primär in einer Sauerstoffgabe.
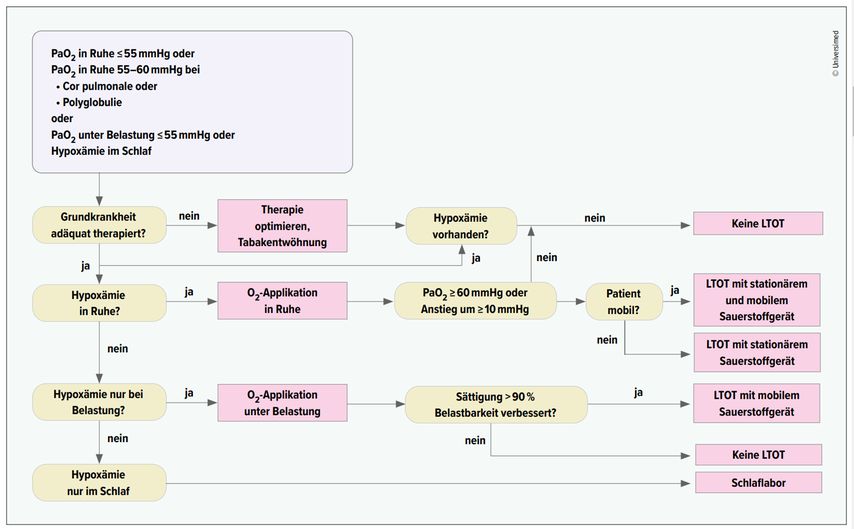
Abb. 2: Algorithmus zur Beurteilung der Indikation zur Langzeit-Sauerstofftherapie (LTOT) (adaptiert nach Magnussen et al.)13
Beeinträchtigungen der Atempumpe (durch Störungen des Atemzentrums, der efferenten Nerven oder der neuromuskulären Endplatte, der Atemmuskulatur oder des knöchernen Thorax) resultieren in einer ventilatorischen, hyperkapnischen Insuffizienz (Typ 2). Durch mangelnde Ventilation frischer, «unverbrauchter» Atemluft in das gasaustauschende Kompartiment kommt es ebenfalls zu einer Hypoxämie, aufgrund der fehlenden Abatmung des entstehenden CO2 aber auch zu einer Hyperkapnie und einer respiratorischen Azidose. Therapeutisch muss primär eine Beatmung evaluiert werden.
Die Messung der transkutanen Sauerstoffsättigung ist nicht ausreichend
Aus dieser Überlegung folgt, dass eine alleinige Sauerstoffmessung nur die Hypoxämie feststellt, jedoch keine Unterscheidung zwischen einer Störung des Gasaustausches und einer Störung der Atempumpe zulässt (hypoxämes vs. hyperkapnisches respiratorisches Versagen) und deshalb eine arterielle Blutgasanalyse mit u.a. Bestimmung des Kohlendioxiddrucks (PaCO2) notwendig ist. Im Weiteren können durch Messung des Sauerstoffdrucks (PaO2) auch häufige Artefakte der transkutanen Messung der Sauerstoffsättigung erkannt werden.
Evidenz für die Langzeit-Sauerstofftherapie stammt aus den 1980er-Jahren
Die richtungsweisenden randomisierten, kontrollierten Studien zum Einsatz der LTOT sind die NOTT(«Nocturnal Oxygen Therapy Trial»)-Studie mit 203 hypoxämen COPD-Patienten und die MRC(«Medical Research Council»)-Studie mit 87 hypoxämen Patienten aus dem Jahr 1980 resp. 1981. In der NOTT-Studie mussten 6 Patienten über 2 Jahre mit einer Langzeit-Sauerstofftherapie (vs. nur nächtliche Therapie) versorgt werden, um einen Todesfall zu vermeiden, in der MRC-Studie 5 Patienten über 5 Jahre (vs. keine Sauerstofftherapie). Die Kohorten der NOTT- und der MRC-Studie erlauben bei ausreichender Vergleichbarkeit eine kombinierte Analyse, deren Ergebnis die Wirksamkeit einer Sauerstofftherapie belegt. Im Vergleich zu Unbehandelten ist das Überleben von COPD-Patienten bei Sauerstoffgabe über mindestens 15h/d deutlich verbessert.
Verglichen mit heutigen Standards weisen diese Studien sehr geringe Patientenzahlen auf und die damals noch sehr limitierte COPD-Behandlung in den Bereichen Pharmakotherapie, Rehabilitation, nichtinvasive Langzeitbeatmung, Lungenvolumenreduktion usw. lässt eine Übertragung auf heutige Verhältnisse nur unter Vorbehalt zu. Dennoch sind diese beiden Studien die beste Evidenz, die zu dieser Fragestellung existiert. Der Endpunkt Überleben spiegelt allerdings nicht Lebensqualität und Leistungsfähigkeit im Alltag wider.
Die Evidenz für die Behandlung anderer hypoxämer Krankheitsbilder wie Lungenfibrose, pulmonale Hypertonie, restriktive Erkrankungen u.a.m. wurde aus diesen Untersuchungen abgeleitet, es existieren jedoch nur in sehr geringem Ausmass Studien, welche diese Fragestellungen direkt adressieren.
Effekte der Sauerstofftherapie
-
Günstige Beeinflussung der pulmonalen Hämodynamik: Es kann einem Anstieg des Drucks im Lungenkreislauf entgegengewirkt werden, teils kommt es sogar zu einem Absinken des Drucks.
Entlastung der Atempumpe: Es kommt zu einem Nachlassen des durch die Hypoxämie verstärkten Atemantriebs und somit zu einem Rückgang des Atemminutenvolumens. Die Reduktion des Atemantriebs vermindert nicht nur das Dyspnoe-Empfinden, sondern entlastet auch die Atemmuskulatur.
Weitere Effekte sind die Zunahme der körperlichen Leistungsfähigkeit, messbar z.B. im 6-Minuten-Gehtest, und auch positive Auswirkungen auf neurokognitive Funktionen. Bei COPD-Patienten konnten ein Rückgang der Exazerbationsrate und eine höhere Wahrscheinlichkeit des Überlebens einer Exazerbation gezeigt werden. Wahrscheinlich infolge der Zunahme der myokardialen Oxygenierung kommt es zu einem Rückgang der kardialen Arrhythmien. Diese Faktoren bewirken neben der verbesserten Prognose eine durchschnittlich bessere Lebensqualität.
Wann besteht die Indikation zur LTOT? Wie wird sie titriert?
Aufgrund der Daten aus den oben genannten Studien ist eine LTOT angezeigt bei (s. auch Abb.2):
-
schwerer Ruhe-Hypoxämie (definiert als PaO2 ≤55mmHg oder 7,3kPa)
oder mittelschwerer Ruhe-Hypoxämie (definiert als PaO2 ≤60mmHg oder 8kPa), wenn zusätzlich eine sekundäre Polyglobulie oder ein Cor pulmonale mit oder ohne Rechtsherzinsuffizienz vorliegen.
Voraussetzung ist, dass die chronische Hypoxämie nach Ausschöpfen anderer adäquater Therapieformen (Rehabilitation, Pharmakotherapie, Lungenvolumenreduktion, Therapie der Komorbiditäten) auch im stabilen Intervall in wiederholten Messungen (optimalerweise im Abstand von 3–4 Wochen) nachweisbar ist.
Falls eine postakute Sauerstofftherapie z.B. im Anschluss an eine Hospitalisation etwa aufgrund einer Exazerbation von COPD oder Lungenfibrose, einer schweren Pneumonie oder Covid-19 erfolgt, muss die Indikation zur langfristigen Weiterführung (und damit eine Transformation in eine LTOT) spätestens nach 6–12 Wochen überprüft und die Therapie bei fehlender weiterer Indikation beendet werden.
Die Titration der Dosis sollte mit dem Ziel eines PaO2 >60mmHg (8,0kPa) und einer SpO2 >90% erfolgen. Eine Hyperkapnie stellt per se keine Kontraindikation für eine LTOT dar, sollte aber weitere Überlegungen hinsichtlich der Ursache der Hypoxämie (Atempumpenversagen?) und der Differenzialtherapie (nicht invasive Beatmung) zur Folge haben. Beim Auftreten einer respiratorischen Azidose oder bei einem Anstieg des PaCO2 um >7,5mmHg (1kPa) unter Sauerstoffgabe muss die Therapie abgebrochen oder ergänzend eine nächtliche nichtinvasive Beatmung evaluiert werden.
Wie lange soll die LTOT täglich angewendet werden?
Ein Überlebensvorteil durch die LTOT ergibt sich bei einer Anwendungsdauer von 15h/d oder mehr, für eine kürzere Anwendungsdauer ist kein prognostischer Benefit belegt. Als Konsequenz ist sowohl die Indikation wie auch die Kostenübernahme für eine LTOT an eine Anwendungsdauer von mindestens 15h/d geknüpft.
Ein Grossteil der Sauerstoffapplikation kann während der Nacht erfolgen. In der aktualisierten Richtlinie der Deutschen Gesellschaft für Pneumologie (DGP) wird explizit darauf hingewiesen, dass aktuelle Beobachtungsstudien keinen Vorteil einer Applikation der LTOT über 24h/d vs. ≥15h/d hinsichtlich Mortalitäts- oder Hospitalisationsraten zeigen. Diese Ergebnisse müssen jedoch in randomisiert kontrollierten Studien validiert werden.
Welche Mechanismen der Dyspnoe und damit welche Symptomatik werden durch die LTOT günstig beeinflusst?
Obwohl dies dem komplexen Pathomechanismus der Dyspnoe nicht gerecht wird, erhoffen sich viele Patienten mit Lungenerkrankungen sowohl mit als auch ohne hypoxäme respiratorische Insuffizienz verständlicherweise eine Besserung der Dyspnoe durch eine Sauerstofftherapie. Auch bei hypoxämen Patienten wird die Dyspnoe in vielen Fällen nur zu einem geringen Teil günstig beeinflusst. Durch Sauerstoffsubstitution kann die Gasaustauschstörung zwar korrigiert werden, andere Mechanismen der Dyspnoe können aber nicht angegangen werden (Atemflussobstruktion, Überblähung, ungünstige Atemmechanik). Um nicht erfüllbare Erwartungen und Enttäuschungen zu vermeiden, muss dieser Aspekt mit den Patienten unbedingt vorgängig besprochen werden.
Mobile Sauerstofftherapie
Bei der mobilen Sauerstofftherapie wird vom Patienten eine mobile Sauerstoffquelle mitgetragen. Aufgrund des erhöhten Sauerstoffbedarfs, der kürzeren Kreislaufzeiten bei höherem Herzzeitvolumen und der dadurch bedingten Akzentuierung der Gasaustauschstörung unter körperlicher Belastung ist die Hypoxämie bei körperlicher Aktivität häufig aggraviert und vermehrt symptomatisch. Durch eine mobile Sauerstofftherapie kann dies partiell kompensiert werden. Meist bleiben die Patienten wegen verminderter Atemflüsse, Überblähung oder Restriktion zwar auch nach Korrektur der Hypoxämie symptomatisch, ein erheblicher Anteil der Patienten kann aber in Bezug auf Symptome (Dyspnoe, Belastungstoleranz) und körperliche Leistungsfähigkeit (Gehstrecke) profitieren.
In welchen Situationen soll eine mobile Sauerstofftherapie erfolgen?
Eine mobile Sauerstofftherapie ist angezeigt, wenn der Patient die angestrebte Therapiezeit einer LTOT von mindestens 15h/d aufgrund seiner hohen Mobilität und Aktivität im Alltag mit einer stationären (Heim-)Therapie nicht erreichen kann (prognostische Indikation).
Eine klinisch relevante Verbesserung unter mobiler Sauerstofftherapie (+30m im 6-Minuten-Gehtest oder Abnahme der Dyspnoe um 1 Punkt auf der Borg-CR10-Skala) erfahren ca. 40–50% der Patienten, hauptsächlich die Subgruppe mit stark eingeschränkter körperlicher Leistungsfähigkeit (symptomatische Indikation). Eine generelle Vorhersage des Effektes bleibt aber unmöglich, sodass eine standardisierte Messung unter kontrollierten Bedingungen mit und ohne ambulante Sauerstofftherapie notwendig ist. Letztlich bleibt die Umsetzung im Alltag individuell, da der symptomatische Benefit der körperlichen und logistischen Mehrbelastung gegenübergestellt werden muss.
Keine Indikation für eine mobile Sauerstofftherapie auch bei hypoxämen Patienten besteht, falls die genannten Voraussetzungen nicht erfüllt sind. In diesen Situationen ist eine Ausdehnung der Sauerstofftherapie auf die mobilen Phasen ausser Haus ohne sicheren Nutzen und sollte nicht mit der Verordnung einer mobilen Sauerstofftherapie erzwungen werden. Das Tragen der Sauerstoffquelle und auch eine befürchtete Stigmatisierung durch Anwendung in der Öffentlichkeit können für den Patienten Hindernisse darstellen und Rückzugstendenzen begünstigen.
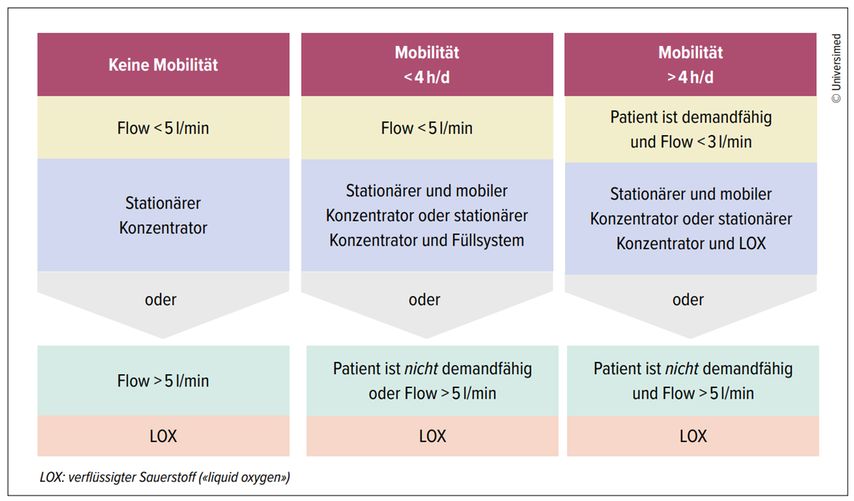
Abb. 3: Welche Sauerstoffversorgung wird benötigt? (Adaptiert nach ResMed Healthcare: Titrations-Kompass Sauerstoff. https://www.resmed-healthcare.de/fachkreise/sauerstoff-und-beatmung-informationsmaterial )
Kein Überlebensvorteil für Patienten mit ausschliesslich nächtlicher Hypoxämie
Die Sauerstofftherapie von Patienten mit ausschliesslich nächtlichen Hypoxämien ist ohne nachweisbaren Effekt auf Morbidität sowie Letalität (eine Ausnahme stellen herzinsuffiziente Patienten mit zentraler Schlafapnoe dar). Der Effekt auf Lebens- und Schlafqualität ist nicht genügend untersucht. Eine Therapie muss in diesen Fällen abhängig von Symptomen und Komorbiditäten individuell indiziert werden. Generell gilt, dass in diesen Situationen primär die Art der schlafassoziierten Atemstörung festgestellt und behandelt werden muss, z.B. mittels nächtlicher CPAP-Therapie bei obstruktivem Schlafapnoe-Syndrom oder nächtliche Beatmung bei Hypoventilations-Syndrom. Der Fokus der Therapie ist nicht die Desaturation während des Schlafs, sondern die (meist) zugrunde liegende schlafassoziierte Atemstörung!
Keine Indikation für palliative Sauerstofftherapie bei nicht hypoxämen Dyspnoepatienten
Nicht selten berichten auch nicht hypoxäme Dyspnoepatienten über einen positiven Effekt einer Sauerstofftherapie. Ursächlich hierfür ist eine Stimulation von sensiblen (v.a. Trigeminus-)Afferenzen, was dem Atemzentrum ein erhöhtes Atemminutenvolumen «vorgaukelt» und einen zentralen Placeboeffekt bewirkt. Die Dyspnoe kann aber in diesen Fällen durch z.B. Anwendung von Ventilatoren (kühler Luftstrom) und Opioidmedikation effizienter behandelt werden und sollte nicht zur Sauerstoffverschreibung führen.
Sauerstoffquellen für die LTOT
Sauerstoffkonzentratoren entziehen der Umgebungsluft O2 und geben diesen in hoher Konzentration wieder ab.
Stationäre Konzentratoren (Gewicht ca. 20kg) sind dem Stromnetz angeschlossen und erlauben die Heimtherapie mit einem Fluss bis 5lO2/min. Die Mobilität innerhalb der Wohnung kann durch lange Schläuche erreicht werden, so kann das Gerät auch fern vom Bett positioniert werden, um die Lärmbelästigung minimal zu halten. Die Patienten müssen allerdings auf die Sturzgefahr durch einen auf dem Boden liegenden Sauerstoffschlauch hingewiesen werden.
Mobile Konzentratoren (Gewicht ca. 2–3kg) können dank wiederaufladbarer Batterien mitgetragen werden. Sie geben den Sauerstoff als Bolus ab, der Patient triggert die Abgabe durch den nasalen Unterdruck bei Beginn der Einatmung («Demand»-Funktion). Bei niedrigem Atemzugvolumen und/oder hoher Atemfrequenz ist dies gelegentlich nicht effizient und der Patient kann nicht mit diesem System versorgt werden.
Falls höhere Flüsse notwendig sind (>5lO2/min) oder der Patient auf mobilen Sauerstoff angewiesen ist, diesen aber im Demand-Modus nicht triggern kann, muss ein kontinuierlicher Fluss angewendet werden (Abb.3). Auf –183°C gekühlter und dadurch verflüssigter Sauerstoff («liquid oxygen»; LOX) wird in Intervallen von ca. 1–3 Wochen angeliefert und in einem in der Wohnung des Patienten stationierten Tank gelagert, von wo er direkt oder über einen portablen «Baby»-Tank bezogen werden kann. Das Verhältnis von Gewicht zu möglicher Flussrate und -dauer ist bei LOX optimal, der logistische und finanzielle Aufwand aber am höchsten. «Sauerstofftankstellen» an verschiedenen Orten in der Schweiz erlauben Reisenden ein Auffüllen ihres portablen Geräts.
Eine Langzeitsauerstofftherapie mit Druckgasflaschen ist obsolet, da der O2-Bedarf dadurch nicht mit vernünftiger Logistik durchführbar ist. Druckgasflaschen bleiben einer bedarfsweisen, punktuellen (sog. «Burst»-)Therapie vorbehalten, wie sie ausserklinisch beispielsweise in palliativen Situationen, für Krankentransporte oder die Behandlung von Cluster-Kopfschmerzen angezeigt ist.
Die Sauerstoffverabreichung geschieht über eine Nasenbrille. Diese kann bedarfsweise in Brillengestelle integriert und damit weniger sichtbar gemacht werden. Die transtracheale Applikation über einen transkutanen Trachealkathether («Scoop») ist aus medikolegalen Gründen in der Schweiz nicht mehr durchführbar.
Die Beimengung von Sauerstoff zu einem hohen Fluss von Umgebungsluft (60l/min) über einen zusätzlichen Flussgenerator mit Befeuchter («nasale High-Flow-Sauerstofftherapie») kann – hauptsächlich über Auswaschen des physiologischen Totraums der Atemwege – die Effizienz der Sauerstofftherapie zusätzlich steigern. Ihr Einsatz erfolgt primär in akuten Situationen bei schwer hypoxämen Patienten. Ein Einsatz im ambulanten Langzeitbereich erfolgt bisher nur in Einzelfällen und ihr Stellenwert ist bisher noch nicht geklärt.
Wichtigkeit der Adhärenz
Die Sauerstofftherapie ist nur dann wirksam, wenn die Hypoxämie über einen ausreichend langen Zeitraum adäquat therapiert wird. Die für den Erfolg der Behandlung entscheidende Therapietreue kann durch mögliche Nebenwirkungen ebenso eingeschränkt werden wie durch eine unrealistische Erwartungshaltung. Patienten sollten daher sowohl hinsichtlich der Handhabung des LTOT-Systems wie auch hinsichtlich der Wirkungen und Nebenwirkungen sorgfältig geschult werden.
Nebenwirkungen der LTOT
Die schwerste mögliche Nebenwirkung einer LTOT ist eine Hyperkapnie als Folge 1.) eines verminderten Atemantriebes durch Korrektur der Hypoxämie, 2.) einer niedrigeren CO2-Bindungskapazität von oxygeniertem Häm und 3.) einer Änderung des Atemmusters und des Ventilations-/Perfusions-Verhältnisses unter Sauerstoffgabe. Eine Ermittlung des Sauerstoffbedarfs und der ventilatorischen Antwort unter Beizug von arteriellen Blutgasanalysen ist daher bei der Verordnung und auch im Verlauf erforderlich.
Neben dem Austrocknen der Nasenschleimhaut und daraus resultierender Epistaxis kann die LTOT zu psychisch belastenden Konsequenzen wie Angst vor Stigmatisierung führen. Gelegentlich besteht eine unbegründete Angst vor einer Sauerstoffabhängigkeit.
Durch die Präsenz von gasförmigem Sauerstoff in Innenräumen kann bei unsachgemässer Handhabung eine Brand- und Explosionsgefahr bestehen.
LTOT und Rauchen
Natürlich soll die Überprüfung der Indikation zur LTOT eine Raucherberatung zur Folge haben, falls eine Nikotinabhängigkeit besteht. Die Beratung muss auch den Progress der Grunderkrankung durch fortgesetztes Rauchen und den dadurch zunichte gemachten prognostischen Benefit einer Sauerstofftherapie thematisieren. Raucherinnen und Raucher mit einer Sauerstofftherapie müssen auch explizit auf die erhöhte Gefahr eines Brandunfalls hingewiesen werden. Eine absolute Kontraindikation stellt das Rauchen allerdings nicht dar.
Verordnung der LTOT
Aufgrund der genannten Überlegungen zur Differenzialdiagnostik und -therapie sowie der Notwendigkeit zur Messung von Blutgasen erfolgen die Indikationsstellung, Verordnung und Verlaufskontrolle einer LTOT idealerweise (wenn auch nicht mehr vom Kostenträger verlangt) durch einen Pneumologen. Das Verordnungsformular muss die Diagnose sowie Indikationskriterien und Resultate der Blutgasanalysen sowie Angaben zur verordneten Dauer, Fluss und Sauerstoffquelle enthalten.
Für die Therapie ist in vielen Situationen eine vorgängige Kostengutsprache des Versicherers notwendig. Nach Klärung der Kostenübernahme kann ein Home Care Provider (Lungenliga, private Anbieter) das notwendige Sauerstoffapplikationssystem bereitstellen und den Patienten in der Anwendung und Handhabe des Systems instruieren. Innerhalb der ersten drei Monate sollte eine erste Verlaufskontrolle unter Therapie erfolgen, anschliessend auch bei optimalem Verlauf für die Wiederholungsverordnungen zumindest jährlich.
AUF EINEN BLICK
Die Langzeit-Sauerstofftherapie (LTOT)
Die Indikation zur LTOT ist gegeben, wenn nach optimaler Therapie auch in einer stabilen Krankheitsphase zu mehreren Zeitpunkten gemessen eine schwere chronische Hypoxämie besteht (PaO2 < 55 mmHg [7,3 kPa] oder > 60 mmHg [8 kPa], sofern eine sekundäre Polyglobulie oder ein Cor pulmonale vorliegen). Eine Messung der Blutgase ist zur sorgfältigen Verschreibung unerlässlich.
Ziel der Therapie ist der Anstieg des PaO2 auf mindestens 60 mmHg bzw. um 10 mmHg. Die Anwendungsdauer muss 15 h/d oder mehr betragen, um einen Überlebensvorteil zu erreichen. Eine mobile Therapie kann zum Erreichen der notwendigen Anwendungsdauer beitragen und allenfalls auch die Leistungsfähigkeit verbessern, die Indikation ist aber individuell zu prüfen
Grundsätzliche Kontraindikationen bestehen nicht. Eine mögliche Nebenwirkung der LTOT isteine Hyperkapnie.
Sauerstoffquellen können Konzentratoren oder Flüssigsauerstoff sein. Flüssigsauerstoff muss häufig nachgeliefert werden, kann aber auch mobil mit konstantem Fluss und geringem Gewicht verabreicht werden. Konzentratoren beziehen den Sauerstoff aus der Umgebungsluft, mobile Geräte arbeiten praktisch ausschliesslich im «Demand»-Modus, die Fähigkeit des Patienten, diesen zu triggern, muss vorgängig geprüft werden.
Literatur:
1 Thomson L, Paton J: Oxygen toxicity. Paediatr Respir Rev 2014; 15: 120-3 2 Windisch W et al.: S2k-Leitlinie: Nichtinvasive und invasive Beatmung als Therapie der chronischen respiratorischen Insuffizienz – Revision 2017. Pneumologie 2017; 71: 722-95 3 Nocturnal Oxygen Therapy Trial Group: Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease: a clinical trial. Ann Intern Med 1980; 93: 391-8 4 Medical Research Council Working Party: Long term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complicating chronic bronchitis and emphysema. Lancet 1981; 1: 681-6 5 Haidl P et al.: Leitlinie zur Langzeit-Sauerstofftherapie. Pneumologie 2020; 74: 813-41 6 Haidl P: Langzeitsauerstofftherapie. Pneumologe 2022; 19: 27-32 7 Brill SE, Wedzicha JA: Oxygen therapy in acute exacerbations of chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis 2014; 9: 1241-52 8 Lacasse Y et al.: Randomized trial of nocturnal oxygen in chronic obstructive pulmonary disease. N Engl J Med 2020; 383: 1129-38 9 Zeineddine S et al.: Oxygen therapy in sleep-disordered breathing. Chest 2021; 160: 701-17 10 Swan F et al.: Airflow relieves chronic breathlessness in people with advanced disease: An exploratory systematic review and meta-analyses. Palliat Med 2019; 33: 618-33 11 Hardavella G et al.: Oxygen devices and delivery systems. Breathe 2019; 15: e108-16 12 Geiseler J, Kissel,M: Ambulante Versorgung mit Sauerstoff. Pneumologe 2022; 19: 33-41 13 Magnussen H et al.: Leitlinien zur Langzeit-Sauerstofftherapie. Pneumologie 2008; 62: 748-56
Das könnte Sie auch interessieren:
Long-Covid-Rehabilitation 2025 – von der klinischen Erfahrung zur Evidenz
Seit 2020 hat sich die Rehabilitation bei Covid-19 und Long Covid von ersten Erfahrungsberichten hin zu einer evidenzbasierten Maßnahme entwickelt. Aktuelle Studien belegen, dass ...
Asthma bronchiale: Herausforderungen bei Kindern und Jugendlichen
Asthma bronchiale ist eine chronische Krankheit, die im Kindesalter andere Herausforderungen mit sich bringt als bei Erwachsenen. Die physikalische Untersuchung sowie die Therapie sind ...