Therapieempfehlungen bei Sarkoidose
Bericht: Mag. Andrea Fallent
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
2021 wurde die erste ERS-Leitlinie zur Behandlung der Sarkoidose publiziert, orale Kortikosteroide bleiben First-Line-Therapie. Aufgrund der ausgesprochen heterogenen Studienlage weisen die meisten Empfehlungen jedoch einen geringen Evidenzgrad auf – einige Fragen, z.B. zur Therapiedauer, sind weiterhin offen. Leitlinienkoautor PD Dr. Dr. Francesco Bonella, Essen, versuchte, mit seinem Vortrag einige davon zu beantworten.
Für die aktuelle Leitlinie screente die Task Force der European Respiratory Society (ERS) ab 2017 mehr als 15000 Publikationen. Dennoch bleiben für diese seltene Erkrankung nur wenige Studien übrig, die evidenzbasierte Empfehlungen zur Diagnostik und Therapie ermöglichen. In seinem Vortrag „Neue ERS-Leitlinie zur Sarkoidose: Hilft uns das weiter?“ bei der DGP-Tagung im Mai 2022 in Leipzig brachte PD Dr. Dr. Francesco Bonella, Zentrum für interstitielle und seltene Lungenerkrankungen, Universitätsmedizin Essen, als Koautor der Leitlinien einen kurzen Überblick über die Behandlungsoptionen und ging auf einige offene Fragen die Leitlinie betreffend ein.
Fragestellungen und Behandlungsindikationen
In der Leitlinie wurden acht klinisch relevante Fragestellungen nach dem PICO (Patient-Intervention-Comparison-Outcome)-System zur Behandlung spezifischer Organmanifestationen präzisiert: zwei zur pulmonalen Sarkoidose, zwei zur Hautbeteiligung, eine zur kardialen Manifestation, eine zur Neurosarkoidose sowie je eine zur Fatigue und zur Small-Fiber-Neuropathie.
Für die Entscheidung, ob und wie nach der Diagnose Sarkoidose behandelt werden sollte, sind die folgenden zwei Fragen essenziell: Wie stark wird die Lebensqualität des Patienten durch die Sarkoidose beeinträchtigt? Und zweitens: Besteht ein erhöhtes Risiko, dass es durch die Sarkoidose zu einem reversiblen Organschaden, einer permanenten Funktionseinschränkung und Morbidität oder frühzeitigem Tod kommen kann? Der Hintergrund: Rund 5% der Sarkoidosepatienten sterben an der Erkrankung, wobei die Beteiligung von Lunge und Herz die häufigste Todesursache darstellt.1
Eine große Herausforderung für die Definition der Leitlinie stellte die Heterogenität der betrachteten Studienergebnisse dar. So gibt es für die Therapie der pulmonalen Sarkoidose keine Orientierungsmöglichkeit mit Evidenz anhand der Lungenfunktion, der Ausprägung der Lungenfibrose oder der präkapillären pulmonalen Hypertonie. Aus diesem Grund enthält die Leitlinie auch keinerlei Referenzwerte bezüglich der Lungenfunktionstests.
Antiinflammatorische Therapie
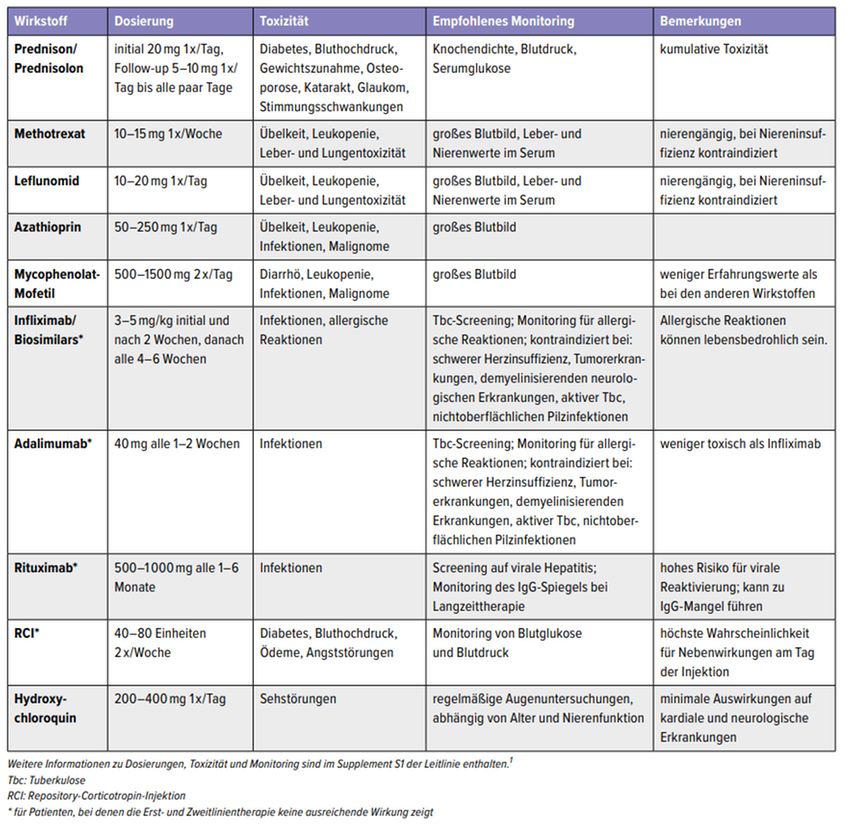
Für Patienten, bei denen kein Risiko für Morbidität oder Mortalität besteht oder bei denen es keine signifikante Beeinträchtigung der Lebensqualität (QoL) gibt, empfiehlt die Leitlinie aufgrund der hohen Prävalenz unerwünschter Arzneimittelwirkungen keine orale Glukokortikoidbehandlung. In allen anderen Fällen wird die Kortikosteroid-Monotherapie in Form von Prednison bzw. Prednisolon generell als First-Line-Therapie definiert. Die Zweitlinientherapie besteht aus Methotrexat, Azathioprin, Leflunomid, Mycophenolat und Hydroxychloroquin. Als Drittlinientherapie kommen Biologika – konkret die Anti-TNF-α-Antikörper Infliximab und Adalimumab sowie Rituximab und Repository-Corticotropin-Injektionen – zum Einsatz. Einen Überblick über die eingesetzten Wirkstoffe bietet die Tabelle 1.1 Die Algorithmen für die immunsuppressive Therapie enthalten aus genannten Gründen keine präzisen Empfehlungen für die Therapiedauer.
Pulmonale Sarkoidose
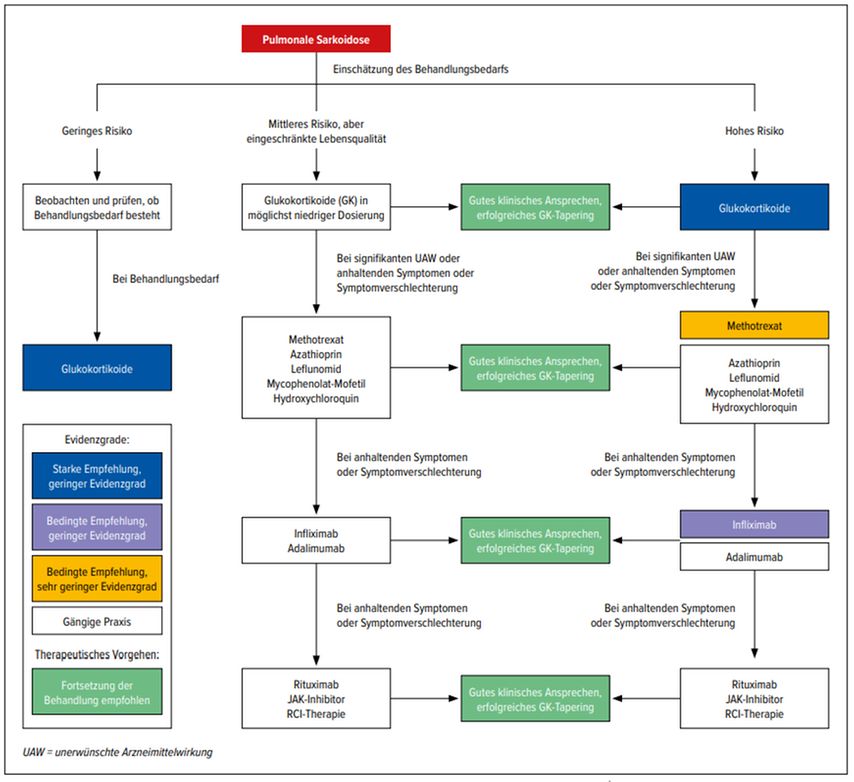
Lungenbeteiligung per se ist keine Indikation für eine Behandlung. Bei der Einschätzung der Behandlungsbedürftigkeit sollten folgende Aspekte gegeneinander abgewogen werden: zum einen die Minimierung des Risikos für eine Behinderung, des Mortalitätsrisikos oder des Verlusts der Lebensqualität aufgrund einer Lungenbeteiligung und zum anderen das Risiko für Komorbiditäten und für den Verlust von Lebensqualität aufgrund einer Therapie. Der Therapiealgorithmus stratifiziert die Patienten nach geringem, mittlerem und hohem Risiko (Abb.1). Zu den Patienten mit hohem Risiko, aufgrund einer pulmonalen Sarkoidose eine dauerhafte Behinderung zu entwickeln oder zu versterben, zählen diejenigen mit reduzierter Lungenfunktion (FVC, DLCO), mittelschwerer bis schwerer Lungenfibrose oder präkapillärer pulmonaler Hypertonie.1
Bisher unbehandelte Patienten mit einem hohen Risiko sollten mit Glukokortikoiden therapiert werden. Ebenso Patienten mit einem mittelgradigen Risiko, bei denen die Lebensqualität beeinträchtigt ist. Die Kortikoidinitialdosis wird in der Leitlinie mit 20mg täglich über sechs bis zwölf Monate angegeben, wobei die Ausschleichprotokolle variieren. Methotrexat (MTX), das am besten untersuchte Second-Line-Medikament, ist genauso wirksam wie Azathioprin und Leflunomid – mit weniger unerwünschten Wirkungen.2 Als MTX-Dosierungsempfehlung gelten 10–15mg einmal pro Woche (Tab. 1).1
Abb. 1: Behandlungsempfehlungen für die pulmonale Sarkoidose (modifiziert nach Baughman RP et al. 2021)1.Sie stellen eine Kombination der Empfehlungen der Leitlinie1 und der Praxiserfahrungen der Task-Force-Mitglieder dar. Die Anwendung von Rituximab, JAK-Inhibitoren und Repository-Corticotropin-Injektion (RCI) sollte individuell entschieden werden.
In diesem Zusammenhang erwähnte Bonella die Delphi-Konsensusempfehlungen für die pulmonale Sarkoidose aus dem Jahr 2020, an der die meisten der Leitlinienautoren mitgewirkt haben.3 Bonella: „In diesem Algorithmus wird eine Prednisoninduktionsdosis von 20 bis 40mg über drei bis sechs Monate angegeben.“ Der Unterschied in den Angaben ergibt sich laut Bonella daraus, dass die Leitlinie die Evidenz als Grundlage für Empfehlungen betrachtet und die Konsensusempfehlungen auf der Praxiserfahrung der Experten basieren.
Kutane Sarkoidose
Bis zu 30% der Sarkoidosepatienten weisen auch nichtspezifische Hautveränderungen auf, u.a. Papeln, Plaques, Knötchen, Vitiligo, Ulcera und Alopezie.1 Sie sind oft die ersten Anzeichen der Erkrankung. Für die kutane Manifestation wurden in der Leitlinie konkrete Fragestellungen und ein Therapiealgorithmus formuliert. Bei schmerzhaften und potenziell entstellenden Läsionen, bei denen topische bzw. intraläsionale Glukokortikoide keine Besserung erzielen, wird eine Behandlung mit systemischem Prednison/Prednisolon empfohlen. Aufgrund der Langzeitnebenwirkungen inkl. Hautveränderungen ist auf einen sparsamen Einsatz zu achten.
Bleiben Verbesserungen unter der Steroidbehandlung aus, rät die Leitlinie zur zusätzlichen Gabe von Hydroxychloroquin und Chloroquin – vor dem Einsatz von Methotrexat bzw. in der Folge Infliximab. Bonella: „Zur systemischen Kortikoidtherapie gibt es allerdings nur eine schwache Empfehlung und eine niedrige Evidenzqualität.“
Für die antimykobakterielle Breitbandtherapie CLEAR (Levofloxacin, Ethambutol, Azithromycin, Rifabutin), die in den USA eingesetzt wird, wurde keine Empfehlung abgegeben, so Bonella: „Wir halten die Therapie für nicht wirksam bei der Hautsarkoidose oder bei anderen Organmanifestationen.“
Kardiale Sarkoidose
In der Leitlinie wird im Zusammenhang mit der kardialen Beteiligung nur auf die Behandlungsindikation bzw. die Therapie mit Glukokortikoiden bei Myokardbeteiligung konkret eingegangen (starke Empfehlung, aber sehr niedriger Evidenzgrad). Die empfohlene Glukokortikoid-Induktionsdosis ist mit 0,5mg/kg höher als bei den vorherigen Indikationen. Bonella betonte, dass ein frühes Absetzen der Medikation, unabhängig vom Erfolg der Therapie, extrem kontraproduktiv wäre. Für den Einsatz weiterer Immunsuppressiva konnte keine GRADE-basierte Empfehlung abgegeben werden.
Small-Fiber-Neuropathie
Für die Small-Fiber-Neuropathie konnte keine Empfehlung abgegeben werden. Die Erkrankung sollte aber auf jeden Fall in Hinblick auf die Lebensqualität der Patienten wahrgenommen und berücksichtigt werden, so Bonella. Ein entsprechender Therapiealgorithmus enthält Behandlungsoptionen wie GABA-Analoga und Antidepressiva.1 Das synthetische Peptid Cibinetid, vormals ARA-290, mit antiinflammatorischen und neuroprotektiven Eigenschaften konnte in der Leitlinie nicht mehr berücksichtigt werden, weil der Wirkstoff nicht erhältlich ist.
Einschränkungen der Leitlinie
Auf Organtransplantationen sowie weitere Organmanifestationen (u.a. Leber, Niere, Knochenmark) und mögliche weitere Therapieoptionen wie die Sauerstofftherapie oder antifibrotische Interventionen wurde in der neuen Leitlinie nicht eingegangen. Weiters wurden Komplikationen der Sarkoidose wie Lungenhochdruck, Hydrocephalus oder Aspergillom nicht thematisiert. Abschließend betonte Bonella, dass es Überlegungen gäbe, „in Zukunft eine eigene Leitlinie zu Studienendpunkten zu formulieren, um die Heterogenität organspezifischer Outcomes zu begrenzen. Vorrangiges Ziel dieser ersten Therapie-Leitlinie ist es, eine Plattform für zukünftige Leitlinien zu bieten, die auch Empfehlungen zur nicht-medikamentösen Therapien enthalten“.
Factbox
Die Sarkoidose ist eine entzündliche Systemerkrankung unbekannter Ätiologie mit nichtverkäsenden Granulomen, vorwiegend mit Lungen-, Lymphknoten-, Haut- und/oder Augenbeteiligung; es kann aber jedes Organ betroffen sein. Die Sarkoidose zählt mit einer Prävalenz von etwa 10–40/100 000 Einwohnern zu den seltenen, aber nicht sehr seltenen Erkrankungen in Europa. Als Allgemeinsymptome können Leistungsminderung, Gewichtsabnahme, febrile oder subfebrile Temperaturen sowie Nachtschweiß auftreten. In rund 90 % der Fälle findet sich eine pulmonale Beteiligung in Form von mediastinalen Lymphknotenschwellungen und Veränderungen des Lungenparenchyms. Der Verlauf der Sarkoidose variiert und reicht von Verläufen mit spontaner Remission bis zu chronischen Erkrankungen mit funktioneller Organeinschränkung. Letztere erfordern häufig eine immunsuppressive Therapie und sind mit einem erhöhten Mortalitätsrisiko assoziiert. Es gibt nur wenige randomisierte kontrollierte klinische Studien zur Sarkoidose, das Wissen über den Schweregrad der Phänotypen und das unterschiedliche Therapieansprechen in den Subgruppen ist begrenzt, was die Behandlung der Sarkoidose schwierig macht.3
Quelle:
„Neue ERS-Leitlinie zur Sarkoidose: Hilft uns das weiter?“, Vortrag von PD Dr. Dr. Francesco Bonella, Essen, beim 62. Kongress der DGP am 26. Mai 2022, Leipzig
Literatur:
1 Baughman RP et al.: ERS clinical practice guidelines on treatment of sarcoidosis. Eur Respir J 2021; 58: 2004079 2 Vorseelas A et al.: Methotrexate vs azathioprine in second-line therapy of sarcoidosis. CHEST 2013; 144(3): 805-12 3 Rahaghi F et al.: Delphi consensus recommendations for a treatment algorithm in pulmonary sarcoidosis. Eur Respir Rev 2020; 29: 190146
Das könnte Sie auch interessieren:
Statine bei idiopathischer Lungenfibrose
Aufgrund von Daten aus Medikamentenstudien und Registern vermutete man bei den häufig verschriebenen Statinen zur Senkung des kardiovaskulären Risikos einen möglichen synergistischen ...
Allergie: wie es beginnt
Allergien sind multifaktorielle Erkrankungen, die in jedem Lebensalter, vornehmlich aber in den ersten Lebensdekaden auftreten. Auch Asthma bronchiale ist eine heterogene, ...