Prostatakarzinom-Management im lokalisierten und metastasierten Setting
Bericht:
Mag. Dr. Anita Schreiberhuber
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine Herausforderung beim lokalisierten Prostatakarzinom (PCa) ist es, prädiktive Faktoren zu identifizieren, die bei der Entscheidungsfindung helfen. Beim metastasierten kastrationsresistenten Prostatakarzinom (mCRPC) kam es zu bedeutenden Therapiefortschritten, wobei die Substanzen nun zunehmend ins hormonsensitive Setting vordringen.
Keypoints
-
AI-basiertes Gleason-Grading könnte in Zukunft eine wichtige Rolle spielen, muss sich aber noch in randomisierten Studien beweisen.
-
„Pharmaco-Staging“ mittels Enzalutamid + AS könnte eine gangbare alternative Strategie statt alleiniger AS sein.
-
ARPI, PARP-Inhibition und PSMA-Lu haben sich in der letzten Dekade beim metastasierten Prostatakarzinom als Therapien etabliert, aber die Immuntherapie enttäuscht.
-
PSMA-Lu + Enzalutamid wurde im metastasierten Setting mit guten Resultaten untersucht, weitere Innovationen könnten bald folgen.
Lokalisiertes Prostatakarzinom
Welche Strategie beim lokalisierten Prostatakarzinom (PCa) in Hinsicht auf die langfristige Mortalität, die Lebensqualität (QoL) und eventuelle Therapiefolgen eingesetzt werden sollte, ist noch nicht abschließend geklärt. Denn fast 20% der Patienten leiden nach einer radikalen Prostatektomie (RP) an Harninkontinenz und 80% an erektiler Dysfunktion. Eine Übersichtsarbeit, die RP und „active surveillance“ (AS) verglich, zeigte nach einem Follow-up (FU) von fast 20 Jahren keine signifikanten Unterschiede im PCa-spezifischen Überleben, die RP ging jedoch mit einer höheren Rate unerwünschter Folgen einher.1 Bestätigt wurde dies durch die Studie ProtecT, in der 1643 Männer im 1:1:1-Design randomisiert einer RP, Radiotherapie (RT) oder AS zugeteilt wurden. Nach dem FU von 15 Jahren war die krebsspezifische Mortalitätsrate niedrig und unabhängig von der Strategie – RP=2,2%; RT =2,9%; AS=3,1%. Die Autoren betonen, dass Benefits einer Therapie und mögliche Schäden abgewogen werden sollten.2
„Noch immer ist unklar, welche prognostische Faktoren für die Therapieentscheidung herangezogen werden könnten. Es stellt sich die Frage, ob Unsicherheit eine potenzielle Übertherapie rechtfertigen kann“, argumentierte Prof. Dr. Olivier Cussenot, Sorbonne Université – Hôpital Tenon, Paris. Das prostataspezifische Antigen (PSA) ist nach wie vor ein Eckpfeiler beim Screening und bei der Diagnose. Es gibt jedoch genetische, klinische und biologische Faktoren wie den Body-Mass-Index, die die PSA-Level im Blut modifizieren können. Ein personalisierter PSA-Test sollte diese Effekte auf den PSA-Spiegel berücksichtigen.3 Basis für verlässliche Aussagen über die Prognose ist die Reproduzierbarkeit von Ergebnissen. Dazu wurde die internationale Studie PANDA durchgeführt, in der anhand von mit Artificial Intelligence (AI) 10616 digitalisierten Prostatabiopsien mithilfe von reduzierbaren AI-basierten Algorithmen ein Gleason-Gradingerfolgte. Die Ergebnisse der AI wurden mit der Befundung sowohl durch US-amerikanische als auch durch europäische Uropathologen verglichen. Die Konkordanz der Ergebnisse von AI und Mensch war in beiden Fällen hoch: 0,862 bzw. 0,868. Dies spricht für die weitere Evaluierung von AI-basiertem Gleason-Grading in prospektiven Studien.4
Eine spannende Entwicklung sieht Cussenot im sogenannten „Pharmaco-Staging“. Es gibt Daten, wonach eine antihormonelle Kurzzeittherapie bei Patienten, die für eine AS geeignet sind, Benefits hinsichtlich der Outcomes bringen kann. So wurde bei 98 Patienten mit indolentem Niedrigrisiko-PCa die Gabe einer Androgendeprivationstherapie (ADT) für 3 Monate untersucht, wobei bei fast jedem zweiten Patienten nach der ADT die Biopsien negativ waren. Dies könnte somit eine innovative Strategie sein, sie muss aber noch in weiteren Studien bestätigt werden.5 In der offenen Studie ENACT wurde die einjährige Einnahme des Androgenrezeptor-Pathway-Inhibitors (ARPI) Enzalutamid bei PCa-Patienten mit niedrigem (LR) oder intermediärem (IR) Risko vs. alleinige AS untersucht. Die Rate negativer Biopsien war unter Enzalutamid vs. AS 3,5x höher. Im Enzalutamid-Arm kam es zu einer signifikanten Verzögerung der PSA-Progression um 6 Monate (p=0,03), was den Schluss zulässt, dass Enzalutamid + AS eine gangbare alternative Strategie sein dürfte.6 Cussenot tritt aufgrund der Datenlage dafür ein, die Standard-Klassifikatoren zu überarbeiten.
Metastasiertes Prostatakarzinom
Univ.-Prof. Dr. Gero Kramer, Medizinische Universität Wien, gab einen Überblick über die Therapie des PCa im fortgeschrittenen Setting und besprach das metastasierte hormonsensitive PCa (mHSPC), das lokalisierte Hochrisiko-PCa (HR-PCa) und das mCRPC. ARPI und PARP-Inhibition (Olaparib) für Patienten mit BRCA2-Mutation sowie die Therapie mit prostataspezifisches Membranantigen-Lutetium (PSMA-Lu) haben die Behandlung des mCRPC entscheidend erweitert.7 Die Immuntherapie dagegen konnte sich beim PCa noch nicht etablieren. So wurden am ESMO-Kongress 2023 zwei negative Studien8,9 zu Pembrolizumab präsentiert, obwohl in der KEYNOTE-641-Studie eine Subgruppe von mCRPC-Patienten (7,3%) identifiziert wurde, die unter Pembrolizumab + Enzalutamid eine komplette Response (CR) erzielten. Die Patientencharakteristika für eine Response bleiben somit unklar.8
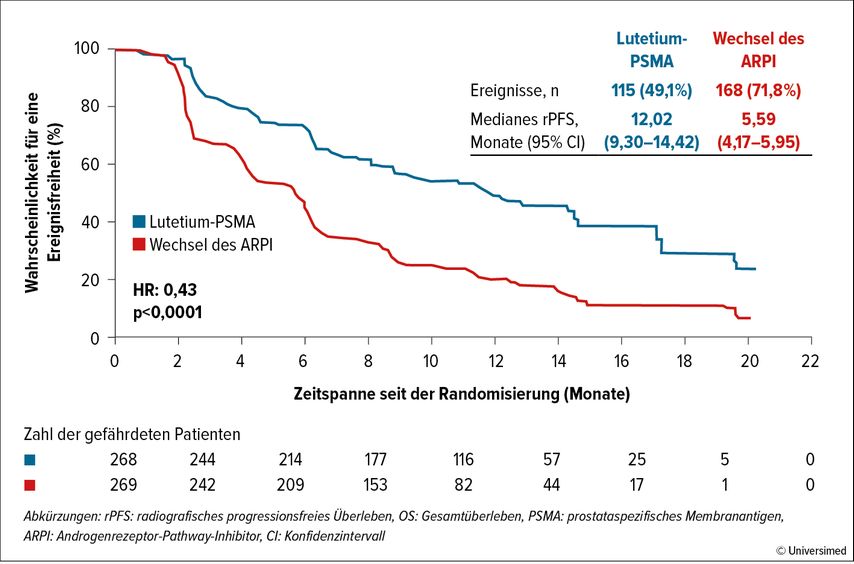
PSMA-Lu wurde als erste Radioligandentherapie (RLT) Ende 2022 für mCRPC-Patienten, die bereits mindestens einen ARPI und eine oder zwei taxanbasierte Chemotherapien (CTx) erhalten hatten, zugelassen.9,10 Nun ist PSMA-Lu auf dem Weg, in Richtung des mHSCP vorzurücken: „PSMA-Lu sollte vor Docetaxel gegeben werden, da es mit einer besseren QoL und weniger ‚adverse events‘ als Docetaxel einhergeht“, so Kramer. In der Studie PSMAfore wurde PSMA-Lu im mCRPC-Setting vs. Wechsel des ARPI (Enza bzw. Abirateron) an 468 Taxan-naiven Patienten untersucht, die unter dem ARPI eine Progression entwickelt hatten und mindestens eine PSMA-positive Läsion aufwiesen. Primärer Endpunkt war das radiografische progressionsfreie Überleben (rPFS). Bereits in der ersten Interimsanalyse mit dem medianen FU (mFU) von 7,3 Monaten wurde unter PSMA-Lu vs. ARPI eine 59%ige Reduktion des Risikos für eine radiografische Progression nachgewiesen (HR: 0,41; p<0,0001). Diese wurde in der zweiten Interimsanalyse (mFU: 15,9 Monate) bestätigt. Das mediane rPFS unter PSMA-Lu vs. ARPI betrug 12,02 vs. 5,59 Monate (HR: 0,43; p<0,0001; Abb. 1). Auch die Raten der radiografischen Response waren beeindruckend, so wurde bei 21,1% der Patienten im PSMA-Lu-Arm eine CR und bei 29,6% eine partielle Response erzielt. Ein Punkt ist, dass Patienten im Kontrollarm die Möglichkeit eines Cross-overs hatten, was von 84% genutzt wurde und zu einer Interferenz mit dem Gesamtüberleben führte.12 „Der primäre Endpunkt wurde aber erreicht, und das zählt“, merkte Kramer an.
Abb. 1: rPFS zum Zeitpunkt der zweiten Interimsanalyse zum OS; Data-Cut-off: 21. Juni 2023 (modifiziert nach Sartor O et al., ESMO 2023)12
PSMA-Lu wurde dosisadaptiert (2–4 Dosen à 7500 MBq statt max. 6 Dosen à 7400 MBq) in Kombination mit Enzalutamid vs. Enzalutamid-Monotherapie im randomisierten Design an CTx-naiven HR mCRPC-Patienten in einer Phase-II-Studie untersucht. Primärer Endpunkt war das PSA-PFS, das unter Kombination vs. Enzalutamid-Monotherapie mit 13 Monaten vs. 7,8 Monate beinahe doppelt so lang (p<0,001) war. Außerdem reduzierte PSMA-Lu + Enzalutamid das Risiko für eine PSA-Progression um 57% (HR: 0,43).13
Derzeit wird im mHSCP-Setting PSMA-Lu + Standard of Care (SOC) mit ADT + ARPI vs. SOC alleine in der offenen, randomisierten Phase-III-Studie PSMAddition an therapienaiven oder minimal vortherapierten Patienten untersucht, wobei der Einschluss bis zu 45 Tage nach Start der ADT/des ARPI ist erlaubt ist. Primärer Endpunkt ist das rPFS, sekundärer Schlüsselendpunkt das OS. Im Falle einer radiografischen Progression ist der Switch auf den Prüfarm erlaubt.14 „Weitere Substanzen werden derzeit im mHSPC-Setting untersucht, von einigen dieser Studien sind Ergebnisse bereits 2024 zu erwarten“, gab Kramer einen Ausblick.
Qualität der Patientenbetreuung
Assoc.Prof. Dr. Ganesh Palapattu, University of Michigan, berichtete über das Projekt MUSIC (Michigan Urological Surgery Improvement Collaborative) und dessen Ziel, die Qualität der PCa-Behandlung zu verbessern und deren Kosten zu senken. Dazu zählen die Reduktion Biopsie-assoziierter Komplikationen, die Verbesserung der Outcomes nach RP inklusive der funktionellen Outcomes und die Verbesserung der patientenzentrierten Entscheidungsfindung bei lokalisiertem PCa.15 Für die Dokumentation von „patient-reported outcomes“ nach RP wurde das nationalweite, Web-basierte System „MUSIC-PRO“ etabliert. Die Angaben der ersten 688 Patienten wurden ausgewertet und tragen dazu bei, Verbesserungsmöglichkeiten im Patientenmanagement zu identifizieren.16
Quelle:
Session „Prostate Cancer – From Research to Modern Care“, am 15. Dezember im Rahmen der Veranstaltung „Visiting Professorships & 9th Michael J. Marberger Meeting“ (13.–18. Dezember, Wien).
Literatur:
1 Wilt TJ et al.: Follow-up of prostatectomy versus observation for early prostate cancer. N Engl J Med 2017; 377(2): 132-42 2 Hamdy FC et al.: Fifteen-year outcomes after monitoring, surgery, or radiotherapy for prostate cancer. N Engl J Med 2023; 388(17): 1547-58 3 Cornu JN et al.: Impact of body mass index, age, prostate volume, and genetic polymorphisms on prostate-specific antigen levels in a control population. Eur Urol 2016; 70(1): 6-8 4 Bulten W et al.: Artificial intelligence for diagnosis and Gleason grading of prostate cancer: the PANDA challenge. Nature Med 2022; 28(1): 154-63 5 Cussenot O et al.: Secondary chemoprevention of localized prostate cancer by short-term androgen deprivation to select indolent tumors suitable for active surveillance: a prospective pilot phase II study. World J Urol 2014; 32(2): 545-50 6 Shore ND et al.: Enzalutamide monotherapy vs active surveillance in patients with low-risk or intermediate-risk localized prostate cancer: the ENACT randomized clinical trial. JAMA Oncol 2022; 8(8): 1128-36 7Mottet N et al.: EAU-Guidelines Prostate Cancer, Version 03.2023. https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-EANM-ESTRO-ESUR-ISUP-SIOG-Guidelines-on-Prostate-Cancer-2023_2023-06-13-141145.pdf 8 Graff JN et al.: ESMO 2023 Abstract #1771M0 9 Gratzke CJ et al.: ESMO 2023; Abstract #1772MO 10 https://www.ema.europa.eu/en/medicines/human/EPAR/pluvicto#ema-inpage-item-authorisation-details 11 Fachinformation PSMA-Lu, Stand: November 2023 12 Sartor O et al.: ESMO 2023; Abstract #LBA13 13 Emmett L et al.: ESMO 2023; Abstract #LBA84 14 Tagawa ST et al.: ESMO 2021; Abstract #T647TiP 15 https://medicine.umich.edu/dept/chop/research/music (Zugriff: 8. Jänner 2024) 16 Lucas SM et al.: Urology 2017; 107: 96-102
Das könnte Sie auch interessieren:
Korrelation von Stoffwechselmetaboliten mit bildmorphologischen, genetischen und biologischen Markern bei Verdacht auf ein Prostatakarzinom
Das Prostata-spezifische Antigen (PSA), die multiparametrische Magnetresonanztomografie (mpMRT) der Prostata und seltener noch der Prostate-Cancer-Antigen-3-Test (PCA-3) haben sich als ...
„Low-carb“, „high-protein“ oder vegane Ernährung: Risiko oder Benefit?
Wer sich heute mit Ernährung beschäftigt, kommt an den Schlagwörtern „low-carb“, keto, „high-protein“ oder vegan kaum vorbei. Fitness- und Lifestyle-Influencer und zunehmend auch ...
Netzwerk-Metaanalyse zur Integration der ARANOTE-Daten
Die Therapie des metastasierten hormonsensitiven Prostatakarzinoms befindet sich in einem dynamischen Wandel. Mit der Integration der ARANOTE-Daten in eine aktuelle Netzwerk-Metaanalyse ...