Wozu PCOS-Phänotypen?
Autorin:
Univ.-Prof. Dr. Barbara Obermayer-Pietsch
Universitätsklinik für Innere Medizin, Klinische Abteilung Endokrinologie und Diabetologie
Universitätsklinik für Frauenheilkunde & Geburtshilfe
Medizinische Universität Graz
E-Mail: Barbara.obermayer@medunigraz.at
Welche anamnestischen Fragestellungen sind bei der Diagnose von PCOS relevant? Welche Diagnosekriterien können zusätzlich herangezogen werden? Welche Frauen sind besonders von PCOS betroffen? Sind sie adipös oder schlank? PCOS-Phänotypen unterstützen bei der individuellen und korrekten Diagnosestellung und bei der Auswahl einer maßgeschneiderten Therapie.
Keypoints
-
PCOS ist sehr häufig. Ca. 20% der Frauen weltweit, aber auch Männer sind betroffen!
-
Das klinische Erscheinungsbild des PCOS ist sehr heterogen. Metabolische Komponenten sind oft unzureichend abgeklärt. Reine Basalwerte des Glukosestoffwechsels sind häufig trotz Insulinresistenz oder gestörter Glukosetoleranz falsch unauffällig.
-
Wichtige Symptome wie psychische Faktoren sollten bewusst angesprochen werden. Ein Tabuisieren seitens der Patientinnen hat eine fehlerhafte Diagnostik und Therapie zur Folge.
-
Phänotypen ergeben sich aus den aktuellen (und zukünftig neu definierten) Symptomkombinationen und geben Hinweise auf zusätzliche vor allem metabolische Risiken, die damit rechtzeitig verringert werden können.
Das PCOS ist komplex – was sind PCOS-Phänotypen?
Die Rotterdam-Kriterien des polyzystischen Ovarsyndroms (PCOS) von 20031 fassen die Symptomatik des PCOS zusammen. Sie werden in Europa für die Definition eines PCOS am häufigsten verwendet,2 auch wenn es mittlerweile weitere Ansätze für Diagnosekriterien gibt. Von den Rotterdam-Kriterien müssen von drei wichtigen Symptomkomplexen mindestens zwei auf eine Patientin zutreffen, damit die Diagnose PCOS gestellt werden kann:
Klinische (vermehrte Körperbehaarung, diffuser Ausfall der Kopfhaare, vermehrt Akne und Ähnliches) oder biochemische Hyperandrogenämie (erhöhtes Testosteron, freies Testosteron, Dehydroepiandrosteron, Androstendion und Ähnliches)
Oligo-/Amenorrhö mit eventuell unerfülltem Kinderwunsch
Sonografisch fassbare polyzystische Ovarien
Weitere häufige Symptome sind eine Insulinresistenz mit erhöhter Insulinantwort auf Nahrungszufuhr bzw. Glukosebelastung und/oder eine Hyperinsulinämie, die sich bereits in einem erhöhten „Homeostasis Model Assessment“(HOMA)-Index oder Nüchternblutzucker äußern kann, aber bei einem Drittel der Patientinnen als Basalmessung normal sein kann. Gewichtszunahme und Übergewicht bzw. Adipositas können, müssen aber kein sichtbares Zeichen dieser Stoffwechselveränderung bei PCOS sein.
Wichtig für eine adäquate Behandlung sind Hinweise, die oft erst auf Nachfrage geschildert werden, wie psychische Belastungen, Depressionen, Angststörungen oder Autoimmunerkrankungen, wie eine Immunthyreopathie oder Neigung zu diversen (auch Nahrungsmittel-)Allergien, die oft mit PCOS assoziiert sind.3 Auch ein anamnestisch gehäuftes familiäres Auftreten von PCOS gilt als wichtiger Hinweis für die Diagnose.4
Aktuell publizierte Erhebungen bei PCOS-Patientinnen zu deren Symptomen zeigen, dass die psychische Belastung von diesen Frauen als wichtigstes Symptom (83,3%) eingeschätzt wurde, gefolgt von dermatologischen Problemen (81,0%) und Zyklusthemen (76,2%). Insgesamt waren 88,1% der Frauen mit PCOS mit ihrer Behandlung unzufrieden, was dringenden Handlungsbedarf dokumentiert.5
Die Europäische Gesellschaft für Endokrinologie (ESE) hat kürzlich eine europaweite Umfrage unter medizinischen Kolleginnen und Kollegen publiziert, wonach 85% weiterhin die Rotterdam-Kriterien als PCOS-Definitionshilfe verwenden. Die Bestimmung von Testosteron wird mit 78,6% als wichtigste Laboruntersuchung angesehen. Weitere Androgenmessungen werden deutlich seltener eingesetzt, ebenso werden psychische Probleme routinemäßig nur von ca. 60% der Behandler angesprochen. Eine chronische Anovulation wird in dieser Erhebung sehr unterschiedlich nach Zykluslänge oder Anzahl der Zyklen pro Jahr oder selten auch mittels standardisierter Progesteronmessung (in 11,5%) beurteilt.6
Aktuelle Daten zum PCOS
Die Prävalenz des PCOS liegt weltweit unabhängig von der Ethnie und Geografie bei 10–20% aller Frauen, wobei ethnische Unterschiede des äußeren Erscheinungsbildes auftreten können.7 So sind höhere Body-Mass-Index(BMI)-Werte und metabolische Komplikationen bei kaukasischen Frauen in den USA und Australien und bei Afrikanerinnen beschrieben, vermehrter Hirsutismus im geografisch mediterranen Bereich, während dieser in Ostasien (auch bei niedrigeren BMI-Werten) nicht so deutlich ausgeprägt ist.8
Interessanterweise gibt es mittlerweile Dutzende Publikationen zu weiblichen Primatinnen, die bei PCOS eine ganz ähnliche Phänotyp-Verteilung und erhöhte Androgene aufweisen,9 was auf potenzielle evolutionsbiologische Vorteile schließen lässt. Hier sei auch auf mögliche Vorteile in der prähistorischen Entwicklung hingewiesen, unter anderem mit selteneren Menstruationsblutungen (geringerem Eisenverlust), weniger (und schonenderen) Schwangerschaften bei gleichzeitig höherer Überlebenschance für den Nachwuchs oder vermehrter Behaarung in Kälteperioden. Aber auch eine verbesserte Energiespeicherung über die Insulinresistenz und insgesamt „energische“ und „initiative“ PCOS-Frauen seien hier erwähnt.
Eine häufige Fehlannahme ist, dass PCOS-Frauen generell adipös sind. Das trifft in Europa auf maximal 50% der Betroffenen zu, wobei in den USA und Australien aufgrund anderer Ernährungsgewohnheiten deutlich häufiger höhere BMI-Werte dokumentiert werden. Interessanterweise werden PCOS-Frauen mit Adipositas insbesondere an medizinischen Zentren und in klinischen Studien häufiger und rascher diagnostiziert als schlanke PCOS-Frauen,10 deren Symptome weniger auffällig erscheinen.
Ein PCOS wird oft schon während der Pubertät symptomatisch. Die Zyklusdaten sollten allerdings in den ersten Jahren nach der Menarche mit Vorsicht interpretiert werden, da sehr viele junge Frauen einige Zeit lang unregelmäßige Zyklen haben können. In der reproduktiven Phase stehen dabei besonders Fragen der Fertilität, kosmetische Symptome oder erhöhtes Risiko für Gestationsdiabetes (GDM) oder Präeklampsie11 im Vordergrund. Ein postmenopausal weiterhin bestehendes PCOS geht mit einem erhöhten Karzinom- und kardiovaskulären Risiko, einem 4–6-fach erhöhten Diabetes-Typ-2-Risiko und dem typischen „Damenbart“ älterer Frauen einher,12 wobei die Hyperandrogenämie weiterbestehen kann, oft aber nicht untersucht oder therapiert wird.
Von besonderer Bedeutung ist die Verschränkung von hormonellen und metabolischen Stoffwechselwegen aufgrund der Tatsache, dass erhöhtes Insulin die Androgenfreisetzung in Ovar und Nebenniere stimuliert, einerseits
-
direkt über Cytochrom-p450-Enzyme oder
-
indirekt unter anderem über das luteinisierende Hormon (LH) und den „insulin-like growth factor 1“ (IGF-1).
Dies führt bei Hyperinsulinämie zu einer Dauerstimulation der Androgenproduktion und zu entsprechenden klinischen, aber auch metabolischen Symptomen.13 Vor dem Hintergrund, dass Insulin und der Wachstumsfaktor IGF-1 eng assoziiert sind, wurde kürzlich bei PCOS eine Stimulation des Follikelwachstums durch IGF-1 in den Ovarien14 beschrieben. Eine weitere enge Assoziation mit dem bei PCOS erhöhten Krebsrisiko ist ebenfalls evident.
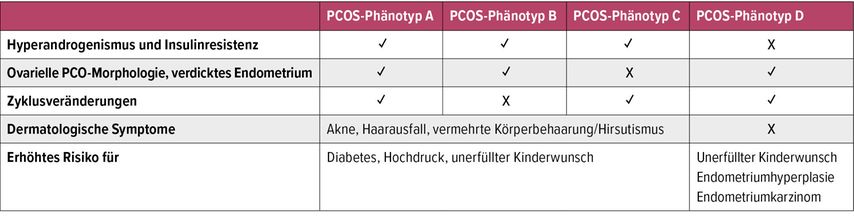
Die bisherigen PCOS-Phänotypen A, B, C und D
Als PCOS-Phänotypen ergeben sich Kombinationen aus den eingangs erwähnten Diagnosekriterien mit Phänotyp A, B, C und D, die teils praktische Konsequenzen haben können (Tab. 1). Zu den Diagnosekriterien zählen Zyklusveränderungen (ZTA), Hyperandrogenismus (HA) und polyzystische Ovarialmorphologie (PCOM). Die Häufigkeit der einzelnen Phänotypen ist dabei sehr unterschiedlich und kann, wie schon ausgeführt, ethnisch variieren:
-
Phänotyp A (alle 3 Kriterien) 20–45%
-
Phänotyp B (ZTA + HA) <10%
-
Phänotyp C (HA + PCOM) 15–30%
-
Phänotyp D (ZTA + PCOM) 15–40%
Tab. 1: Definition der PCOS-Phänotypen A–D und Risikoeinschätzungen (modifiziert nach Myers SH et al. 2023)13
Abb. 1: Grafische Darstellung und Häufigkeiten der PCOS-Phänotypen A–D (modifiziert nach Myers SH et al. 2023)13
Für die Praxis wichtig sind die bei PCOS-Phänotyp A, B und C klassische Hyperandrogenämie und oft ausgeprägte Insulinresistenz, die bei adipösen, aber auch bei schlanken Patientinnen auftreten kann. Hier ist die erste klinische Frage jene nach „Süßhunger“ oder „Kohlenhydrat-Craving“ (kann süß oder pikant sein), die man bereits vor Durchführung eines oralen Glukosetoleranztests (oGTT) abfragen kann.15 Interessanterweise haben Frauen mit nur einem PCOS-Kriterium (z.B. Hyperandrogenämie) ebenfalls ein höheres Risiko für Insulinresistenz.14 Es gibt also einen Zusammenhang zwischen dem metabolischen Risiko und der Hyperandrogenämie bzw. vice versa, worauf bei der Diagnostik besonders geachtet und wobei z.B. ein oGTT mit Insulinmessung durchgeführt werden sollte.
Auswirkungen der Phänotypen
Klinische Bedeutung haben die aktuellen PCOS-Phänotypen mit einer individuellen und korrekt gestellten Diagnose, um maßgeschneiderte Therapien abhängig vom Phänotyp zu ermöglichen. Dabei sind folgende Optionen in Einklang mit den Wünschen und Erwartungen der PCOS-Patientin einzusetzen:
-
Ernährungsmodifikation und Lebensstilintervention
-
Kontrazeptiva („Pille“), Clomiphen, Gonadotropine, Letrozol
-
Metformin und andere Insulinsensitizer
Die Effizienz der pharmakologischen Therapie kann in Relation zum Phänotyp unterschiedlich sein, zudem sollten unnötige Nebenwirkungen vermieden werden.14
Neue Aspekte, neue Phänotypen
Es gibt weltweit neue Erkenntnisse, die unser Wissen um die PCOS-Phänotypen weiter verfeinern und aktuell intensiv beforscht werden.
Neue Steroidmessungen
Zu den neuen Steroidmessungen zählt die Messung neuer Biomarker, wie die 11-oxygenierten Androgene, die einen Großteil des Steroidpools ausmachen, unter anderem aus der Nebenniere stammen und bisher kaum erfasst wurden. Sie tragen mit minimaler Überlappung zu drei spezifischen Steroidphänotypen bei:16
-
Phänotyp 1 – gonadale Androgene (Testosteron, Dihydrotestosteron) mit Hirsutismus und Alopezie, als „Gonadal-derived androgen excess“(GAE)-Cluster bezeichnet, anteilig 21,5% der PCOS-Frauen
-
Phänotyp 2 – adrenale Androgene („11-oxygenated androgens“) mit Insulinresistenz und erhöhter Glukosetoleranzstörung bzw. erhöhtem Diabetes-Typ-2-Risiko, als „Adrenal-derived androgen excess“(AAE)-Cluster bezeichnet, mit 21,7% Häufigkeit und
-
Phänotyp 3 – mit milder Hyperandrogenämie und milden klinischen Symptomen, als „Mild androgen excess“ (MAE)-Cluster bezeichnet, bei 56,8% der PCOS-Frauen
Nach der Vorstellung der aktuellen Ergebnisse im Rahmen des ENDO Society Boston 2024 wird es demnächst eine große Publikation dazu geben.16
Neue Genetik-Daten
Ein internationales PCOS-Genetik-Konsortium mit n=11653 PCOS-Patientinnen und n=423614 Kontrollen aus über 100 Forschungsinstitutionen inklusive der UK-Biobank hat aktuell viele genomweit signifikante Genorte für PCOS identifiziert. Die Publikation wurde in Nature Genetics 2025 akzeptiert, zum Zeitpunkt dieser Zusammenfassung jedoch noch nicht gedruckt. Daher sind Informationen dazu über den PrePrint Server erhältlich.17,29 Hauptgene sind mit einer PCOS-Ausprägung assoziiert. Im Polygenic Risk Score (PRS) befinden sich viele dieser hormonell wichtigen Gene, wie etwa die Genloci für Luteinisierendes-Hormon(LH)-, für Follikelstimulierendes-Hormon(FSH)- oder sogar für die Anti-Müller-Hormon(AMH)-Regulation, aber auch zahlreiche Insulin-assoziierte Genorte, allen voran DENND1A oder THADA, die bereits in anderem Zusammenhang als essenziell für die Insulin- bzw. mögliche Fehlregulationen bekannt sind. Es bestätigt sich hier eine wechselseitige Assoziation, die aber, wie bereits ausgeführt, evolutionsbiologisch durchaus wichtig für eine rasche und effiziente Energiespeicherung in Zeiten geringeren Nahrungsangebotes und anderer evolutionsbedingter Umweltanpassungen gewesen sein könnte.
PCOS bei Männern
Interessanterweise sind diese genetischen Untersuchungen sowohl für PCOS-Frauen als auch für Männer durchgeführt worden. Dabei fanden sich für den beschriebenen PRS ganz ähnliche Risiken und Wahrscheinlichkeiten bei Männern wie bei PCOS-Frauen. Dies war hochsignifikant für BMI, Adipositas, Typ-2-Diabetes-Risiko, koronare Herzkrankheit, aber auch unerfüllten Kinderwunsch, Hormon- und Stoffwechselwerte oder Depressionen.
Praxistipp
Etwa die Hälfte der PCOS-Patientinnen ist schlank. Oft besteht trotzdem eine Insulinresistenz oder eine Hyperinsulinämie, was relevant für eine adäquate Behandlung sein kann. Eine wichtige Anamnesefrage ist daher: „Kennen Sie Heißhunger auf Süßes (oder Pikantes)?“Zum Thema Männer und PCOS gibt es seit etwa 15 Jahren schon wichtige klinische Beobachtungen, wonach männliche erstgradige Verwandte von PCOS-Frauen nicht nur signifikant höhere Androgenspiegel, sondern auch mehr Haarausfall am Kopf und mehr metabolische Veränderungen haben.18 Das kardiovaskuläre Risiko war bei Vätern von PCOS-Frauen um etwa das 12-Fache erhöht, kaum jedoch bei deren Müttern. Die Ovarien aus dem historischen Begriff PCOS dürften also weniger für die Namensgebung bedeutungsvoll sein, was in der brandneuen Genetikstudie auch zum Ausdruck kommt.
Zusammenfassung und Ausblick
Stoffwechsel, Reproduktion und das PCOS hängen eng zusammen. Die aktuellen Phänotypen A, B, C und D sind wichtige Kriterien zur individuellen Diagnostik und Therapie. Eine ovarielle PCO-Morphologie (PCOM) allein macht allerdings noch kein PCOS aus. Der Zusammenhang von Hyperandrogenämie und metabolischem Risiko ist aber besonders wichtig. Es gibt neue PCOS-Phänotypen am Horizont, die aktuell intensiv beforscht werden, einerseits in Bezug auf neue, spezifische Steroidmessungen und andererseits auf genetische Daten mit sogenannten Polygenic Risk Scores (PRS).
Diese Forschungen haben gezeigt, dass auch Männer von PCOS betroffen sein können, mit erheblichen Risiken für metabolische und kardiovaskuläre Folgeerkrankungen. Deren PCOS-Phänotypen (wie individuelle Glatzenbildung und Gewichtszunahme), spezielle metabolische und hormonelle Symptome sowie Risiken werden daher in einer geplanten EU-COST-Action zu PCOS mit 20 beteiligten Ländern zukünftig weiter erforscht.
Literatur:
1 Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group: Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Fertil Steril 2004; 81(1): 19-25 2 Livadas S et al.: European survey of diagnosis and management of the polycystic ovary syndrome: full report on the ESE PCOS Special Interest Group’s 2023 Questionnaire. Eur J Endocrinol 2024; 191(2): 134-43 3 Gaberšček S et al.: Mechanisms in endocrinology: thyroid and polycystic ovary syndrome. Eur J Endocrinol 2015; 172(1): R9-21 4 Steiner-Victorin E, Deng Q: Epigenetic inheritance of polycystic ovary syndrome - challenges and opportunities for treatment. Nat Rev Endocrinol 2021; 17(9): 521-33 5 Elghobashy M et al.: Concerns and expectations in women with polycystic ovary syndrome vary across age and ethnicity: findings from PCOS Pearls Study. Front Endocrinol (Lausanne) 2023; 14: 1175548 6 Livadas S et al.: European survey of diagnosis and management of the polycystic ovary syndrome: full report on the ESE PCOS Special Interest Group’s 2023 Questionnaire. Eur J Endocrinol 2024; 191(2): 134-43 7 March WA et al.: The prevalence of polycystic ovary syndrome in a community sample assessed under contrasting diagnostic criteria. Hum Reprod 2010; 25(2): 544-51 8 www.nih.giv/women 9 Abbott DH et al.: Clustering of PCOS-like traits in naturally hyperandrogenic female rhesus monkeys. Hum Reprod 2017; 32(4): 923-36 10 Lizneva D et al.: Phenotypes and body mass in women with polycystic ovary syndrome identified in referral versus unselected populations: systematic review and meta-analysis. Fertil Streil 2016; 106(6): 1510-20 11 Joshi A et al.: PCOS and the risk of pre-eclampsia. Reprod Biomed Online 2022; 45(5): 961-9 12 Pinola P et al.: Normo- and hyperandrogenic women with polycystic ovary syndrome exhibit an adverse metabolic profile through life. Fertil Steril 2017; 107(3): 788-95 13 Misra S et al.: Comparative study of insulin sensitivity and resistance and their correlation with androgens in lean and obese women with polycystic ovary syndrome. Reprod Sci 2024; 31(3): 754-63 14 Myers SH et al.: Questioning PCOS phenotypes for reclassification and tailored therapy. Trends Endocrinol Metab 2023; 34(11): 694-703 15 Wen X et al.: Metabolic characteristics of different phenotypes in reproductive-aged women with polycystic ovary syndrome. Front Endocrinol (Lausanne) 2024; 15: 1370578 16 Melson E et al.: ENDO Society 2024; Abstract, 1.–4. Juni 2024, Boston 17 https://www.medrxiv.org/content/10.1101/2024.04.18.24306020v1 18 Taylor MC et al.: Evidence for increased cardiovascular events in the fathers but not mothers of women with polycystic ovary syndrome. Hum Reprod 2011; 26(8): 2226-31
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Notfall Diabetische Ketoazidose: Leitliniengerechtes Handeln kann Leben retten
Akute Stoffwechselentgleisungen können lebensbedrohlich sein und erfordern eine rasche und leitliniengerechte Diagnostik und Therapie. Pathogenese, Klinik, typische Befunde und die ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...