Differenzierte gynäkologische Sonografie: Adenomyose
Autorinnen:
Dr. med. Annkathrin Butenschön
PD Dr. med. Gwendolin Manegold-Brauer
Abteilung für gynäkologische Sonographie und Pränataldiagnostik, Frauenklinik, Universitätsspital Basel
E-Mail: annkathrin.butenschoen@usb.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Adenomyose ist eine häufige Ursache von Dysmenorrhoe und Hypermenorrhoe. Sie wird histologisch anhand des Vorliegens von endometrialen Drüsen- und Stromazellen im Myometrium gestellt. Die Prävalenz der Erkrankung ist unbekannt, da nur ein kleiner Anteil an Patientinnen eine histologische Diagnose erhält. Mit Hilfe der gynäkologischen Sonografie kann die Adenomyose heute anhand typischer Merkmale erkannt werden.
Keypoints
-
Das Myometrium wird bei jedem gynäkologischen Ultraschall detailliert beurteilt.
-
Zu den typischen Zeichen der Adenomyose gehören: ein vergrösserter/kugeliger Uterus, eine asymmetrische Wandverbreiterung, intramurale Zysten, hyperechogene Inseln, fächerartige Schallschatten, subendometriale Linien und Knospen, eine irreguläre oder unterbrochene Junktionalzone und eine transläsionale Vaskularität.
-
Die Adenomyose ist häufig mit Komorbiditäten (z.B. Endometriose, Uterus myomatosus) assoziiert.
-
Bei sonografischen Zeichen der Adenomyose sollten die einzelnen Herde im Hinblick auf die Ausdehnung charakterisiert werden.
-
Die Therapie der Adenomyose richtet sich nach den klinischen Beschwerden und der Frage des Kinderwunsches.
Bei der Adenomyose handelt es sich um eine symptom- und facettenreiche gutartige Erkrankung des Myometriums. Mögliche Symptome sind Blutungsstörungen, Dysmenorrhoe und chronische Unterbauchschmerzen.1 Auch vermutet man einen negativen Effekt auf die Fertilität. Eine hohe Inzidenz bestehender Komorbiditäten wie Myome und Endometriose macht es jedoch schwierig, der Adenomyose ein bestimmtes pathognomonisches Symptom zuzuordnen. Viele Aspekte sind wissenschaftlich wenig untersucht. Die endometrialen Drüsen- und Stromazellen im Myometrium führen häufig zu einer Hypertrophie des umgebenden Myometriums. Sowohl eine fokale als auch eine diffuse Ausbreitung im Uterus ist möglich.
Die Pathogenese der Erkrankung ist nicht endgültig geklärt. Einerseits wird eine Einstülpung des basalen Endometriums in das Myometrium durch die fehlende oder durch Trauma veränderte endomyometriale Grenzschicht (Junktionalzone) diskutiert. Offenbar scheinen aber andererseits auch pluripotente embryonale Stammzellen der Müller-Gänge in der Lage zu sein, ektopes endometriales Gewebe de novo im Myometrium zu bilden.2 Als Risikofaktoren werden Multiparität und vorangegangene Operation am Uterus diskutiert.
Im klinischen Alltag stellt die transvaginale Sonografie die Bildgebung der ersten Wahl zur Diagnostik der Adenomyose dar. Sie ist allseits verfügbar, kostengünstig, nicht invasiv und ohne Nebenwirkungen. Eine ausführliche Anamnese sowie eine Spekulum- und bimanuelle Tastuntersuchung sollten zuvor durchgeführt werden, um weitere mögliche Ursachen der Symptome auszuschliessen bzw. Komorbiditäten aufzudecken.
Die Therapie der Adenomyose richtet sich nach den klinischen Beschwerden und der Frage des Kinderwunsches. Zu den therapeutischen Optionen zählen u.a. levonorgestrelhaltige Spiralen, kombinierte orale Kontrazeptiva, reine Gestagene oder GnRH-Analoga. Chirurgisch steht die Hysterektomie im Vordergrund. Die sogenannte konservative Chirurgie, also die Exzision fokaler Adenomyose, hat ihren Stellenwert bei Kinderwunsch.3,4
Sonografische Zeichen der Adenomyose
Die sonografische Beurteilung des Myometriums sollte nach einem internationalen Konsensus-Statement anhand definierter Kriterien der MUSA(Morphological Uterus Sonographic Assessment)-Gruppe erfolgen.5
Eine Auswahl der wichtigsten Merkmale:
-
vergrösserter/kugelförmiger Uterus
-
asymmetrische Wandverbreiterung
-
intramurale Zysten
-
echogene subendometriale Linien und Knospen
-
hyperechogene Inseln
-
fächerartige Schallschatten
-
irreguläre oder unterbrochene Junktionalzone
transläsionale Vaskularität
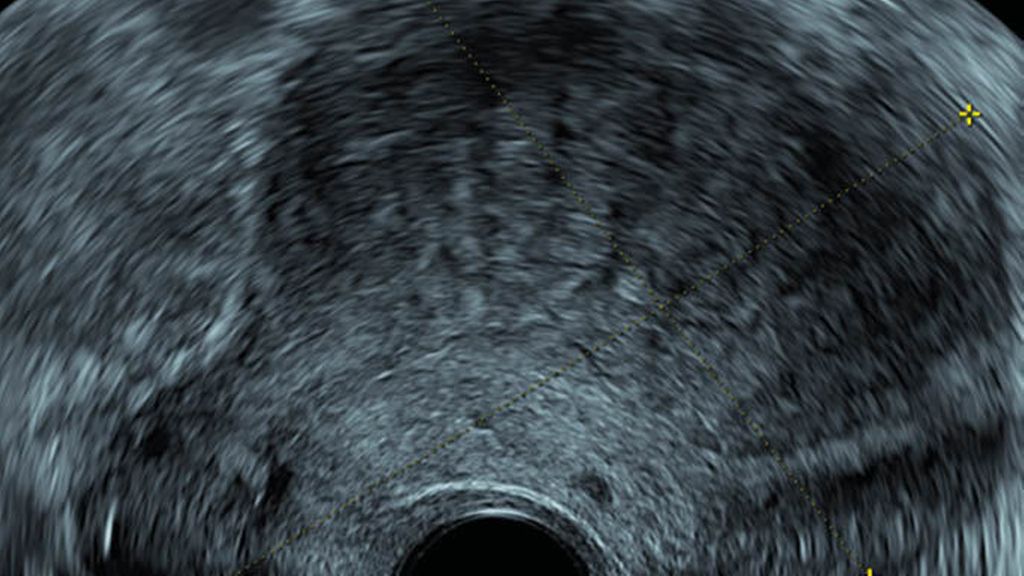
Eine Veränderung, die für das Vorliegen einer Adenomyose spricht, ist ein global vergrösserter, kugeliger Uterus (Abb. 1). Auch eine asymmetrische Wanderverdickung des Myometriums kann auf das Erkrankungsbild hinweisen (Abb. 2). Diese genannten Kriterien zeigen sich in der medianen Sagittalebene, also der Standardebene des gynäkologischen Ultraschalls. Der gesamte Uterus sollte nun sowohl sagittal von links nach rechts als auch transversal vom Fundus bis zur Zervix systematisch untersucht werden. Bei dieser dynamischen Untersuchung kennzeichnen fächerartige Schallschatten eine Adenomyose (Abb. 3). Diese Schallschatten sind ein indirektes Zeichen, sie entstehen sekundär durch morphologische Veränderungen des Myometriums z.B. durch hyperechogene Inseln (Abb. 4) oder intramurale Zysten (Abb. 5,7).
Die innerste Schicht des Myometriums, welche direkt an das Endometrium grenzt, wird als endometriale/myometriale Grenzschicht oder Junktionalzone (JZ) bezeichnet. Bei einer Adenomyose kann diese JZ irregulär oder unterbrochen sein und es können hyperechogene subendometriale Knospen und Linien visualisiert werden. Die 2D-Sonografie ist dafür häufig wegweisend (Abb. 5). Die 3D-Sonografie ist hier allerdings ein ergänzendes hilfreiches Tool zur Beurteilung (Abb. 6 und 7), da die Darstellung der Koronarebene eine vollständigere Beurteilung ermöglicht.
Abb. 5: Unterbrochene Junktionalzone im Bereich der Vorderwand (kurze Pfeile), hyperechogene Inseln (langer Pfeil), intramurale Zysten (Kreis)
Abb. 7: Unterbrochene Junktionalzone fundal (kurze Pfeile), subendometriale Knospen (lange Pfeile), intramurale Zyste (Kreis)
Läsionen im Bereich des Myometriums werden unterschieden in «gut abgrenzbar» und «schlecht abgrenzbar». Myome sind typischerweise eher gut abgrenzbar, Adenomyoseherde im Gegensatz dazu meist schlecht abgrenzbar. Bei schlecht abgrenzbaren Adenomyoseherden weiss man typischerweise oft nicht, wo man einen Messknopf zur Grössenbestimmung ansetzen soll.
Nach der systematischen Untersuchung des Myometriums im B-Bild folgt die Dopplersonografie. Der Power-Doppler ist dem Color-Doppler bezüglich der Darstellung von kleinen Gefässen mit niedrigen Flussgeschwindigkeiten überlegen. Die Dopplersonografie liefert zur Unterscheidung wichtige Zusatzinformationen. Während Myome eine zirkuläre randständige Durchblutung aufweisen (Abb. 8), sind Adenomyoseherde durch eine transläsionale Vaskularität charakterisiert – in anderen Worten also durch eine Durchblutung, die senkrecht zum Endometrium durch die gesamte Läsion zieht (Abb. 9).
Es wird allgemein angenommen, dass die Diagnose einer Adenomyose umso wahrscheinlicher ist, je mehr der oben genannten sonografischen Zeichen vorliegen. Zu erwähnen ist jedoch, dass die oben genannten Kriterien nicht pathognomonisch für die Adenomyose sind. Beispielsweise ist eine unterbrochene JZ auch bei Myomen vom Typ FIGO 1–3 und bei einer Myometriuminvasion im Rahmen eines Endometriumkarzinoms darstellbar. Auch findet man teilweise fächerartige Schallschatten bei Myomen.6
Befunddokumentation
Liegt der Verdacht auf eine Adenomyose vor, sollten die Befunde wie in Tabelle 1 aufgeführt beschrieben werden, um die Ausdehnung möglichst genau zu charakterisieren. Bei mehreren Läsionen kann jede einzeln beschrieben werden.7
Literatur:
1 Gordts S et al.: Symptoms and classification of uterine adenomyosis, including the place of hysteroscopy in diagnosis. Fertil Steril 2018; 109(3): 380-8 2 Garcia-Solares J et al. : Pathogenesis of uterine adenomyosis: invagination or metaplasia? Fertil Steril 2018; 109: 371-9 3 Vannuccini S et al.: Role of medical therapy in the management of uterine adenomyosis. Fertil Steril 2018; 109(3): 398-405 4 Younes G, Tulandi T: Conservative surgery for adenomyosis and results: a systematic review. J Minim Invasive Gynecol 2018; 25(2): 265-76 5 Van den Bosch T et al.: Terms, definitions and measurements to describe sonographic features of myometrium and uterine masses: a consensus optinion from the Morphologic Uterus Sonographic Assessment (MUSA) group. Ultrasound Obstet Gynecol 2015; 46: 284-98 6 Van den Bosch T, Van Schoubroeck D: Ultrasound diagnosis of endometriosis and adenomyosis: State of the art. Best Pract Res Clin Obstet Gynaecol 2018; 51: 16-24 7 Van den Bosch T et al.: Sonographic classification and reporting system for diagnosing adenomyosis. Ultrasound Obstet Gynecol 2019; 53: 576-82
Das könnte Sie auch interessieren:
Der frühe Ultraschall hat auch in Zeiten des NIPT nicht ausgedient
Beim Ersttrimesterscreening geht es bei Weitem nicht nur um Nackenfaltenmessung und die Wahrscheinlichkeitsberechnung für Trisomien. Auch rund 50% der schweren fetalen Fehlbildungen ...
Die Kunst ärztlicher Kommunikation bei Breaking Bad News
Worte haben entscheidende Wirkungen. In Gesprächen mit Patient:innen und Angehörigen gibt es meist eine hohe Erwartungshaltung gegenüber der Ärztin, dem Arzt. Vor allem die Übermittlung ...
Was brauchen Mädchen für eine selbstbewusste Sexualität?
Die Entwicklung der eigenen Sexualität ist zentraler Bestandteil des Erwachsenwerdens. Manchen Mädchen fällt es jedoch nicht leicht, ihre Sexualität selbstbewusst und selbstbestimmt zu ...












