Moderne Behandlung supraventrikulärer Tachykardien
Oberarzt, Rhythmologie und Kardiologie<br>Klinik für Kardiologie<br>Universitätsspital Zürich<br>Rämistrasse 100<br>8091 Zürich<br>E-Mail: daniel.hofer@usz.ch
Abteilung für Rhythmologie und Kardiologie<br>Klinik für Kardiologie<br>Universitätsspital Zürich<br>
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Supraventrikuläre Tachykardien sind in der täglichen Praxis ein häufiges Krankheitsbild mit breiter Differenzialdiagnose und vielen Therapiemöglichkeiten. Ein strukturierter Ansatz in der Beurteilung kann sowohl die notfallmässige Diagnostik als auch die anschliessende Therapiewahl massgeblich vereinfachen. Mit der modernen kathetergestützten elektrophysiologischen Untersuchung und Ablation steht heutzutage eine komplikationsarme und sehr erfolgversprechende Möglichkeit für die langfristige Behandlung zur Verfügung, welche der medikamentösen Langzeittherapie meistens vorzuziehen ist.
Keypoints
-
Supraventrikuläre Tachykardien sind eine häufige Erkrankung im internistischen Alltag.
-
Karotissinusmassage, modifiziertes Valsalva-Manöver und Adenosin eignen sich gut zur Akuttherapie und Differenzialdiagnostik.
-
Als medikamentöse Rezidivprophylaxe stehen primär Betablocker zur Verfügung.
-
Die elektrophysiologische Untersuchung mit Katheterablation stellt für alle supraventrikulären Tachykardien eine Klasse-IA-Indikation bezüglich Langzeittherapie dar.
Unter physiologischen Bedingungen nimmt die elektrische kardiale Erregung ihren Ursprung im rechtsatrial gelegenen Sinusknoten im Bereich des Eintritts der Vena cava superior in den rechten Vorhof. Nach der Impulsbildung im Sinusknoten gelangt die elektrische Aktivierung über die Vorhöfe auf Klappenhöhe zum AV-Knoten, wo der Impuls verzögert und anschliessend über das His’sche Bündel auf den linken und rechten Tawara-Schenkel und von dort aus über Purkinje-Fasern ins ventrikuläre Myokard weitergeleitet wird (Abb. 1). Anhand der Erregungsausbreitungsrichtung in den Vorhöfen (von superior nach inferior sowie von rechts nach links gerichtet) ergibt sich die typische elektrokardiografische Morphologie der P-Welle im Sinusrhythmus: regelmässige P-Wellen mit positiver Deflektion in den inferioren EKG-Ableitungen (positive P-Wellen in II/III/aVF) sowie positiv in den nach links orientierten Ableitungen (positiv in I, dominant negativ in V1) (Abb. 2a, 3a).
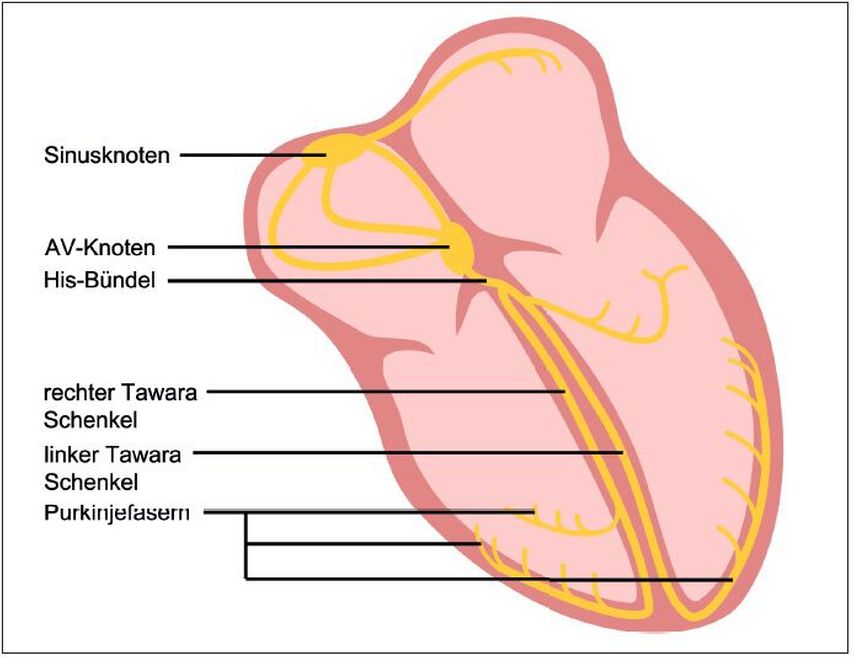
Abb. 1: Unter physiologischen Bedingungen entspringt die elektrische Erregung dem rechtsatrial gelegenen Sinusknoten mit nachfolgender Ausbreitung über das Bachmann-Bündel nach links und über das rechte Atrium zum knapp septal gelegenen AV-Knoten. Nach Verzögerung im AV-Knoten erfolgt die Weiterleitung über das His-Bündel, den linken und rechten Tawara-Schenkel und schliesslich die Purkinje-Fasern in das ventrikuläre Myokard
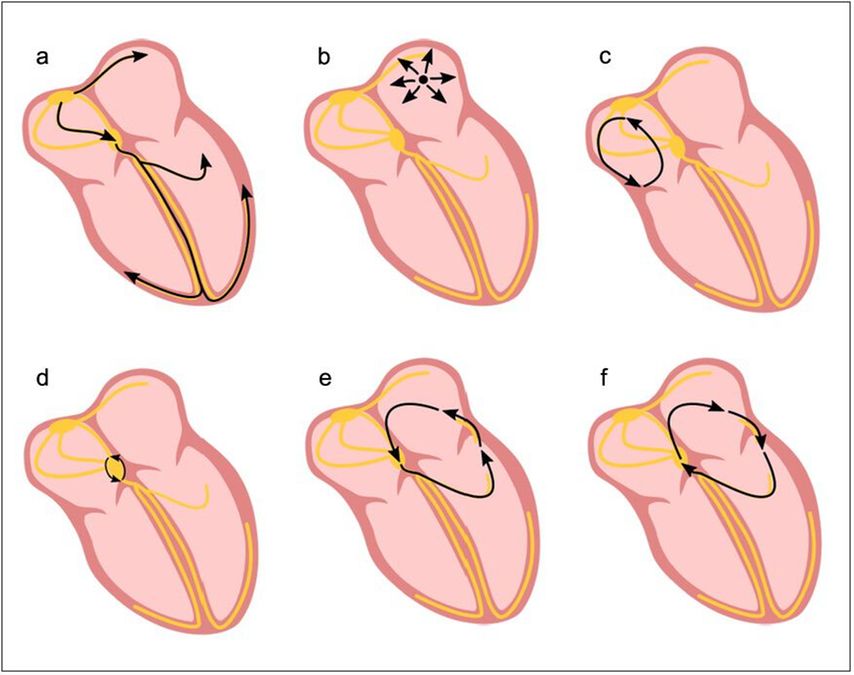
Abb. 2: Übersicht über verschiedene Mechanismen supraventrikulärer Tachykardien: a) normaler Sinusrhythmus; b) fokale atriale Tachykardie mit Ursprung im linken Atrium; c) typisches Vorhofflattern mit Erregungsverlauf entgegen dem Uhrzeigersinn entlang der freien Wand nach inferior, über den kavotrikuspidalen Isthmus und zurück nach superior entlang des Septums; d) AV-Knoten-Reentry-Tachykardie (AVNRT) mit kreisender Erregung zwischen zwei Leitungsbahnen im AV-Knoten; e) orthodrome atrioventrikuläre Tachykardie (AVRT); f) antidrome AVRT
Das Kollektiv der supraventrikulären Tachykardien (SVT) umfasst Herzrhythmusstörungen mit Ursprung oberhalb des His’schen Bündels und mit Herzfrequenzen >100Schläge/min in Ruhe.1 Paradoxerweise wird dabei üblicherweise das Vorhofflimmern (das seinen Ursprung ebenfalls im Vorhof hat) als separate Entität behandelt und entsprechend in dieser Zusammenstellung auch nicht weiter beleuchtet. Andererseits gelten atrioventrikuläre Tachykardien (AVRT) trotz ventrikulärer Beteiligung als Teil des «Ursprungs» der Rhythmusstörung als supraventrikuläre Tachykardien und werden nachfolgend ebenfalls diskutiert. Mit einer geschätzten Prävalenz von 0,2% und Inzidenz von 35/10000 Personenjahre in der Allgemeinbevölkerung handelt es sich bei den SVT um eine häufige Erkrankung im internistischen und kardiologischen Alltag.2 Weibliches Geschlecht, Alter, Herzinsuffizienz, Lungenerkrankungen und Diabetes sind mit einem erhöhten Risiko für SVT assoziiert.3 Die Symptomatik bei SVT ist breit und reicht von einfachen Palpitationen über Schwindel bis zu Synkopen. Bei Letzteren sind allerdings nebst der Tachykardie häufig auch begleitende Faktoren wie eine vasomotorische Komponente oder eine strukturelle Herzerkrankung mitursächlich.4, 5
Klassifikation
SVT können gemäss Ursprung und Mechanismus in atriale, AV-Knoten-Tachykardien und atrioventrikuläre Tachykardien unterteilt werden. Die erste Gruppe umfasst sowohl adäquate wie auch inadäquate Sinustachykardien, fokale und multifokale atriale Tachykardien sowie atriale Makro-Reentry-Tachykardien wie das typische bzw. atypische Vorhofflattern. Die AV-Knoten-Reentry-Tachykardie (AVNRT) ist Hauptbestandteil der zweiten Gruppe. Die Subklasse der atrioventrikulären Tachykardien (AVRT) umfasst schliesslich als dritte Gruppe Tachykardien mit Beteiligung einer akzessorischen atrioventrikulären Bahn. Die AVNRT ist mit insgesamt 51% im klinischen Alltag am häufigsten vertreten, wobei sich eine klare Geschlechtsspezifität mit einer doppelt so hohen Häufigkeit im weiblichen als im männlichen Kollektiv zeigt.6 Mit 38% ist die AVRT die zweithäufigste Gruppe, wobei sie häufiger beim männlichen Geschlecht auftritt. Atriale Tachykardien und Sinustachykardien bilden mit lediglich 11% die kleinste Fraktion. Die Prävalenz des Vorhofflatterns ist aufgrund der häufigen Koexistenz mit Vorhofflimmern insgesamt schwierig zu beziffern; es findet sich eine Häufung des Vorhofflatterns bei kardial vorerkrankten Patienten, v.a. bei koronarer Herzkrankheit und bei Herzinsuffizienz.6, 7
Sinustachykardie
Bei der Sinustachykardie wird primär zwischen einer adäquaten und einer inadäquaten Genese unterschieden. Kardiale Erkrankungen wie beispielsweise eine Herzinsuffizienz, aber auch extrakardiale Faktoren wie Schmerzen, Anämie, Hypovolämie, Infekt, Lungenembolie, psychische Erkrankungen oder Hyperthyreose führen zu einer physiologisch adäquat begründeten Tachykardie, welche primär durch das Erkennen und die Korrektur des auslösenden Problems therapiert wird. Autonome Dysregulation und Hyperaktivität des Sinusknotens sind Beispiele für bis anhin unzureichend erforschte inadäquate Sinustachykardien, wobei die inadäquaten Sinustachykardien aber einen benignen Verlauf zeigen.8
Fokale atriale Tachykardie
Vermehrte automatische Aktivität oder Mikro-Reentry aus den Vorhöfen können zu atrialen Tachykardien führen: Bei fokalem Ursprung mit nachfolgend zentrifugaler Ausbreitung sind dabei die P-Wellen monomorph und die atriale Zykluslänge stabil, was als Kriterium der Unterscheidung zum Vorhofflimmern dienen kann. Im Vergleich zu den nachfolgend genannten Makro-Reentry-Tachykardien findet sich im EKG üblicherweise eine isoelektrische Strecke zwischen den atrialen Depolarisationen (Abb. 2b, 3b). Die atriale Tachykardie kann ihren Ursprung überall in den Vorhöfen haben, wobei die Crista terminalis im rechten Vorhof, der atrioventrikuläre Klappenanulus sowie die Mündungen der Venae cavae klassische Prädilektionsstellen darstellen. Die jeweilige elektrokardiografische Morphologie der P-Wellen gibt Aufschluss über den Ursprung der Tachykardie: Negativität in I und aVL legt einen linksatrialen und Negativität in V1 einen rechtsatrialen Fokus nahe; eine isoelektrische bis positive Konfiguration in V1 spricht für die Nähe zum interatrialen Septum. Negative P-Wellen in den inferioren Ableitungen stehen im Gegensatz zum Sinusrhythmus für einen kaudalen Ursprung (Tab. 1).7, 9
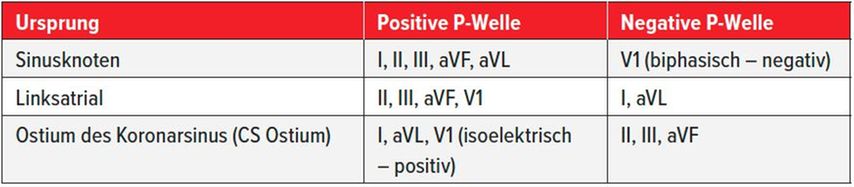
Tab. 1: Ursprung der Tachykardie aufgeschlüsselt nach P-Wellen-Vektor7, 10
Vorhofflattern
Das typische Vorhofflattern ist anatomisch und pathophysiologisch an den Isthmus zwischen der Mündung der Vena cava inferior und der Trikuspidalklappe gebunden. Die Erregung verläuft üblicherweise entgegen dem Uhrzeigersinn entlang der freien Wand nach inferior, über den kavotrikuspidalen Isthmus und zurück nach superior entlang des interatrialen Septums. Dies führt zur klassischen Präsentation mit Sägezahnmuster im EKG, wobei diese in den inferioren Ableitungen negativ und in V1 positiv ausfallen (Abb. 2c, 3c). Geht der Makro-Reentry-Kreislauf in die entgegengesetzte Richtung (aber noch immer durch den kavotrikuspidalen Isthmus), wird die Rhythmusstörung als «reverse-typical» Vorhofflattern bezeichnet. Antiarrhythmische Medikation sowie ausgeprägte Vernarbung des Vorhofs nach extensiver Radiofrequenzablation oder vorgängige operative Eingriffe können allerdings die typische Morphologie stark beeinflussen, sodass das Fehlen des typischen Sägezahnmusters insbesondere in solchen Situationen einen Isthmus-abhängigen Mechanismus nicht ausschliesst. Klinisch findet sich zudem eine häufige Koexistenz von Vorhofflattern und Vorhofflimmern. Vorhofflattern ohne Beteiligung des kavotrikuspidalen Isthmus wird als atypisches Vorhofflattern bezeichnet, welches sowohl im rechten als auch im linken Vorhof seinen Ursprung haben kann. Als Substrate hierfür dienen Narben, Fibroseareale und anatomische Strukturen wie beispielsweise Pulmonalvenenmündungen.11–13Das Risiko für thromboembolische Hirninfarkte ist bei Vorhofflattern niedriger als bei Vorhofflimmern, trotzdem wird nach Abwägen gegenüber Blutungskomplikationen eine Antikoagulation empfohlen gemäss gängiger Indikationsstellung anhand des CHA2DS2VASC-Scores.14, 15
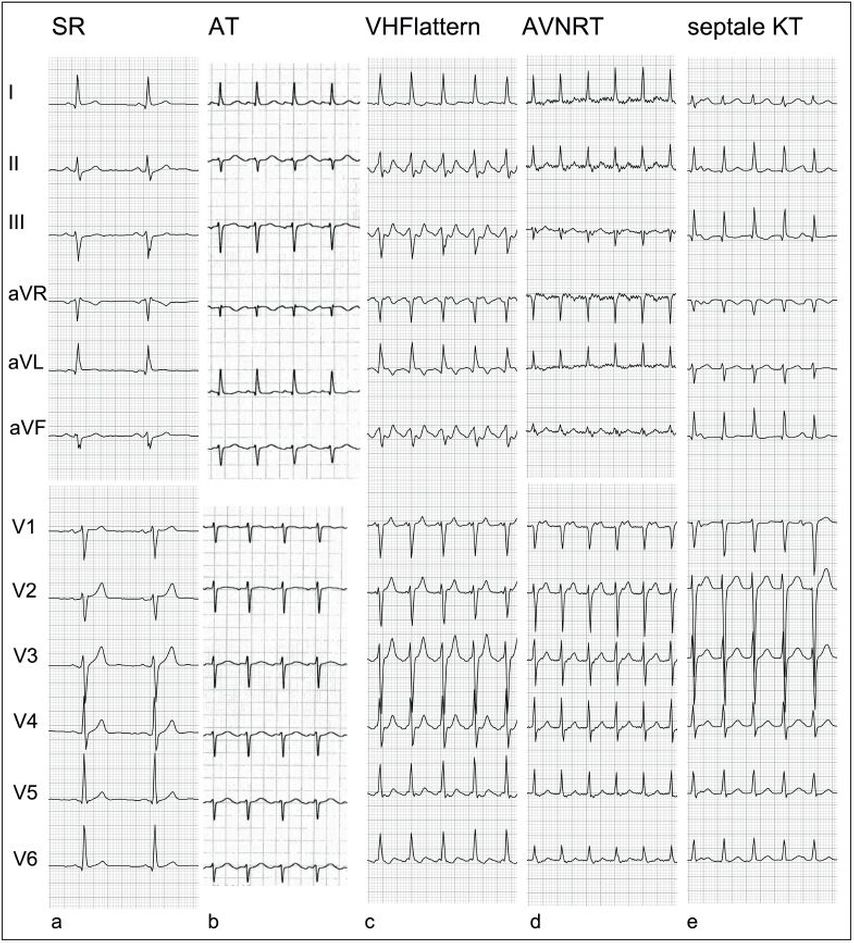
Abb. 3: Typische EKG: a) Erregungsausbreitung im Sinusrhythmus (SR). Positive P-Welle in den inferioren Ableitungen (II, III, aVF) sowie positiv in den lateralen Ableitungen (I, aVL, V5, V6); b) atriale Tachykardie (AT) als Long-RP-Tachykardie; Ursprung am Trikuspidalklappenanulus (positive P-Wellen in I, aVL und dominant negativ in V1 [= von rechtsatrial], negativ in II, III und aVF [= von inferior]); c) typisches Isthmus-abhängiges Vorhofflattern (VHFlattern); d) AV-Knoten-Reentry-Tachykardie (AVNRT) als Short-RP-Tachykardie mit RP < 90 ms; e) septale Kammertachykardie (septale KT) mit AV-Dissoziation, P-Wellen nach dem 1. und 4. QRS-Komplex
AV-Knoten-Reentry-Tachykardie (AVNRT)
Grundlage für die AVNRT ist eine duale Leitungsphysiologie des AV-Knotens mit kreisender Erregung zwischen zwei Leitungsbahnen des AV-Knotens und somit fast simultaner Erregung von Vorhof und Ventrikel. Bei der typischen AVNRT erfolgt die antegrade Erregungsausbreitung über ein langsam leitendes Bündel (sog. «slow pathway») vom Vorhof in den Ventrikel und mit retrograder Leitung über ein schnell leitendes Bündel (sog. «fast pathway») gleichzeitig wieder zurück (Abb. 2d, 3d). Bei der atypischen AVNRT verläuft die Erregung in die Gegenrichtung; alternativ können Reentry-Tachykardien auf dem Boden von mehreren «slow pathways» entstehen. Im EKG findet sich charakteristischerweise eine sehr regelmässige Schmalkomplextachykardie. Bei der typischen AVNRT liegen die retrograde P-Welle und der QRS-Komplex aufgrund der schnellen Rückleitung des «fast pathways» eng zusammen, sodass die retrograde P-Welle oft nur als kleine Deflektion gleich am Ende des QRS-Komplexes erkannt werden kann (am besten in Ableitung V1) oder komplett im QRS-Komplex verschwindet. Bei der selteneren atypischen Form führt die langsamere Rückleitung häufig zu einer besseren Identifizierung der P-Welle nach dem QRS-Komplex.16
Atrioventrikuläre Reentry-Tachykardie (AVRT)
AVRT benötigen sowohl eine Beteiligung des AV-Knotens als auch eine davon unabhängige, akzessorische Leitungsbahn zwischen den Vorhöfen und Ventrikeln. 60% der akzessorischen Bahnen liegen in der linken freien Wand im Bereich der Mitralklappe, 25% inserieren septal und nur 15% befinden sich rechtsseitig.17–19 Akzessorische Bahnen können zu verschiedenen Rhythmusstörungen führen: Es kann eine orthodrome AVRT mit antegradem Verlauf über das intrinsische Reizleitungssystem und retrograder Erregung über das akzessorische Bündel auftreten. Orthodrome Tachykardien zeichnen sich durch schmale QRS-Komplexe aus und sind mit >90% aller AVRT die häufigste Präsentation (Abb. 2e). Läuft die kreisende Erregung in die Gegenrichtung, wird dies als antidrome AVRT bezeichnet und die Tachykardie präsentiert sich entsprechend als Breitkomplextachykardie (Abb. 2f). Ist eine akzessorische Bahn mit Leitung vom Vorhof in den Ventrikel bereits im 12-Kanal-EKG erkennbar (PQ-Verkürzung, Deltawelle) und klagt der Patient über Rhythmusstörungen, liegt ein offenes Wolff-Parkinson-White(WPW)-Syndrom vor. Circa 28% aller akzessorischen Bahnen leiten aber nur vom Ventrikel in den Vorhof; dann ist das Oberflächen-EKG unauffällig und es liegt ein «concealed», also verborgenes, WPW vor.20, 21 Besteht lediglich eine im EKG erkennbare akzessorische atrioventrikuläre Bahn (PQ-Verkürzung, Deltawelle) ohne symptomatische Rhythmusstörungen wird dies als ventrikuläre Präexzitation bzw. «WPW-pattern» bezeichnet.
Abklärung und Differenzialdiagnose
Die Erstabklärung einer SVT beinhaltet nebst Anamnese und körperlicher Untersuchung ein 12-Ableitungs-EKG zur Dokumentation sowie eine laborchemische Basisdiagnostik mit Hämatologie und Chemie inkl. Bestimmung der Schilddrüsenfunktion. Eine transthorakale Echokardiografie ist obligat und liefert wertvolle Informationen bezüglich kardialer Pumpfunktion sowie struktureller Pathologien. Bei typischen Beschwerden, aber fehlender EKG-Dokumentation sind Langzeit-EKG, Anfalls-EKG-Recorder oder implantierbare Event-Recorder sinnvolle Abklärungsschritte. Bei Patienten mit pektanginösen Beschwerden während einer supraventrikulären Tachykardie und vaskulären Risikofaktoren sollte eine myokardiale Ischämietestung zum Ausschluss einer Koronarischämie evaluiert werden.7
EKG-Interpretation
Eine strukturierte Interpretation kann die korrekte Differenzierung von Schmalkomplextachykardien vereinfachen (Abb. 4). Bei dokumentierter Tachykardie sollte als Erstes die Regelmässigkeit beurteilt werden. Liegt eine unregelmässige Tachykardie vor, sind Vorhofflimmern, Vorhofflattern mit variierender Überleitung in Wenkebach-Periodik oder multifokale Tachykardien die wahrscheinlichsten Diagnosen. Bei regelmässigen Tachykardien mit höherer Vorhoffrequenz als Ventrikelfrequenz ist von einem Vorhofflattern oder einer fokalen atrialen Tachykardie auszugehen. Als letztes Differenzierungskriterium kann das Intervall zwischen R-Zacke und P-Welle herangezogen werden: Die «Absenz» von P-Wellen bzw. das «alleinige» Vorhandensein einer kleinen Deflektion am Ende des QRS-Komplexes legt die Diagnose einer typischen AVNRT nahe. Liegt die P-Welle kurz hinter dem QRS-Komplex und beträgt das RP-Intervall (Abstand des QRS-Komplexes zur P-Welle) ≤90ms, spricht dies für eine typische AVNRT, ein RP-Intervall >90ms hingegen eher für eine AVRT, atypische AVNRT oder atriale Tachykardie. Liegt die P-Welle kurz vor dem QRS-Komplex (RP>PR) macht dies eine atriale Tachykardie oder (seltener) eine atypische AVNRT wahrscheinlicher. Auch eine ventrikuläre Tachykardie muss in die grundsätzliche Differenzialdiagnose miteinbezogen werden, da ein Ursprung im basalen interventrikulären Septum verhältnismässig schmale QRS-Komplexe erzeugen kann(Abb. 3e).7

Abb. 4: Diagnostischer Pfad zur Klassifikation von Schmalkomplextachykardien
Vagale Manöver
Vagale Manöver (Bauchpresse, Schlucken von kaltem Wasser und Karotissinusdruck) stellen bei allen AV-Knoten-abhängigen supraventrikulären Tachykardien eine schnelle und ubiquitär verfügbare Therapieoption dar. Die beste Erfolgsquote weist dabei das modifizierte Valsalva-Manöver auf: Der Patient befindet sich auf einer Liege in aufrecht sitzender Position und wird angeleitet, ein Valsalva-Manöver durchzuführen (z.B. Aufforderung, eine 5ml-Spritze durch Aufblasen zu füllen). Unmittelbar nach Beendigung des Manövers erfolgt die Lagerung des Patienten auf den Rücken mit Hochheben der Beine. Mit dieser posturalen Modifikation zum klassischen Valsalva-Manöver erreicht man bei 43% aller Patienten eine Konversion in den Sinusrhythmus, was signifikant häufiger ist als mit der ursprünglichen Version ohne Lagerung.22
Adenosin-Gabe
Scheitern die beschriebenen vagalen Manöver, steht mit der intravenösen Bolusgabe von Adenosin eine zweite, einfache und vergleichsweise risikoarme Therapieoption zur Verfügung. Adenosin führt bei rascher Applikation zu einem kurzzeitigen kompletten AV-Block mit Unterbrechung von AV-Knoten-abhängigen Reentry-Tachykardien (AVNRT und AVRT). Es gilt aber zu bedenken, dass atriale Tachykardien selten Adenosin-sensibel sein können und somit nach Applikation von Adenosin manchmal ebenfalls terminieren. Meist demaskiert Adenosin aber im EKG ein Vorhofflattern oder atriale Tachykardien (keine Termination) und hat somit mindestens einen diagnostischen Wert (Abb. 5, Tab. 2). Länger anhaltende Bradykardien sind dabei ungewöhnlich23 und auch unerwünschte pulmonale Nebenwirkungen sind mit lediglich 7 Bronchospasmen in einem Kollektiv von 9256 Patienten (0,08%) selten.24 Eine manifeste pulmonale Obstruktion wie z.B. bei unkontrolliertem Asthma bronchiale stellt allerdings eine Kontraindikation dar. Die Applikation bei Patienten mit Status nach denervierter, orthotoper Herztransplantation wird kritisch diskutiert, es gibt jedoch auch hier Daten zur sicheren Anwendung bei vorsichtiger Titration.25
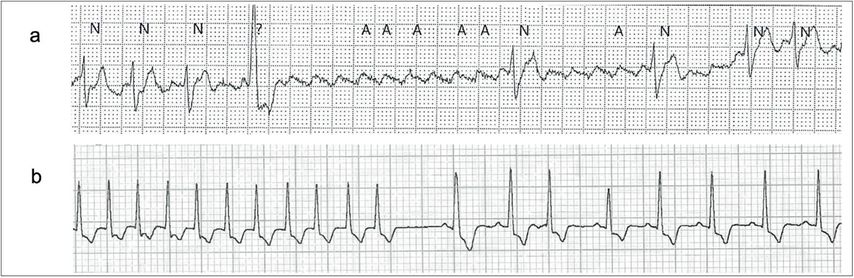
Abb. 5: Reaktion auf intravenöse Bolusgabe von Adenosin: a) Demaskierung von Vorhofflattern nach Blockierung des AV-Knotens; b) Termination einer AV-Knoten-Reentry-Tachykardie (AVNRT) mit Übergang in einen Sinusrhythmus

Tab. 2: Mögliche Antworten auf Bolusgabe von Adenosin7
Therapie
Akuttherapie
Äquivalent zum Vorgehen bei Breitkomplextachykardien stellt auch bei supraventrikulären Tachykardien die synchronisierte Elektrokonversion das Mittel der Wahl bei hämodynamischer Instabilität dar. Bei hämodynamischer Stabilität sind vagale Manöver, wie beispielsweise das oben beschriebene modifizierte Valsalva-Manöver, Mittel der Wahl. Alternativ kann nach vorgängiger Auskultation auch ein Druckversuch der Arteria carotis durchgeführt werden. Dies kann beidseitig, nie aber simultan durchgeführt werden. Ferner ist bei vorbestehender zerebrovaskulärer Verschlusskrankheit oder bekanntermassen stark verkalkten Gefässen Vorsicht geboten.
Als Nächstes ist ein Therapieversuch mit intravenöser Bolusgabe von Adenosin indiziert: Initial wird eine Dosis von 6mg, im Verlauf 12(–18)mg empfohlen. Zeigt sich die Tachykardie darunter therapierefraktär können alternativ Kalziumkanal-Antagonisten wie Verapamil und Diltiazem oder Betablocker intravenös verabreicht werden. Dafür besteht lediglich eine Kontraindikation bei ventrikulärer Präexzitation im EKG (und somit antegrad leitender akzessorischer atrioventrikulärer Bahn) aufgrund des Risikos für vermehrte tachykarde Überleitung direkt in den Ventrikel über die akzessorische Bahn. Falls Adenosin bei Breitkomplextachykardien zur Anwendung kommt, sollte dies nur unter kontrollierten Bedingungen erfolgen mit entsprechenden Vorsichtsmassnahmen und Monitorisierung. Die intravenöse Gabe von Amiodaron stellt die letzte medikamentöse Therapieoption dar und ist primär anzuwenden bei atrialen Tachykardien oder atypischem Vorhofflattern bei älteren und polymorbiden Patientenpopulationen.7
Langfristige Therapie
Sämtliche supraventrikulären Tachykardien sind diagnostisch grundsätzlich der elektrophysiologischen Untersuchung zugänglich. Nach inguinaler venöser Punktion kann mit diagnostischen Kathetern die Erregungsausbreitung intrakardial vermessen und je nach Befund gezielt therapiert werden. Die Erfolgswahrscheinlichkeit variiert dabei in Abhängigkeit vom Mechanismus der SVT (Tab. 3).
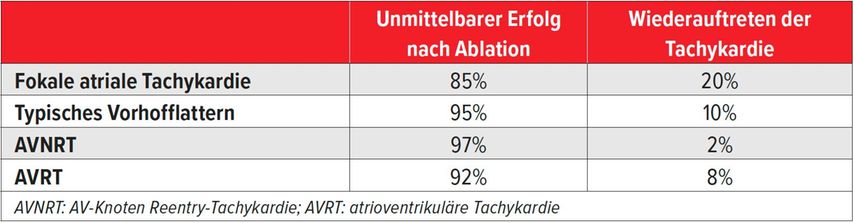
Tab. 3: Erfolg nach Katheterablation7
Die Komplikationsrate ist mit <1–2% sehr niedrig und umfasst primär Blutungskomplikationen im Bereich der venösen Punktionsstellen. Seltene schwerwiegende Komplikationen sind Perikardtamponade, zerebrovaskulärer Insult und Schrittmacherabhängigkeit nach akzidenteller Verletzung des intrinsischen Reizleitungssystems. Aufgrund dieser sehr guten Nutzen-Risiko-Konstellation besteht für die elektrophysiologische Untersuchung in den neusten europäischen Guidelines entsprechend eine Klasse-1A-Indikation für die Langzeittherapie aller supraventrikulärer Tachykardien (Abb. 6, 7).26–28 Dies gilt insbesondere für die AVNRT, die AVRT und das typische Vorhofflattern. Bei Ablehnen einer interventionellen Therapie kann eine medikamentöse Langzeittherapie versucht werden. Dafür kommen ähnlich wie bei der Akuttherapie Betablocker oder Kalziumkanal-Antagonisten vom Verapamil-Typ infrage. Bei Letzteren ist allerdings bei der Anwendung bei herzinsuffizienten Patienten aufgrund der in der Regel ausgeprägten negativ inotropen Wirkung Vorsicht geboten. Bei atrialen Tachykardien und AVRT steht als weitere Therapieoption bei strukturell gesundem Herzen Flecainid als Dauertherapie oder «pill in the pocket» zur Verfügung, aber immer kombiniert mit einem Betablocker. Insgesamt sind pharmakologische Therapieoptionen bezüglich Rezidivprophylaxe bei allerdings variierender Datenlage den interventionellen Therapien unterlegen (Tab. 4).7, 29
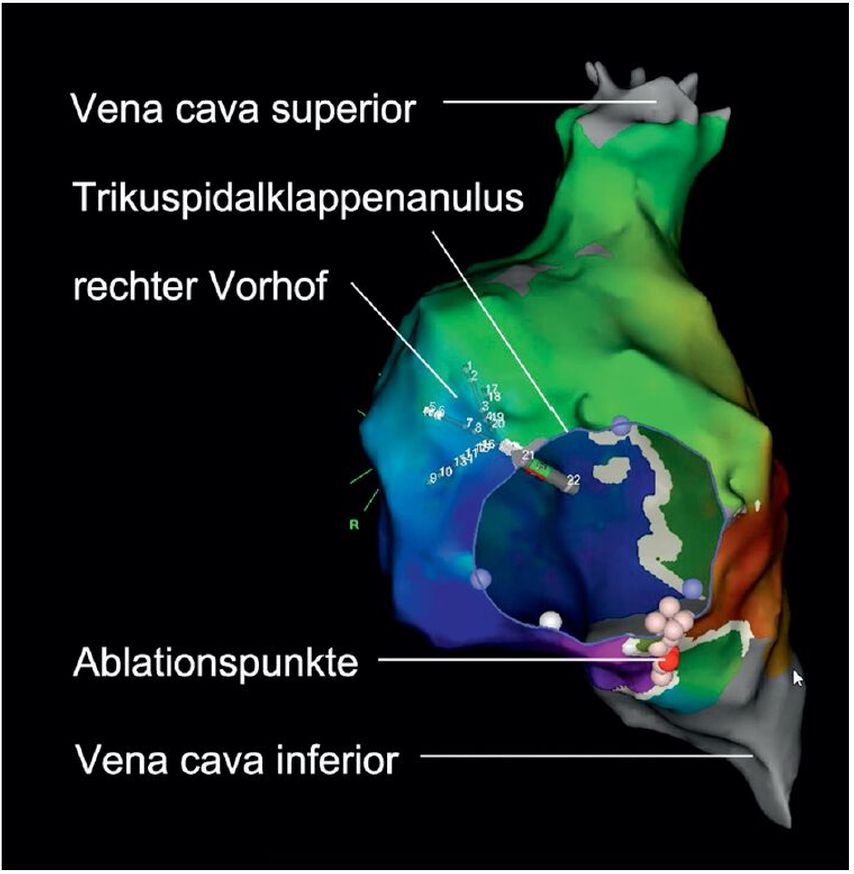
Abb. 6: Ablation eines typischen Vorhofflatterns mit elektroanatomischem Mapping-Verfahren, LAO-Projektion, die Farben entsprechen einer elektroanatomischen Aktivierungskarte von früh nach spät: rot, gelb, grün, blau, violett. Rote Punkte = erfolgreiche Ablationspunkte
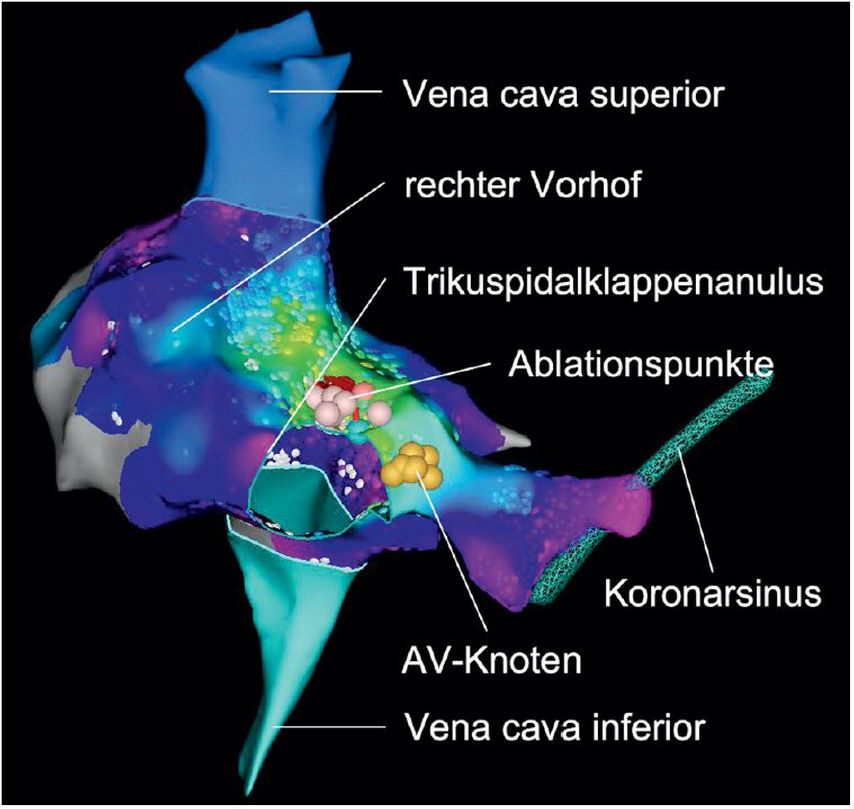
Abb. 7: Ablation einer fokalen atrialen Tachykardie aus dem rechten Vorhofdach nahe dem Trikuspidalklappenanulus mit elektroanatomischem Mapping-Verfahren, LAO-Projektion, die Farben entsprechen einer elektroanatomischen Aktivierungskarte von früh nach spät: rot, gelb, grün, blau. Rote Punkte = erfolgreiche Ablationspunkte
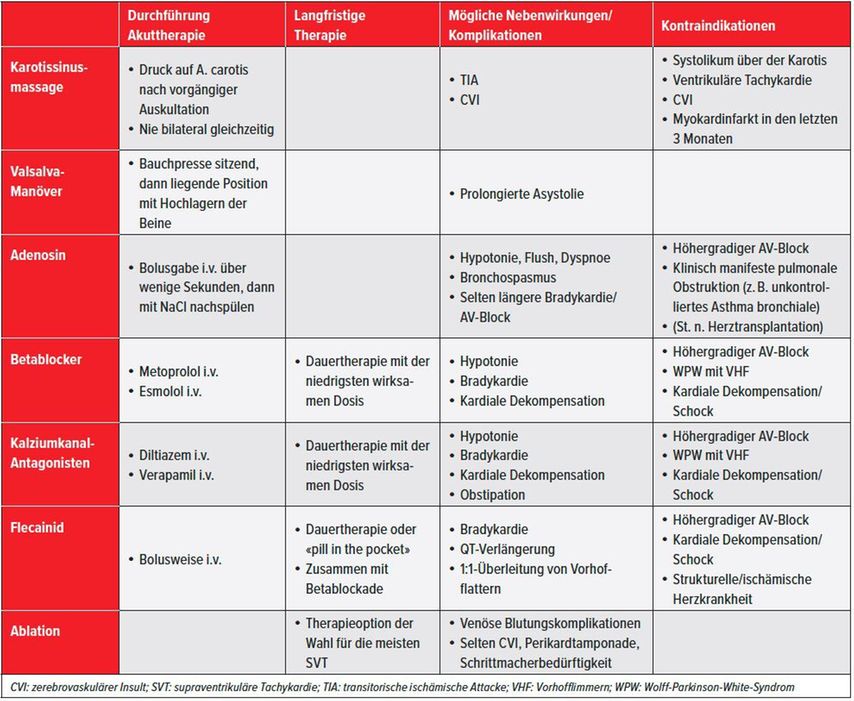
Tab. 4: Übersicht über mögliche Therapien bei supraventrikulären Tachykardien1, 7, 22
Deklarationen:
D. H. erhielt Educational Grants, Consultant Fees, Speaker Fees oder Fellowship Support von Abbott (SJM), Medtronic, Biotronik, Boston Scientific, Biosense Webster, Novartis, Bayer. A. B. gibt an, Beratungshonorare von BMS/Pfizer, Biotronik, Medtronic, Daiichy Sankio, Boston Scientific und Bayer Health Care erhalten zu haben sowie Forschungsstipendien von Biosense Webster, Biotronik und Actelion und Referentenhonorare von BMS/Pfizer, Bayer Health Care, Abbott, Spectranetics, Biotronik und Medtronic. J. S. erhielt Consultant oder Speaker Fees von Abbott, Amgen, Astra-Zeneca, Atricure, Bayer, Berlin-Chemie/Menarini, BiosenseWebster, Biotronik, Boehringer-Ingelheim, Boston Scientific, Bristol-Myers Squibb, Daiichi Sankyo, Medscape, Medtronic, Merck/MSD, Novartis, Pfizer, Sanofi-Aventis, WebMD und Zoll. J. S. ist Miteigentümer von CorXL. J. S. erhielt zudem Research Support für seine Institution von Abbott, Bayer Healthcare, Biosense Webster, Biotronik, Boston Scientific, Daiichi Sankyo und Medtronic.
Literatur:
1 Page RL et al.: 2015 ACC/AHA/HRS Guideline for the management of adult patients with supraventricular tachycardia: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol 2016; 67: e27-115 2 Orejarena LA et al.: Paroxysmal supraventricular tachycardia in the general population. J Am Coll Cardiol 1998; 31: 150-7 3 Go AS et al.: Contemporary burden and correlates of symptomatic paroxysmal supraventricular tachycardia. J Am Heart Assoc 2018; 7: e008759 4 Leitch JW et al.: Syncope associated with supraventricular tachycardia. An expression of tachycardia rate or vasomotor response? Circulation 1992; 85: 1064-71 5 Zimetbaum P, Josephson ME: Evaluation of patients with palpitations. N Engl J Med 1998; 338: 1369-73 6 Josephson ME: Clinical cardiac electrophysiology. 4th ed. Lippincott Williams & Wilkins, 2008 7 Brugada J et al.; ESC Scientific Document Group: 2019 ESC Guidelines for the management of patients with supraventricular tachycardia. The Task Force for the management of patients with supraventricular tachycardia of the European Society of Cardiology (ESC). Eur Heart J 2020; 41: 655-720 8 Still AM et al.: Prevalence, characteristics and natural course of inappropriate sinus tachycardia. Europace 2005; 7: 104-12 9 Roberts-Thomson KC et al.: Focal atrial tachycardia I: clinical features, diagnosis, mechanisms, and anatomic location. Pacing Clin Electrophysiol 2006; 29: 643-5 10 Kistler PM et al.: P-wave morphology in focal atrial tachycardia: development of an algorithm to predict the anatomic site of origin. J Am Coll Cardiol 2006; 48: 1010-7 11 Pérez FJ et al.: Long-term outcomes after catheter ablation of cavo-tricuspid isthmus dependent atrial flutter: a meta-analysis. Circ Arrhythm Electrophysiol 2009; 2: 393-401 12 Stevenson ICH et al.: Scar-related right atrial macroreentrant tachycardia in patients without prior atrial surgery: electroanatomic characterization and ablation outcome. Heart Rhythm 2005; 2: 594-601 13 Halligan SC et al.: The natural history of lone atrial flutter. Ann Intern Med 2004; 140: 265-8 14 Chen YL et al.: Clinical outcomes of solitary atrial flutter patients using anticoagulation therapy: a national cohort study. Europace 2019; 21: 313-21 15 Vadmann H et al.: Atrial flutter and thromboembolic risk: a systematic review. Heart 2015; 101: 1446-55 16 Katritsis DG, Josephson ME: Classification of electrophysiological types of atrioventricular nodal re-entrant tachycardia: a reappraisal. Europace 2013; 15: 1231-40 17 Jackman WM et al.: Catheter ablation of accessory atrioventricular pathways (Wolff-Parkinson-White syndrome) by radiofrequency current. N Engl J Med 1991; 324: 1605-11 18 Katritsis D et al.: Radiofrequency ablation of accessory pathways: implications of accumulated experience and time dedicated to procedures. Eur Heart J 1994; 15: 339-44 19 Schlüter M et al.: Catheter ablation using radiofrequency current to cure symptomatic patients with tachyarrhythmias related to an accessory atrioventricular pathway. Circulation 1991; 84: 1644-61 20 Bhatia A et al.: Preexcitation syndromes. Curr Probl Cardiol 2016; 41: 99-137 21 Kuck KH et al.: Sites of conduction block in accessory atrioventricular pathways. Basis for concealed accessory pathways. Circulation 1990; 82: 407-17 22 Appelboam A et al.; REVERT trial collaborators: Postural modification to the standard Valsalva manoeuvre for emergency treatment of supraventricular tachycardias (REVERT): a randomised controlled trial. Lancet 2015; 386: 1747-53 23 Camm AJ, Garratt CJ: Adenosine and supraventricular tachycardia. N Engl J Med 1991; 325: 1621-9 24 Cerqueira MD et al.: Safety profile of adenosine stress perfusion imaging: results from the Adenoscan Multicenter Trial Registry. J Am Coll Cardiol 1994; 23: 384-9 25 Flyer JN et al.: Prospective study of adenosine on atrioventricular nodal conduction in pediatric and young adult patients after heart transplantation. Circulation 2017; 135: 2485-93 26 Holmqvist F et al.: A decade of catheter ablation of cardiac arrhythmias in Sweden: ablation practices and outcomes. Eur Heart J 2019; 40: 820-30 27 Hosseini SM et al.: Catheter ablation for cardiac arrhythmias: utilization and in-hospital complications, 2000 to 2013. JACC Clin Electrophysiol 2017; 3: 1240-8 28 Ibáñez Criado JL et al.: Spanish catheter ablation registry. 18th official report of the Spanish Society of Cardiology Working Group on Electrophysiology and Arrhythmias (2018). Rev Esp Cardiol 2019; 72: 1031-42 29 Hohnloser SH, Zabel M: Short- and long-term efficacy and safety of flecainide acetate for supraventricular arrhythmias. Am J Cardiol 1992; 70: 3A-9A