La douleur chez le sujet âgé: particularités du traitement
Auteures:
Dre méd. Petra Hoederath
Fachärztin FMH für Neurochirurgie
SPS Schmerzspezialistin
Sabine Schweiger
Klinische Pharmazeutin FPH
Hirslanden Klinik Stephanshorn
Brauerstrasse 95
9016 St.Gallen
E-mail: petra.hoederath@hirslanden.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le nombre de personnes âgées au sein de la population totale ne cesse d’augmenter et l’attention se porte sur les problèmes de santé, dont font partie les douleurs aiguës et chroniques, qui affectent durablement la qualité de vie des sujets âgés et très âgés. La multimorbidité, la polypharmacie qui en découle et les changements physiques et psychiques qui surviennent avec l’âge représentent un défi particulier pour le traitement des patients gériatriques souffrant de douleurs. Dans le cadre de la pharmacothérapie des patients algiques âgés et très âgés, il convient de tenir compte de ces particularités et de procéder à une évaluation correspondante des bénéfices et des risques dans un contexte d’absence de données probantes spécifiques à la gériatrie.
Keypoints
-
Les changements physiologiques et psychiques qui surviennent dans le cadre du processus de vieillissement nécessitent un traitement médicamenteux adapté: «start low – go slow».
-
Des listes basées sur un consensus peuvent servir de repère.
-
Des traitements conformes aux directives permettent une prise en charge adéquate de la douleur qui peut contribuer à une amélioration de la qualité de vie.
La prévalence des douleurs est élevée. Ainsi, environ 16%1 de la population suisse souffre de douleurs chroniques et on estime que la probabilité d’être atteint de douleurs chroniques augmente avec l’âge pour atteindre un taux de 55%.2 Parallèlement, l’étude SHELTER montre p.ex. que près d’un tiers des résidents allemands et un quart des résidents européens d’établissements médico-sociaux/de maisons de retraite, présentant des douleurs modérées à sévères ne reçoivent aucun médicament ou seulement un médicament administré à la demande.3
Un traitement suffisant et adéquat de la douleur n’est pas uniquement efficace pour réduire l’intensité de la douleur, maintenir ou accroître la mobilité, optimiser l’intégration psychosociale et améliorer ainsi la qualité de vie, mais aussi pour éviter la chronicisation de la douleur qui semble augmenter avec l’âge.4
Rendre la douleur visible
Pour comprendre la douleur et pouvoir la traiter de façon adéquate, il est important de la «rendre visible».
Cette «visualisation» s’effectue habituellement à l’aide d’instruments de dépistage. En raison de la multimorbidité gériatrique (nombre accru d’origines de la douleur, variabilité des zones du corps rendant difficile l’évaluation de la localisation et de l’intensité de la douleur), mais aussi de la déficience cognitive ou de la présence d’une démence entraînant une restriction de la communication, ces instruments ne peuvent toutefois être utilisés que de manière insuffisante dans le cadre de l’évaluation de la douleur gériatrique.5
Chez les patients âgés, il faut donc tenir compte du fait qu’ils ne sont justement plus en mesure d’évaluer correctement la douleur sur une échelle de 0 à 10 et encore moins de décrire le type de douleur dont ils souffrent.
Outre un instrument de dépistage dans le cadre du projet Pain Detect qui peut être facilement et rapidement utilisé au cabinet médical et fournit des informations sur la probabilité d’une douleur neuropathique, il existe pour les patients âgés des outils, tels que le questionnaire ZOPA© (Zurich Observation Pain Assessment), l’échelle Doloplus-2 ou le score BESD (évaluation de la douleur en cas de démence). Ainsi, le comportement renseigne sur les douleurs, en tenant compte des vocalisations, des expressions du visage, du langage corporel et des indicateurs physiologiques.
En complément de l’auto-évaluation de l’intensité de la douleur, pour laquelle nous utilisons généralement des échelles simples, de 0 signifiant l’absence de douleur à la pire douleur imaginable, le patient peut dessiner les zones douloureuses sur un simple «bonhomme». Une fois que l’on connaît le site de la douleur, on peut alors approfondir. Outre l’intensité et la localisation, le caractère de la douleur est également déterminant. Les patients doivent décrire avec leurs propres mots leur ressenti de la douleur.
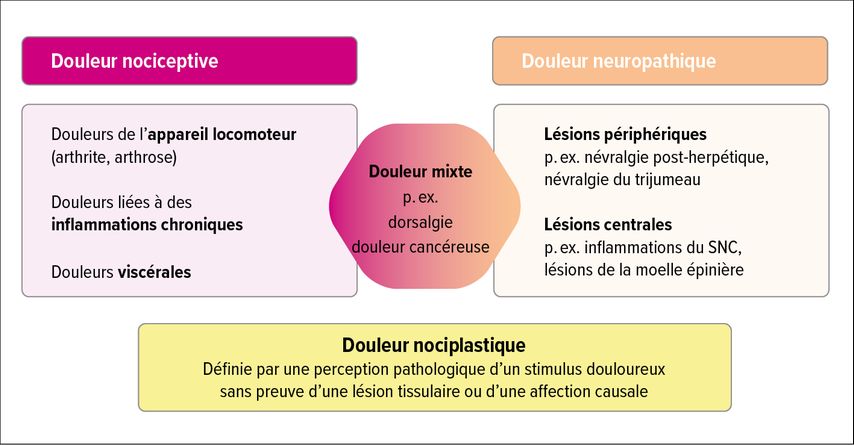
Il est important de faire la distinction entre douleur nociceptive et douleur neuropathique (Fig.1). Il y a aussi la douleur mixte, telle que la dorsalgie, qui a généralement une composante nociceptive dans les articulations de la colonne vertébrale et une composante neuropathique due à une compression neuronale. Il existe un autre type de douleur, la douleur nociplastique, qui se définit par une perception pathologique d’un stimulus douloureux sans qu’une lésion ou qu’une affection tissulaire existante ne puisse être attestée comme en étant la cause.
Étant donné que les divers types de douleurs sont traités par des médicaments différents, cette information est essentielle. Il existe bien entendu des questionnaires d’évaluation de la douleur détaillés, mais ils sont principalement utilisés dans les cliniques/centres de la douleur, mais aussi à des fins de recherche et de collecte de données.
Généralement, le diagnostic peut également fournir des renseignements sur le caractère de la douleur. Ainsi, en cas d’arthrose dans les articulations, il s’agit souvent d’une douleur nociceptive. En présence d’affections de la colonne vertébrale, d’ostéoporose et de tumeurs, la douleur est souvent mixte et a une composante nociceptive et neuropathique. La névralgie du trijumeau et le zona sont des exemples classiques de douleurs neuropathiques. Il faut également distinguer la douleur viscérale et la migraine/les céphalées.
Le traitement multimodal de la douleur comporte différents éléments qui sont mis en place de manière individualisée. Outre la physiothérapie/l’ergothérapie, les infiltrations, une aide psychologique, mais aussi l’indication éventuelle d’une intervention chirurgicale, en tenant compte des comorbidités chez les personnes âgées, le traitement médicamenteux de la douleur est l’un des principaux piliers.
Modifications de la pharmacocinétique et de la pharmacodynamique chez le sujet âgé
Au cours du processus de vieillissement, de nombreux paramètres physiologiques changent, ce qui implique des modifications afférentes des processus pharmacocinétiques et pharmacodynamiques. Les modifications pharmacocinétiques ont été mieux analysées que les modifications pharmacodynamiques, et les adaptations pharmacodynamiques sont également plus difficiles à mesurer dans la pratique clinique quotidienne.6
Les modifications pharmacocinétiques liées à l’âge présentées dans le Tableau 1 entraînent dans l’ensemble une durée d’action plus longue des médicaments chez le sujet âgé. Le principe directeur, applicable en gériatrie au traitement médicamenteux en général et aux opioïdes en particulier, qui en résulte est donc le suivant: «Start low, go slow, don’t stop» (commencer par une faible dose et augmenter lentement la posologie), tout en tenant compte du fait qu’au début du traitement médicamenteux, il est difficile d’évaluer les effets sur l’organisme des patients multimorbides. «Don’t stop» signifie dans ce contexte qu’il ne faut pas arrêter les opiacés en cas de bon contrôle de la douleur et que la dose doit être augmentée si l’analgésie n’est pas suffisante.
Le traitement analgésique est effectué principalement selon le schéma par paliers de l’OMS, que nous, médecins, avons tous appris dans nos cours de pharmacologie. Ce schéma a été conçu par l’OMS pour le traitement de la douleur cancéreuse et ne tient compte ni des dernières connaissances pharmacologiques, ni des mécanismes physiopathologiques, ni du fait qu’aujourd’hui, le traitement est plutôt axé sur les mécanismes.
Lors du choix de la substance utilisée pour le traitement de la douleur chez les patients gériatriques, il convient de prendre en considération en particulier la diminution de la fonction hépatique et rénale et de procéder à une évaluation stricte des bénéfices et des risques.
Paracétamol
L’effet analgésique du paracétamol est certes moins puissant que celui des anti-inflammatoires non stéroïdiens (AINS), mais il a un profil bénéfice/risque favorable par rapport aux AINS, une grande marge thérapeutique et un taux d’effets indésirables (EI) plus faible que les AINS. La survenue d’un EI hépatotoxique dépend de la dose et est donc prévisible/gérable.7 Pour les patients gériatriques, il est question d’une dose journalière maximale de 3g, dose à laquelle des EI hépatotoxiques majeurs sont peu probables.7
En ce qui concerne les interactions se produisant chez les patients gériatriques souvent polymédicamentés, le faible potentiel d’interaction du paracétamol est un avantage.8 Une interaction avec les antagonistes classiques de la vitamine K peut conduire à une potentialisation de leur effet (tendance accrue aux hémorragies).9
Métamizole
L’intensité de l’effet analgésique du métamizole peut être comparée à celle des AINS, mais son profil bénéfice/risque est plus favorable en dépit d’une hématotoxicité potentielle. L’effet hypotenseur, qui accroît la tendance aux chutes chez les patients gériatriques présentant des troubles circulatoires orthostatiques assez prononcés, semble nettement moins marqué en cas d’administration orale qu’en cas d’administration parentérale.10
Le potentiel d’interaction relativement faible du métamizole constitue un avantage dans le traitement des patients gériatriques algiques qui sont souvent polymédicamentés. Dans ce contexte, l’interaction avec l’AAS 100 doit être considérée comme étant cliniquement pertinente: dans le cadre de cette association médicamenteuse, l’AAS 100 doit être pris dans l’idéal au moins 60minutes avant la première administration de métamizole.
En cas d’insuffisance rénale, il convient d’envisager une réduction posologique, et en cas de diminution de la fonction hépatique, d’évaluer le rapport bénéfice/risque en conséquence.
En vue de réduire le risque d’agranulocytose, il faut procéder à une anamnèse détaillée avant d’instaurer le traitement et garantir une surveillance étroite des éventuels effets secondaires (p.ex. fièvre, état pseudo-grippal, nécroses des muqueuses buccales) pendant le traitement, afin de pouvoir les traiter rapidement si nécessaire. Pour le traitement à long terme, il est recommandé de surveiller les paramètres biologiques après 4 à 6 semaines.
Dans son protocole de traitement de la douleur chez les personnes très âgées, la Société autrichienne de gériatrie et de gérontologie (ÖGGG) recommande en première intention le métamizole à une posologie maximale de 4g/j.11
AINS
Les AINS qui sont de puissants analgésiques sont considérés comme une classe de substances problématiques et ne sont pas recommandés chez les personnes âgées en raison de leur toxicité gastro-intestinale, rénale, cardiaque et cérébrovasculaire.22
La griffe du diable (harpagophytum procumbens) peut être utilisée comme alternative. Même si les données ne sont pas indiscutables, sa faible toxicité organique plaide néanmoins en faveur de son utilisation.
Opioïdes
Tramadol
Le tramadol, faible agoniste du récepteur µ et inhibiteur de la recapture de la sérotonine et de la noradrénaline, est une option thérapeutique insuffisante pour les patients gériatriques du fait de son effet sérotoninergique indésirable central, de son profil dose-effet défavorable (augmentation posologique quasiment impossible en raison de l’augmentation des effets indésirables) et de son taux d’élimination rénale élevé (jusqu’à 90%). De plus, les vertiges sont un EI du tramadol qui génèrent un risque de chute accru chez les patients âgés.12
Opioïdes puissants
L’effet des opioïdes puissants peut être qualifié d’équipotent à dose équivalente. Ils ont différents mécanismes d’action, comme le montre le Tableau 2.
Même si l’on peut postuler l’absence de toxicité organique des opioïdes par rapport aux AINS, les effets secondaires doivent être pris en compte lors de leur utilisation dans le cadre du traitement de la douleur gériatrique. La constipation, les nausées, les troubles de la vigilance, le délire et les myoclonies sont considérés comme des EI dose-dépendants. Dans ce cas, si la douleur est bien contrôlée, une réduction prudente de la dose de 25% ( à 50%) peut être tentée.13 De surcroît, les opioïdes sont un facteur de risque de chute, ce risque augmentant en cas d’association avec d’autres médicaments également à action centrale, tels que les benzodiazépines ou les neuroleptiques sédatifs.14 Des données de registre danoises suggèrent que le risque de chute sous opioïdes est inexistant avec la buprénorphine.15 La fréquence et la sévérité des EI peuvent augmenter avec l’âge et en cas de multimorbidité par rapport aux sujets plus jeunes.16 Étant donné que les EI sont souvent non spécifiques (constipation, vertiges, etc.) et peuvent survenir également indépendamment de la prise d’opioïdes, leur évaluation est problématique chez le sujet âgé.17
L’administration constante de formes à libération prolongée est recommandée, notamment pour les opioïdes. Les formes pharmaceutiques à libération rapide doivent être utilisées uniquement pour déterminer la dose ou comme traitement de réserve et doivent être administrées avec retenue, en particulier chez les personnes âgées, en raison de la distribution rapide des médicaments et du risque de chute.18
En cas d’altération de la fonction rénale, il convient de procéder à des ajustements appropriés, notamment avec la morphine. La base de données dosing.de19 de l’Hôpital universitaire de Heidelberg sert de repère pour la posologie de médicaments en présence d’insuffisance rénale.
Les directives LONTS donnent des recommandations générales sur l’utilisation des opioïdes en cas de douleurs chroniques non cancéreuses. Il s’agit d’une directive S3 sur l’utilisation à long terme des opioïdes en cas de douleurs chroniques non cancéreuses, qui a été actualisée en 2020.20 Un résumé des recommandations est présenté dans le Tableau 3.
Tab. 3: Recommandations relatives au traitement opioïde dans la pratique issues de la nouvelle version de la directive LONTS20
Liste de médicaments basée surun consensus
Afin d’améliorer la qualité du traitement médicamenteux des patients gériatriques, il est utile de recourir à des listes de médicaments basées sur un consensus. La liste FORTA («Fit for the Aged») de l’Hôpital universitaire de Mannheim par exemple, peut être utilisée (Tab. 4).21
Tab. 4: Liste FORTA («Fit for the Aged») de l’Hôpital universitaire de Mannheim pour la classification des médicaments destinés aux patients âgés21
Ainsi, dans la catégorie «Douleurs chroniques», les AINS sont classés dans la catégorie D, le métamizole dans la catégorie B et le paracétamol dans la catégorie A. Concernant les opioïdes, la buprénorphine, l’oxycodone, l’hydromorphone et le fentanyl sont classés dans la catégorie B, la morphine et le tramadol dans la catégorie C.
Co-analgésiques fréquemment utilisés dans le traitement des douleurs neuropathiques chez le sujet âgé
Étant donné que les données probantes spécifiques à la gériatrie concernant l’administration de co-analgésiques font également défaut, il convient dans l’optique d’une évaluation des bénéfices et des risques, de se baser sur le profil d’effets secondaires, la fréquence des effets secondaires et le potentiel d’interaction lors de l’utilisation d’antidépresseurs et d’antiépileptiques chez les patients gériatriques.
L’utilisation de l’antidépresseur amitriptyline doit être considérée comme étant défavorable chez les patients gériatriques en raison de ses EI anticholinergiques et cardiaques, mais aussi du risque accru de chute.22 Les antiépileptiques prégabaline, gabapentine et duloxétine se caractérisent également par un profil d’EI défavorable chez les personnes âgées, comportant l’hyponatrémie, la sédation et les troubles cognitifs. Un traitement médicamenteux avec ces substances doit donc être mis en œuvre selon le principe «Start low, go slow», ce qui se traduit par un schéma posologique prudent: prégabaline (25 à 300mg/j maximum), gabapentine (100 à 1800mg/j maximum) et duloxétine (30 à 60mg/j maximum).
Cannabis
Le cannabis à usage médical doit également être pris en compte dans le traitement multimodal de la douleur. Actuellement, il n’y a pas d’indication pour le THC/CBD en traitement de première intention, mais des études ont montré que le profil bénéfice/sécurité est meilleur que pour les opiacés, les antiépileptiques et les antidépresseurs.23 Malgré une littérature abondante, nous disposons de données très hétérogènes et il est nécessaire d’effectuer d’autres études cliniques prospectives contrôlées.
Littérature:
1 Hüllemann P, Baron R: Schmerzen. In: Maetzler W et al. (ed.): Neurogeriatrie. Berlin: Springer, 2019. 273-8 2 Oggier W: Schweiz Ärzteztg 2007; 88: 1265-9 3 Lukas A et al.: Schmerz 2015; 29: 411-21 4 Mattenklodt P: Schmerzchronifizierung. In: Schuler M (ed.): Schmerztherapie beim älteren Patienten. Berlin/Boston: De Gruyter, 2016 5 Stromer W: Schmerznachrichten 2017; 2 6 Hughes SG: Br J Clin Pharmacol 1998; 46: 531-3 7 Burkhardt H: Non-Opioide und Adjuvantia zur Schmerzbehandlung bei älteren Patienten. In:Schuler M (ed.): Schmerztherapie beim älteren Patienten. Berlin/Boston: De Gruyter, 2016 8 Preston CL: Stockley's Drug Interaction. London: Pharmaceutical Press, 2016 9 www.mediq.ch 10 Verspohl EJ: Analgetika mit antipyretischer und antiphlogistischer Wirkungskomponente. In: Ammon HPT: Arzneimittelneben-und -wechselwirkungen. Stuttgart: Wissenschaftliche Verlagsgesellschaft, 2001 11 ÖSG: Schmerztherapie bei hochbetagten Menschen. Expertenforum. Universum Innere Medizin. 2016 12 Vorsanger G et al.: Clin Ther 2007; 29(Suppl): 2520-35 13 Schuler M: Opioide. In: Schuler M (ed.): Schmerztherapie beim älteren Patienten. Berlin/Boston: De Gruyter, 2016 14 Rolita L et al.: J Am Geriatr Soc 2013; 61: 335-40 15 Vestergaard P et al.: J Intern Med 2006; 260: 76-87 16 Husebo BS et al.: BMJ 2011; 343: 4065 17 Schuler M et al.: Der Schmerz 2015; 29: 380-401 18 Güttler K: Anästhesiol Intensivmed Notfallmed Schmerzther 2012; 47: 224-30 19 https://dosing.de/nierebck.php 20 Deutsche Schmerzgesellschaft e.V. (ed.): Leitlinie Langzeitanwendung von Opioiden bei chronischen nicht-tumorbedingten Schmerzen (LONTS). 2. Aktualisierung, 2020 21 https://www.umm.uni-heidelberg.de/klinische-pharmakologie/forschung/forta-projekt/ 22 Wehling M, Burkhardt H: Arzneitherapie für Ältere. Berlin: Springer, 2019 23 Nutt DJ et al.: Cannabis Cannabinoid Res 2021 [epub ahead of print]
Das könnte Sie auch interessieren:
Diabète de type 1: recherche de stratégies cardio- et néphroprotectrices
Malgré tous les succès obtenus dans la prise en charge de cette maladie au cours des décennies, les patients souffrant de diabète de type 1 (DT1) continuent d’enregistrer une mortalité ...
Étude GDAC: la personnalisation du taux d’HbA1c se concrétise
Le taux d’HbA1c, mesure de la charge glycémique à long terme, est largement accepté et a été associé au risque de complications du diabète il y a plus de 30 ans déjà.1 Cependant, la ...
Psychologie clinique dans le cadre de la réadaptation cardiovasculaire: approches de mise en pratique
Les patient·es atteint·es de maladies cardiovasculaires souffrent souvent de troubles psychiques. Cela peut avoir un impact considérable sur la qualité de vie et le pronostic. Grâce à un ...