Neue Daten zu zielgerichteten Therapien in Kombination
Bericht: Dr. Ine Schmale
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Zielgerichtete Therapien haben sich zu Grundpfeilern der Behandlung von urologischen Tumoren entwickelt. Auch die konventionelle Chemotherapie und die Immuntherapie haben einen hohen Stellenwert, z.B. auch als Kombinationspartner. Im Folgenden eine Zusammenfassung von wichtigen Studien mit zielgerichteten Substanzen beim Prostata- und Urothelkarzinom, die beim ASCO Genitourinary Cancers Symposium in den Oral Sessions präsentiert wurden.
Die neuen Androgenrezeptor(AR)-gerichteten Hormontherapien haben die Prognose für Patienten mit metastasiertem Prostatakarzinom relevant verbessert. Beim ASCO GU Symposium wurden die Ergebnisse von zwei Phase-III-Studien mit AR-gerichteten Kombinationstherapien in verschiedenen Erkrankungsstadien präsentiert.
Darolutamid plus ADT beim hormonsensitiven PC
In der ARASENS-Studie wurde der Effekt von Darolutamid in Kombination mit einer Androgendeprivationstherapie (ADT) und Docetaxel auf das Gesamtüberleben (OS) von Patienten mit metastasiertem hormonsensitivem Prostatakarzinom (mHSPC) untersucht.1 Dazu erhielten 1305 Patienten 6 Zyklen Docetaxel plus randomisiert Darolutamid (600mg, bid) plus ADT oder Placebo plus ADT. Die Patienten waren median 67 Jahre alt. Der Gleason Score betrug in 78% der Fälle ≥8.
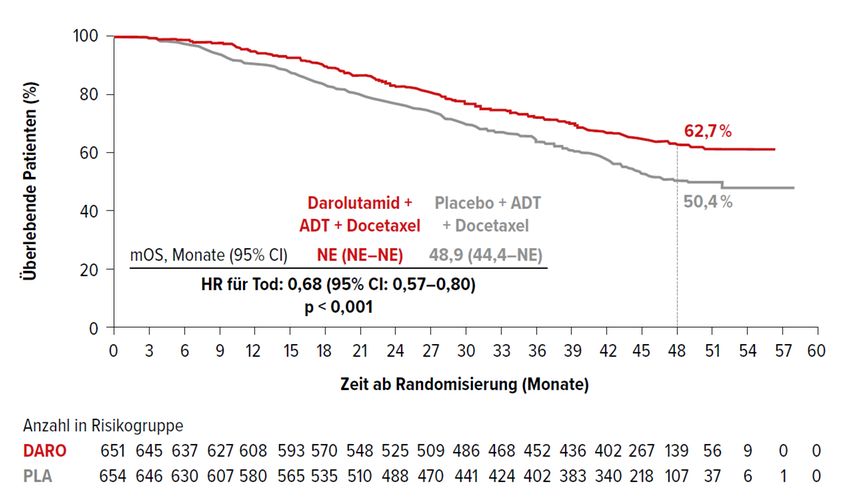
Der primäre Endpunkt wurde erreicht, das Risiko zu sterben wurde um 32,5% reduziert (HR: 0,68; 95% CI: 0,57–0,80; p<0,001; Abb. 1). Nach 48 Monaten lebten 62,7% im Darolutamid- versus 50,4% im Placebo-Arm. Dieses Ergebnis wurde erreicht, obwohl 56,8% bzw. 75,6% der Patienten eine potenziell lebensverlängernde Folgetherapie erhielten. In Subgruppenanalysen wurde ein Überlebensvorteil unter Darolutamid für alle untersuchten Subgruppen beobachtet. Die Zeit bis zum kastrationsresistenten Stadium (CRPC) wurde durch Darolutamid um 64% verlängert (HR: 0,36; 95% CI: 0,30–0,42; p<0,001). Der Median war im Darolutamid-Arm noch nicht erreicht und betrug 19,1 Monate im Placebo-Arm. Die mediane Zeit bis zum Schmerzprogress lag im Placebo-Arm bei 27,5 Monaten und war im Darolutamid-Arm ebenfalls noch nicht erreicht (HR: 0,79; 95% CI: 0,66–0,95; p=0,01). Der Median bezüglich der Zeit bis zum ersten skelettalen Ereignis war in beiden Studienarmen noch nicht erreicht (HR: 0,71; 95% CI: 0,54–0,94; p=0,02). Auch die Zeit bis zur ersten nachfolgenden antineoplastischen Therapie wurde signifikant verlängert (HR: 0,39; 95% CI: 0,33–0,46; p<0,001). Der Median war im Darolutamid-Arm noch nicht erreicht und betrug 25,3 Monate im Placebo-Arm.
Die Autoren schlossen aus den Ergebnissen, dass Darolutamid in Kombination mit ADT und Docetaxel der neue Standard in der Behandlung des mHSPC sein sollte.
Abb. 1: Gesamtüberleben von von Patienten mit mHSPC unter Darolutamid, ADT und Docetaxel versus Placebo, ADT und Docetaxel ARASENS-Studie. Modifziert nach Smith MR et al.1
Kontinuierliches Enzalutamid plus Chemotherapie beim mCRPC
Die randomisierte, doppelblinde, placebokontrollierte Phase-IIIb-Studie PRESIDE untersuchte den Effekt der kontinuierlichen Enzalutamid-Gabe bei chemotherapienaiven mCRPC-Patienten, die nach Progress auf Enzalutamid mit Docetaxel plus Prednisolon behandelt wurden.2 Die Studienhypothese war, dass mit der kontinuierlichen Enzalutamid-Gabe responsive Tumorläsionen weiter kontrolliert werden, während mit Docetaxel proliferierende klonale Subpopulationen reduziert werden können.
Im ersten Teil der Studie erhielten 687 mCRPC-Patienten mit leichten oder keinen Symptomen Enzalutamid als Monotherapie. Von 392 Patienten mit Progress erhielten im zweiten Studienabschnitt 271 Patienten randomisiert Enzalutamid oder Placebo sowie Docetaxel und Prednisolon. Primärer Studienendpunkt war das progressionsfreie Überleben (PFS).
Die in die Studie eingeschlossenen Patienten waren im Median 70 Jahre alt und zeigten bei Eintritt in den zweiten Teil der Studie einen PSA-Wert von median 36,9µg/l im Enzalutamid- und 28,1µg/l im Placebo-Arm. Der Gleason Score lag bei 56 bzw. 57% der Patienten ≥8.
Die Studie erreichte ihren primären Endpunkt. Das mediane PFS betrug 9,53 versus 8,28 Monate (HR: 0,72; 95% CI: 0,53–0,96; p=0,027). Es profitierten insbesondere Patienten <75 Jahre und Patienten mit einem Gleason Score ≥8 von der kontinuierlichen Enzalutamid-Gabe. Patienten profitieren unabhängig vom PSA-Wert bei Therapiebeginn. Patienten mit reiner Knochenmetastasierung zeigten keinen zusätzlichen Effekt durch die weitergeführte Enzalutamid-Gabe. Bezüglich der sekundären Endpunkte wurde durch kontinuierlich gegebenes Enzalutamid die Zeit bis zum PSA-Progress von median 6,24 auf 8,44 Monate verlängert (HR: 0,58; 95% CI: 0,41–0,82; p=0,002), die Ansprechrate von 25,9 auf 31,6% sowie die Rate an Komplettremissionen (CR) von 12,6 auf 19,1% erhöht.
Diese Ergebnisse geben Hinweise darauf, dass die kontinuierliche Therapie mit Enzalutamid plus Docetaxel eine mögliche Therapieoption für ausgewählte Patienten mit Progress nach Enzalutamid-Monotherapie sein könnte.
Neoadjuvante Therapie mit Enfortumab Vedotin beim UC
Für Patienten mit Urothelkarzinom (UC) wurden Ergebnisse im neoadjuvanten Setting für das Nectin-4-gerichtete Antikörper-Wirkstoff-Konjugat (ADC) Enfortumab Vedotin gezeigt.3 In die Kohorte H der Phase-I/IIb-Studie EV-103 wurden 22 Patienten mit muskelinvasivem Blasenkarzinom, die für eine Cisplatin-haltige Therapie nicht geeignet waren, aufgenommen und vor radikaler Zystektomie neoadjuvant mit 3 Zyklen Enfortumab Vedotin behandelt. Das mediane Alter der Patienten betrug 74,5 Jahre und bei 95,5% der Patienten handelte es sich um (ehemalige) Raucher. Die Mehrheit der Studienteilnehmer (68,2%) befand sich im Stadium cT2N0, 27,3% waren im Stadium cT3N0 und 4,5% im Stadium cT4aN0. Am häufigsten wurden Patienten aufgrund der Kreatinin-Clearance als nichtCisplatin-geeignet eingestuft, gefolgt von Hörverlust/SchwerhörigkeitGrad ≥2.
19 der 22 Patienten komplettierten die 3 Zyklen mit dem ADC und konnten ohne Verzögerung der Operation zugeführt werden. 3 Patienten verstarben vor Komplettierung des dritten adjuvanten Therapiezyklus. Die Rate an pathologischer CRbetrug 36,4%, die Rate an pathologischem Downstaging (definiert als ypT0, ypTis, ypTa, ypT1 und N0) 50%.
Insgesamt zeigten 18% der Patienten therapieassoziierte Nebenwirkungen Grad ≥3. 3 Patienten (13,6%) brachendie Studienmedikation aufgrund von therapieassoziierten Nebenwirkungen ab.
Rucaparib in der Erhaltungstherapie beim metastasierten UC
Auch PARP(Poly[ADP-Ribose]-Polymerase)-Inhibitoren wurden für die Therapie von Urothelkarzinompatienten geprüft. Die Phase-II-Studie ATLANTIS untersuchte in einem von drei experimentellen Studienarmen die Erhaltungstherapie mit dem PARP-Inhibitor Rucaparib nach Chemotherapie bei Patienten mit metastasiertem Urothelkarzinom.4 Als Kontrolle wurde randomisiert gegen Placebo verglichen, primärer Endpunkt war das PFS. Beim ASCO GU Symposium wurden die finalen Daten für den Rucaparib-Arm präsentiert.5
Die Rekrutierung für den Rucaparib- und den Vergleichsarm wurde nach 40 Patienten aufgrund verminderter Möglichkeiten mit Ausbruch der Coronapandemie und den guten Ergebnissen für Avelumab in der Erhaltung abgebrochen. Von den eingeschlossenen Patienten zeigten 27,5% eine DNA-Reparatur-Defizienz (DRD) und 55% einen Verlust der Heterozygotie (≥10% LOH). Beide Biomarker wurden bei 17,5% der Patienten identifiziert. Das mediane Alter der Patienten lag bei 70 Jahren und bei 65% der Patienten handelte es sich um (ehemalige) Raucher. 40–50% der Patienten hatten Viszeralmetastasen.
Das mediane PFS wurde von 15,1 auf 35,5 Wochen verlängert (HR: 0,53; 80% CI: 0,30–0,92; p=0,07). Das OS unterschied sich zwischen den Studienarmen nicht signifikant (HR: 1,22; 80% CI: 0,62–2,38). Die Patienten erhielten im Median 10 Zyklen Rucaparib bzw. 6 Zyklen Placebo. Bei einem Patienten wurdeunter Rucaparib eine partielle Remission beobachtet. Es traten im Rucaparib-Arm häufiger Nebenwirkungen auf, insbesondere Anämie, Fatigue und Übelkeit.
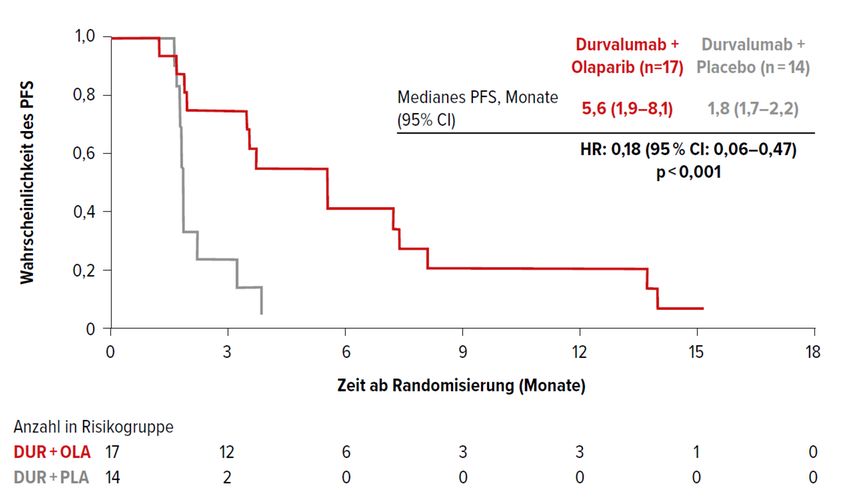
Abb. 2: Progressionsfreies Überleben unter Olaparib zusätzlich zu Durvalumab als Erstlinientherapie in der Subgruppe der HRR-mutierten Patienten mit nichtresektablem Urothelkarzinom im Stadium IV (Phase-II-Studie BAYOU). Modifiziert nach Rosenberg JE et al.6
Kombination von Olaparib und Durvalumab beim UC
Auch die doppelblinde Phase-II-Studie BAYOU untersuchte die Gabe eines PARP-Inhibitors, in diesem Fall Olaparib, zusätzlich zu Durvalumab als Erstlinientherapie bei Platin-ungeeigneten Patienten mit nichtresektablem Urothelkarzinom im Stadium IV.6 150 Patienten erhielten randomisiert Durvalumab plus Olaparib oder Durvalumab plus Placebo. Als primärer Endpunkt wurde das PFS untersucht. Die Nachbeobachtungszeit der präsentierten Auswertung betrug median 9,8 Monate für den Olaparib- und 10,7 Monate für den Placebo-Arm.
Die Patienten waren median 79 (Olaparib-Arm) bzw. 72 (Placebo-Arm) Jahre alt und waren in 44% bzw. 37% der Fälle in einem schlechten Allgemeinzustand (ECOG PS 2). 22% bzw. 18% der Patienten wiesen einen mutierten HRR(„homologous recombination repair“)-Status auf und bei 44% bzw. 42% der Patienten lag eine hohe PD-L1(„Programmed cell death 1 ligand 1“)-Expression vor.
Für die ITT-Population konnte kein Unterschied bezüglich des PFS ermittelt werden (HR: 0,94; 95% CI: 0,64–1,39; p=0,789). Für die Subgruppe der HRR-mutierten Patienten wurde das mediane PFS durch die Olaparib-Gabe von 1,8 auf 5,6 Monate verlängert (HR: 0,18; 95% CI: 0,06–0,47; p<0,001; Abb. 2). In den Subgruppenanalysen gab es zudem Hinweise auf einen besseren Therapieerfolg mit Olaparib für Patienten mit Bajorin-Risiko-Index 0 (HR: 0,42; 95% CI: 0,18–0,92). Das OS war sowohl für die ITT-Population (HR: 1,07; 95% CI: 0,72–1,61) als auch für die HRR-mutierte Subgruppe (HR: 0,56; 95% CI: 0,25–1,23) nicht signifikant unterschiedlich.
Ein Ansprechen wurde bei 28,2% versus 18,4% der Patienten der ITT-Population sowie bei 35,3% versus 0%der Patienten der HRR-mutierten Population gesehen. Die mediane Dauer des Ansprechens betrug 8,9 Monate im Olaparib-Arm versus 14,8 Monate im Placebo-Arm für Patienten der ITT-Population sowie 6,7 Monate für Patienten mit HRR-mutierten Tumoren unter Olaparib plus Durvalumab. Es wurden keine neuen Sicherheitssignale für die Kombination von Durvalumab plus Olaparib beobachtet.
Quelle:
ASCO Genitourinary Cancers Symposium (ASCO GU), 17.–19. Februar 2022, San Francisco und virtuell
Literatur:
1 Smith MR et al.: Overall survival with darolutamide versus placebo in combination with androgen-deprivation therapy and docetaxel for metastatic hormone-sensitive prostate cancer in the phase 3 ARASENS trial. ASCO GU 2022; Abstr. #13 2 Merseberger AS et al.: A randomised, double-blind, placebo-controlled, phase 3b study of the efficacy and safety or continuing enzalutamide in chemotherapy-naive metastatic castration-resistant prostate cancer patients treated with docetaxel plus prednisolone who have progressed on enzalutamide alone – PRESIDE. ASCO GU 2022; Abstr. #15 3 Petrylak DP et al.: Study EV-103 cohort H: Antitumor activity of neoadjuvant treatment with enfortumab vedotin monotherapy in patients with muscle invasive bladder cancer who are cisplatin-ineligible. ASCO GU 2022; Abstr. #435 4 Fulton B et al.: ATLANTIS: A randomised multi-arm phase II biomarker-directed umbrella screening trial of maintenance targeted therapy after chemotherapy in patients with advanced or metastatic urothelial cancer. Trials 2020; 21: 344 5 Crabb SJ et al.: A randomized, double blind, biomarker selected, phase II trial of maintenance PARP inhibition following chemotherapy for metastatic urothelial carcinoma: Final analysis of the ATLANTIS rucaparib arm. ASCO GU 2022; Abstr. #436 6 Rosenberg JE et al.: BAYOU: A phase II, randomized, multicenter, double-blind, study of durvalumab in combination with olaparib for the first-line treatment of platinum-ineligible patients with unresectable, stage IV urothelial carcinoma. ASCO GU 2022; Abstr. #437
Das könnte Sie auch interessieren:
Grosse Studie zu pflanzenbasierter Ernährung startet
Die sogenannte Coplant-Studie wird die nächsten Jahrzehnte den Einfluss des Essverhaltens auf die Gesundheit untersuchen.
Kampf gegen Antibiotikaresistenzen: Das sind die Pläne des Bundesrats
Der Bundesrat hat den neuen One Health-Aktionsplan für den Zeitraum 2024 bis 2027 verabschiedet. Leading Opinions Wochenbulletin skizziert den Sechs-Punkte-Plan.
Alkoholkonsum tötet jährlich Millionen Menschen
Eine neue Studie der Weltgesundheitsorganisation warnt vor den Auswirkungen von Alkoholkonsum. Die Schweiz liegt dabei über dem europäischen Durchschnitt.