Asthma und FeNO: Was der Biomarker leisten kann
Bericht:
Mag. Andrea Fallent
Redaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Messung des FeNO (fraktioniertes exhaliertes Stickstoffmonoxid) in der Ausatemluft ist eine nicht invasive, einfache und schnelle Methode zur Bewertung, Überwachung und Therapieoptimierung bei Atemwegsentzündungen wie Asthma bronchiale.
Die Rolle der Biomarker in der Medizin hat in den vergangenen 10 bis 15 Jahren massgeblich an Bedeutung gewonnen, nicht zuletzt auch in der Pneumologie und hier insbesondere zur Differenzierung verschiedener Asthma-Phänotypen. Biomarker können dabei helfen, bestimmte Krankheiten zu diagnostizieren, Behandlungen zu steuern und die Therapiewirkung zu überprüfen.
FeNO als Biomarker bei Asthma
«Das fraktionierte exhalierte Stickstoffmonoxid (FeNO) ist ein Biomarker, der das Ausmass einer Typ-2-Inflammation in der Lunge anzeigt», erklärte PD Dr. med. Robab Breyer-Kohansal, Abteilung für Atmungs- und Lungenerkrankungen und Ludwig Boltzmann Institut für Lungengesundheit, Klinik Hietzing, Wien, einleitend.
Die Bedeutung des FeNO als Biomarker wird bereits seit Beginn der 1980er-Jahre erforscht. Damals wurde erkannt, dass auch gesunde Epithelzellen der Atemwege Nitritoxid (NO) produzieren und freisetzen und die Menge durch bestimmte Trigger beeinflusst wird. Geringe Mengen an ausgeatmetem NO sind physiologisch. Das Spezielle am FeNO als Biomarker ist, dass es im Zusammenhang mit Asthma auch auf einen speziellen Phänotyp hinweist. Durch eine Interleukin-Aktivierung, im Besonderen von IL-4 und IL-13 als Trigger der Typ-2-Inflammation, wird vermehrt NO in den Epithelzellen der Bronchialwände freigesetzt.
1992 wurde NO zum Molekül des Jahres gekürt und 1998 stand es im Mittelpunkt des Nobelpreises für Medizin bzw. Physiologie. «Es ist beeindruckend, dass man mit einer derart einfachen Messung ein Problem in den Atemwegen detektieren kann», so Breyer-Kohansal. «Wir wissen mittlerweile, dass zwei sehr prävalente Erkrankungen, die allergische Rhinitis und das allergische Asthma bronchiale, durch eine FeNO-Erhöhung gekennzeichnet sind.»
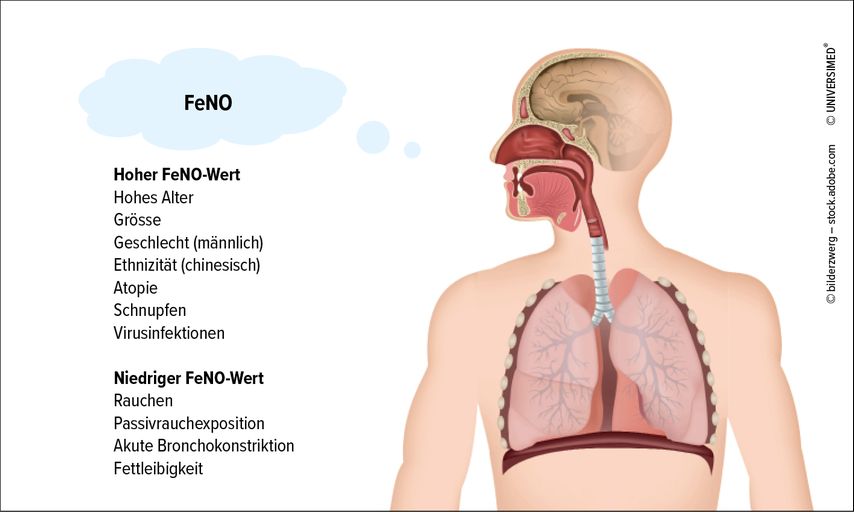
Wichtige Einflussfaktoren, die den Wert erhöhen, sind Alter, Grösse, Geschlecht, Ethnizität, Atopie, Rhinitis und virale Infektionen. Rauchen, Passivrauchen, Übergewicht und akute Bronchokonstriktion können den Wert vermindern (Abb. 1).2
Im Zuge der LEAD-Studie, die am Ludwig Boltzmann Institut für Lungengesundheit in Wien läuft, wurden die bisherigen Proband:innen auch auf ihren FeNO-Wert und dessen Beeinflussung durch Alter, Geschlecht und Körpergrösse untersucht. Ergebnisse dazu wurden 2022 am ERS-Kongress präsentiert.3 Die Daten unterstreichen, dass die Etablierung von konkreten FeNO-Referenzwerten in Bezug auf diese Parameter wünschenswert wären. «Doch so weit sind wir noch nicht. Bis jetzt arbeiten wir mit einem Cut-off, der ganz gut funktioniert», so Breyer-Kohansal.
Parameter für Diagnose und Therapie
Das FeNO ist ein sehr guter Parameter mit einer hohen Sensitivität und Spezifität für allergisches Asthma und wird vor allem in der Differenzialdiagnostik unterstützend zur Abgrenzung von anderen Erkrankungen, vor allem COPD, eingesetzt. Es ist ein gutes Mass für die Zahl der Eosinophilen im Blut. Breyer-Kohansal: «Liegt der FeNO-Wert über 40ppb, ist die Wahrscheinlichkeit für Asthma um das 7-Fache erhöht».
Beim Asthma-Management nimmt FeNO zudem bei der Prophylaxe bzw. Reduzierung und auch der Detektion von Exazerbationen eine wichtige Rolle ein.4,5 In diesem Sinne ist es auch ein Marker für den Nutzen von inhalativen Kortikosteroiden (ICS) in der Behandlung bzw. für die Therapieadhärenz: «Der FeNO-Spiegel kann in vier Tagen um bis zu 50% gesenkt werden, wenn ICS regelmässig appliziert werden.»
FeNO bei Covid-19 und interstitiellen Lungenerkrankungen
Die Art der entzündlichen und fibrotischen Prozesse, die bei Patient:innen mit Post-Covid-19-Syndrom auftreten, lässt darauf spekulieren, dass in diesem Zusammenhang das FeNO ein nützlicher Biomarker sein könnte. In einer Studie wurden 68Post-Covid-Patient:innen untersucht, nachdem sie innerhalb von zwei Monaten nach Ausbruch der Krankheit wegen persistierender klinischer Manifestationen ins Krankenhaus eingeliefert worden waren, 29 gesunde Proband:innen standen als Kontrollgruppe zur Verfügung.6 Keine der Post-Covid-Patient:innen hatte Asthma bronchiale oder wurde mit einem Kortikosteroid behandelt. Das Ergebnis: Nur 19 von 68 Post-Covid-19-Patient:innen hatten einen FeNO-Wert >25ppb. Der mittlere FeNO-Wert betrug 18,55ppb (95%-CI: 15,50–21,58), während er bei den gesunden Testpersonen 17,46ppb (95%-CI: 15,75–19,17) betrug. Die in dieser Studie generierten Daten deuten darauf hin, dass die FeNO-Messung als Biomarker bei Post-Covid-19 nicht nützlich ist.
Etwas anders präsentiert sich die Situation im Zusammenhang mit interstitiellen Lungenerkrankungen (ILD),7 da NO auch an fibrotischen Prozessen beteiligt ist, wie Breyer-Kohansal ausführte: «FeNO hat Potenzial bei der Unterscheidung von idiopathischen ILD und ermöglicht eine gute Abschätzung in Hinblick auf Überleben, Krankheitsverlauf und Verminderung der Lungenfunktion.» Auch hier kommen die Vorteile wie Reproduzierbarkeit, Wiederholbarkeit und die nicht invasive Durchführung zum Tragen, die eine Umsetzung im klinischen Management attraktiv machen würden. Allerdings reiche die Datenlage derzeit dafür noch nicht aus, so die Referentin.
Wichtige Aspekte der FeNO-Messung
FeNO-Messungen sind sicher, schnell und einfach ab einem Alter von circa vier Jahren durchzuführen, selbst wenn die Lungenfunktion stark eingeschränkt ist. Die FeNO-Messung erfordert eine hohe Empfindlichkeit und eine kurze Ansprechbarkeit des Messgerätes. Laut internationalen Empfehlungen sollten Messegeräte eine Empfindlichkeit von 1ppb, eine Genauigkeit von <1 ppb und eine Ansprechbarkeit von <500ms aufweisen.
Beeinflussung durch Lebensmittel
Ein Nachteil dieses Biomarkers ist seine Beeinflussbarkeit durch weitere Faktoren, u.a. auch durch den Lifestyle und die Ernährung. So können nitratreiche Blattgemüse wie Salat, Spinat, Kohl sowie Randen den Wert um bis zu 150% erhöhen.8,9 Koffein, Alkohol und Tabak können den FeNO-Spiegel wiederum reduzieren, bei Zigaretten ist der Effekt langfristig, wie Messungen bei Ex-Raucher:innen zeigen.10 Auf diese Faktoren sollten Patient:innen vor der Messung hingewiesen werden. Ebenso, dass Sport ein bis zwei Stunden vor der Messung vermieden werden sollte.
Natürliche Variabilität
Auch ohne Inflammation der Atemwege weist der FeNO-Spiegel eine gewisse Schwankungsbreite auf, bei Gesunden sind es etwa 10%, bei Asthmatiker:innen bis zu 20%. Eine Variation von mehr als 20% gilt als klinischsignifikant. «Als wichtige Anhaltspunkte gelten daher die Verlaufswerte bzw. die Differenz zwischen vorhergehenden und aktuellen Messungen», so Breyer-Kohansal.
Resümee
Abschliessend fasste die Expertin die wesentlichen Punkte der FeNO-Bestimmung zusammen (Tab. 1) und wies nochmals darauf hin, dass die Messung nur als wertvolle Ergänzung zur Überprüfung der Lungenfunktion gedacht ist: «FeNO ist ein Teil der diagnostischen Kaskade und kein Ersatz dafür.»
Quelle:
Online-Livestream «Fraktioniertes exhaliertes Stickstoffmonoxid (FeNO) in der Diagnose und Therapie von Asthma bronchiale» der Österreichischen Medizinischen Gesellschaft für Real World Evidence, 2. März 2023; Vortrag abrufbar in der Mediathek unter https://rwe-online.at/e-learning
Literatur:
1 Alving K et al.: Basic aspects of exhaled nitric oxide. European Respiratory Society Monograph 2010; doi:10.1183/1025448x.erm4910 2 Ricciardolo F et al.: A pathophysiological approach for FeNO: A biomarker for asthma. Allergol Immunopaothol 2015; 43: 609-16 3 Bal C et al.: FeNO in a healthy population: normal ranges and contributing factors. Eur Respir J 2022; 60 (Suppl.66): 4523 4 Peirsman E et al.: Exhaled nitric oxide in childhood allergic asthma management: A randomised controlled trial. Pediatr Pulmonol 2014; 49: 624-31 5 Syk J et al.: Anti-inflammatory treatment of atopic asthma guided by exhaled nitric oxide: a randomized, controlled trial. J Allergy Clin Immunol Pract 2013; 1: 639-48 6 Maniscalco M et al.: Can FeNO be a biomarker in the post-COVID-19 patients monitoring? Respir Med 2022; 193: 106745 7 Cameli P et al.: Extended exhaled nitric oxide analysis in interstitial lung diseases: a systematic review. Int J Mol Sci 2020; 21: 6187 8 Kroll JL et al.: Acute ingestion of beetroot juice increases exhaled nitric oxide in healthy individuals. PLoS One 2018; 13: e0191030 9 Kerley CP et al.: Dietary nitrate acutely and markedly increased exhaled nitric oxide in a cystic fibrosis case. Clin Med Res 2016; 14: 151-5 10 Jacinto T et al.: Differential effect of cigarette smoke exposure on exhaled nitric oxide and blood eosinophils in healthy and asthmatic individuals. J Breath Res 2017; 11: 036006
Das könnte Sie auch interessieren:
COPD: die Suche nach undiagnostizierten Patienten
Zahlreiche von COPD und/oder Asthma betroffene Menschen haben niemals eine Diagnose erhalten und stehen folglich nicht unter Behandlung. Mehrere in den vergangenen Monaten publizierte ...
Innovative Pharmakotherapien bei ILD
Derzeit befinden sich mehrere Wirkstoffe für die Behandlung von idiopathischer pulmonaler Fibrose (IPF) und progredienter pulmonaler Fibrose (PPF) in der Entwicklung, wobei verschiedene ...