Was müssen Pneumologen bei der HRCT beachten?
Autor:
Dr. med. Mathis Hochrainer
Abt. für Innere Medizin und Pneumologie mit ICU
Klinik Floridsdorf, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die hochauflösende Computertomografie (HRCT) stellt gerade bei interstitiellen Lungenerkrankungen (ILD) einen wichtigen Eckpfeiler in der Diagnostik dar. Die Beantwortung von vier Fragen kann hilfreich sein, CT-morphologische Krankheitsmuster in HRCT-Bildern zu interpretieren und die Differenzialdiagnosen einzugrenzen.
Keypoints
-
HRCT-Bilder haben einen hohen Stellenwert in der Diagnostik von interstitiellen Lungenerkrankungen.
-
Mit HRCT-Bildern kann im ersten Schritt eingeschätzt werden, ob pathologische radiologische Veränderungen vorliegen.
-
Direkt radiologisch beweisend für eine Lungenfibrose ist das Vorliegen des sogenannten «Honeycombing».
-
Das Muster einer gewöhnlichen interstitiellen Pneumonie (UIP-Muster) sollte von alternativen radiologischen Mustern anderer häufig vorkommender interstitieller Lungenerkrankungen abgegrenzt werden.
Die Rolle der Radiologie in der Diagnostik interstitieller Lungenerkrankungen
Bei der Diagnostik interstitieller Lungenerkrankungen (ILD) nimmt die hochauflösende Computertomografie (HRCT) der Lunge eine zentrale Rolle ein. Ihre Aufgabe besteht in der Eingrenzung der Differenzialdiagnosen durch die Bestimmung des vorliegenden CT-morphologischen Erkrankungsmusters. In vielen Fällen ist die Radiologie hier in Kombination mit Anamnese und klinischer Untersuchung ausreichend, sodass gemäss aktuellen Leitlinien bei entsprechendem Verdacht und typischem radiologischem Befund auf eine weiterführende invasive Diagnostik verzichtet werden kann. Wird zur differenzialdiagnostischen Abklärung doch eine Biopsieentnahme benötigt, erfolgt diese heute meist in Form einer bronchoskopischen Kryobiopsie sowie in selteneren Fällen durch eine chirurgische Lungenbiopsie. Die so gewonnenen histologischen und zytologischen Ergebnisse werden dann im Rahmen eines ILD-Boards, also einer multidisziplinären Fallkonferenz von Vertretern aus Pneumologie, Radiologie, Pathologie und immer häufiger auch Rheumatologie, diskutiert und letztlich gemeinsam mit anderen Befunden zu einer Diagnose bzw. Arbeitsdiagnose zusammengefügt. Hierbei sind Radiologie und Pathologie jeweils Puzzleteile, die einander gleichwertig gegenübergestellt werden. Insofern unterscheidet sich der diagnostische Zugang bei ILD von jenem, den wir beispielsweise aus der Onkologie gewohnt sind, wo letztlich das histopathologische Ergebnis über die Diagnose entscheidet.
Mögliche Herangehensweise bei der Interpretation von HRCT-Bildern
Es gibt in der Diagnostik von ILD eine Vielzahl möglicher Algorithmen zur Interpretation von HRCT-Bildern. Eine Herangehensweise, die sich in der klinischen Praxis bewährt hat, soll im Folgenden beschrieben werden. Hierbei werden bei der Betrachtung der HRCT-Bilder 4 Fragen gestellt und beantwortet:
1. Sind die vorliegenden radiologischen Veränderungen pathologisch?
In den dorsalen Lungenabschnitten kommt es gelegentlich durch Hypostaseareale zu CT-morphologischen Veränderungen in Form von Retikulationen oder Milchglas, die eine Lungenfibrose vortäuschen können. Durch Umlagerung bilden sich diese Veränderungen zurück, im Zweifelsfall können sie durch die Anfertigung einer HRCT in Bauchlage von persistierenden interstitiellen Veränderungen unterschieden werden.
2. Liegt eine pulmonale Fibrose vor?
Es gibt drei starke radiologische Hinweise auf das Vorliegen einer pulmonalen Fibrose. Radiologisch beweisend ist hierfür nur das Vorliegen von «Honeycombing» (HC). Dabei handelt es sich um aneinandergrenzende luftgefüllte Zysten mit scharfer Wandbegrenzung, die mehrreihig angeordnet und typischer-, aber nicht notwendigerweise in subpleuraler Verteilung auftreten.
Indirekte Hinweise auf einen fibrosierenden Prozess bieten darüber hinaus Traktionsbronchiektasien (TB). Infolge der Fibrose kommt es zu einem Schrumpfungsprozess des Lungenparenchyms, der durch Zug an den Bronchial- und Bronchiolarwänden zu einer irregulären Erweiterung des Lumens der betroffenen Atemwege führt. Dabei müssen TB von Bronchiektasien abgegrenzt werden, denen keine fibrosierende Veränderung des Lungenparenchyms zugrunde liegt.
Eine Volumenreduktion einzelner Lungenabschnitte ist an sich ein relativ unspezifisches Merkmal, kann jedoch ein indirekter Hinweis auf das Vorliegen einer pulmonalen Fibrose sein.
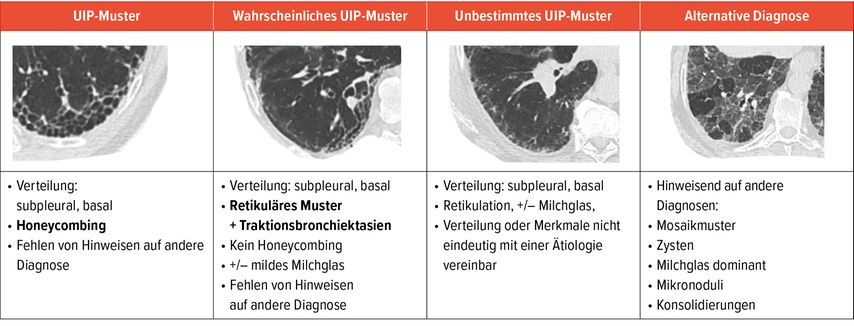
3. Entspricht das radiologische Bild dem einer gewöhnlichen interstitiellen Pneumonie (UIP)?
UIP bezeichnet ein klar definiertes radiologisches oder histopathologisches Muster, aber keine Diagnose. Obligat sind das Vorliegen von Honeycombing und eine charakteristische Verteilung der Veränderungen mit subpleuraler, basaler Prädominanz.
Ein UIP-Muster kann bei Erkrankungen unterschiedlicher Ätiologie, wie beispielsweise der idiopathischen pulmonalen Fibrose (IPF), der exogen-allergischen Alveolitis (EAA) oder im Zuge der Lungenbeteiligung diverser rheumatologischer Erkrankungen, beobachtet werden. Alleine für sich genommen ist das Vorliegen eines radiologischen UIP-Musters unzureichend, um eine klinische Diagnose zu stellen. Findet sich jedoch bei radiologischem UIP-Muster auch nach sorgfältiger klinischer Evaluation kein Hinweis auf eine zugrunde liegende Erkrankung, die als Ursache der UIP infrage käme, kann die Diagnose einer IPF gestellt werden. Das UIP-Muster wird vom wahrscheinlichen («probable») UIP-Muster und dem unbestimmten («indeterminate») UIP-Muster abgegrenzt. Jedes radiologische UIP-Muster hat jedenfalls seine eigenen Kriterien (Tab. 1).
Bei entsprechendem klinischem Verdacht entscheiden in der Diagnostik der IPF Anamnese, Serologie und die radiologische Klassifikation in Zusammenschau über das empfohlene weitere Vorgehen. (Abb. 1). Während beim Vorliegen eines UIP-Musters keine Biopsie notwendig ist, wird beim unbestimmten UIP-Muster die Durchführung von Kryobiopsie und bronchoalveolärer Lavage (BAL) empfohlen. Handelt es sich um ein wahrscheinliches UIP-Muster, determiniert das individuelle Risikoprofil des Patienten in Bezug auf die Entwicklung einer IPF den nächsten diagnostischen Schritt. Höheres Alter (über 60 Jahre), männliches Geschlecht und (Ex-)Raucheranamnese sind bekannte Risikofaktoren einer IPF. Liegen diese vor, kann auf eine Kryobiopsie verzichtet werden. In diesem Fall wird lediglich die Durchführung einer BAL empfohlen, die v.a. der Abgrenzung von der wichtigen Differenzialdiagnose der EAA dient. Liegen diese Risikofaktoren nicht vor, wird die Diagnose einer IPF unwahrscheinlicher. In diesen Fällen ist zur weiteren Abklärung neben der BAL auch eine Kryobiopsie empfohlen.
Abb. 1: Algorithmus zur Vorgehensweise bei idiopathischer Pulmonalfibrose (IPF) (modifiziert nach Behr J et al. 2020)
4. Liegt ein zur UIP alternatives, radiologisches Muster vor?
Es gibt eine Reihe radiologischer Differenzialdiagnosen zur UIP. V.a. zwei, die in der Praxis besonders wichtig sind, werden im Folgenden beschrieben.
Nicht spezifische interstitielle Pneumonie (NSIP)
Das radiologische Bild einer NSIP findet sich häufig im Zuge der Lungenbeteiligung bei Systemerkrankungen, wie beispielsweise systemischer Sklerose, systemischem Lupus erythematodes, Dermatomyositis und anderen Kollagenosen. Wenn sich keine Ursache der NSIP finden lässt, wird eine idiopathische NSIP (iNSIP) diagnostiziert. Die HRCT bei NSIP ist durch das Vorliegen von Milchglas, Retikulationen, Traktionsbronchiektasien und Volumenverlust der Unterlappen charakterisiert. Die typische Verteilung zeigt eine basale Dominanz. Eine Aussparung des Subpleuralraums ist charakteristisch, liegt aber nicht immer vor.
Exogen-allergische Alveolitis (EAA)
Eine EAA kann nur in Zusammenschau von Klinik und Radiologie diagnostiziert werden kann. Sie wird in eine fibrosierende und eine nicht fibrosierende Form eingeteilt. Die grosse Variabilität der radiologischen Präsentation macht die Diagnose der EAA besonders herausfordernd. Die typische Radiologie der EAA erfordert sowohl Hinweise auf eine Erkrankung der kleinen Atemwege als auch auf eine Parenchyminfiltration bzw. pulmonale Fibrose. Das charakteristische Verteilungsmuster ist diffus, mit einer fakultativen Aussparung der basalen Lungenabschnitte.
Fazit
Die interdisziplinäre Fallkonferenz in Form eines ILD-Boards ist der Goldstandard in der Diagnose interstitieller Lungenerkrankungen. Mittels HRCT kann das CT-morphologische Erkrankungsmuster beschrieben und dadurch in vielen Fällen die Diagnose eingegrenzt werden. Neben dem radiologischen UIP-Muster, das bei der IPF, aber auch anderen ILD auftritt, stellen NSIP und EAA wichtige Differenzialdiagnosen dar.
Literatur:
● Behr J et al.: S2K-Leitlinie zur Diagnostik der idiopathischen Lungenfibrose. Pneumologie 2020; 74: 263-93 bzw. Korrektur in Pneumologie 2020; 74: e1-e2 ● Hansell DM et al.: Fleischner society: glossary of terms for thoracic imaging. Radiology 2008; 246: 697-722 ● Jacob J, Hansell DM: HRCT of fibrosing lung disease. Respirology 2015; 20: 859-72 ● Raghu G et al.: Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. Am J Respir Crit Care Med 2018; 198: e44-e68 ● Raghu G et al.: Diagnosis of hypersensitivity pneumonitis in adults. An official ATS/JRS/ALAT clinical practice guideline. Am J Respir Crit Care Med 2020; 202: e36-e69 ● Travis WD et al.: An official American Thoracic Society/European Respiratory Society statement: Update of the international multidisciplinary classification of the idiopathic interstitial pneumonias. Am J Respir Crit Care Med 2013; 188: 733-48
Das könnte Sie auch interessieren:
COPD: die Suche nach undiagnostizierten Patienten
Zahlreiche von COPD und/oder Asthma betroffene Menschen haben niemals eine Diagnose erhalten und stehen folglich nicht unter Behandlung. Mehrere in den vergangenen Monaten publizierte ...
Innovative Pharmakotherapien bei ILD
Derzeit befinden sich mehrere Wirkstoffe für die Behandlung von idiopathischer pulmonaler Fibrose (IPF) und progredienter pulmonaler Fibrose (PPF) in der Entwicklung, wobei verschiedene ...